基于QbD理念优化黄体素类脂质体工艺研究
2022-03-17孔繁铭贾珍珍霍文凯张炜煜
孔繁铭,胡 悦,辛 宇,贾珍珍,霍文凯,张炜煜
(长春中医药大学药学院,长春 130117)
植物黄体素(lutein),又称叶黄素,属于类胡萝卜素中的一种四萜类化合物,广泛存在于果蔬、在藻类植物中,是维生素A的重要来源[1]。天然黄体素为菱格状的鲜艳黄色晶体[2],其结构中含有两个紫罗酮环,可作为强氧化剂用于抗氧化、抗视疲劳以及预防心血管疾病,被广泛应用于医疗、保健品等领域[3]。但黄体素水溶性较差,微溶于油,存在多个不饱和键和末端双羟基结构,化学性质较不稳定,易受温度、光照、金属离子等各种理化因素的影响而产生变化[4]。
类脂质体复合物是一种良好的药物载体,利用非离子型表面活性剂与胆固醇在水合介质中形成双分子层的结构,含有疏水基团和亲水基团[5]。其制备方法与脂质体制备方法相似,区别为将磷脂替换为非离子型表面活性剂,增强其抗氧化性,降低制备的成本。Minamisakamoto等[6]研究发现DOXPEG类脂质体贯穿给药可大幅度提高抗肿瘤效果,Damrongrungruang等[7]近期研究发现将紫糯玉米和蓝蝶豌豆花瓣提取物通过类脂质体复合物包合可加速创面愈合。因此,本实验通过拟制备黄体素类脂质体以解决黄体素理化性质不稳定、水溶性差等问题,同时降低工艺成本。
1 仪器与试剂
1.1 仪器设备
KQ200B型超声波清洗器(昆山市超声仪器有限公司)、85-2数显恒温磁力搅拌器(常州市江南实验仪器厂)、AR2140型电子天平(梅特勒-托利多仪器有限公司)、高速台式离心机(上海安亭科学仪器厂)、UV-5100型紫外-可见分光光度计(山东析远仪器有限公司)。
1.2 材料与试剂
叶黄素原料药(上海源叶生物有限公司)、叶黄素对照品(上海源叶生物有限公司)、胆固醇(上海源叶生物有限公司)、硬脂山梨坦(上海麦克林生化科技有限公司)、聚山梨酯80(上海麦克林生化科技有限公司)、无水乙醇(天津新通精细化工有限公司)。
2 方法与结果
2.1 黄体素类脂质体制备
取处方量黄体素、胆固醇、Span60与Tween80溶于无水乙醇中,恒温水浴下将有机相缓慢注入水相中,并搅拌至无水乙醇完全蒸发,0.22 μm微孔滤膜过滤,即得。
2.2 体外分析方法建立
2.2.1 对照品溶液的制备 精密称定黄体素标准品0.005 g,置25 mL棕色量瓶中,加无水乙醇定容,摇匀,制成0.2 mg.mL黄体素的对照品溶液。
2.2.2 供试品溶液的制备 取黄体素类脂质体分散液于离心管中,以12 000 r·min-1转速下离心20 min,取下层蒸干后用无水乙醇溶解,吸取200 uL于10 mL棕色量瓶中,定容,混匀,滤过,即得。
2.2.3 确定最佳吸收波长 精密称取0.002 g叶黄素,加无水乙醇溶解,移至25 mL棕色量瓶,定容。移取1.0 mL置25 mL棕色量瓶中,加无水乙醇定容。用紫外分光光度计进行光谱扫描发现叶黄素在447 nm处有最大吸收,故选447 nm作为最大吸收波长。见图1、图2。
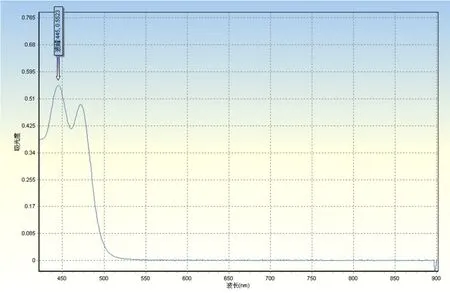
图1 黄体素对照品在各波长下的吸光度
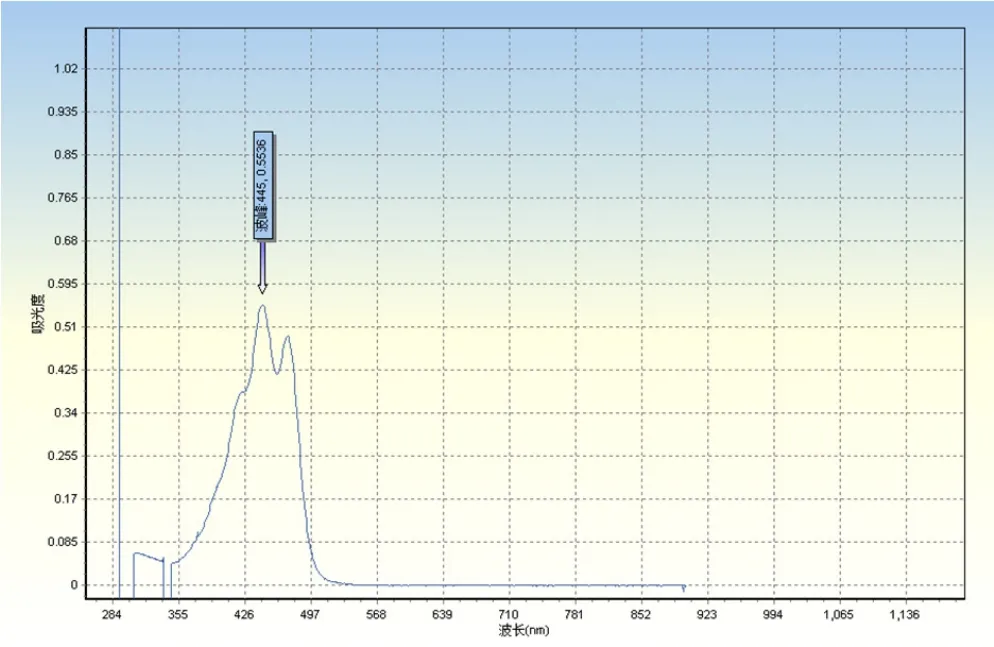
图2 黄体素供试品在各波长下的吸光度
2.2.4 标准曲线建立 量取2.2.1项下对照品溶液0.6 mL、0.7 mL、0.8 mL、0.9 mL、1.0 mL、1.1 mL分别加入10 mL棕色量瓶中,定容。在447 nm处测定吸光度,重复3次,绘制标准曲线。
如图3所示,黄体素的标准曲线为Y= 25.143X+0.011 6,R2=0.999 2,表明黄体素的吸光度与浓度在0.012 mg·mL-1~0.022 mg·mL-1范围内线性关系良好。
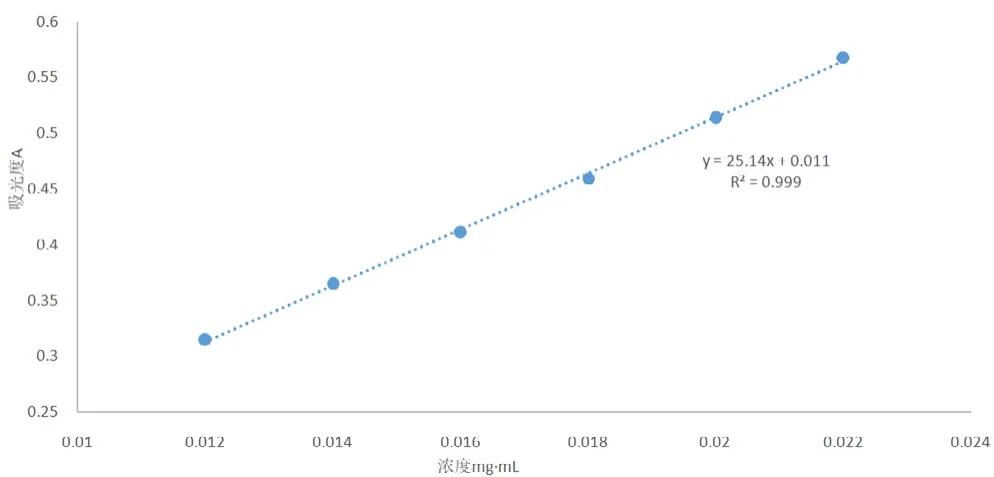
图3 黄体素标准曲线
2.2.5 精密度实验 取黄体素类脂质体,按2.2.2项下制备供试品溶液,按紫外分光光度法在447 nm处测定溶液吸光度,1 d内测定5次。根据表3,测量RSD值<2%(n= 5),此分析方法的精密度良好。见表1。
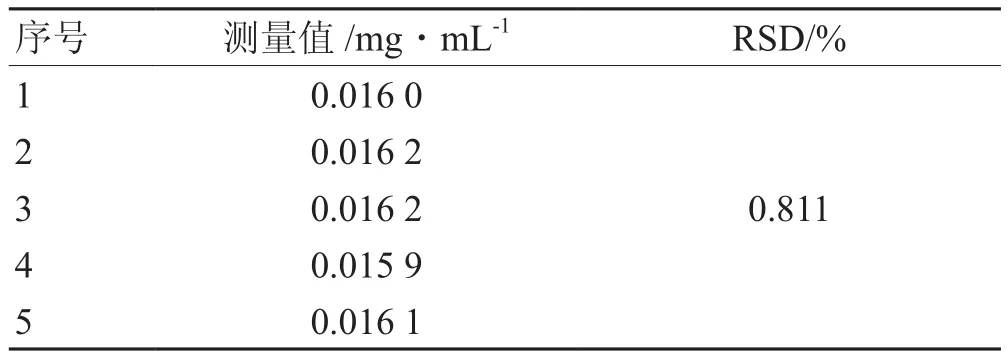
表1 精密度试验结果
2.2.6 加样回收率实验 按处方量120%、100%、80%,按2.2.2项下制备3种不同浓度的供试液,平均回收率99.29%,RSD值0.910%,表明此分析方法准确度良好。见表2。
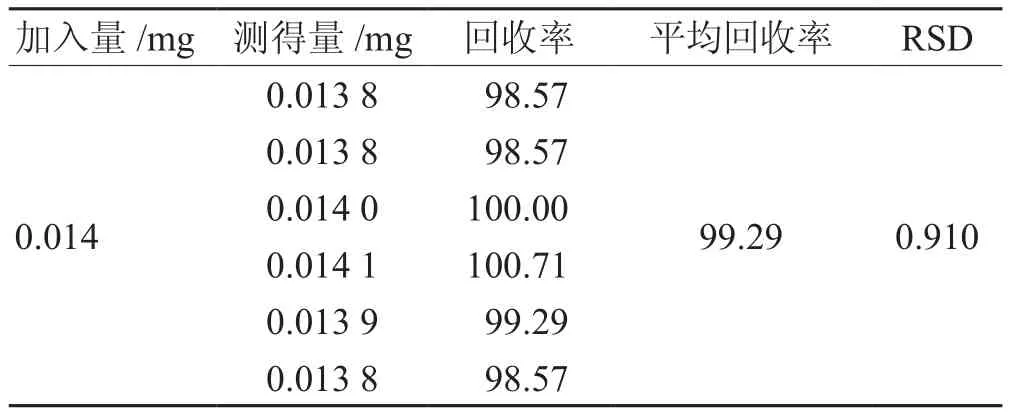
表2 加样回收率试验结果 %
2.2.7 包封率、载药量测定 取黄体素类脂质体分散液2 mL于12 000 r·min-1下离心20 min,取上清液200 μL置10 mL棕色量瓶,加无水乙醇定容,摇匀,0.22 μm微孔滤膜过滤,根据黄体素标准曲线用紫外分光光度计法计算游离药物的含量,进而计算包封率与载药量。包封率=(总药量-游离药量)÷总药量×100%。载药量=类脂质体中所含药重÷类脂质体总重×100%
2.3 处方单因素考察
2.3.1 表面活性剂用量 固定黄体素用量0.01g,胆固醇用量0.05 g,Span60与Tween80比例为4:1,水化温度50 ℃,水相体积为40 mL,搅拌时间30 min,有机相注入速度为0.8 mL·min-1,有机相体积5 mL,搅拌速度450 r·min-1。考察不同用量Span60 与Tween80(0.04 g、0.06 g、0.08 g、0.10 g、0.12 g)对包封率与载药量的影响。结果表明,表面活性剂用量为0.08 g时包封率达到峰值,超过0.08 g后,包封率呈下降趋势,因此初步确定表面活性剂用量为0.08 g。见表3。
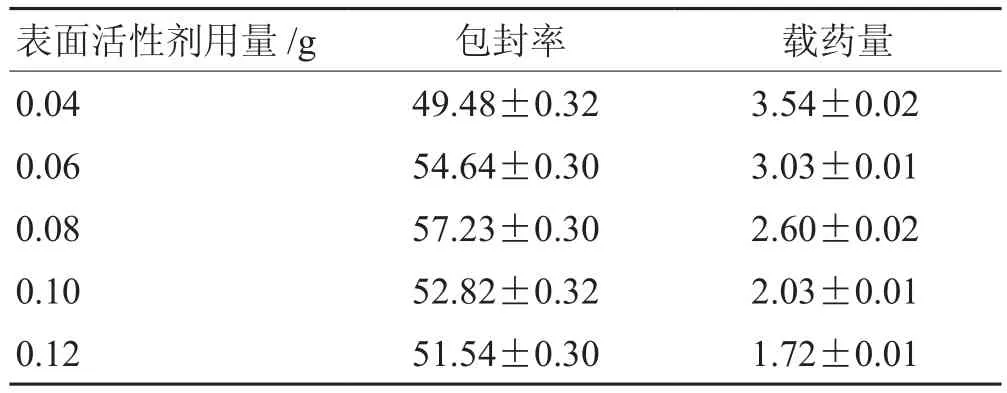
表3 非离子表面活性剂用量单因素考察结果 %
2.3.2 表面活性剂比例 固定其他条件同“2.3.1”。考察不同比例Span60与Tween80(4:1、4:2、4:3、4:4、4:5)对包封率与载药量的影响。结果表明,表面活性剂比例为4:4时包封率达到峰值,随着Tween80的比例的增加,包裹亲脂性药物的能力减弱,因此初步确定表面活性剂比例为4:4。见表4。
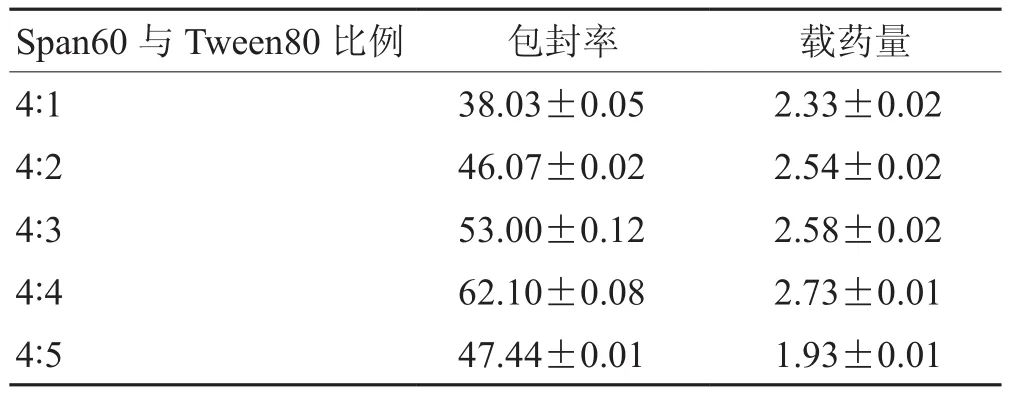
表4 表面活性剂比例单因素考察 %
2.3.3 胆固醇用量 固定其他条件同“2.3.1”。考察不同用量的胆固醇(0.03 g、0.04 g、0.05 g、0.06 g、0.07 g)对包封率和载药量的影响,结果表明,包封率与载药量最好呈现先升高后下降的趋势,当胆固醇用量达到0.05 g时包封率和载药量最好。见表5。
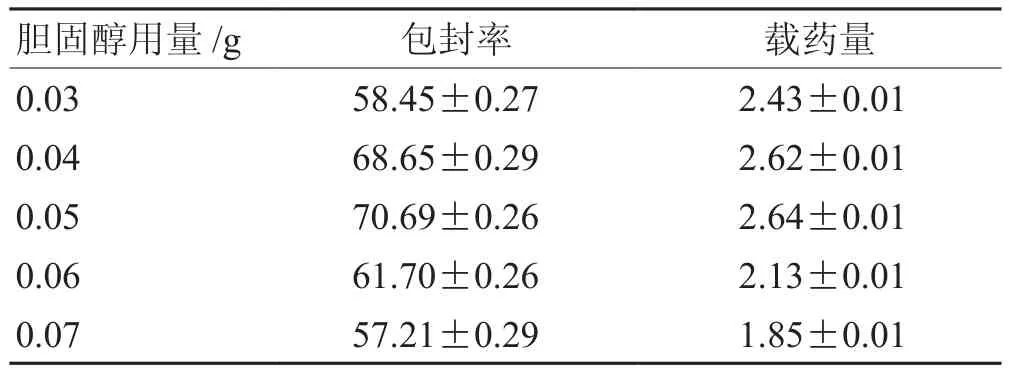
表5 胆固醇用量单因素考察结果 %
2.3.4 黄体素用量 固定其他条件同“2.3.1”。考察不同用量的黄体素(0.005 g、0.010 g、0.015 g、0.020 g、0.025 g)类对包封率和载药量的影响。结果表明,当黄体素用量为0.015 g时包封率达最峰值。随着黄体素用量继续增加,超过类脂质体承载能力的黄体素保留在溶液中,包封率和载药量也随之下降,因此选择黄体素最佳用量为0.015 g。见表6。
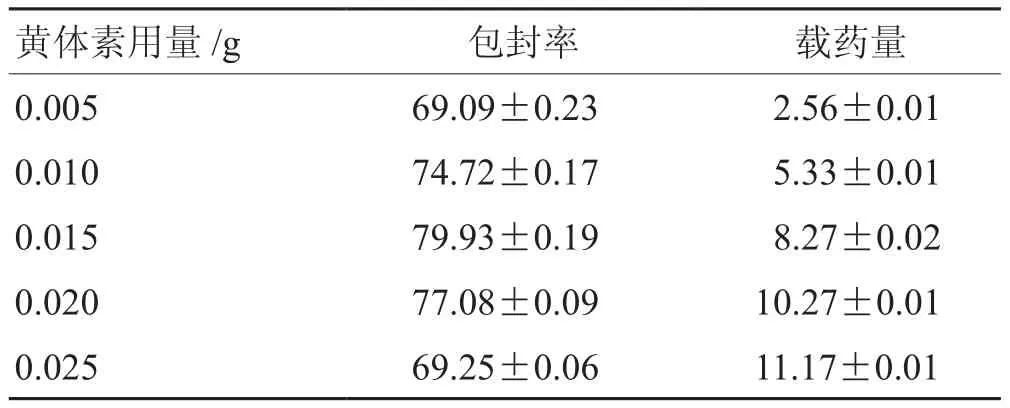
表6 黄体素用量单因素考察结果 %
2.3.5 水化温度 固定其他条件同“2.3.1”。考察水化温度(30 ℃、40 ℃、50 ℃、60 ℃、70 ℃)对黄体素类脂质体理化性质的影响,结果表明,当水化温度为60 ℃时包封率与载药量达到峰值,当水化温度大于60 ℃时,包封率与载药量逐渐降低,分析原因可能为高温致使黄体素分解。因此判断最佳水化温度为60 ℃。见表7。
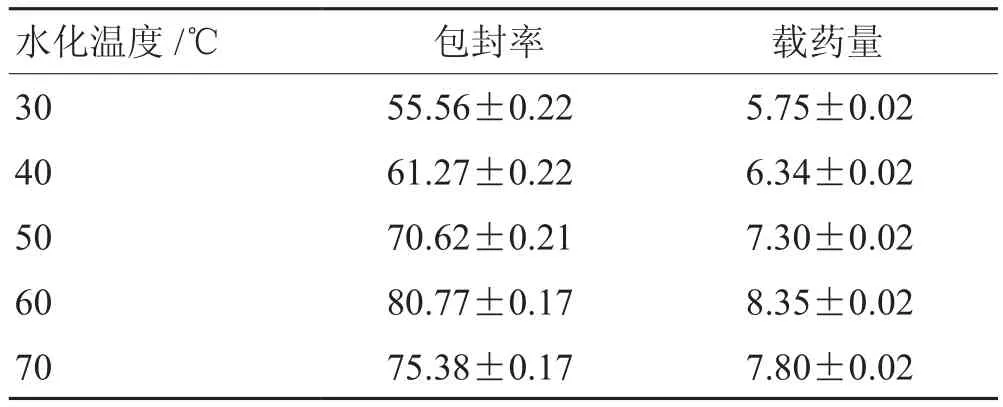
表7 水化温度单因素考察结果 %
2.3.6 水相体积 固定其他条件同“2.3.1”。考察不同体积水相(10 mL、20 mL、30 mL、40 mL、50 mL),对黄体素类脂质体包封率和载药量的影响。结果表明,水相体积为30 mL时包封率、载药量均达到峰值,随着水相增加,包封率与载药量呈下降趋势。见表8。
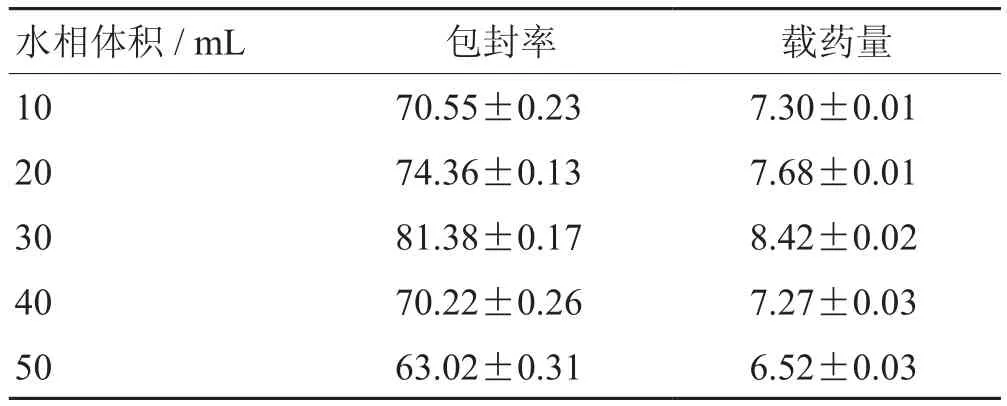
表8 水相体积单因素考察 %
2.3.7 搅拌时间 固定其他条件参照“2.3.1”,考察不同搅拌时间(20 min、30 min、40 min、50 min、60 min)对黄体素类脂质体包封率及载药量的影响。结果表明,搅拌时间为50 min时包封率与载药量均达到峰值,之后包封率与载药量有所下降,原因可能是超过50 min后黄体素分解过多。因此初步判断最佳搅拌时间为50 min。见表9。

表9 搅拌时间单因素考察 %
2.3.8 有机相注入速度 固定其他条件参照“2.3.1”。考察不同有机相注入速度(0.4 mL·min-1、0.8 mL·min-1、1.6 mL·min-1、2.4 mL·min-1、3.2 mL·min-1)的包封率与载药量情况,结果表明,有机相注入速度为0.8 mL·min-1时包封率与载药量均到达峰值,速度大于0.8 mL·min-1后黄体素无法及时进入类脂质体的囊泡中,导致包封率与载药量减低,因此初步确定有机相最佳注入速度为 0.8 mL·min-1。见表10。
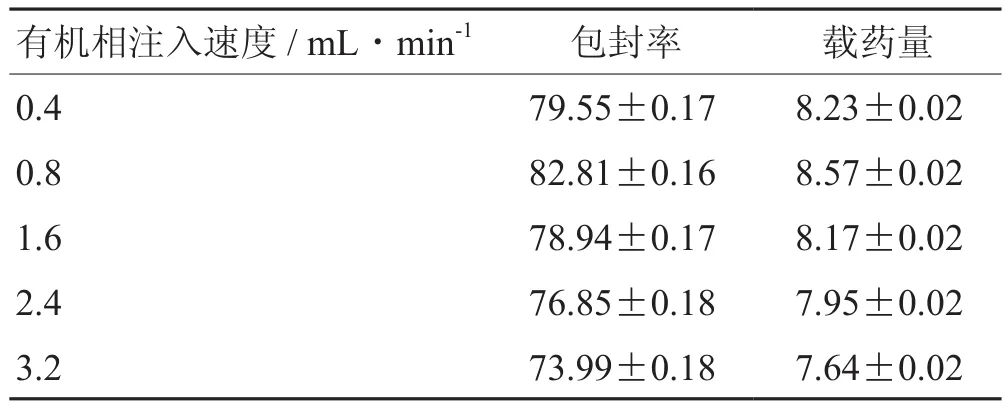
表10 有机相注入速度单因素考察 %
2.3.9 有机相体积 固定其他条件参照“2.3.1”。考察不同体积无水乙醇(2 mL、3 mL、4 mL、5 mL、6 mL)对包封率与载药量的影响。结果表明,有机相体积为5 mL时包封率与载药量均达峰值,随着有机相体积增大,包封率与载药量逐渐降低,因此初步确定有机相最佳体积为5 mL。见表11。
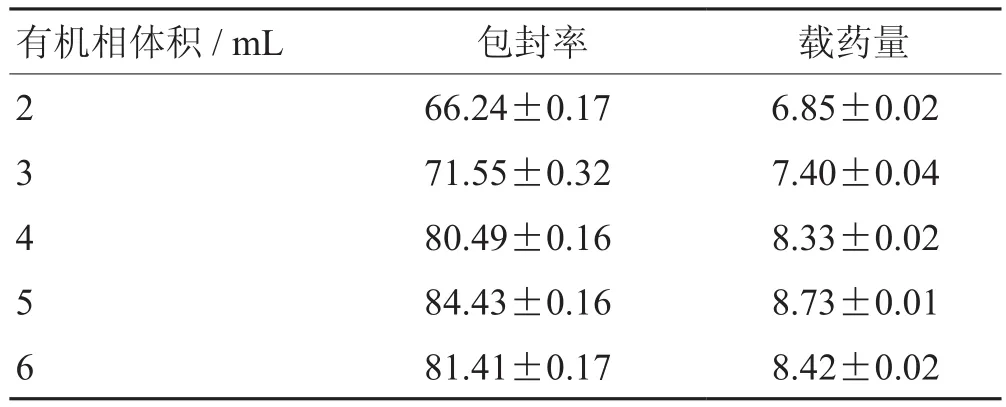
表11 有机相体积单因素考察 %
2.3.10 搅拌速度 固定其他条件同“2.3.1”。考察不同搅拌速度(100 r·min-1、150 r·min-1、300 r·min-1、450 r·min-1、600 r·min-1)对包封率与载药量的影响。结果表明,搅拌速度为300 r·min-1时包封率与载药量均达峰值,当搅拌速度超过300 r·min-1时包封率与载药量逐渐下降,因此初步判断最佳搅拌速度为300 r·min-1。见表 12。
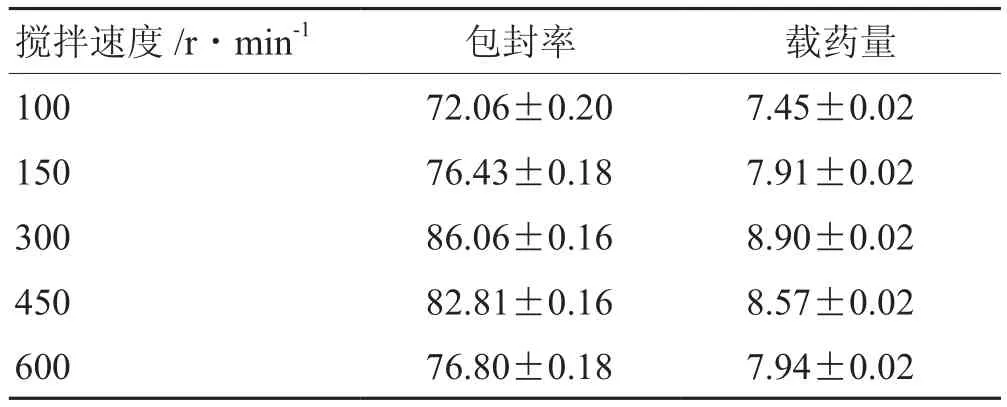
表12 搅拌速度单因素考察 %
2.4 归一化值(OD)的计算
评价指标综合包封率和载药量的归一化值(overall desirability,OD)。对取值越大越好的EE%、DL%分别进行数学转换,求各个指标归一值(d)。公式如下:
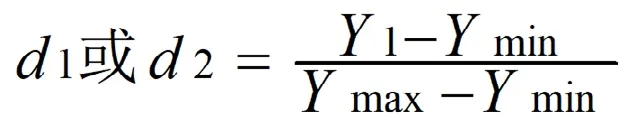
式中d1、d2分别代表黄体素脂质体的EE%和DL%归一化值,Y1为实测值,Ymin是实验中包封率和载药量测得最小值,Ymax是实验中测得的包封率和载药量最大值。将各指标的归一值综合求算,得总归一化值,公式如下:
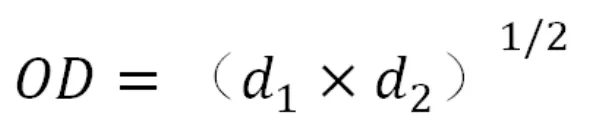
2.5 处方优化
2.5.1 Plackett-Burman试验设计 在前期单因素考察研究的基础上,设置表面活性剂用量(A)、表面活性剂比例(B)、胆固醇用量(C)、叶黄素用量(D)、水化温度(E)、水相体积(F)、搅拌时间(G)、有机相注入速度(H)、有机相体积(J)、搅拌速度(K)10个主要影响因素为自变量,以黄体素类脂质体的OD值为响应值,设定各因素两水平(-1、+1)的取值。设计因素水平设计见表13。
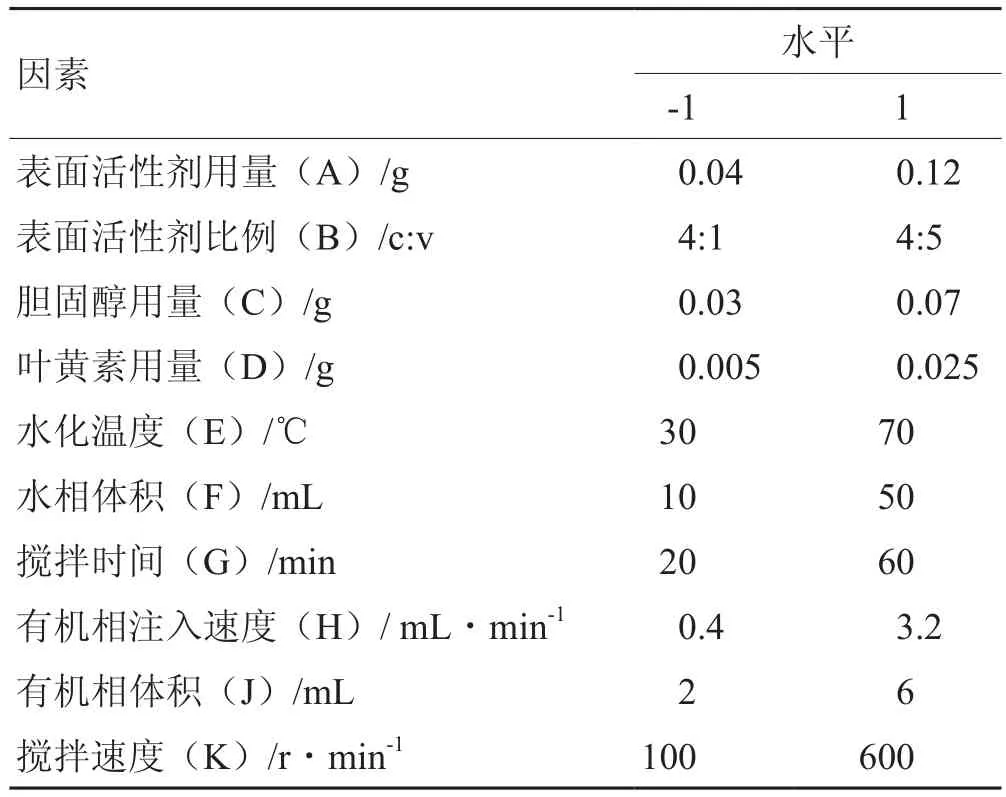
表13 Plackett-Burman试验因素及水平
实验结果见表14,用 Minitab 17.0 软件进行数据分析处理,得到其回归模型方程为OD =0.39846-0.01985A+0.16169B+0.01011C+0.17627D+0.20907E-0.08436F-0.02202G+0.02961H+0.00730J-0.06576K,通过对实验数据进行多元回归分析,结果见表15,模型P值为0.049,差异有统计学意义(P<0.05);F值为252.92,r= 0.986 5,提示回归拟合程度较好。由图4可知,B、D及E差异有统计学意义(P<0.05),对黄体素类脂质体OD值显著性排列为E>B>D;其余因素对OD值无显著性影响(P>0.05)。
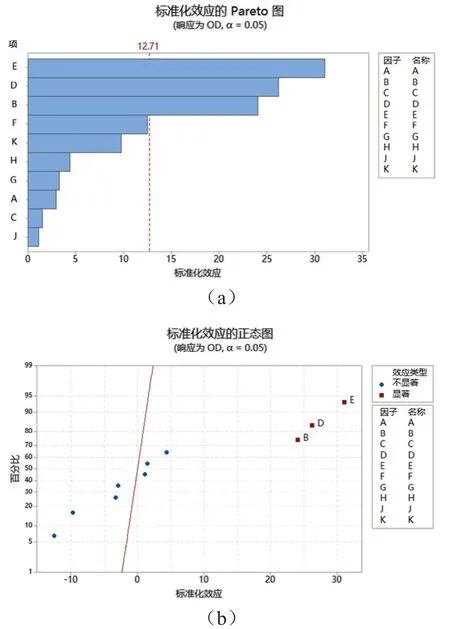
图4 响应值(Y)的Pareto图(a)及正态图(b)
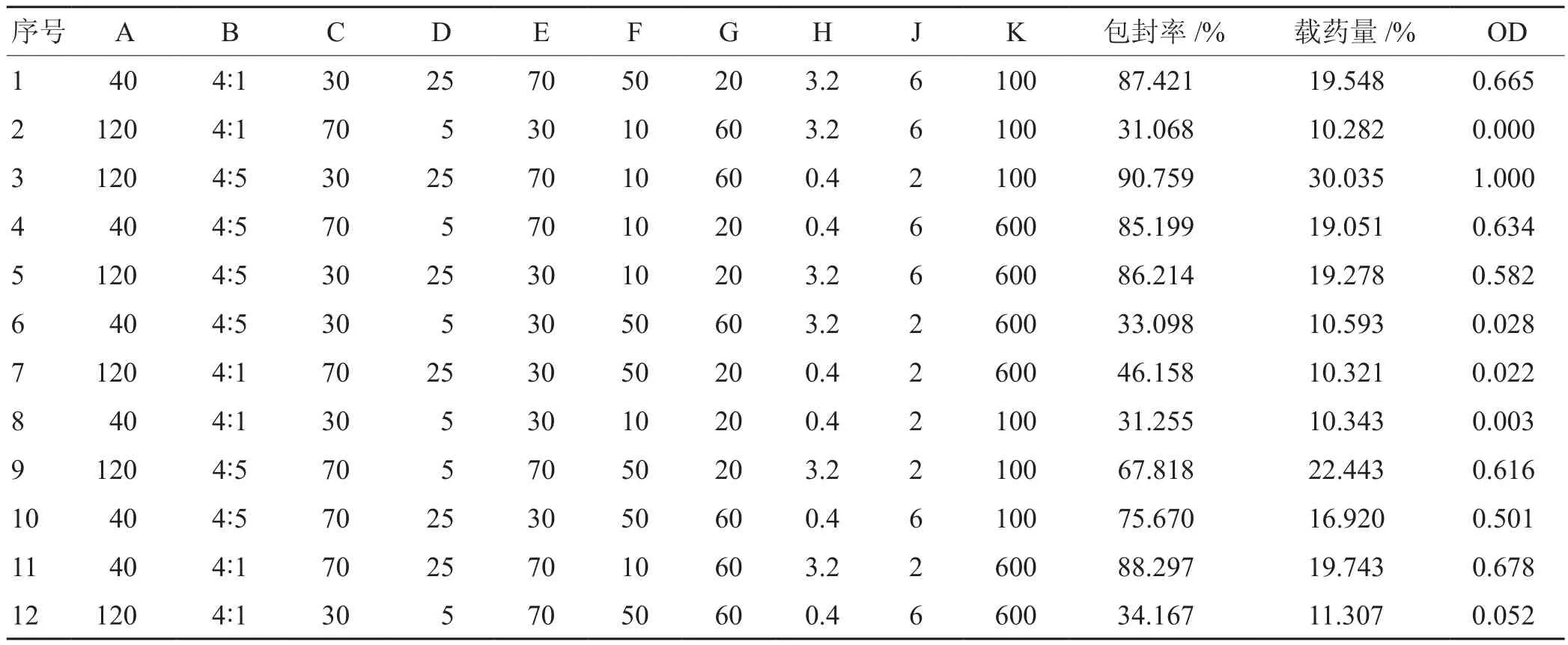
表14 Plackett-Burman试验结果
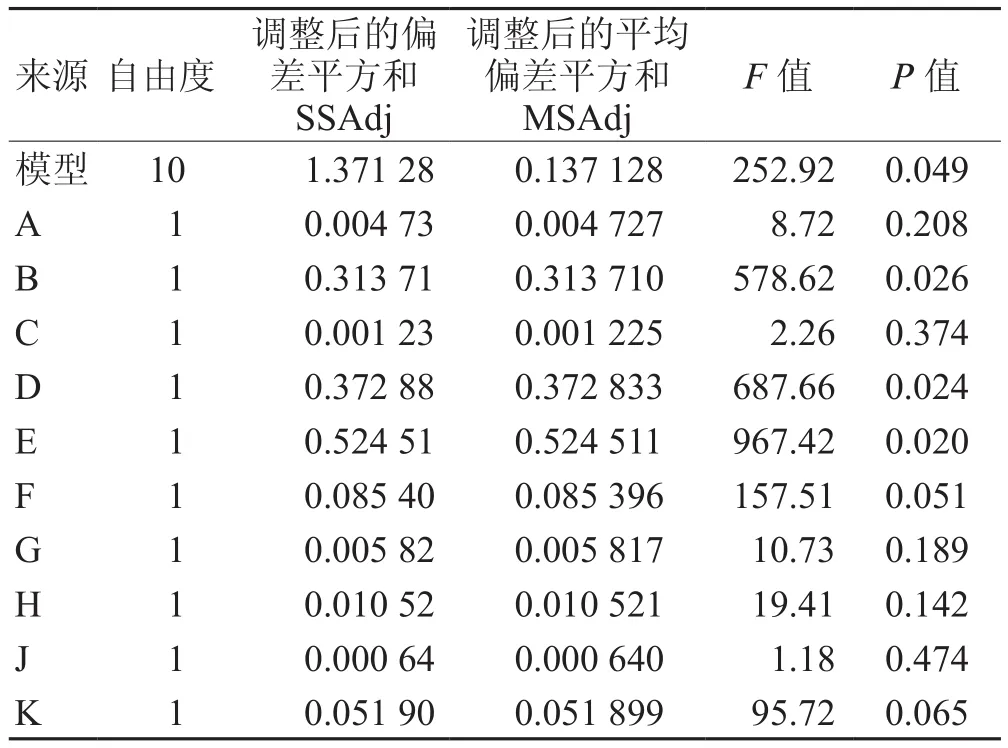
表15 Plackett-Burman试验设计的显著性结果
2.5.2 Box-Behnken响应面法 应用 Design-Expert.V8.0.6.1软件设计表进行实验,本实验采用Box-Behnken响应面法,以表面活性剂比例(A)、黄体素用量(B)、水化温度(C)为考察因素,以OD值为响应值,对3个因素进行优化。
应用 Design-Expert.V8.0.6.1对表17进行分析,结果见表18,以OD值对各因素自变量进行模型拟合,通过拟合得到的二次回归方程为OD = 0.8582+0.0725A+0.0803B-0.0838C-0.0845AB-0.0875AC-0.0265BC-0.1914A2-0.1474B2-0.0983C2(R2=0.9393,失拟度检验F值为1.45,P= 0.3537>0.05),由拟合方程结果可知拟合模型F值为12.04(P<0.05),说明拟合模型拟合度高,失拟项 F值较小为1.45(P=0.353 7>0.05),表明失拟项不显著,该拟合模型拟合结果良好,可用于实验结果分析。信噪比值为10.70,相对较高,证明该模型可用于实验结果分析。
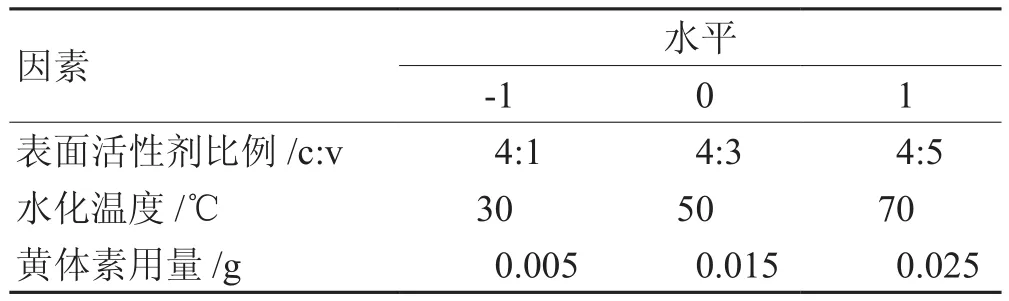
表16 Box-Behnken试验因素及水平
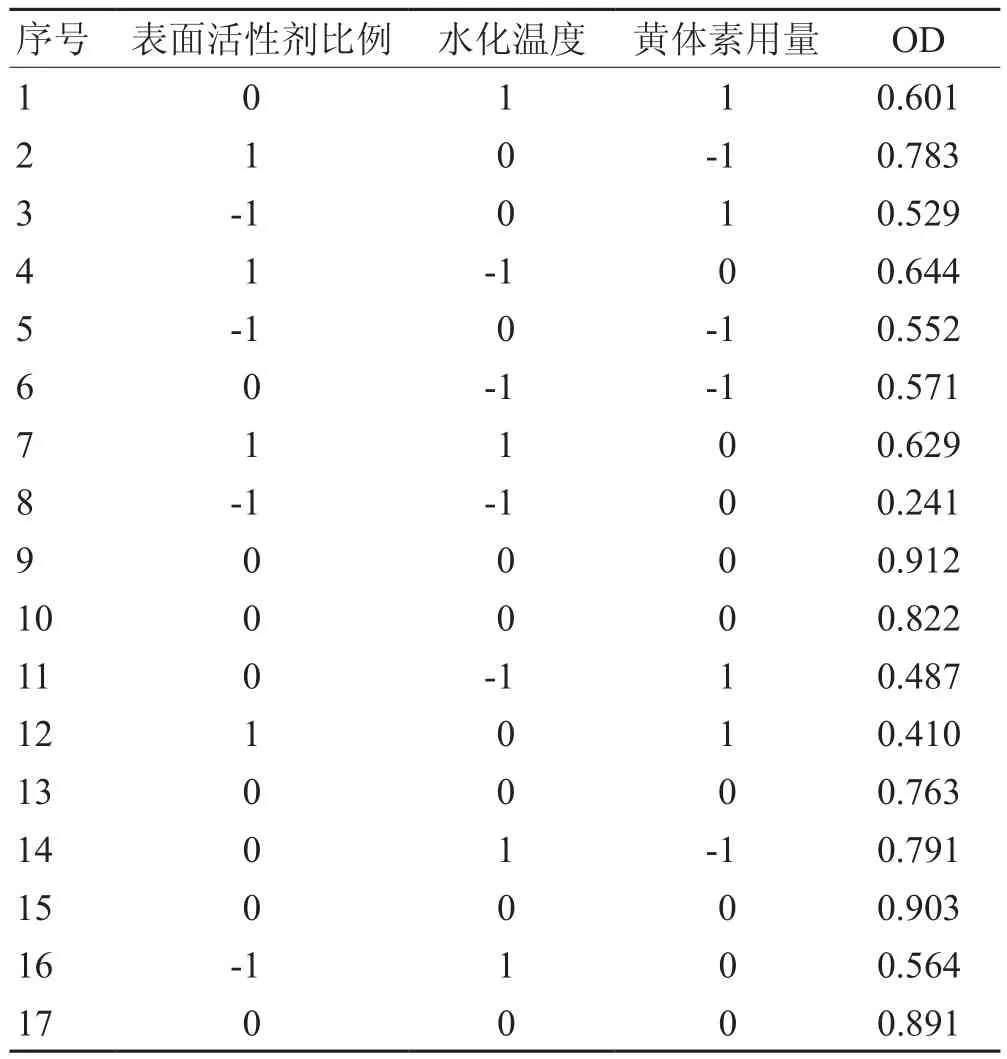
表17 Box-Behnken实验设计与结果
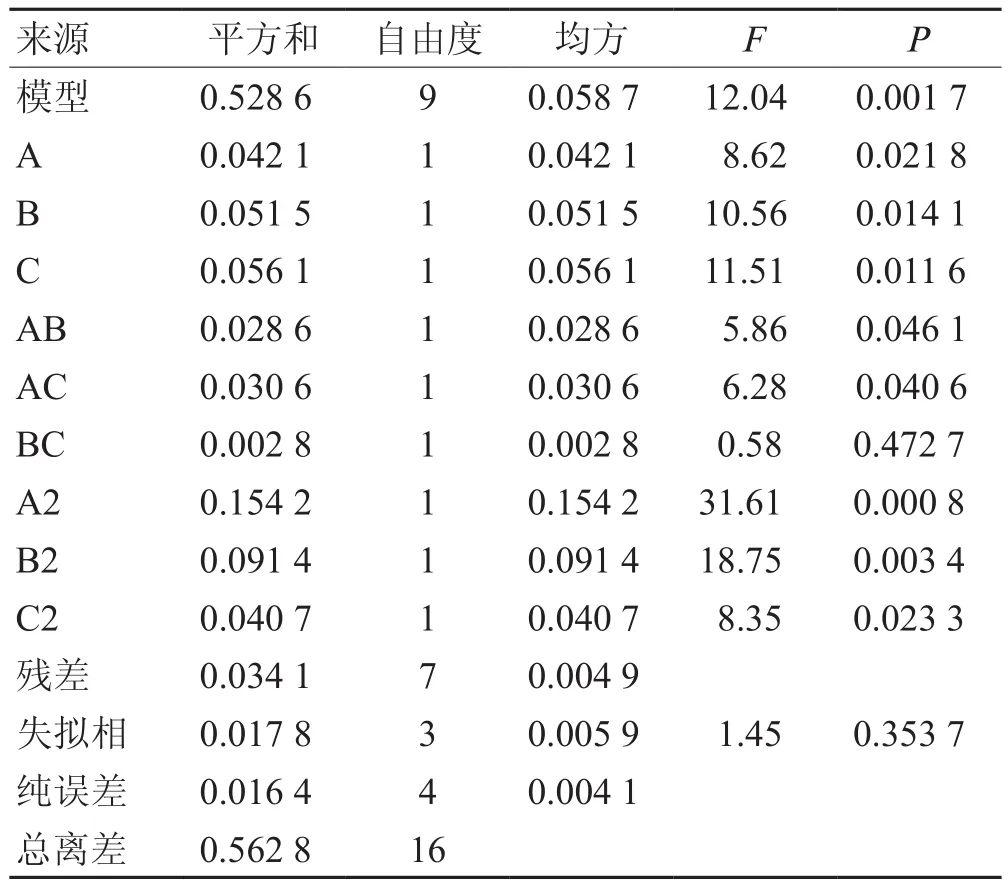
表18 Box-Behnken实验设计方差分析结果
根据二次回归方程拟合结果,将一个因素固定,进行OD对其他两个因素的拟合,可得到实验结果的等高线与三维效应曲面图对黄体素类脂质体工艺参数的优选。处方优化结果为:表面活性剂比例为0.703:1,叶黄素用量为15.4 mg,水化温度为32 ℃。见图5、图6。
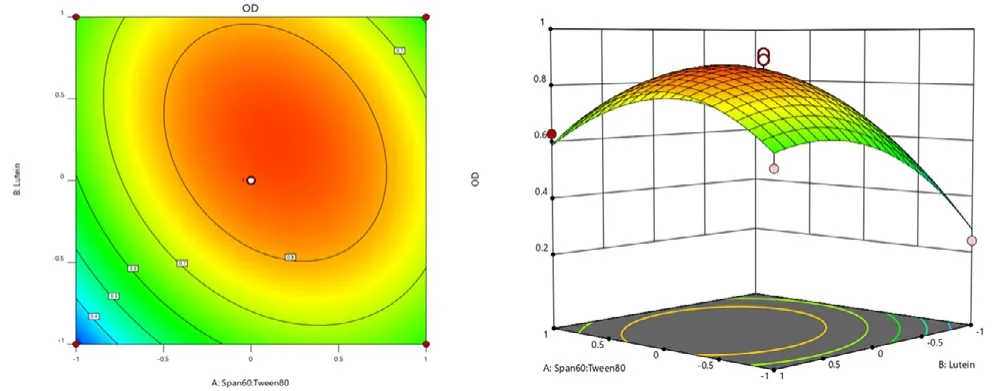
图5 因素A及因素B对综合评分OD的等高线图和三维响应图

图6 因素A及因素C对综合评分OD的等高线图和三维响应图
2.5.3 工艺验证 根据响应面实验结果的最佳工艺,即表面活性剂比例为0.703:1,叶黄素用量为15.4 mg,水化温度为32 ℃,预测OD值为0.81,进行验证。结果表明3批黄体素类脂质体的平均包封率为(75.283±0.22)%,平均载药量为(38.512±0.21)%,平均OD值为0.794。证明黄体素类脂质体最佳制备工艺稳定可行。
3 讨论
实验发现黄体素受外界因素影响较大,导致药物快速分解。在单因素实验、PBD实验、BBD实验中,过高的温度使水相蒸发速率加快,从而影响包封率与载药量的测定,故本实验制备类脂质体时,将反应容器半封口,以减少水相的流失。
类脂质体的材料主要由非离子表面活性剂和胆固醇组成,二者在水合介质中形成的双分子层包括了亲水部分和亲脂部分,由于黄体素亲脂性相对较好,因此在包合过程中,黄体素进入亲脂部分较多,而亲水部分几乎不含有黄体素,因此可利用亲水腔作后续的创新。
本研究运用质量源于设计理念,对影响黄体素类脂质体制备因素进行剖析,结合 PBD及BBD,优化黄体素类脂质体的制备工艺。传统的正交实验设计利用线性数学模型,分析出多个因素水平的最佳组合;但正交设计只能分析离散型数据,其科学性及预测性较差。PBD联合BBD,采取线性模型得到回归方程,通过合理预测得出最佳工艺条件更具有科学性。
