低温室颤性停搏在胸腔镜辅助下再次二尖瓣置换术中的应用
2022-03-12王树伟崔勇周冰梅富杨刘志芳胡志斌
王树伟,崔勇,周冰,梅富杨,刘志芳,胡志斌
浙江省人民医院 心脏大血管外科,浙江 杭州 310014
由于瓣膜手术的广泛开展,特别是生物瓣膜置换手术的广泛应用,因机械瓣膜功能失灵、生物瓣膜衰败等原因导致的再次手术的病例增多。传统正中开胸再次手术需要广泛分离纵膈粘连组织,导致手术操作相对困难,严重并发症的发生率和病死率也较高[1]。胸腔镜辅助下微创二尖瓣置换术已经逐渐成为二尖瓣病变的重要手术方式[2]。由于心包粘连,升主动脉阻断困难等原因,胸腔镜下经胸再次二尖瓣置换术的应用受到一定限制,其治疗效果也远未阐明。浙江省人民医院应用低温诱导室颤性停搏(hypothermic fibrillatory arrest,HFA)技术在胸腔镜辅助下经右胸微创切口行再次二尖瓣置换术,取得满意的近期效果,现报告如下。
1 资料和方法
1.1 一般资料 选取2017年10月至2019年12月在浙江省人民医院接受二尖瓣置换手术(或同期三尖瓣成形术)共207例患者。排除标准:①既往曾接受冠状动脉搭桥手术;②接受正中开胸术;③需同期行射频消融、冠脉搭桥术或主动脉瓣置换术;④术前合并严重肝肾功能不全、感染或恶性肿瘤者。根据纳入和排除标准进行筛选。共有113例接受胸腔镜辅助下二尖瓣置换术(或同期三尖瓣成形术)患者最终被纳入本研究。其中35 例患者既往曾接受心脏手术(previous cardiac surgery,PCS),作为PCS组;其余78例患者接受首次心脏手术(first cardiac surgery,FCS),作为对照组。
2组患者均接受胸腔镜辅助下腋下小切口入路,经左心房切口行二尖瓣置换术(或同期经右心房切口三尖瓣成形术)。PCS组使用中低温(26~28 ℃)诱导室颤性停搏技术,对照组常规使用升主动脉阻断,并经主动脉根部灌注心脏停跳液,于左心房切口手术。
1.2 手术方法 2组患者均采用双腔气管内插管,静吸复合麻醉,体表粘贴除颤电极片。患者取仰卧位,右侧肩背部垫高约30°。所有患者麻醉后置入经食道超声探头,以评估心脏和瓣膜的整体功能。选择右侧腋前线垂直切口并经第四肋间进胸,于右侧腋前线第3 肋间置入电视胸腔镜导鞘和胸腔镜,经导鞘连接二氧化碳导管充填胸腔[3]。经股动、静脉插管建立体外循环,体外循环辅助后即开始缓慢全身降温。PCS组患者:游离胸腔内粘连组织,观察心包外观并判断右侧膈神经位置。于膈神经前方 2 cm处切开心包,仔细游离心包与右心房之间的粘连,显露右上肺静脉,向下游离并显露下腔静脉与右房连接处。患者鼻咽温降至26~30 ℃时出现室颤性停搏。在右肺静脉和房间沟之间行左心房切口并行左心引流。置入左房牵拉器显露二尖瓣口。在体外循环期间,血压保持在70~80 mmHg (1 mmHg=0.133 kPa)。使用4-0 prolene线缝闭左心耳后,剪除原二尖瓣成形环或人工瓣膜,根据患者瓣叶病变情况,选择切除或保留部分二尖瓣瓣叶组织,应用间断褥式缝合法置换人工瓣膜。将患者体位左倾,在左心房缝闭前充分排除左心气体,并将左心引流管通过二尖瓣口置入左心室,在复温过程中持续引流排气。平行右房室沟切开右心房,应用人工成形环行改良三尖瓣成形术[4]。复温至鼻咽温32~34 ℃后心脏自动复跳,或经体表除颤后复跳。患者循环稳定后停止体外循环辅助。对照组患者常规使用升主动脉阻断,并经主动脉根部灌注心脏停跳液后完成手术,心内操作完成后经灌注管行左心排气。2组患者完成手术后均应用经食道心脏超声检查,判断左心排气效果,进一步明确人工瓣膜功能状态和三尖瓣成形效果。患者术后至少接受一次出院前经胸超声心动图和心电图检查。
1.3 随访方式 患者分别于手术后1个月、6个月来院复查。通过询问病史、活动能力和心功能不全等情况,并完成心电图、经胸心脏超声等辅助检查。
1.4 统计学处理方法 采用SPSS17.0软件进行统计分析。计量资料以表示,2组间比较采用t检验。计数资料采用例数(百分比)表示,组间比较采用Pearson χ2检验或Fisher精确检验。P<0.05为差异有统计学意义。
2 结果
2.1 术前资料 2组患者在年龄、性别、三尖瓣病变、合并疾病和左心室射血分数(left ventricle ejection fraction,LVEF)等术前指标方面差异均无统计学意义(均P>0.05),见表1。PCS组患者距离上次心脏手术中位时间为8.4(5.5~25.5)年。
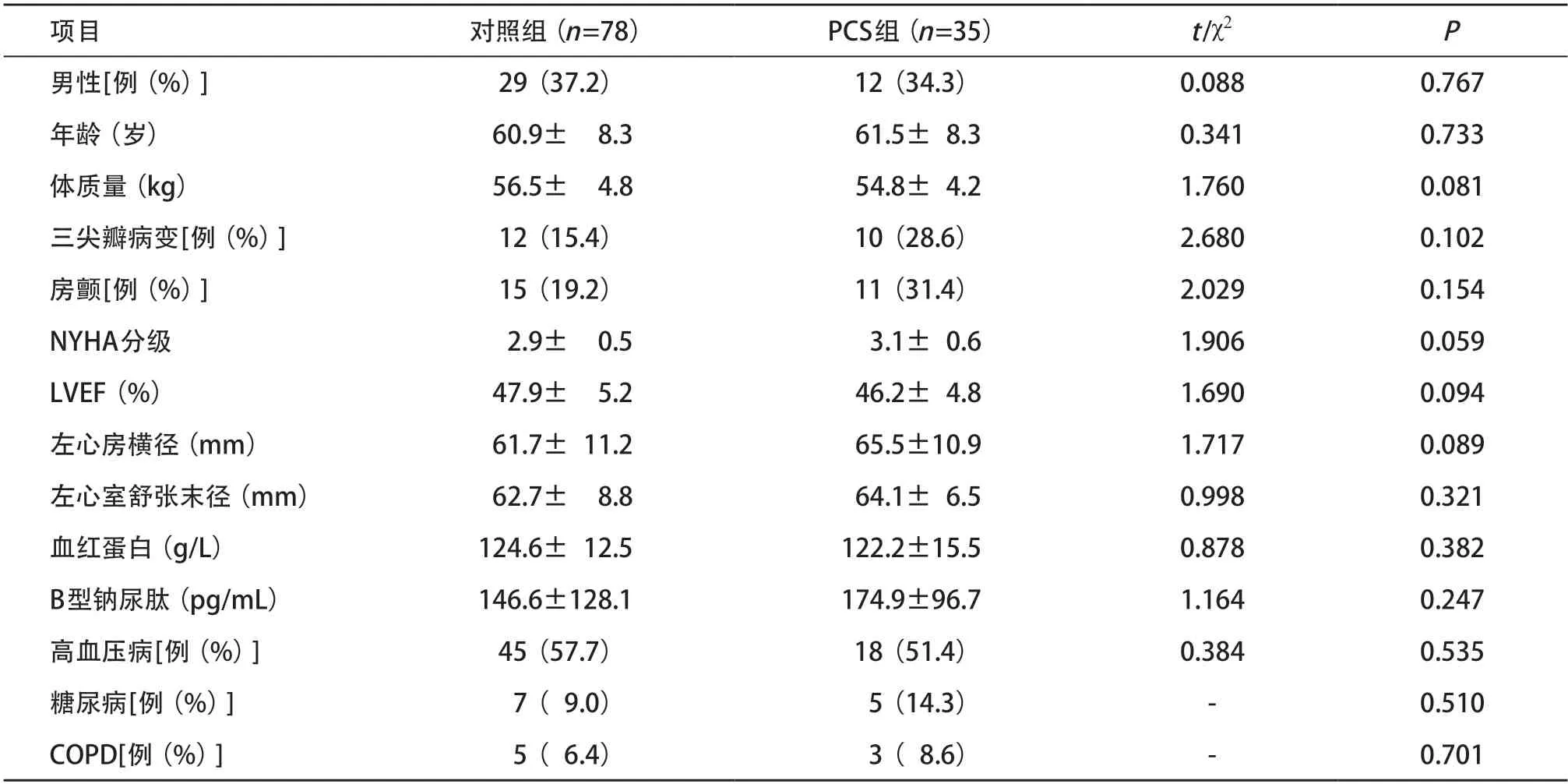
表1 2组患者术前一般临床资料比较
2.2 术中和围术期结果 与对照组相比,PCS组手术时间和体外循环时间延长。两组患者术后24 h引流液量和围术期输血率差异无统计学意义(均P>0.05)。术后心肌肌钙蛋白I(cardiac troponin I,cTnI)峰值和血气乳酸峰值指标差异无统计学意义(均P>0.05)。全组无中转正中开胸患者。术后呼吸机辅助时间、重症监护室(intensive care unit,ICU)停留时间和术后住院时间两组间差异无统计学意义(均P>0.05)。见表2。

表2 2组患者术中及围手术期临床资料比较
所有患者术后均未发生严重神经系统和呼吸系统并发症。全组共11例(PCS组8例,对照组3例)患者术中发现右侧胸腔内粘连,其中PCS组1例患者术后复查CT提示右侧少量气胸,未行穿刺排气,于术后1个月复查胸部CT提示气胸完全吸收。全组共8 例患者出现术后谵妄症状,2组发生比例差异无统计学意义[2例(5.7%)vs.6例(7.7%),P>0.05],经对症治疗,谵妄症状均消失。出院前头颅CT检查均未发现明确出血或新发梗死征象。
2.3 随访结果 所有患者完成术后6个月随访,两组均无心因性死亡或心功能衰竭再次住院者。全组共3例患者术后腋下切口因脂肪液化导致愈合不良,给予换药处理后愈合良好。术后6个月随访时,心功能分级及左心室射血分数指标两组间差异无统计学意义(均P>0.05)。见表3。

表3 两组患者术后6个月随访资料比较
3 讨论
有研究提示,再次心脏瓣膜手术明显增加围手术期风险[5-6]。微创MitraClip技术在二尖瓣和三尖瓣病变患者中的临床应用,使得部分患者获得了优良的治疗效果[7-9]。但是由于该技术本身适应证的限制,多数瓣膜病患者再次开胸接受手术治疗或不可避免。由于纵膈粘连,常规正中开胸再次心脏手术有直接损伤右心室并发大出血的潜在风险,术中需要广泛的心脏和大血管表面组织的游离,从而增加了手术难度和心脏与大血管出血风险。由于经胸途径二尖瓣修复或置换避免了胸骨再次劈开所致的心脏损伤等风险,且不需要进行广泛的心脏和大血管表面的游离等操作,成为具有重要潜在优势的手术方式[10]。
随着微创技术在临床的广泛应用,胸腔镜技术已经被安全地应用于二尖瓣病变的外科治疗[2]。与传统正中开胸手术相比,胸腔镜下首次二尖瓣置换手术可获得理想的临床效果[11-13]。随着腔镜技术的逐渐成熟,胸腔镜辅助下手术逐渐被应用到再次心脏手术领域。多组研究已证明了微创经胸途径再次二尖瓣手术的有效性和安全性[14-16]。本研究中,PCS组患者均采用经胸途径行再次二尖瓣置换术,术中仅需游离心包与右心房之间的粘连,明显简化了手术操作。PCS组患者围术期输血率与对照组相比差异无统计学意义,两组均无再次开胸止血患者。需要注意的是,与对照组相比,PCS组患者术后24 h引流量有增多趋势(P=0.056),这可能与PCS组患者需要进行更多的胸腔或心包内粘连的分离操作有关。虽然术中遇到的右侧胸腔或心包内粘连通常可以利用直视或胸腔镜辅助下顺利分离,但是由于部分患者胸膜腔或心包粘连致密,游离过程中应尽量避免不必要的分离以减少术后出血。分离胸腔粘连过程中应注意肺组织的保护,必要时应及时修补脏层胸膜,防止术后出血及气胸等并发症。
HFA技术较早应用于冠状动脉旁路移植术 中[17]。动物实验研究显示HFA技术对心肌细胞具有良好的保护效果[18]。相关研究结果为微创手术应用于再次心脏瓣膜手术提供了重要借鉴。随着HFA技术逐渐应用于多种类型微创心脏手术,其可行性得到初步验证[19-21]。本研究中,PCS组35例患者采用HFA技术,均顺利完成手术,由于术中避免了升主动脉游离和阻断,可明显简化手术操作。相关研究表明:低温诱导室颤120 min时心肌细胞可出现一定程度的损害[18]。本研究中,PCS组围术期心肌肌钙蛋白I及术后血气乳酸峰值指标与对照组相比虽差异无统计学意义,但仍有升高趋势,提示术中应尽量减少低温室颤的时间,防止心肌损伤导致的相关并发症。本研究中,PCS组患者在经股动、静脉插管体外循环辅助后即开始降温,并根据患者胸腔和心包内粘连的实际情况,控制适当的降温速度,尽可能在心脏出现低温室颤之前完成左心房切口显露的操作。在心脏室颤性停搏后即开始左心房切开和后续手术操作,从而最大限度减少低温室颤的时间。
由于术中未阻断升主动脉,为了防止气栓所致脑卒中等并发症,左心系统的充分排气是HFA技术应用的关键环节。本研究中,PCS组术中防止气栓的要点包括:开胸后即于胸腔内持续充入二氧化碳气体;体外循环过程中维持灌注压力在70~80 mmHg, 以保持主动脉瓣良好的关闭状态;术中应用器械牵拉左心房并显露二尖瓣瓣口时应注意动作轻柔,防止主动脉瓣变形导致血液返流或气体进入主动脉;在关闭左心房之前,可将手术床左倾,使左心室充满血液,并将左心引流管通过二尖瓣口置入左心室,在复温并等待心脏复跳之前适当引流,进一步排空左心气体。通过上述措施,PCS组患者心脏复跳后经食道超声均未发现明显左心残余气体存在。PCS组术后共有2例患者出现谵妄症状,与对照组相比差异无统计学意义。所有患者在术后随访过程中均未发现神经系统异常表现。
两组患者术后主要临床指标如术后ICU时间、呼吸机辅助时间、术后住院时间等差异均无统计学意义。术后6个月随访时,两组均无心因性死亡或心功能衰竭再次住院者,心功能分级和左心室射血分数指标两组间差异无统计学意义。研究结果提示应用HFA技术进行胸腔镜辅助下再次二尖瓣置换具有较好的安全性和可行性,与胸腔镜辅助下首次二尖瓣置换术具有相似的近期手术效果。
总之,应用HFA技术在胸腔镜辅助下经胸途径行再次二尖瓣置换手术能够避免胸骨劈开所致的心脏损伤等风险,可明显简化手术操作,并获得良好的心肌保护效果,具有较好的安全性和有效性。由于术中避免了升主动脉的游离和阻断,该技术尤其适用于升主动脉明显钙化或其他不适宜行术中主动脉阻断的患者。
