肌少症在维持性血液透析患者中的发生率及其相关危险因素分析
2022-03-08周加军高潮清
刘 勇,周加军,高潮清
(皖南医学院第一附属医院 弋矶山医院 血液净化中心,安徽 芜湖 241001)
肌少症是指全身肌肉质量及肌肉力量的逐渐丢失,且随着机体年龄增长而表现出的一种身体机能的衰退,多发生于老年人[1]。维持性血液透析患者在长期的血液透析治疗过程中,会产生营养物质丢失、慢性微炎症状态等不良因素,因此相较于健康人群,其肌少症发生情况更加显著。此外肌少症能明显增加血液透析患者不良事件的发生,包括跌倒、骨折、心血管事件及全因死亡[2]。所以肌少症的早期识别及干预可延长透析患者的生命,改善其生活质量。
国外研究发现肌少症的危险因素包括营养不良、慢性疾病、炎症状态[3]。而这些危险因素均与血液透析患者密切相关。但国外研究对肌少症的诊断多采用欧洲老年肌少症工作组的诊断标准,为更符合中国患者的实际情况,本研究采用2019年亚洲肌少症工作组所制定的诊断标准来分析肌少症在维持性血液透析患者中的发生情况及其可能的危险因素。
1 资料与方法
1.1 研究对象 选取2020年7月1日~12月31日在弋矶山医院血液净化中心门诊行维持性血液透析治疗的100例患者为研究对象。纳入标准:①年龄≥18岁;②血液净化治疗时间≥6个月;③每周规律行血液净化治疗3次,每次治疗时间3.5~4 h;④6个月内至少行一次人体测量学检查及全面血液学检查。排除标准:①患有恶性肿瘤、肝病、结核、消化道溃疡或认知功能障碍;②6个月内曾患有急性感染或心、脑血管意外;③曾行甲状旁腺切除术;④无行动能力或双目失明等一般情况较差而无法行InBody检查。
1.2 研究方法
1.2.1 一般资料 收集并记录所有患者的年龄、性别、透析时间、原发病种类等一般资料。
1.2.2 实验室指标检测 所有患者的血常规、血生化、全段甲状旁腺激素(iPTH)等指标均为透析当日透析前空腹采集血样测得,同时记录6个月内的最近一次实验室指标。
1.2.3 人体测量学指标检测 使用人体成分分析仪InBody770检测并记录身高、体质量、体质量指数(BMI)、人体蛋白质含量(PM)、脂肪含量(FM)、体脂百分比(PBF)、去脂体质量(FFM)、四肢骨骼肌质量指数(ASMI)等指标。肌肉力量检测:使用握力器评估患者的肌肉力量。内瘘患者检测非内瘘手的握力,若为长期导管患者则用优势手检测握力。所有患者握力均检测2次,记录其平均值。身体活动能力检测:采用步行速度或5次起坐时间来评估患者的身体活动能力。所有患者步行6米或起坐5次,并用秒表记录其所用时间,检测2次,记录其平均值。
1.2.4 营养状况评估 使用改良定量主观评估表(modified quantitative subjective global assessment,MQSGA)对患者营养状况进行评估,包括病史、症状及体检、体征共7个项目。每项定量为1(无变化)~5分(非常严重),总分为7~35分,总分越高表明营养状况越差。中重度营养不良为18~35分,轻度营养不良为11~17分,正常营养≤10分。
1.2.5 肌少症诊断标准 采用2019年亚洲肌少症工作组制定的诊断标准,包括ASMI、肌肉力量、身体活动能力[4]。

2 结果
2.1 维持性血液透析患者肌少症发生情况 纳入的100例维持性血液透析患者中24例被诊断为肌少症(24.00%)。进一步将研究对象按年龄分为≥60岁组及<60岁组,≥60岁组有11例患者诊断为肌少症(35.48%),<60岁组有13例患者诊断为肌少症(18.84%)。
2.2 肌少症组与非肌少症组一般资料、人体测量学指标及营养评分比较 肌少症组患者MQSGA评分、年龄、透析时间较非肌少症组高(P<0.05),而BMI、PM、FFM较非肌少症组低(P<0.05)。见表1。
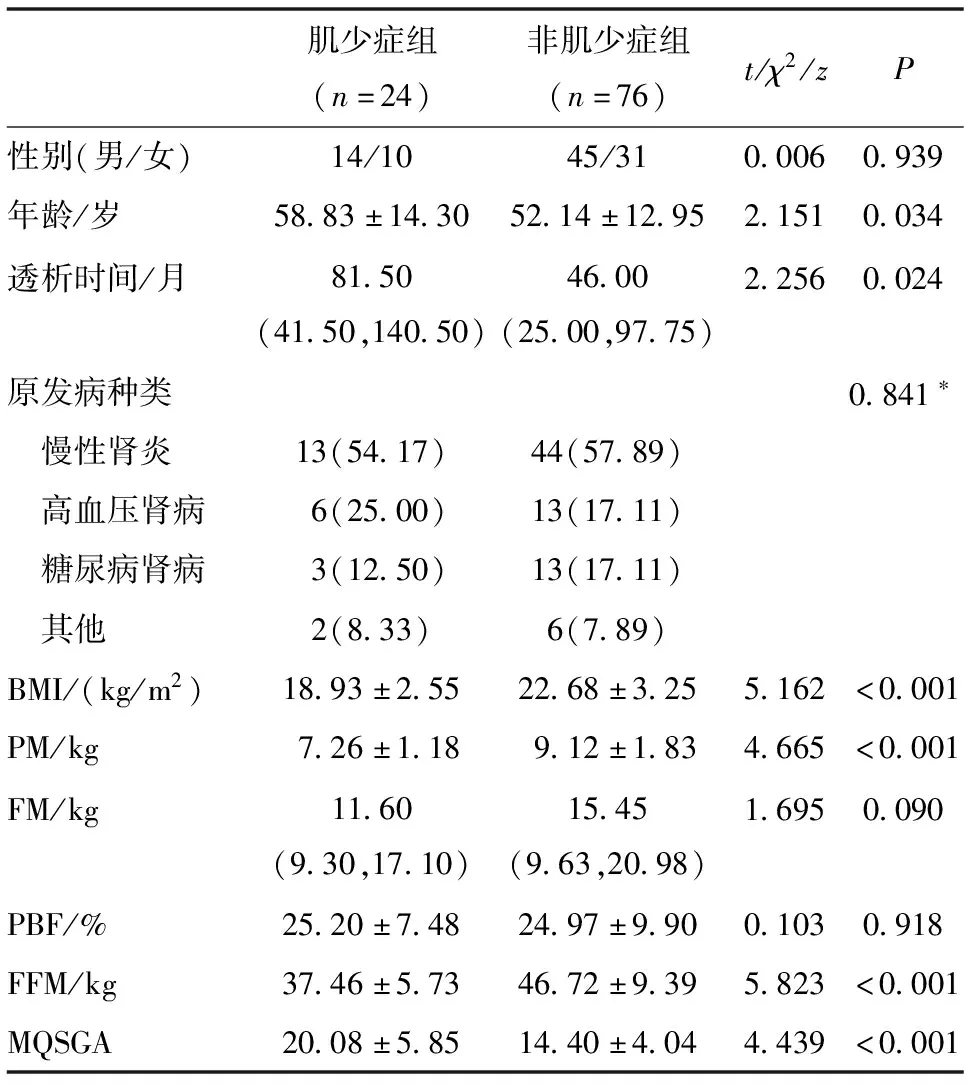
表1 两组患者一般资料、人体测量学指标及营养评分比较
2.3 肌少症组与非肌少症组实验室指标比较 肌少症组的超敏C反应蛋白(hs-CRP)较非肌少症组高(P<0.05),而血清白蛋白、血磷较非肌少症组低(P<0.05)。见表2。

表2 两组患者实验室指标比较
2.4 肌少症相关危险因素分析 根据单因素分析结果,按照P<0.10的标准,共有12个指标纳入多因素的二分类Logistic回归分析,其中MQSGA评分高、透析时间长、hs-CRP水平高是肌少症发生的独立危险因素(P<0.05);高血磷和高BMI是肌少症发生的保护因素(P<0.05)。见表3。

表3 肌少症发生的相关危险因素分析
3 讨论
亚洲流行病学研究发现,目前肌少症的发生率为5.50%~25.70%,而在维持性血液透析患者中,肌少症的发生率可能更高[5]。本研究发现,维持性血液透析患者肌少症发生率为24.00%。年龄<60岁的患者肌少症发生率为18.84%,年龄≥60岁的患者肌少症发生率为35.48%,与Ren等研究结果基本一致[6],表明高龄血液透析患者更易发生肌少症,但是慢性疾病、营养状况等也与肌少症的发生密切相关,因此<60岁的透析患者也有较高的肌少症发生率。
肌少症的发病机制目前尚不明确,可能是多因素共同作用结果,包括炎性因子活化、线粒体功能降低及体质量丢失等[7]。本研究中,营养状况差、透析时间长、hs-CRP高是肌少症发生的危险因素。Bataille等研究发现,肌肉量的丢失与BMI、去脂体质量、体脂肪量、血清白蛋白等营养指标密切相关[8]。当予以改善营养状况后,则可以有效治疗及预防肌少症的发生[9]。国内学者研究发现,透析时间越长,营养物质丢失越多,肌少症发生的风险也越高[10]。此外,高龄透析患者往往还伴随着激素失衡、ATP丢失、生活方式改变等,这些都会诱发肌少症的发生,并增加致残率和病死率[6]。
高磷血症是血液透析患者常见的慢性并发症之一,与血管钙化、皮肤瘙痒、心血管死亡密切相关[11]。但本研究却发现血磷是肌少症发生的保护因素。我们推测这可能是由于高蛋白饮食是血磷的主要来源,当透析患者蛋白摄入不足,则会引发肌少症及低血磷。肾病型肠内营养制剂可以有效提高血液透析患者营养水平同时,不引起血磷水平升高,为透析患者改善营养状况开辟了新的途径[12]。
有研究表明,以CRP及炎症因子水平增高为特征的炎症状态可以抑制食欲,促进蛋白质和脂肪的分解代谢以及能量的消耗,最终对患者的营养状况产生负面影响。同时炎症状态又会刺激泛素-蛋白酶体途径的活化,诱导线粒体动力学的改变,限制肌肉的修复和再生,这些机制都可能促进肌肉量的减少及肌肉功能的萎缩[13]。一项涉及16个临床研究的Meta分析表明,3 072例肌少症患者与8 177例非肌少症患者相比,肌少症患者的CRP水平会更高[14],而这个结果在血液透析患者中可能会更明显。因为血液透析患者常伴有慢性微炎症状态。本研究结果也表明,肌少症组的CRP水平更高,炎症状态是肌少症发生的独立危险因素。
综上所述,肌少症在维持性血液透析患者中有较高的发生率,尤其是老年透析患者中的发生率可能更高。营养状况、透析时间、炎症状态均是其独立危险因素。因此临床医师在实践工作中应该充分认识肌少症,尽早针对危险因素采取干预措施。
