雾化吸入不同给药剂量布地奈德与静脉用甲泼尼龙治疗AECOPD 疗效与安全性的Meta 分析
2022-02-22陈丽金王若伦李秋雯冯霞
陈丽金,王若伦,李秋雯,冯霞
广州医科大学附属第二医院,广东 广州 510260
慢性阻塞性肺疾病急性加重期(acute exacerbation of chronic obstructive pulmonary disease,AECOPD)患者常表现为局部气道炎症加重,国内外指南推荐[1-2]其药物治疗宜在应用支气管扩张剂的基础上加用全身用糖皮质激素(口服/静脉),以改善患者1 s 用力呼气量(FEV1)、氧合状态及缩短康复和住院时间;国内相关专家共识[3-5]则在指南的基础上进一步提出吸入性糖皮质激素(inhaled corticosteroid,ICS)如布地奈德可替代或部分替代全身用糖皮质激素。据调查,我国AECOPD 患者雾化激素使用率达78.51%,其中雾化吸入布地奈德的给药日剂量为(3.5±1.69)mg[6];而相关文献[7-8]报道,雾化吸入布地奈德6~8 mg 与注射用甲泼尼龙40 mg/d 疗效相当。可见,目前国内雾化吸入布地奈德的具体给药剂量尚不明确,且不同给药剂量治疗AECOPD 缺乏循证药学证据。本研究旨在通过循证药学方法,分亚组并进一步做敏感性分析以充分评估雾化吸入不同给药剂量布地奈德与注射用甲泼尼龙对比治疗AECOPD 患者的动脉血气、肺功能及不良反应发生率等,以供临床用药参考。
1 资料与方法
1.1 纳入标准
(1)研究类型。随机对照试验(Randomized controlled trials,RCTs),按随机数字表或抽签取样法分组,不论是否采用分配隐藏或盲法。不限研究地域,语种仅设定为中文和英文。(2)研究对象。符合《慢性阻塞性肺疾病诊治指南(2021 年修订版)》中AECOPD 诊断标准的患者,实验人群年龄≥18岁,且试验组与对照组患者在基本生理状态上无明显差异。不限患者来源。(3)干预措施。试验组为雾化吸入布地奈德,按给药剂量不同分为低剂量组(≤4 mg)和高剂量组(6~8 mg),对照组为注射用甲泼尼龙,剂量不限;两组药物疗程不限。(4)结局指标。主要观察指标为治疗后动脉血氧分压(PaO2)和动脉血二氧化碳分压(PaCO2),次要观察指标为1 s 用力呼气量(FEV1)、1 s 用力呼气量占用力肺活量的百分比[(FEV1/FVC)%]和药品不良反应(ADR)发生情况。
1.2 排除标准
(1)非RCT 研究如文摘、综述、病例报告及重复发表等;(2)诊断非AECOPD 患者;(3)试验组和对照组各研究病例数少于20 例;(4)布地奈德给药途径非雾化吸入;(5)试验组和对照组常规基础治疗及疗程不一致;(6)观察指标无具体数据或<2 种的文献;(7)硕士研究生毕业论文。
1.3 文献检索
以“慢性阻塞性肺疾病急性加重期、慢阻肺急性加重期、AECOPD、布地奈德、雾化吸入”等为检索词,检索中国知网、万方、维普及PubMed 等数据库,并手工检索中、英文相关的会议论文集和灰色文献。检索时间范围均从各数据库建库至2021年12 月31 日。
1.4 文献筛选和资料提取
按照预先制定的数据提取表(纳入研究的基本特征,包括作者、发表时间、人数、剂量,结局指标均数及其标准差等),由两名评价员独立阅读文题和摘要,在排除明显不符合纳入标准的试验后,对可能符合纳入标准的随机对照试验阅读全文,以确定是否真正纳入,而后交叉核对纳入试验的结果,如有分歧则通过讨论解决或由第三名评价者决定是否纳入。
1.5 质量评价
参照Cochrane Handbook 6.2 推荐使用的偏倚风险评估工具的偏倚风险评价标准[9],对纳入文献的随机序列产生、隐藏分配、盲法、结果数据的完整性、选择性报告研究结果等进行评价,每项内容评价结果分为低风险(low risk)、不确定风险(unclear risk)和高风险(high risk)三个级别,最终以偏倚风险图(risk of bias graph)表示。两名评价者交叉核对纳入试验的质量评价结果,对有分歧而难以确定的则通过讨论或由第三名评价者协助解决。
1.6 统计学方法
采用Cochrane 协作网提供的RewMan5.3 软件进行Meta 分析。疗效指标为数值变量,采用均数差(mean difference,MD)为合并统计量,不良反应发生率为二分类变量,采用比值比(odds ratio,OR)为合并统计量;各效应量以95%CI表示,P<0.05 为差异有统计学意义。各纳入研究结果间的异质性采用X2检验或用I2来衡量。当各研究间同质性较好时(P>0.10,I2<50%),采用固定效应模型进行合并分析;若各研究间存在统计学异质性(P<0.10,I2>50%),则分析导致异质性的原因,同时选择随机效应模型进行合并分析。若临床试验提供的数据不能进行Meta 分析,则只对其进行描述性分析。
2 结果
2.1 文献检索结果及纳入研究的基本特征
共纳入12 篇RCTs,筛选流程及结果见图1。低剂量组5 篇[10-14],共411 例患者,基本特征见表1;高剂量组7 篇[15-21],共458 例患者,基本特征见表2。
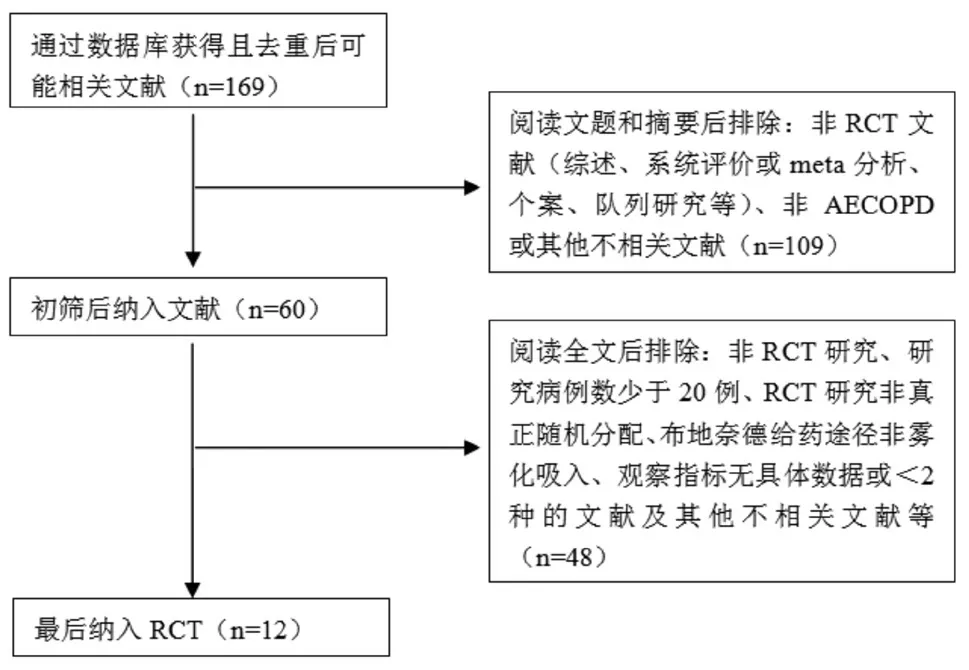
图1 雾化吸入不同给药剂量布地奈德与静脉用甲泼尼龙治疗AECOPD文献筛选流程
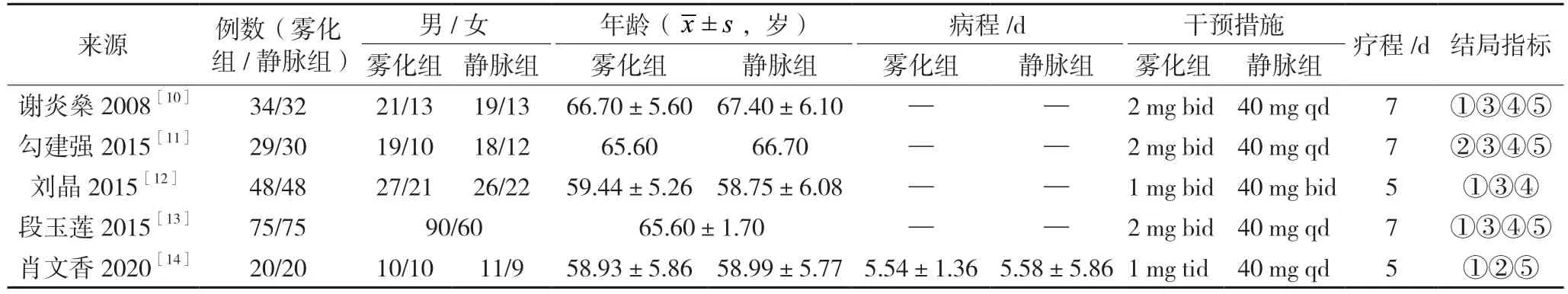
表1 雾化吸入布地奈德低剂量组(≤4 mg)与静脉用甲泼尼龙治疗AECOPD纳入文献的基本特征
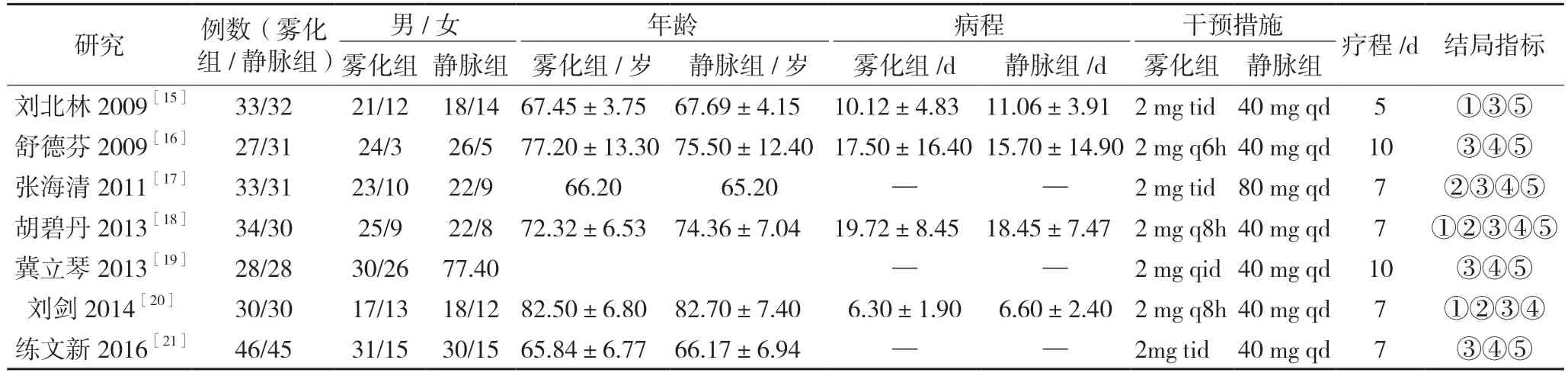
表2 雾化吸入布地奈德高剂量组(6~8 mg)与静脉用甲泼尼龙治疗AECOPD纳入文献的基本特征
2.2 纳入研究的方法学质量评价
纳入的12 篇文献均提及使用随机数字表或抽签取样法分组,有1 篇文献提及分配隐藏情况。各纳入研究的方法学质量评价见表3。
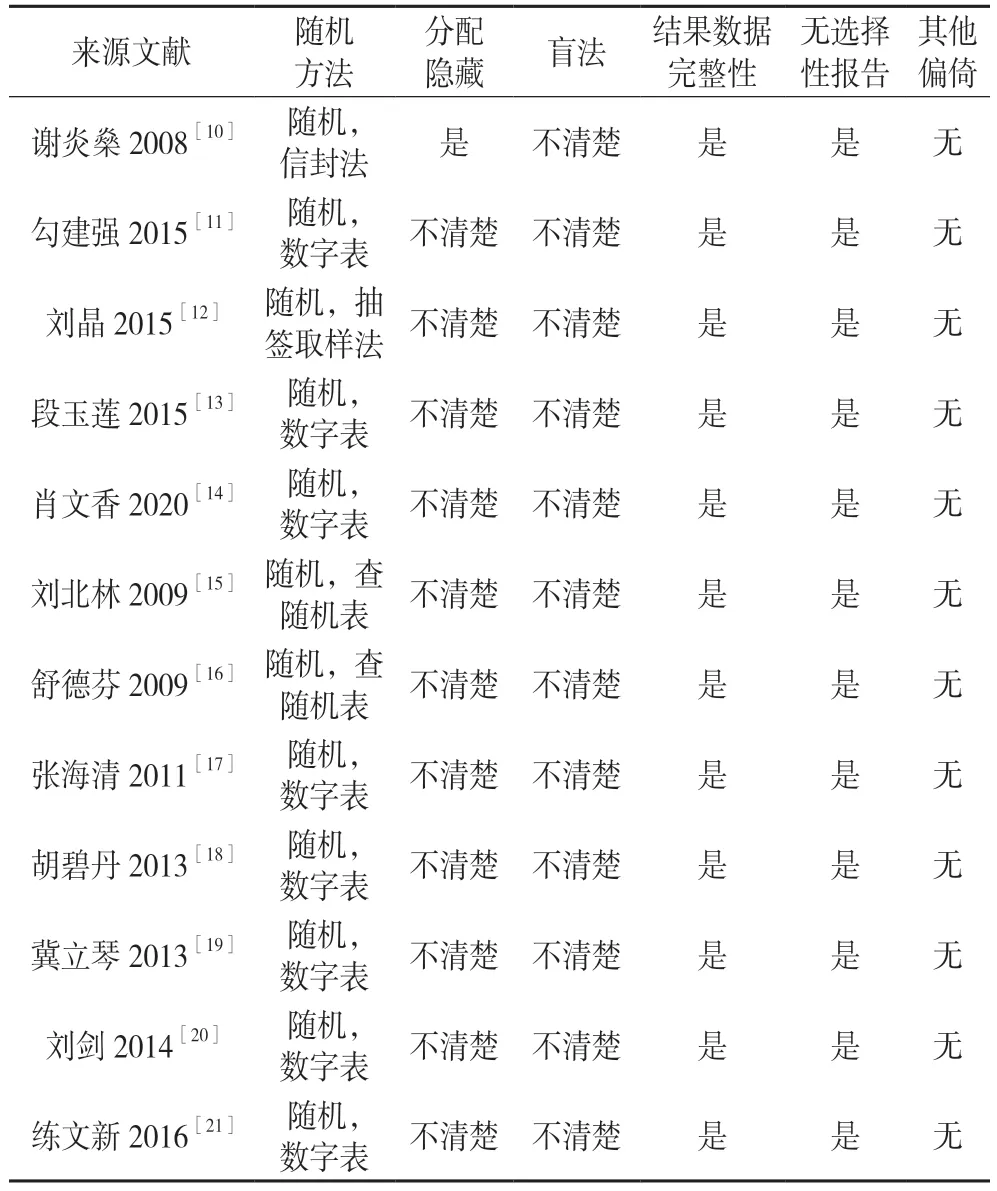
表3 各纳入研究的方法学质量评价
2.3 Meta 分析结果
2.3.1 主要观察指标PaO2共11 篇研究比较雾化组与静脉组治疗后PaO2水平,各纳入研究间存在统计学异质性(I2=96%),采用随机效应模型进行Meta分析;结果显示,两组治疗后PaO2差异无统计学意义(见图2),提示两组治疗后PaO2水平相当。
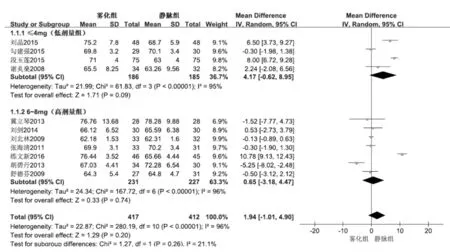
图2 AECOPD829例患者雾化组与静脉组激素治疗后PaO2的森林图
亚组分析结果显示,低剂量组和高剂量组各纳入研究间均存在统计学异质性(I2>50%),采用随机效应模型进行Meta 分析;结果显示,两个剂量组雾化组与静脉组治疗后PaO2均差异无统计学意义,提示两个剂量组雾化组与静脉组治疗后PaO2水平相当。
2.3.2 主要观察指标PaCO2共10 篇研究比较雾化组与静脉组治疗后PaCO2水平,各纳入研究间存在统计学异质性(I2=96%),采用随机效应模型进行Meta分析;结果显示,两组治疗后PaCO2差异无统计学意义(见图3),提示两组治疗后PaCO2水平相当。
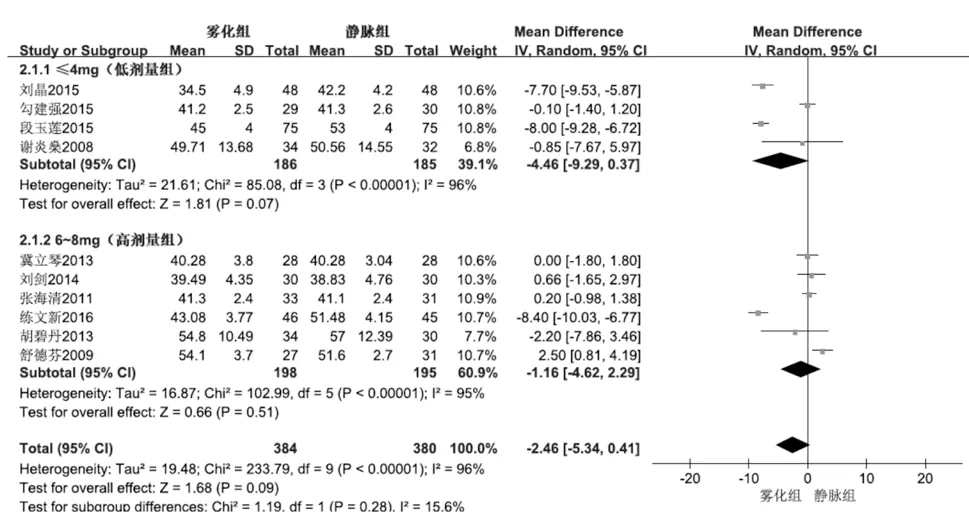
图3 AECOPD764例患者雾化组与静脉组激素治疗后PaCO2的森林图
亚组分析结果显示,低剂量组和高剂量组各纳入研究间均存在统计学异质性(I2>50%),采用随机效应模型进行Meta 分析;结果显示,两个剂量组雾化组与静脉组治疗后PaCO2均差异无统计学意义,提示两个剂量组雾化组与静脉组治疗后PaCO2水平相当。
2.3.3 次要观察指标FEV1共7 篇研究比较雾化组与静脉组治疗后FEV1水平,各纳入研究间存在统计学异质性(I2=95%),采用随机效应模型进行Meta分析;结果显示,两组治疗后FEV1差异无统计学意义(见图4),提示两组治疗后FEV1水平相当。
亚组分析结果显示,低剂量组各纳入研究间存在统计学异质性(I2=97%),采用随机效应模型进行Meta 分析;结果显示,两组治疗后FEV1差异无统计学意义(见图4 低剂量组)。高剂量组各纳入研究之间无统计学异质性(I2=15%),采用固定效应模型进行Meta 分析;结果显示,两组治疗后FEV1差异无统计学意义[MD=-0.03,95%CI(-0.11,0.04),P=0.40];提示两个剂量组雾化组与静脉组治疗后FEV1水平相当。
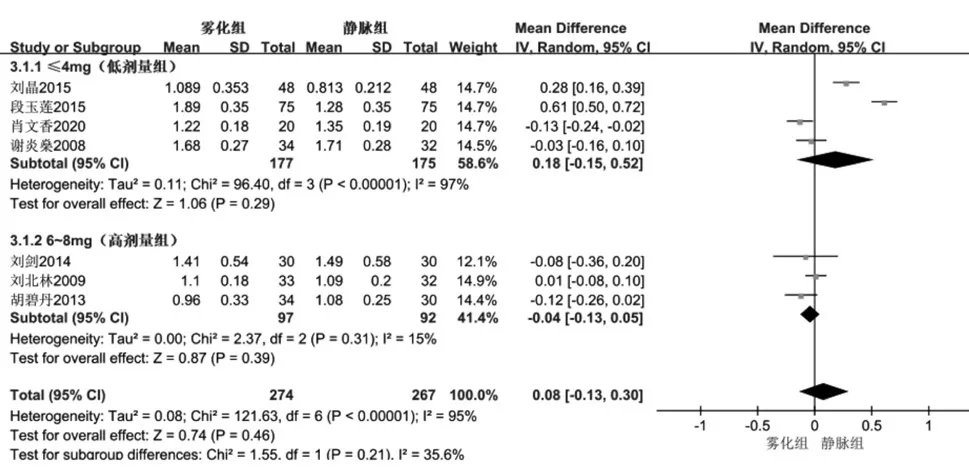
图4 AECOPD541例患者雾化组与静脉组激素治疗后FEV1的森林图
2.3.4 次要观察指标FEV1/FVC(%)共5 篇研究比较雾化组与静脉组治疗后FEV1/FVC(%)水平,各纳入研究间无统计学异质性(I2=36%),采用固定效应模型进行Meta 分析;结果显示,两组治疗后FEV1/FVC(%)差异有统计学意义(见图5),提示雾化组治疗后FEV1/FVC(%)水平优于静脉组。
亚组分析结果显示,低剂量组纳入的两个研究间存在统计学异质性(I2=83%),采用随机效应模型进行Meta 分析;结果显示,两组治疗后FEV1/FVC(%)差异无统计学意义[MD=-5.86,95%CI(-17.64,5.92),P=0.33],提示两组治疗后FEV1/FVC(%)水平相当。高剂量组各纳入研究间无统计学异质性(I2=0%),采用固定效应模型进行Meta 分析;结果显示,两组治疗后FEV1/FVC(%)差异有统计学意义(见图5 高剂量组),提示雾化组治疗后FEV1/FVC(%)水平优于静脉组。

图5 AECOPD 287例患者雾化组与静脉组激素治疗后FEV1/FVC(%)的森林图
2.3.5 次要观察指标ADR共10 篇研究比较雾化组与静脉组治疗后ADR 发生情况,各纳入研究间无统计学异质性(I2=27%),采用固定效应模型进行Meta 分析;结果显示,两组治疗后ADR 差异有统计学意义(见图6),提示雾化组治疗后ADR发生率低于静脉组。
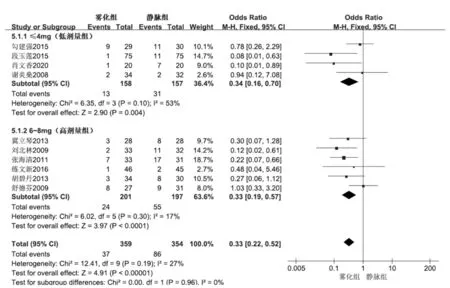
图6 AECOPD713例患者雾化组与静脉组激素治疗后ADR的森林图
2.3.6 敏感性分析对主要观察指标PaO2和PaCO2、次要观察指标FEV1,Meta 分析显示各纳入研究间存在较明显的异质性,分别剔除影响PaO2(参考文献12-13,18,21)、PaCO2(参考文献12-13,21)和FEV1(参考文献12-13)结果较大的研究后做敏感性分析,各纳入研究间无统计学异质性(I2<50%),采用固定效应模型进行Meta 分析;结果显示,两组治疗后PaO2、PaCO2和FEV1均差异无统计学意义[PaO2:MD=-0.14,95%CI(-0.74,0.46),P=0.65;PaCO2:MD=0.45,95%CI(-0.22,1.12),P=0.19;FEV1:MD=-0.06,95%CI(-0.11,0.00),P=0.05],均与剔除数据前保持一致,提示结果稳定。
亚组分析显示,低剂量组中所有观察指标各纳入研究间均存在较明显异质性,分别剔除影响结果较大的研究(参考文献12-13)后做敏感性分析,各纳入研究间无统计学异质性(I2<50%),采用固定效应模型进行Meta 分析;结果显示,低剂量组中雾化组与静脉组治疗后PaO2、PaCO2、FEV1和ADR 均差异无统计学意义[PaO2:MD=0.04,95%CI(-1.53,1.60),P=0.96;PaCO2:MD=-0.13,95%CI(-1.40,1.15),P=0.85;FEV1:MD=-0.09,95%CI(-0.17,-0.00),P=0.05;ADR:OR=0.52,95%CI(0.23,1.17),P=0.11],均与剔除数据前保持一致,提示结果稳定;两组治疗后FEV1/FVC(%)仅纳入2 篇文献,剔除影响结果较大的研究(参考文献14)后无法做Meta分析,仅做描述性分析。
高剂量组中主要观察指标PaO2和PaCO2各纳入研究间存在较明显异质性,剔除影响结果较大的研究(参考文献18,21)后做敏感性分析,各纳入研究间无统计学异质性(I2<50%),采用固定效应模型进行Meta 分析;结果显示,高剂量组中雾化组与静脉组治疗后PaO2和PaCO2亦差异无统计学意义[PaO2:MD=-0.17,95%CI(-0.82,0.48),P=0.61;PaCO2:MD=0.67,95%CI(-0.12,1.46),P=0.10],与剔除数据前保持一致,提示结果稳定。
2.3.7 发表性偏倚分析分别对主要观察指标PaO2和PaCO2、次要观察指标ADR 发生率纳入的研究绘制倒漏斗图,见图7~9。结果显示,对于主要观察指标PaO2和PaCO2各数据点未均匀对称分布在坐标轴的两侧,提示存在一定发表偏倚;对于次要观察指标ADR,各数据点基本均匀对称分布在坐标轴的两侧,且大部分位于倒漏斗图的顶端,提示偏倚性较小。
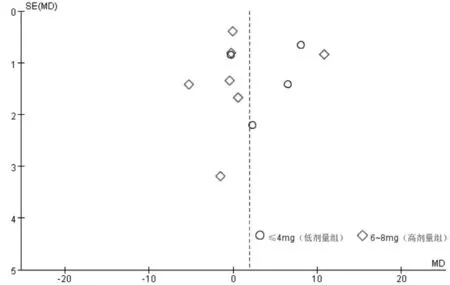
图7 AECOPD 829例患者治疗后PaO2的漏斗图
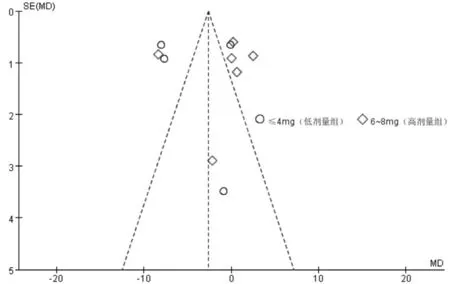
图8 AECOPD 764例患者治疗后PaCO2的漏斗图
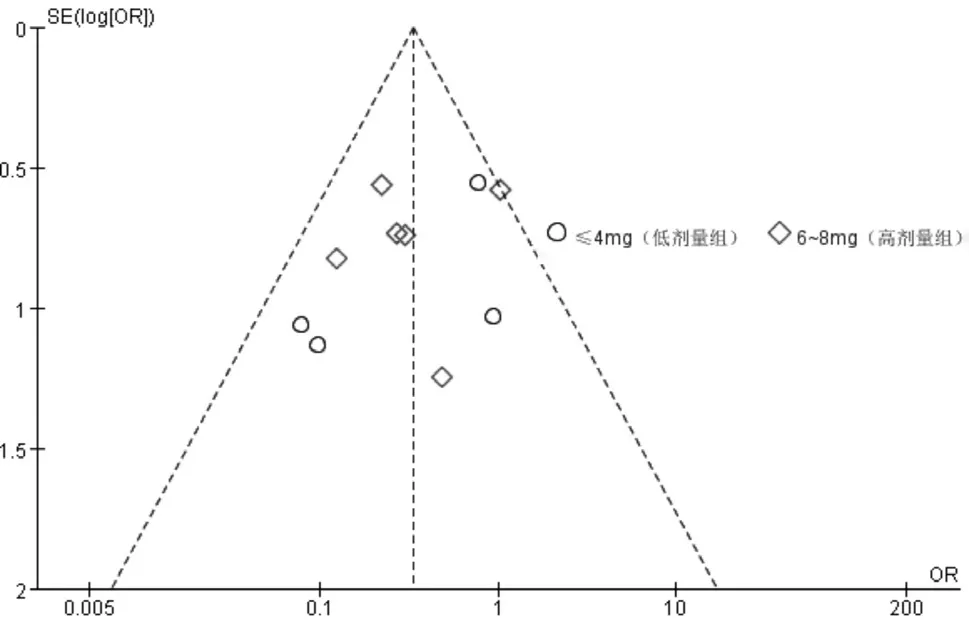
图9 AECOPD 713例患者治疗后ADR的漏斗图
3 讨论
对于AECOPD 需要住院治疗的患者而言,动脉血气(PaO2和PaCO2)是评价其加重期疾病严重程度的重要指标,而肺功能检查因患者难以满意地进行且检查结果不够准确,急性加重期间不推荐进行[4]。所以,本研究系统评价雾化吸入不同给药剂量布地奈德与静脉用甲泼尼龙对比治疗AECOPD 的疗效评估以PaO2和PaCO2为主要观察指标,肺功能检查中FEV1和FEV1/FVC(%)为次要观察指标。
从森林图所示,雾化吸入不同给药剂量布地奈德治疗AECOPD 的疗效(主要观察指标PaO2和PaCO2、次要观察指标FEV1)与静脉用甲泼尼龙相当,且结果稳定可靠;亚组分析及敏感性分析显示,不管低剂量组还是高剂量组,雾化组与静脉组治疗AECOPD 的PaO2、PaCO2和FEV1水平亦相当,且结果稳定可靠。再者,对于次要观察指标FEV1/FVC(%)和ADR,Meta 分析结果显示,雾化组治疗AECOPD 的FEV1/FVC(%)水平高于静脉组,ADR 发生率低于静脉组;亚组分析显示低剂量组两组FEV1/FVC(%)水平、ADR 发生率相当,而高剂量组结果与总体结果一致(雾化组FEV1/FVC(%)水平高于静脉组,ADR 发生率低于静脉组)。
此外,Meta 分析结果显示,低剂量组中所有观察指标各纳入研究间均存在较明显异质性,异质性来源考虑有两方面:一是低剂量组纳入研究相对较少,二是影响结果较大的主要是刘晶[12]和段玉莲[13]的研究,从研究方法和研究方案等考虑不排除与研究的对照组静脉用甲泼尼龙的给药方案及疗程有关;段玉莲[13]的研究在入组病例中各组男女比例、平均年龄等基线水平更是未描述清楚,这可能对结果造成一定影响。
本研究将布地奈德不同给药剂量分亚组分析并进一步做敏感性分析,结果稳定可靠;但仍存在一定局限性。首先,因语种仅限中文和英文,可能导致研究人群的局限;第二,检出的英文文献很少,考虑与国外研究少、国外指南未提及雾化吸入布地奈德可替代全身用糖皮质激素等有关,个别检出的文献[7]因试验组和对照组数据无法提取而被排除。第三,纳入研究大部分对方法学中分配隐藏描述得较粗略。第四,主要观察指标纳入的研究间存在异质性,可能与不同研究者对同一观察指标检测方法差异有关。
4 结论
基于当前的临床数据,亚组分析和敏感性分析均提示雾化吸入不同给药剂量布地奈德治疗AECOPD 的疗效与静脉用甲泼尼龙相当,且不良反应发生率较少,结果稳定可靠;其中雾化吸入低剂量(≤4 mg)布地奈德治疗AECOPD 的疗效需要更多循证药学数据进一步验证。
