醒脑静注射液联合阿替普酶治疗缺血性脑卒中疗效和安全性的系统评价
2022-02-22郭飞黄云慧黄宇靖牛慧芳杜爱玲
郭飞 黄云慧 黄宇靖 牛慧芳 杜爱玲
1新乡医学院第二附属医院(河南新乡453002);2新乡市第一人民医院(河南新乡453000);3新乡医学院(河南新乡453003)
缺血性脑卒中(ischemic stroke,IS)又称脑梗死,是一种由脑部供血障碍引起的高发病率和高致死率的疾病[1-2],多发于老年患者,而该人群机体功能逐步衰退,病情发展和治疗手段相对复杂[3],所以该疾病一直是临床医生和科研人员研究的重点。另外IS 发生后48 h 内患者通常出现严重的神经功能损伤[4],且伴有炎症因子升高和生活质量下降等症状的发生[5]。现阶段对于IS 的治疗多采用溶栓,改善脑供血[6]、修复受损神经[7]等方法。有文献报道,阿替普酶可选择性地激活纤溶酶原,起到溶栓和恢复脑供血的效果[8]。中医认为缺血性脑卒中是机体气血失调、经脉阻滞、血脉不畅所致[8],对于该疾病的治疗应活血化瘀、舒经活络、化痰开窍[9]。而由麝香、栀子、郁金和冰片等组成的醒脑静注射液除具有疏通经络、开窍醒脑、散结活络的功效[8],还有较好的神经功能修复、降低颅内压[3]和炎症因子的功能[5],可有效改善IS 患者的生活质量和大脑血流[10]。因此有研究报道采用醒脑静注射液联合阿替普酶治疗IS 患者,达到标本兼治、提高疗效的目的[11]。但现阶段关于两者联用的研究质量良莠不齐,且纳入的样本量较少,评价指标相对局限,不能全面反映两者联用的优点和所能改善的临床指标。因此本研究采用Meta 分析的方法,系统评价醒脑静联合阿替普酶的有效性和安全性,并将其可能影响的临床指标和炎症因子进行客观评价,以期为临床了解该疾病相关特征、疾病治疗和药物评价提供参考。
1 资料与方法
1.1 文献纳入与排除标准
1.1.1 研究类型有关醒脑静注射液联合阿替普酶治疗缺血性脑卒中的随机对照研究,语言限定为中文和英文。
1.1.2 研究对象符合缺血性脑卒中临床诊断标准,且经颅脑CT 或MRI 等影像学确诊;国籍、种族、性别和年龄不限。
1.1.3 干预措施观察组患者采用醒脑静注射液联合阿替普酶联合治疗;对照组患者阿替普酶治疗,两组除分别进行上述治疗,还同时进行常规治疗,如采用脱水、降颅压、神经保护、维持水和电解质平衡和常规护理等,两组患者均系统治疗2 周。
1.1.4 结局指标(1)有效率;(2)神经功能:NIHSS、NDS;(3)认知功能:MoCA;(4)日常生活能力:ADL;(5)脑血流:基底动脉、大脑中动脉、大脑前动脉、大脑后动脉、椎动脉血流速度;(6)炎症因子:TNF⁃α、PS、hs⁃CRP、IL⁃1、IL⁃6、IL⁃8;(7)缺血面积;(8)不良反应。
1.1.5 排除标准(1)重复发表或数据雷同的文献;(2)诊断不规范、数据不完整或无法提取相关研究数据的文献;(3)无法获取全文的文献;(4)研究对象为动物的相关研究;(5)其他明显不符合本研究纳入标准的文献。
1.2 计算机检索策略由两名专业人员采用计算机检索方式,对中国知网、万方、维普、CBM、PubMed、The Cochrane Library、Embase 等数据库进行系统检索。中文检索词为“脑卒中”、“脑梗死”、“中风”、“醒脑静注射液”、“阿替普酶”,英文检索词为“cerebral infarction”、“stroke”、“ischemic stroke”、“xingnaojing injection”、“alteplase”,文献检索时间段为建库到2020年11月。
1.3 文献选取、资料提取和质量评价由两名专业人员严格依据本研究的纳入和排除标准独立进行文献检索、筛选和资料提取,并交叉核对相关数据。对此过程中所遇分歧问题,应咨询第三名研究人员协助判断。本研究提取的相关数据分别为相关研究的第一作者、文献发表年份、研究对象、年龄、病程、样本量、干预措施和相关结局指标。偏倚风险评估:采用Cochrane 系统评价手册5.3 进行文献质量评价,评价内容包括随机序列的生成、分配隐藏、盲法、不完整的结果数据、选择性报告研究结果和其他偏倚风险。
1.4 统计学方法本研究采用RevMan 5.3 软件进行Meta 分析,计数变量采用比值比(odds ratio,OR)或相对危险度(risk ratio,RR)及95%置信区间(confidence interval,CI)表示;计量资料采用均数±标准差及95%CI表示。异质性检验采用Q 检验,当检验结果无异质性或异质性较小时(I2≤50%),采用固定效应模型(fixed effect model);当检验结果异质性较大时(I2>50%),但临床异质性不明时,采用随机效应模型(random effect model)[12];当存在明显异质性时,应分析异质性来源。采用倒漏斗图对纳入的9 篇文献进行发表偏倚评价。
2 结果
2.1 文献检索结果及流程共检索到64 篇文献,经逐层查重,纳入研究的文献共9 篇[6-9,13-17],文献检索流程见图1。
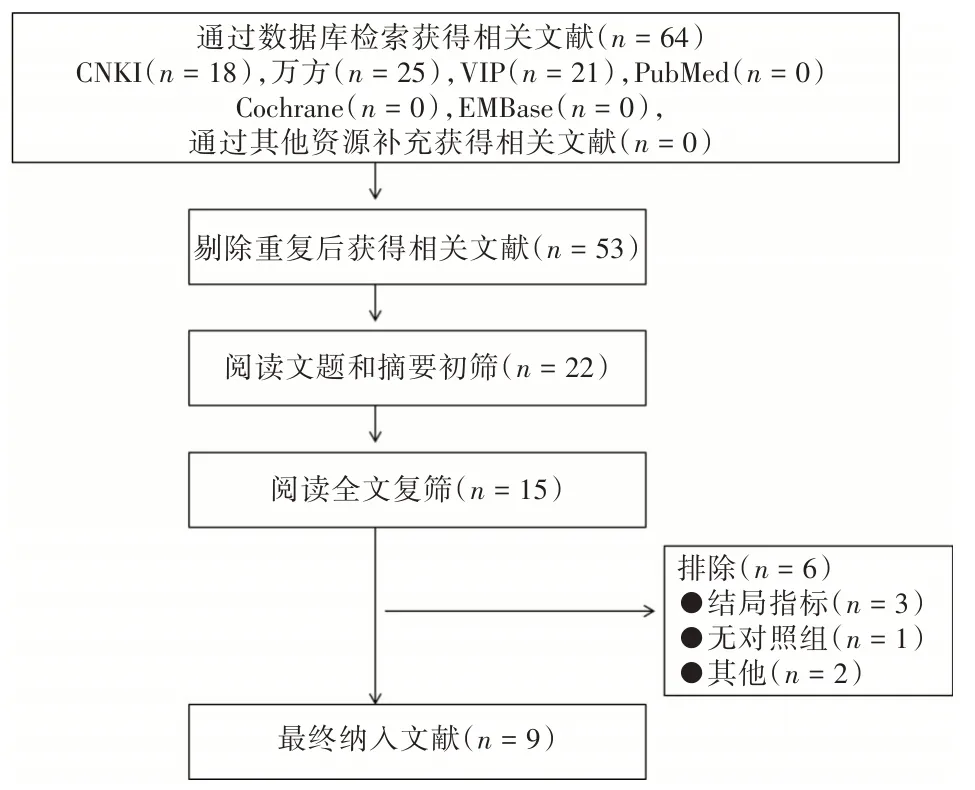
图1 文献筛选流程与结果Fig.1 Flow chart of literature screening
2.2 纳入文献的基本特征本研究共纳入9 篇文献[6-9,13-17],涉及1 005 例患者,其中观察组504 例,对照组501 例,有6 项研究[6,8-9,13,15,17]明确提示所纳入的研究对象为首次发病的缺血性脑卒中患者,3 项研究未提及患者类型,见表1。
表1 纳入文献的基本信息Tab.1 Basic characteristics of included studies ±s
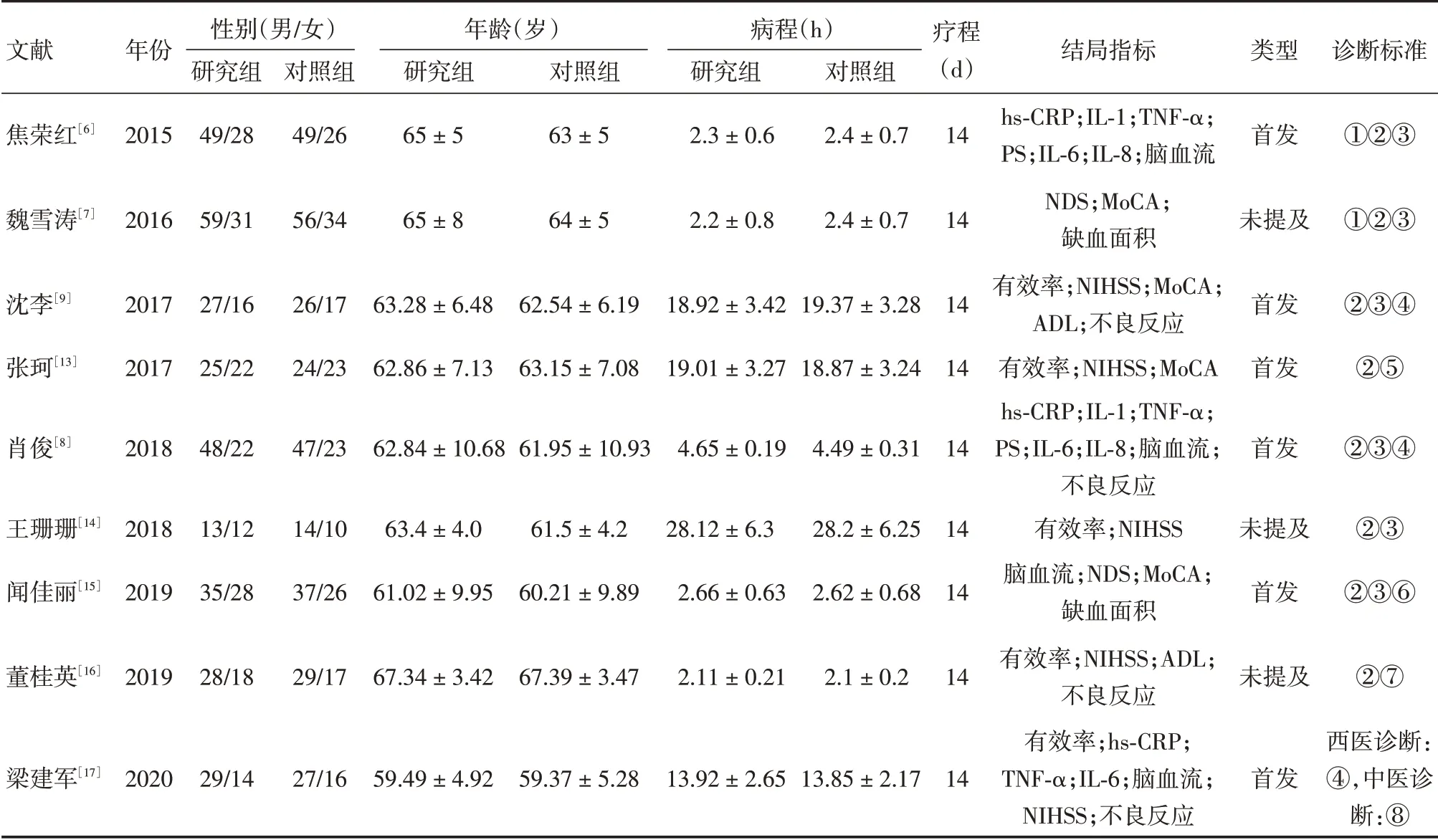
表1 纳入文献的基本信息Tab.1 Basic characteristics of included studies ±s
注:①短暂性脑缺血发作的中国专家共识2011年更新版;②颅脑CT;③MRI;④中国急性缺血性脑卒中诊治指南2010;⑤急性脑卒中诊断标准;⑥全国第4次脑血管疾病会议中对缺血性脑卒中的相关诊断标准;⑦脑梗死诊断标准;⑧《中医内科病证诊断疗效标准(十三)》
文献焦荣红[6]魏雪涛[7]沈李[9]张珂[13]肖俊[8]王珊珊[14]闻佳丽[15]董桂英[16]梁建军[17]年份2015 2016 2017 2017 2018 2018 2019 2019 2020性别(男/女)研究组49/28 59/31 27/16 25/22 48/22 13/12 35/28 28/18 29/14对照组49/26 56/34 26/17 24/23 47/23 14/10 37/26 29/17 27/16年龄(岁)研究组65±5 65±8 63.28±6.48 62.86±7.13 62.84±10.68 63.4±4.0 61.02±9.95 67.34±3.42 59.49±4.92对照组63±5 64±5 62.54±6.19 63.15±7.08 61.95±10.93 61.5±4.2 60.21±9.89 67.39±3.47 59.37±5.28病程(h)研究组2.3±0.6 2.2±0.8 18.92±3.42 19.01±3.27 4.65±0.19 28.12±6.3 2.66±0.63 2.11±0.21 13.92±2.65对照组2.4±0.7 2.4±0.7 19.37±3.28 18.87±3.24 4.49±0.31 28.2±6.25 2.62±0.68 2.1±0.2 13.85±2.17疗程(d)14 14 14 14 14 14 14 14 14结局指标hs⁃CRP;IL⁃1;TNF⁃α;PS;IL⁃6;IL⁃8;脑血流NDS;MoCA;缺血面积有效率;NIHSS;MoCA;ADL;不良反应有效率;NIHSS;MoCA hs⁃CRP;IL⁃1;TNF⁃α;PS;IL⁃6;IL⁃8;脑血流;不良反应有效率;NIHSS脑血流;NDS;MoCA;缺血面积有效率;NIHSS;ADL;不良反应有效率;hs⁃CRP;TNF⁃α;IL⁃6;脑血流;NIHSS;不良反应类型首发未提及首发首发首发未提及首发未提及首发诊断标准①②③①②③②③④②⑤②③④②③②③⑥②⑦西医诊断:④,中医诊断:⑧
2.3 纳入文献的偏倚风险评价9 篇文献中有4 篇[9,14,16-17]文献明确采用随机数字表法进行分组,3 篇[6-8]仅提示采用随机方法,9 篇文献对分配隐藏、结局评价人员是否实施盲法描述均不清楚,研究者和患者是否实施盲法风险程度较高,见图2。
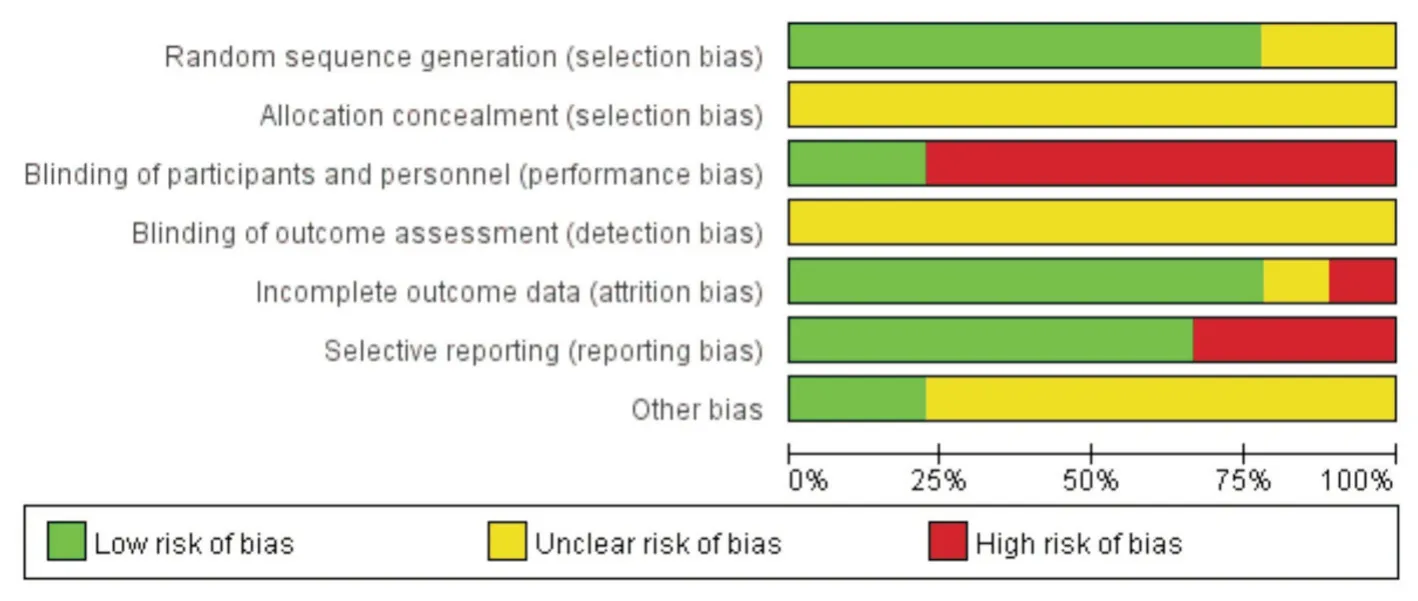
图2 纳入研究的风险偏倚评估Fig.2 Risk bias assessment of included studies
2.4 Meta 分析结果
2.4.1 有效率评价有效率为痊愈、显效和有效人数的总和除以该组总人数,纳入文献中共4 项研究[9,13-14,16]提及有效率,Meta 分析结果显示异质性较小(I2=0%,P=0.77),故采用固定效应模型。经过治疗后,观察组有效率高于对照组(P=0.000 2),见图3。
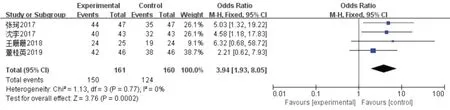
图3 两组有效率的Meta 分析森林图Fig.3 Forest plots of Meta⁃analysis of comparison of effective rate between two groups
2.4.2 功能及炎症因子评价(1)神经功能评价:6 篇文献[8-9,13-14,16-17]采用NIHSS 和2 篇文献[7,15]采用NDS 评价,结果显示,观察组NIHSS 评分和NDS评分均低于对照组(P< 0.000 01)。(2)认知功能评价:4 篇文献[7,9,13,15]采用MoCA 进行评价,观察组MoCA评分明显高于对照组(P<0.000 01)。(3)缺血面积评价:有两篇文献[7,15]采用颅脑CT 扫描方法测量了患者的缺血面积,观察组缺血面积明显低于对照组(P< 0.000 01)。(4)脑血流速度评价:有4 篇文献[6,8,15,17]描述了血流速度,观察组基底动脉、大脑中动脉左侧、大脑中动脉右侧、大脑前动脉左侧、大脑前动脉右侧、大脑后动脉左侧、大脑后动脉右侧、椎动脉左侧和椎动脉右侧血流速度均高于对照组(P<0.000 01)。(5)日常生活能力评价:有两篇文献[9,16]采用ADL 进行评价,观察组ADL 评分明显高于对照组(P< 0.000 01)。(6)炎症因子评价:有四篇文献[6,8,15,17]报道了两组治疗后的炎症因子变化,观察组TNF⁃α(P< 0.001)、PS(P<0.001)、hs⁃CRP(P=0.01)、IL⁃1(P=0.002)、IL⁃6(P=0.000 6)和IL⁃8(P<0.001)水平低于对照组,见表2。

表2 缺血性脑卒中治疗后的Meta 结果Tab.2 Meta⁃analysis of xingnaojing injection with alteplase in the treatment of ischemic stroke
2.4.3 不良反应有四篇文献[8,9,16-17]描述了不良反应发生情况,仅三篇[9,16-17]具体描述不良反应发生类型,基于固定效应模型的Meta 分析结果显示,观察组和对照组的不良反应发生率差异无统计学意义(P=0.84),见图4。

图4 两组不良反应的Meta 分析森林图Fig.4 Forest plots of Meta⁃analysis of comparison of adverse drug reactions between two groups
2.4.4 发表偏倚评估以脑血流速度为指标绘制倒漏斗图,纳入的研究散点对称性不好,提示纳入的研究存在发表偏倚的可能性相对较大。见图5。
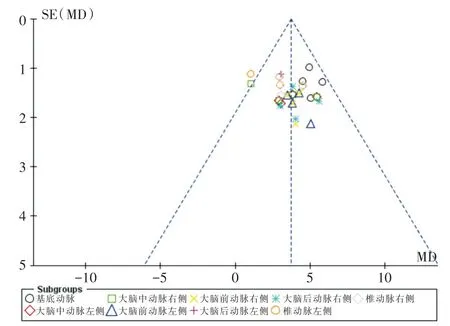
图5 脑血流速度的倒漏斗图Fig.5 Funnel plot of intracranial blood flow velocity
3 讨论
缺血性脑卒中是一类严重危及患者生命健康的疾病,当疾病发生后及时有效地矫正临床症状和改善脑供血,更有利于患者康复和神经功能恢复。有研究显示醒脑静注射液中有效成分可通过血脑屏障,直接作用于中枢神经系统,改善IS 患者的神经损伤和炎症反应[18],另外其与阿替普酶联用能达到更好的治疗效果[16]。各研究虽提示醒脑静注射液联合阿替普酶能改善患者神经功能、日常生活能力和认知功能,但评价方法和质量存在较大差异,因此本研究采用Meta 分析的方法对各研究进行系统评价,并尽可能全面地呈现其改善的临床指标。
Meta 分析结果显示,两者联用可提高IS 患者治疗有效率,但部分研究有效率的评价过于主观[9],评价方法更应结合相对客观的量表评分进行判断[19]。另有研究显示醒脑静注射液可改善IS患者的神经功能,且能显著降低患者的NIHSS 评分[4],本研究采用NIHSS和NDS两种量表进行评价,结果均显示两者联用能较好的改善神经功能,同时MoCA 结果显示其对认知功能也有改善作用。有文献报道IS 的发生和发展与细胞炎症因子有密切关系,其中包括hs⁃CRP、TNF⁃α[20]、IL⁃6、IL⁃8[21],且醒脑静注射液可有效降低炎症因子水平。本研究结果显示两者联用可降低IS 患者的hs⁃CRP、IL⁃1、IL⁃6、IL⁃8、PS、TNF⁃α 水平。另外及时有效的恢复缺血区脑供血和增加脑血流速度对IS 患者的康复至关重要[22],因此本研究也评价了治疗后患者的脑梗死面积和脑血流速度,结果显示醒脑静注射液联合阿替普酶可有效降低缺血面积和增加脑血流速度,并能增强患者日常生活能力。而对于不良反应的评价,两者联用不增加不良反应的发生。
本Meta 分析的局限和不足:(1)纳入的研究多数缺乏中医诊断,仅一篇提及中医诊断标准,因此作为中药注射液的醒脑静注射液,其适应证和患者具体临床症状是否一致仍需进一步考证。(2)部分研究尚无严格的随机双盲等诸多偏倚控制方法,可能存在一定的选择偏倚和发表偏倚。(3)各研究所依据的西医诊断标准稍有不同,可能对患者疾病诊断略有差异,因此各研究结果的一致性需进一步评价,但基于各研究所纳入的患者均依据权威机构或部门发布的诊断标准进行筛选,因此所得结果具有一定的可靠性。(4)检索结果仅为中文文献,且未对其他非英语语种进行检索,可能造成检索不全面。综上所述,醒脑静注射液联合阿替普酶可改善缺血性脑卒中的神经功能损伤、认知功能和日常生活能力,降低诸多炎症指标和缺血面积,增加脑血流速度,且具有一定的安全性。但鉴于纳入的研究质量不高,因此今后仍需更大样本、多中心、长时间、诊断标准一致的高质量的随机对照试验进行验证,以便为临床提供更加可靠的治疗依据。
