同步脱氮除硫燃料电池的电化学特性研究
2022-02-21蔡靖刘思懿吴媛媛郑紫凌王如意李强标
蔡靖,刘思懿,吴媛媛,郑紫凌,王如意,李强标
(浙江工商大学环境科学与工程学院,浙江 杭州)
0 引言
含氮污水对生态环境危害严重,需对其进行处理[1]。在污水的生物脱氮处理过程中,普遍面临反硝化碳源不足的难题[2]。与此同时,我国的支柱工业,如发酵、化工、制药、造纸等,在获得经济效益的同时,产生了大量的含硫废水[3]。在厌氧处理含硫废水过程中,硫酸盐被还原,产生的硫化物具有强烈的腐蚀作用,严重时可致人昏迷和死亡[4]。研究证明,一些微生物能以硫化物为电子供体将硝酸盐还原为氮气[5]。以此为依据,研发出同步厌氧生物脱氮除硫工艺(简称“同步脱氮除硫工艺”),即在缺氧状态下,将厌氧过程的副产物——硫化物作为电子供体,用以还原硝态氮,实现以废治废,同时去除氮和硫2种污染物[6]。不少研究者对同步脱氧除硫工艺进行了深入研究,在性能及调控操作等方面取得了可喜进展,且国内外已有深度处理城市污水以及含氨含硫工业废水的工程案例和应用[7]。微生物燃料电池(microbial fuel cell,MFC)是一种全新的废水处理方法,既能处理废水中的污染物,又能产生电能[8]。据此,笔者将同步脱氮除硫工艺与MFC相结合,开发了同步脱氮除硫MFC,证实该MFC可同步进行废水处理和生物发电,且产电功能与基质去除功能之间是相互耦联的[9-10]。
然而,硫化物化学性质活泼,易发生电化学氧化[11]。同步脱氮除硫工艺属于氧化还原过程,在MFC的阳极上通常发生氧化反应,微生物在基质去除过程中是否起主导作用?已有研究涉及同步脱氮除硫MFC电化学性质的较少。基于此,本文通过构建双室型同步脱氮除硫MFC,分别考查同步脱氮除硫MFC及其化学对照组的产电性能和基质去除性能,探究微生物的作用,并通过测绘同步脱氮除硫MFC的循环伏安曲线、极化曲线及电化学阻抗Nyquist曲线,进一步探讨同步脱氮除硫MFC的电化学特性。
1 材料与方法
1.1 试验装置及运行方式
构建双室型MFC,阳极室和阴极室的有效体积均为300 mL,两室之间用质子交换膜(Ultrax CMI-7 000 Membrane International,USA)分隔[9]。以石墨棒(6 cm×Φ1 cm)作为阳极和阴极,外接负载为1 000 Ω。阳极液为模拟废水,且通过回流泵回流,加强进水与污泥的混合[6],阴极液为高锰酸钾溶液(浓度为100 mg·L-1,pH=7.0)。
采用间歇进水方式运行同步脱氮除硫MFC,反应周期为20 h,每天更换基质。试验废水为模拟废水[9]。进水硫化物中硫的浓度和硝酸盐中氮的浓度分别约为540和94.50 mg·L-1(物质的量之比为5∶2,理论产物为单质硫和氮气)。采用2个相同构型的MFC,分别记为MFC1和MFC2。其中,MFC1为对照组,阳极室不接种富集污泥,设3组平行,进水20 h后测定出水基质浓度,取其平均值进行分析;MFC2为实验组,阳极室内接种100 mL富集后具有同步脱氮除硫功能的污泥,其中污泥悬浮固体(SS)浓度为95.03 g·L-1,挥发性悬浮固体(VSS)浓度为68.68 g·L-1。待出水基质浓度稳定后(3~5个反应周期),取出水基质浓度平均值进行分析。
试验过程中,进水pH为7.0±0.1,环境温度为25°C±2°C。
1.2 分析方法
MFC输出电压数据由数据采集系统(Agilent 34970A Data Acquisition/Switch Unit)收集,收集频率为10 min。电流密度根据电流和电极净表面积进行计算。待MFC2稳定运行1个月后,测定其电化学特性。通过电化学工作站(660C,CH Instruments Inc.,USA)测定循环伏安曲线。其中,以MFC的阳极作为工作电极,铂丝电极作为对电极,Ag/AgCl电极作为参比电极。电位扫描范围为-1.6~+1.6 V,扫速为10 mV·s-1。每组试验重复3次。采用稳态放电法绘制极化曲线,保持MFC处于开路状态,待稳定后,逐步改变外电路电阻(100~90 000 Ω),记录MFC在每个外电阻的准稳电压,分别计算电流密度和功率密度,并绘制相应的极化曲线。MFC保持开路状态,待稳定后,采用三电极体系,用恒电位仪测试交流阻抗,以阳极作为工作电极,铂丝电极作为对电极,Ag/AgCl电极作为参比电极,正弦扰动电压为10 mV,频率为10-3~105Hz。用软件ZsimpWin拟合电化学阻抗谱等效电路。
2 结果与讨论
2.1 基质去除情况
MFC1和MFC2的进水硫化物浓度均为540 mg·L-1,反应20 h后,MFC1出水硝态氮浓度略有提高,与进水相比,出水硝态氮浓度提高了(6.69±1.58)%;出水亚硝态氮浓度略有增高,增高率为0.04%;MFC1的硫化物去除率为(77.30±0.35)%,其中(64.92±3.06)%的硫化物被氧化为单质硫,(12.38±0.53)%的硫化物进一步被氧化为硫酸盐。
MFC2的氮素基质去除情况与MFC1不同,而其硫素基质去除情况与MFC1较为相似,但去除率更高。MFC2的出水硝态氮浓度仅为进水硝态氮浓度的(3.50±0.47)%,去除率高达96.50%,且出水亚硝态氮浓度仅占进水硝酸盐浓度的(0.19±0.02)%,即(96.32±0.89)%的硝态氮被还原为氮气;MFC2的出水硫化物浓度仅为进水硫化物浓度的(0.36±0.05)%,去 除 率 高 达99.64%,其 中,(28.50±1.70)%的 硫 化 物 被 氧 化 为 单 质 硫,(71.14±1.57)%的硫化物进一步被氧化为硫酸盐。
实验结果表明,MFC1的硝态氮不但没有被去除,反而有所增加,且氨氮减少,推测可能是因为氨氮发生电化学氧化,产生硝态氮和亚硝态氮[13];硫化物的氧化产物为单质硫和硫酸盐,且产物以单质硫为主,这与文献报道[14]一致。MFC2的硝态氮和硫化物的去除速率分别可达4.61和26.90 mg·(L·h)-1,出水硝态氮和硫化物浓度分别为3.34和1.95 mg·L-1。其中硝态氮的还原产物为亚硝态氮和氮气,且以氮气为主;硫化物的氧化产物为单质硫和硫酸盐,且以硫酸盐为主。这表明,在同步脱氮除硫MFC中,微生物不仅将硝态氮还原为氮气,还将单质硫进一步氧化为硫酸盐。魏炎等[15]以硫化物作为阳极电子供体,硝酸盐作为阴极电子受体,采用双室型MFC处理含硫化物和硝酸盐的废水。当进水硫化物浓度为(118.9±14.7)mg·L-1时,出水硫化物被消耗殆尽,硫酸盐浓度逐渐升至88.4 mg·L-1,约占进水硫化物浓度的74.35%;阴极中出水硝酸盐浓度则低于0.01 mg·L-1,与本文结果类似。

图1 同步脱氮除硫MFCs的基质去除情况Fig.1 Performance of substrate removal in MFCs treating sulfide and nitrate simultaneously
2.2 产电性能
图2为同步脱氮除硫MFC的产电情况。MFC1的电流密度在进水初期最大,为184.74 mA·m-2;0.5 h后,迅速降至39.92 mA·m-2,降幅达78.39%;随后,下降趋缓,最终降至15.76 mA·m-2。MFC2的电流密度在进水初期最大,为457.20 mA·m-2;0.3 h后,迅速降至376.69 mA·m-2,降幅为17.61%;随后2 h内,电流密度维持在376.69~338.44 mA·m-2;后出现断崖式下降,在第5 h时,降为68.40 mA·m-2;最终缓慢降至30.33 mA·m-2。可见,MFC2与MFC1的产电趋势存在明显差异。LEE等[16]构建了可处理含有机物、硫化物和硝态氮废水的双室型MFC,其稳定电压为25~30 mV,平均电流密度高达14.8 mA·m-2,这与其阳、阴极材料(碳毡)具有较大比表面积有关。

图2 同步脱氮除硫MFCs的产电情况Fig.2 Performance of electricity generation in MFCs treating sulfide and nitrate simultaneously
在MFC1的产电过程中,因电极极化,电流密度迅速下降;而在MFC2的产电过程中,电流密度稳定,处于“平台期”。这表明,在同步脱氮除硫MFC中,微生物的存在有利于产电,这与文献报道结果一致。SUN等[17]发现,在以硫化物为单一基质的MFC中加入微生物,其产电性能更优。而在同步脱氮除硫MFC中,硫化物被氧化所提供的电子数(31.7 mmol)大于硝态氮被还原所接受的电子数(9.87 mmol),多余电子则由阳极传递至阴极,产生电流,这与文献报道[9]一致。
2.3 循环伏安曲线
循环伏安法有多种用途,如用于确定氧化还原活性物质的氧化还原电位、考查微生物菌株或种群的电化学活性[18]以及测定电极表面的氧化还原反应[19]等。在MFC2稳定运行1个月后,其循环伏安曲线如图3所示。该循环伏安曲线有2个氧化还原峰,分别在-0.03 V和-1.24 V处,电流峰值分别为20 mA和52 mA。YIN等[20]采用循环伏安法研究了电化学法还原硝酸盐机理,发现硝酸盐还原峰的电压出现在-1.0~-1.3 V;龚园园[21]采用循环伏安法研究了硫化物在电极上的形态变化,发现硫化物氧化峰的电压出现在0~0.1 V。因此,推测这2个氧化还原峰分别为硝酸盐还原峰和硫化物氧化峰,从而证实了MFC2电极上发生了同步脱氮除硫反应。

图3 同步脱氮除硫MFC2的循环伏安曲线Fig.3 Cyclic voltammetry scans of MFC2 treating sulfide and nitrate simultaneously
2.4 极化曲线
极化曲线通常可分为活化极化区、欧姆极化区和浓差极化区。在大多数MFC中,活化极化区和欧姆极化区较常见,浓差极化区较少见[22]。同步脱氮除硫MFC2也不例外,极化曲线分为活化极化区(I)和欧姆极化区(II),如图4所示。在活化极化区,电流密度较小,电压损失主要来自于活化极化,对应于微生物电极反应的活化过程;随着电流密度的增大,极化曲线进入欧姆极化区,电压损失主要来自于欧姆极化,此时,电压与电流密度呈线性关系,所得拟合直线的斜率可代表电池的表观内阻[23]。根据实验结果,表观内阻为1 923 Ω(R2=0.997 9)。
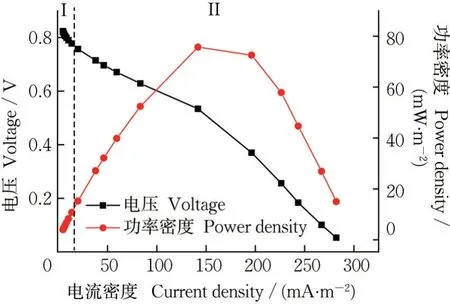
图4 同步脱氮除硫MFC2的极化曲线Fig.4 Polarization curve of MFC2 treating sulfide and nitrate simultaneously
随着电流密度的增大,同步脱氮除硫MFC2的功率密度随之增大。当电流密度为172 mA·m-2(外接负载为2 000 Ω)时,其功率密度达到最大值,为75.70 mW·m-3。随后,功率密度随着电流密度的增大而减小。通常认为,当内阻与外阻一致时,功率密度达到最大值,因此判断同步脱氮除硫MFC2的内阻为2 000 Ω,该结果与极化曲线法的结果一致。
2.5 电化学阻抗分析
同步脱氮除硫MFC2的电化学阻抗(EIS)分析结果如图5所示。MFC的典型Nyquist曲线包括中高频区的半圆形部分和低频区的线形部分,可直观体现电池中的不同极化过程,用于分析内阻及其组成[24]。中高频区的半圆形与横轴相交,交点值表示欧姆内阻,中高频区的半圆直径表示极化内阻,低频区的半圆直径表示有限扩散步骤控制的阻抗[25]。
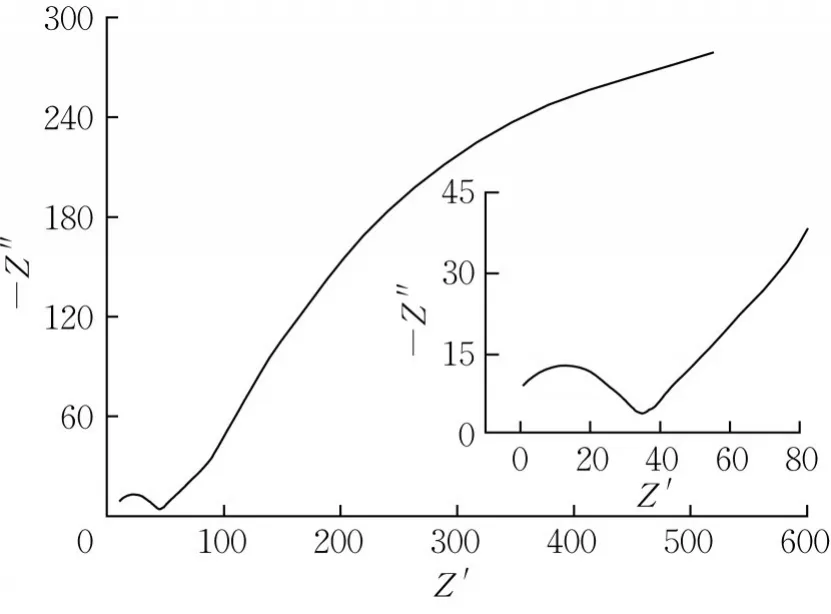
图5 同步脱氮除硫MFC2的Nyquist曲线Fig.5 Nyquist curve of MFC2 treating sulfide and nitrate simultaneously
EIS分析结果用ZSimpWin软件进行拟合,等效电路示意如图6所示。其中,Rohm为欧姆电阻,Rct为电荷转移内阻,Rd为扩散内阻,||为常相位角元件。欧姆内阻主要由电池构型、电极材料电阻、质子交换膜电阻及溶液内阻产生;电荷转移内阻主要由电极反应产生,包括电极上发生的氧化还原反应以及电子传递过程的活化损失;扩散内阻则是由物质向电极表面迁移引起的传质损失[26]。EIS拟 合 结 果 显 示,Rohm=20.84 Ω,Rct=44.78 Ω,Rd=2 407 Ω,拟 合 优 度 卡 方 参 数(χ2)为1.37×10-3。表明在同步脱氮除硫MFC2中,低频区的扩散内阻(Rd)在总内阻中所占比例最大(97.36%),说明扩散内阻限制同步脱氮除硫MFC2的电化学性能。另外,由于硫化物在氧化过程中产生的单质硫沉积在电极上,故硫化物向电极表面扩散的速度降低[27]。

图6 等效电路示意Fig.6 Equivalent circuit diagram
3 结论
构建了具有良好同步脱氮除硫性能的双室型微生物燃料电池(MFC2)。当进水硫化物浓度为540 mg·L-1时,反 应20 h后,MFC2的 硝态氮和 硫 化物去除率分别高达96.50%和99.64%,且其最大电流密度可达457.20 mA·m-2,稳定电流密度为30.33 mA·m-2。由循环伏安曲线知,同步脱氮除硫MFC2电极上发生了同步脱氮除硫反应。分析极化曲线和电化学阻抗知,MFC2的最大功率密度为75.70 mW·m-3,内阻约为2 473 Ω,其中扩散内阻是限制同步脱氮除硫MFC电化学性能的因素。
