抓住实验异常 挖掘背后成因
2022-02-20刘瑛
刘瑛

【摘 要】实验异常现象的出现,会使师生产生不同程度的认知冲突或出现情绪紧张的状态。对异常现象的应对和处理,是体现教学机智和专业素养的重要时刻。本文分析了高中化学必修第二教学中出现的几个实验异常现象,并作出了科学合理的解释,最后就合理规避或利用异常现象提出了思考与建议。
【关键词】化学实验;异常现象;认知冲突
一、问题的提出
化学是一门建立在实验基础上的学科,实验在化学教学中有着不可替代的作用。凡事预则立,不预则废,化学实验亦然。明确实验目的、分析实验原理和预测实验现象是进行化学实验前所必须完成的步骤。实验教学中的种种情况都在预设范围内,教师在课堂上就会游刃有余,得心应手。
在上现场课和公开课时,异常现象的出现会加重紧张情绪,大多数教师都愿退避三舍,敬而远之。在进行演示实验或分组实验时,执教者多期望看到预期的实验现象,对异常现象存有畏惧之心。实验异常的出现,会让教师或学生的原有观念与新经验之间产生对立性矛盾,并对异常现象产生疑惑、出现情绪紧张或不适的状态,即产生认知冲突。如何应对此种状况,是值得我们思考的地方。
二、关注异常现象,挖掘背后成因
实验教学中出现的异常现象,多与试剂来源、装置设计、反应原理和实验操作等有关,但是理论分析是一枝独秀,实际情况却是百花齐放。专业知识的大量储备和实践经验的长期积累,是应对复杂多变的课堂教学的有效保障。笔者在进行高中化学必修二的教学时,实验中出现了几个异常现象,现分析如下。
(一)“探究影响化学反应速率的因素”实验教学中的异常及应对
1.教学片段
学生在实验中发现了异常现象,标注为0.1mol/L盐酸与Zn片反应的速率竟然比1mol/L盐酸与同样大小同样形状的Zn片反应速率快。这一异常现象让笔者也紧张了起来,用“实验员可能将标签贴反了,可能是药品配制过程中出了差错,也可能是其他什么原因,老师下课了解一下”搪塞过去了,但是学生在下课聊天的时候乐此不疲地与同伴分享着这一趣事。笔者意识到这一“乌龙事件”可能会产生无法估量的蝴蝶效应,必须揭示背后成因,在课堂上与同学共同分析讨论。
2.揭示原因
实验小组所用的0.1mol/L盐酸是从药品柜中拿出来的,且从初次配制至此次使用已相隔几年时间。因滴瓶的橡胶塞全部老化开裂,故在使用前全部替换成新橡胶塞。笔者用5-8小组使用的盐酸和药品柜中保存的0.1mol/L的盐酸分别再次进行了实验,与学生所得实验现象相同;而用准备室中台面上放置的相应浓度的盐酸做实验,现象却是与预期相同的。因此,实验员贴错标签的可能性为零,造成实现现象异常的原因与盐酸在保存过程中发生的变化有关。浓盐酸具有挥发性,会使其浓度变小,按照思维定势,实验室保存的0.1mol/L的盐酸亦会变稀,实验对比结果应该不会逆转,但是实验事实确是如此,通过查阅大学《物理化学》课本找到了原因。
对于同一系统,其所含物质数量的多少随人们研究问题的出发点不同而不同,但是平衡系统的组分数却始终保持一定值,所以,组分数是表征系统性质的一个重要参数。组分数不仅与物质种数有关,还与化学反应条件、浓度限制条件等有关。组分数等于系统中的物种数减去独立的化学平衡数,再减去同一相的独立浓度限制条件数。对于HCl和H2O组成的溶液而言,若不考虑它们的电离,其平衡系统中所含的组分数是2。若要考虑,则根据反应:2H2O H3O++OH-,HCl=H++Cl-,可知组分数=6-2-2=2,仍然不变。
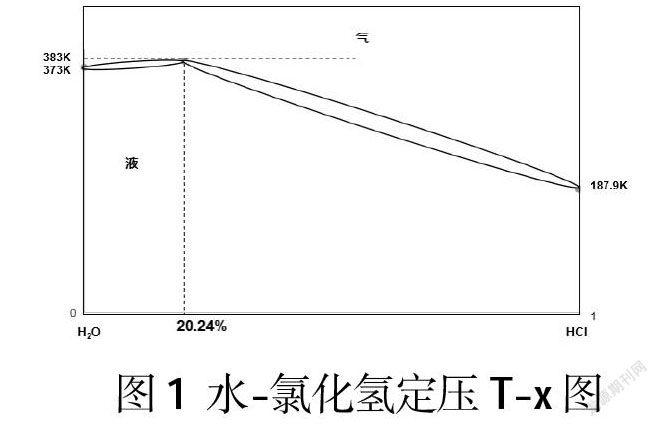
对于二组分系统而言,影响其状态的因素有温度、压力和组成。试剂是在常压下保存的,所以可以固定压力,绘制沸点(T)-组成(x)图(见图1)。由于HCl溶于水后完全电离,使得挥发性发生改变,在T-x图上出现最高点,即最高恒沸点383K,该点上气、液两相组成相同,HCl的质量分数为20.24%。373K、187.9K分别为水和氯化氢的沸点。根据柯诺华诺夫第一规则,较易挥发组分在气相中的成分大于在液相中的成分,即溶液中沸点低的组分在气相中的成分总比在液相中的大,所以T-x图的气相线总是在液相线上方。
据图可知,当组分处于左半部时,则分馏结果得到纯水和HCl-H2O恒沸混合物。当组分利于右半部分时,则分馏结果得到HCl和和HCl-H2O恒沸混合物。药品柜中保存的盐酸初始浓度是0.1mol/L,恒沸混合物的浓度约为6mol/L,故保存于药品柜中的稀盐酸在存放过程中,因滴瓶胶塞老化、密封性较差等原因,气相物质会不断挥发,且挥发出来的是较多的H2O和较少的HCl,液相组成逐渐向中间恒沸混合物移动,浓度逐渐增大。由此可知,稀盐酸(质量分数小于20%)在长期存放过程中,因较多的H2O和较少的HCl挥发,导致浓度升高,故出现异常实验现象。
(二)“乙醇的性质”实验教学中的异常及应对
1.教学片段
“乙醇的性质”教学中,通过复习巩固乙烯的性质,引出乙醇的工业制法——乙烯直接水化法,即在加热、加压和有催化剂存在的条件下,乙烯与水发生加成反应得到乙醇,继而进行乙醇的性质探究部分。为了验证乙醇与Na的反应,教师提出思考问题:实验所需试剂有何要求?乙烯水化法所得乙醇能否直接进行实验?如若不行,如何使其满足实验要求。因水可以与Na反应,学生多认为需要用纯乙醇来进行实验。乙烯水化法所得乙醇中混有水,可利用蒸馏的方法得到纯乙醇。教师给出事实证据——蒸馏法得到的乙醇浓度最高为95.6%。这一事实与学生的原有认知产生冲突,据此介绍无水乙醇的制备方法之一——将新煅烧的CaO置于95%的乙醇中,先冷凝回流一段时间后,再蒸馏,可得无水乙醇。
教學中对无水乙醇的制备进行了重点强调,但是在后期作业评价中发现,学生的掌握得并不是很好,多停留在原有认知的水平上。故需要在形成认知冲突处再下一剂猛药,让学生知其然,亦知所以然。
2.揭示原因
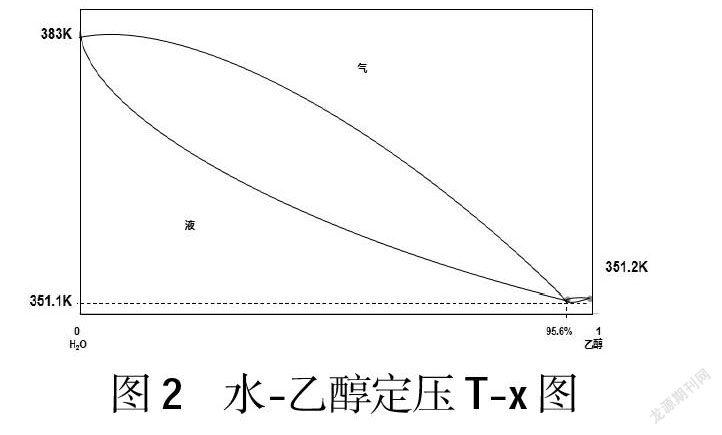
乙醇与水组成的溶液是二组分系统,绘制沸点(T)-组成(x)图(见图2)。由于乙醇溶于水后与水分子间形成氢键,使得挥发性发生改变,在T-x图上出现最低点,即最低恒沸点351.1K。该点上气、液两相组成相同,乙醇的质量分数为95.6%,改变温度时,气相和液相的组成均保持恒定。373K、351.2K分别为水和乙醇的沸点,气相线在液相线上方。
乙烯水化法所制得的乙醇,其组分处于图像左半部,故在蒸馏过程中,挥发出来的是较多的乙醇和较少的水,气相取出后再部分冷凝,经过多次反复降温、冷凝,气相组成将逐渐往右下端移,直至恒沸混合物。在进一步的蒸馏过程中,组成保持不变,得到的始终是乙醇-水恒沸混合物,得不到纯乙醇。所以为了得到纯乙醇,需要在高浓度乙醇的基础上,利用CaO与水的反应将微量的水除去。
(三)“乙烯的性质”实验教学中的异常及应对
1.教学片段
浓硫酸分子内脱水是实验室制备乙烯的常用方法,但是笔者亲自进行实验后发现效率低且副反应明显,故放弃了利用此法制备乙烯。有一线教师利用乙烯利来快速制备乙烯,笔者自己在花卉市场也买了一瓶乙烯利,以便进行乙烯与溴的四氯化碳反应的演示实验。
实验猜想:根据乙烯的结构特点,类比甲烷的性质,乙烯和溴的四氯化碳能反应吗?若反应,可以观察到什么现象?若反应,属于什么反应类型,是取代反应吗?如何用实验进行验证?实验验证:教师进行演示实验,将乙烯利与NaOH混合,现场制乙烯,并将其通入到溴的四氯化碳溶液中,溶液褪色;再向溶液中滴加几滴HNO3酸化的AgNO3溶液,产生白色沉淀。
产生白色沉淀这一实验现象属异常现象,与学生通过预习所得认知相冲突,与教师预期现象亦有不同,属于课堂生成问题。
2.揭示原因
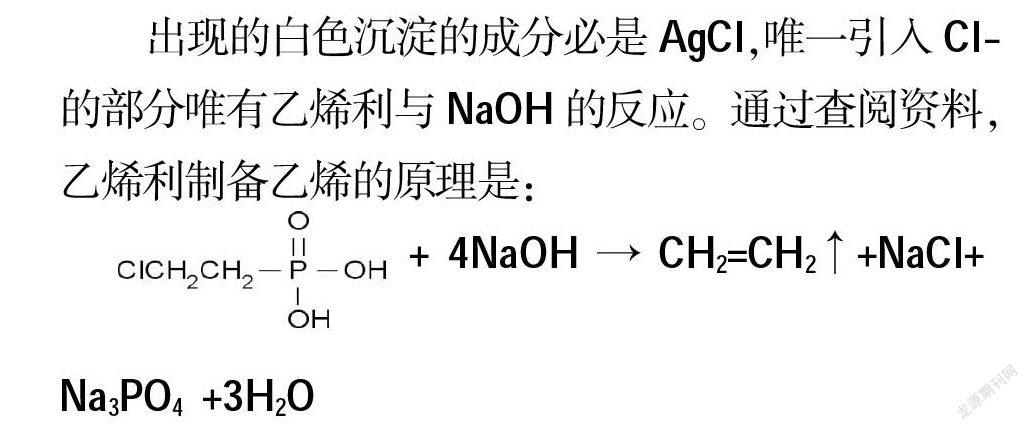
出现的白色沉淀的成分必是AgCl,唯一引入Cl-的部分唯有乙烯利与NaOH的反应。通过查阅资料,乙烯利制备乙烯的原理是:
+ 4NaOH → CH2=CH2↑+NaCl+
Na3PO4 +3H2O
该反应中,NaOH溶于水大量放热,且演示实验中所用分液漏斗管口处离底部较近,导致乙烯气体快速生成时,溶液中的NaCl随气流一起进入后续装置,即HNO3酸化的AgNO3溶液中。故要排除NaCl等因素的影响,可将气流进行降温处理,使得NaCl进入液相,不随气相一起进入后续装置。为了避免干扰,笔者进行了实验改进,提前将乙烯制备好并收集在储气袋中,再进行实验,未观察到沉淀生成。另外,考虑到HBr难溶于CCl4,易挥发,且溴可与水反应生成HBr干扰实验结果,所以向通入乙烯之后的溴的CCl4溶液中加入HNO3酸化的AgNO3溶液来检验HBr的存在有不合理之处。在第二个教学班进行教学时,做出了改进,即将乙烯与溴的CCl4溶液反應后的气体先通入CCl4中除去可能挥发出来的溴蒸气,再通入HNO3酸化的AgNO3溶液中。在出现异常现象的教学班中,对产生异常的原因做了详尽的分析,并引导学生改进了设计方案,以实现培养学生科学探究的能力,并强化学生的证据推理意识。
3.点击高考
对“乙烯的性质”实验教学中异常现象的分析,并非闭门造车、自圆其说,实则有理可依、有迹可循。在2020年浙江卷中,浓硫酸与浓盐酸混合制备HCl时,生成的气体通入硝酸钡溶液中产生白色沉淀。分析其原因,亦是因二者混合过程中放热,HCl气体将硫酸带出,使其进入硝酸钡溶液中产生白色沉淀。
在2019年北京卷中,Cu与浓硫酸在加热条件下反应制备二氧化硫,生成的气体通入硝酸银溶液之前,用饱和亚硫酸氢钠除去SO2中的杂质,其作用亦是除去可能被气流带出的硫酸。
三、对“异常现象”的教学思考
对实验异常现象的应对和处理,是体现教学机智和专业素养的重要时刻。当学生因实验异常现象产生认知冲突时,多会产生主动探究的欲望。教师可因势利导,顺势而为,在解决冲突的过程中提升学生的认知水平和学科能力,帮助学生形成敢于质疑、勇于创新、崇尚真理和严谨求实的科学态度。当教师因实验异常现象产生认知冲突时,应当有自觉探究的意识。平时教学中的意外实验现象背后都隐藏着必然,严谨的科学态度是教师需要教会学生的珍贵品质。
【参考文献】
[1]范楼珍,王艳,方维海.物理化学[M].北京:北京师范大学出版社,2009:131-165.
[2]陈兆先,高俊.初中化学恒沸现象探析——以加热通有二氧化碳的石蕊溶液未能恢复紫色为例[J].化学教育,2019(11):79-81.
[3]应春晓.乙烯性质实验的再改进[J].化学教学,2019(04):69-71.
