可逆性后部白质脑病综合征临床及影像学特点分析
2022-02-18韩丽娟陈燕婷
韩丽娟 李 政 黄 嵘 徐 运 陈燕婷▲
1.南京大学医学院附属鼓楼医院神经内科,江苏南京 210008;2.南京大学医学院附属鼓楼医院康复医学科,江苏南京 210008
可逆性后部白质脑病综合征由Hinchey 等[1]在1996 年首次提出,是一组急性起病,有典型神经系统症状和影像学特征的综合征。高血压、血压波动、肾功能不全、子痫/子痫前期、免疫抑制剂或细胞毒性药物的使用及自身免疫系统疾病等均是本病的诱因。常见的临床表现有意识障碍、癫痫、头痛、视觉障碍、恶心、呕吐及局灶性神经功能缺损等[2]。影像学特征为双侧皮层/皮层下的血管源性水肿,以顶-枕叶最为常见[3]。本病总体预后良好,但也有致残、致死的可能[4]。本研究旨在通过回顾性分析和总结17 例可逆性后部白质脑病综合征患者的临床和磁共振成像(magnetic resonance imaging,MRI)特点,提高临床医师对本病的认识,从而及时诊治,改善患者的预后。
1 资料与方法
1.1 临床资料
收集2017 年5 月至2020 年6 月南京大学医学院附属鼓楼医院经临床随访证实的17 例可逆性后部白质脑病综合征患者的资料。对17 例患者的临床表现及影像学特征进行分析。
1.2 仪器与方法
采用Philips 公司3.0T MR 扫描仪,行头颅MR检查,检查序列包括:T1WI、T2WI、T2 液体反转(fluid attenuated inversion recovery,FLAIR),弥散加权(diffusion-weighted imaging,DWI)和表观弥散系数(apparent diffusion coefficient,ADC)。
1.3 图像分析
由两位资深神经内科医师分别对患者的影像学图像进行独立分析。如两者意见不一致,则讨论后取得一致意见。
2 结果
2.1 临床特点
本研究共纳入17 例患者,均为女性,平均年龄(31.06±12.84)岁。临床表现以癫痫发作最常见,其次为意识障碍、头痛及视物模糊。大约1/3 的患者癫痫发作超过2 次,癫痫持续状态少见。绝大多数患者发病时血压升高,平均血压178/116 mmHg(1 mmHg=0.133 kPa)。收缩压和舒张压峰值分别为220 mmHg 和150 mmHg。
危险因素方面,妊娠相关最常见,共有13 例(76.4%),其中子痫/子痫前期10 例,产褥期1 例,合并再生障碍性贫血后输血1 例,产后出血休克大量输血合并肾功能不全1 例。产前子痫/重度子痫前期发生在孕26~39 周,产后子痫/重度子痫前期常发生在产后24 h内(80%,4/5)。其他危险因素包括酪氨酸激酶抑制剂(安罗替尼、阿西替尼)的使用、系统性红斑狼疮和肾病综合征。见表1。
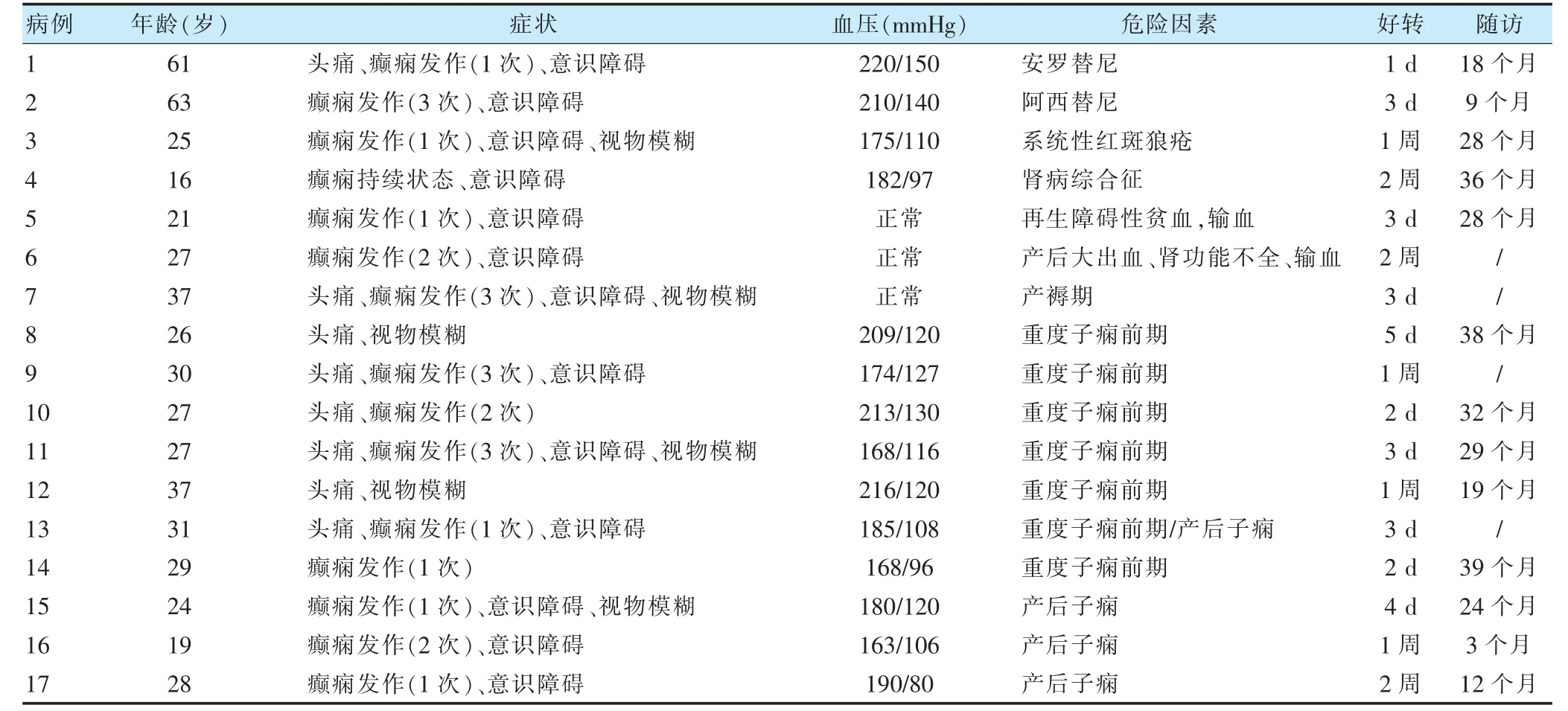
表1 17 例可逆性后部白质脑病综合征患者的临床特点
2.2 MRI 表现
17 例患者脑部病变共112 个,其中绝大部分累及双侧顶枕叶,顶叶34 个(30.36%)、枕叶29 个(25.89%)、额叶24 个(21.43%)、颞叶13 个(11.61%)、基底节7 个(6.25%)、小脑3 个(2.68%)、脑干2 个(1.79%)。病灶信号提示血管源性水肿,T1WI 等或低信号,T2WI、FLAIR 及ADC 均为高信号,DWI 以等或低信号为主,部分患者有散在点状高信号。6 例行MRI 增强检查,仅1 例有强化。8 例患者复查影像,最早在发病1 周后,大部分病灶可明显吸收。发病24 h 内MRI 表现和发病后5 d 复查MRI 见图1。
2.3 其他检查
4 例患者行腰椎穿刺术,脑脊液压力正常1 例,增高2 例,未测1 例。3 例行脑脊液细胞学及生化检查。细胞学、糖和氯化物基本正常,蛋白均增高,范围在603.0~2618.5 mg/L。其中脑脊液蛋白2618.5 mg/L 的患者,在产后8 d 发病,1 周后脑脊液蛋白降至451.3 mg/L。行眼底检查患者共4 例,仅1 例有眼底异常,表现为视网膜灰白色隆起,黄斑水肿,为双眼视网膜脱离。
2.4 治疗与预后
可逆性后部白质脑病综合征治疗以去除危险因素及对症处理为主,包括降血压、止痫、降颅压及呼吸支持等。解痉和终止妊娠是子痫/子痫前期可逆性后部白质脑病综合征患者的主要治疗手段。
患者多数预后良好。8 例患者的症状在3 d 内明显好转,6 例患者的症状在1 周内明显好转。其余患者的症状在2 周后也明显缓解。共随访14 例,随访时间为发病后3~39 个月,无再发可逆性后部白质脑病综合征,无癫痫发作。影像学病灶基本吸收。
3 讨论
可逆性后部白质脑病综合征见于各年龄段,以中青年为主,女性多发。本研究纳入患者均为女性,临床表现以癫痫发作、意识障碍、头痛和视物模糊为主。眼底检查多数正常,所测脑脊液蛋白均增高,与文献报道基本一致[4-5]。
3.1 可逆性后部白质脑病综合征发病危险因素及发病机制
可逆性后部白质脑病综合征发病的危险因素繁多,发病机制复杂,目前尚未明确[6-10]。目前认为,内皮损伤及血脑屏障破坏是可逆性后部白质脑病综合征发病的核心环节[2]。可能的发病机制包括:①脑血管自动调节功能受损[2];②内皮细胞激活释放血管活性物质,增加血管通透性[11];③内皮细胞直接受损[2]。此外,低灌注可能参与可逆性后部白质脑病综合征发病[2,12]。
本组患者的诱因中,子痫/子痫前期占比最高。子痫/子痫前期患者血容量增加,血压升高及血管调节功能受损,均可诱发可逆性后部白质脑病综合征[13-14]。文献报道,62.5%~98.0%的子痫患者及10.5%~19.2%的子痫前期患者合并可逆性后部白质脑病综合征[15]。其中,初产妇、血小板减少、蛋白尿及高血压与可逆性后部白质脑病综合征相关。产后可逆性后部白质脑病综合征也很常见,大部分见于产后子痫,多见于产后48 h[14-16]。子痫/子痫前期所致可逆性后部白质脑病综合征的影像学表现较轻,细胞毒性水肿、出血及强化等恶性表现少,病灶通常可完全吸收,遗留病灶少[13-14]。
酪氨酸激酶抑制剂会直接损伤内皮细胞,诱发高血压及可逆性后部白质脑病综合征[7,17]。本研究2 例酪氨酸激酶抑制剂使用患者,均在服药2 周左右发生可逆性后部白质脑病综合征,发病时血压显著增高。予降压及停药处理,随访未再出现意识障碍、癫痫等。
在系统性红斑狼疮患者狼疮活动时,内皮细胞功能障碍会诱发可逆性后部白质脑病综合征[18]。系统性红斑狼疮患者合并可逆性后部白质脑病综合征并不常见,发生率<1%[19]。系统性红斑狼疮患者合并可逆性后部白质脑病综合征时,是否需要停用免疫抑制剂或激素仍有争论。虽然免疫抑制剂或激素有可能诱发可逆性后部白质脑病综合征[20],但继续治疗可以控制狼疮活动,减少液体潴留及降低血压[20]。
在少数情况下,输血也能诱发可逆性后部白质脑病综合征。多见于慢性贫血患者,因快速纠正贫血可导致血管源性水肿[21]。本研究中,1 例慢性再生障碍性贫血患者,在3 d 内快速纠正贫血(血红蛋白由51 g/L升至90 g/L,血小板由9×109/L 升至13×109/L)后,突发抽搐伴意识丧失,予抗癫痫对症治疗有效。
3.2 可逆性后部白质脑病综合征影像学特征
影像学特征是可逆性后部白质脑病综合征诊断的核心条件之一。MRI 能清晰地显示血管源性水肿,特别是T2 及FLAIR 序列。DWI 联合ADC 序列可区分细胞毒性水肿与血管源性水肿。可逆性后部白质脑病综合征典型影像学表现为双侧顶枕叶皮层下、对称性的血管源性水肿。依据受累部位,可分为顶枕型、半球分水岭型、额上回型[22]。此外,“非典型”影像学表现也可见于可逆性后部白质脑病综合征患者。例如,脑干、基底节区、内囊后肢、小脑、脑室周围及深部白质等也可受累[3]。其他不典型表现还包括单侧病变、弥散受限、出血、微出血或强化病灶等[23]。本研究17 例患者几乎均有双侧顶枕叶受累,“非典型”部位包括基底节、小脑及脑干。病灶信号为血管源性水肿,部分患者在血管源性水肿背景中表现为散在点状弥散受限高信号,结合ADC 均为高信号,考虑T2 穿透效应。此外,强化病灶少见。
3.3 可逆性后部白质脑病综合征治疗
可逆性后部白质脑病综合征治疗以对症支持治疗为主,需平稳降压,最初数小时,血压降低不能超过20%~25%,平均动脉压建议控制在105~125 mmHg[4]。癫痫发作常在24~48 h 内发生,如危险因素持续存在,癫痫可复发[4]。长期癫痫发作少见,常与非典型部位病变及海马硬化相关[24]。目前,可逆性后部白质脑病综合征患者抗癫痫治疗尚无统一标准。大部分可逆性后部白质脑病综合征患者,无需长期抗癫痫治疗。当症状缓解,危险因素得到控制后,可及时减药及停药,疗程为2~7 个月[4]。地西泮、德巴金、左乙拉西坦等可有效控制癫痫发作。对子痫/子痫前期患者,首选硫酸镁解痉,并需尽快终止妊娠。
3.4 可逆性后部白质脑病综合征预后
可逆性后部白质脑病综合征总体预后良好,通常在数小时至数天内缓解[2]。但也有病变严重者,预后不佳。研究显示可逆性后部白质脑病综合征患者的死亡率和致残率可分别高达19%和44%[4],有4%的患者可能复发,与危险因素控制不佳、严重脑病及并发症等相关[4]。
目前,大部分研究以单中心、回顾性病例分析为主,有关可逆性后部白质脑病综合征发病机制、临床表现、影像学特点及治疗仍存在诸多争议[25]。多中心、前瞻性研究及脑灌注影像学研究是未来研究重点。
