禽源烟曲霉菌和黄曲霉菌的分离鉴定及几种中药抑菌作用研究
2022-02-15薛文慧赵千惠王明迪霍书英
薛文慧,赵千惠,梁 天,王明迪,孙 鹏,霍书英,李 永
(1.河北农业大学动物医学院,保定 071001;2.河北定农农业科技集团股份有限公司,保定 073000)
霉菌污染一直是全球关注的问题,特别是在动物的养殖环境及饲料加工、运输和储存过程中的霉菌污染,霉菌及霉菌代谢产生的毒素对人和动物的健康造成极大的危害[1-2]。霉菌在自然界中普遍存在,其中烟曲霉菌和黄曲霉菌是最常见的致病菌,易引起人类和动物急性或慢性呼吸道疾病,造成肺损伤,被称为曲霉肺炎[3]。每年有大量家禽因垫料和饲料霉变而感染黄曲霉菌和烟曲霉菌,引发中毒死亡[4]。霉菌饲料产生的霉菌毒素影响家禽生产性能,同时引起家禽免疫功能下降等各种疾病,最终通过家禽产品危害人类健康[5]。
目前,临床用于抗烟曲霉菌、黄曲霉菌的药物有唑类、多烯类、脂质体类、棘白素类等。其中唑类包括伏立康唑和伊曲康唑,多烯类包括两性霉素B等。这些抗菌药物不仅价格昂贵,还易产生耐药性[6]。为保障动物健康和人类的安全,寻找安全、具有抗菌活性的天然药物已成为研究热点。石菖蒲[7](Acorusgramineus)、决明子[8](Cassiaobtusifolia)、黄柏[9](Phellodendronchinensis)、苦参[10](Sophoraflavescens)、辣蓼[11](Polygonumhydropiper)、白头翁(Pulsatillaadans)、蒲公英[12](Herbataraxaci)均具有清热祛湿、抗虫消炎和抑菌等药理作用,Zhang等[13]前期研究发现石菖蒲和辣蓼对光滑念珠菌的生长有明显的抑制作用,故本试验针对禽源烟曲霉菌和黄曲霉菌探究中草药石菖蒲、决明子、黄柏、苦参、白头翁、辣蓼、蒲公英的抑菌作用,以期为禽类抗霉菌天然药物的研发提供科学依据。
1 材料与方法
1.1 材料
1.1.1 病料 河北省保定市农翔畜禽诊所临床病鸭,病鸭精神不振,羽毛蓬松,排淡绿色稀便,站立不稳,剖检肺部有灰白色结节,取其病变肺脏组织分离病原菌。
1.1.2 试验动物 20只2周龄的SPF鸡由河北省保定市定农集团提供。
1.1.3 主要试剂及仪器 葡糖糖、蛋白胨、酵母粉、琼脂均购自北京奥博星生物技术有限公司;Taq酶、TaqBuffer、dNTP均购自宝生物工程(大连)有限公司;Omega真菌DNA提取试剂盒购自北京博迈德生物技术有限公司;石菖蒲、黄柏、决明子、苦参、白头翁、辣蓼、蒲公英均购自安国药材市场。DNP-9082培养箱购自上海福玛实验设备有限公司;超声提取仪购自上海育模仪器有限公司;SHZ-D循环水式多用真空泵购自河南省予华仪器有限公司;Bio-Rad酶标仪购自北京线上生物科技有限公司。
1.2 方法
1.2.1 病原菌分离与形态观察 临床剖检送检病鸭,发现米粒大小的灰白色结节覆盖在肺脏表面,肝脏发黄、肿大呈豆腐渣状。采集肺部结节混于无菌生理盐水中,取100 μL 均匀涂抹于SDA培养基上,37 ℃恒温培养42 h后观察,挑取单菌落于载玻片上进行显微镜观察,并运用划线法将单菌落进行分离纯化。
1.2.2 分子生物学鉴定 用真菌DNA提取试剂盒提取培养48 h时SDA培养基中的培养物DNA。鉴定真菌通用引物序列为:ITS1:5′-TCCG-TAGGTGAACCTGCGG-3′;ITS4:5′-TCCTCCG-CTTATTATTGATATGC-3′。引物由生工生物工程(上海)股份有限公司合成,预期扩增片段大小约为560 bp。PCR反应体系50 μL:10×ExTaqBuffer 5 μL,2.5 mmol/L dNTP Mix 4 μL,上、下引物各2 μL,5 U/μL ExTaq0.5 μL,DNA模板2 μL,DEPC水34.5 μL。PCR反应条件:94 ℃预变性3 min;94 ℃变性30 s,55 ℃退火30 s,72 ℃延伸1 min,共35个循环;72 ℃延伸10 min。PCR产物进行1.5%琼脂糖凝胶电泳检测后,送至上海派森诺生物技术有限公司测序,比对测序结果,并利用Mega 7.0构建系统进化树。
1.2.3 动物回归试验 将20只雏鸡随机分为对照组和试验组,每组10只,连续7 d给试验组雏鸡鼻腔涂抹分离的病原菌后剖检,对照组雏鸡不作任何处理,正常饲喂,剖检后观察脏器是否发生病变及病变部位是否长出类似病鸭肺部的灰白色结节,并对病变部位做病理切片进行组织学观察。
1.2.4 中药提取 参考Zhang等[14]方法,将中药石菖蒲、黄柏、决明子、苦参、白头翁、辣蓼和蒲公英粉碎后分别称取100 g,用60%乙醇按料液比1∶10的比例浸泡24 h, 30 ℃超声提取3次,每次15 min,药液减压抽滤2次,滤液3 000 r/min离心10 min,取上清于80 ℃旋转蒸发仪中浓缩至2 g/mL,4 ℃保存备用。
1.2.5 最小抑菌浓度MIC80测定 依据CLSI编订的M27-E4标准测定各中药MIC80,使用改良微量肉汤稀释法进行药敏试验。取2 g/mL药液混于SDA液体培养基中,运用倍比稀释法将浓度依次稀释为1 024、512、256、128、64、32、16和8 μg/μL,取100 μL于无菌96孔板内,每个浓度3个重复。用SDA液体培养基将菌液稀释为103CFU/mL,取100 μL于中药孔中使中药终浓度分别为512、256、128、64、32、16、8和4 μg/μL,取100 μL菌液和100 μL培养基做阳性对照,取200 μg/μL培养基做阴性对照,37 ℃恒温培养48 h,测定D630 nm值,试验重复3次。
1.2.6 体外药敏试验 取2 g/mL中药液混于SDA琼脂培养基中,使培养基中中药浓度分别为256、128、64、32和16 μg/μL,无菌生理盐水制备10 CFU/mL菌液,均匀涂抹于培养基中,37 ℃恒温培养24、48和72 h,记录菌落数量,测定菌落直径。
1.3 数据统计分析
试验数据使用SPSS 11.5软件进行统计分析,结果用平均值±标准差表示,所有试验至少重复3次。
2 结 果
2.1 病原菌形态观察结果
在SDA培养基中分离纯化后发现2种形态不同的病原菌,暂称为菌落1和菌落2。菌落1培养12 h呈白色,24 h中心呈亮黄色,48 h变为黄绿色呈棉花状,菌丝分散,菌核大小为10 mm(图1A)。培养12 h时菌落2呈白色,24 h呈绿色,48 h呈灰绿色,菌丝呈分散蓬松绒毛状,菌核大小为14 mm(图1B)。40倍显微镜下菌落1孢子头部呈球形,顶部双层呈放射性排列(图1C);菌落2孢子呈球形,顶部呈瓶状,周围布满绿色小刺(图1D)。
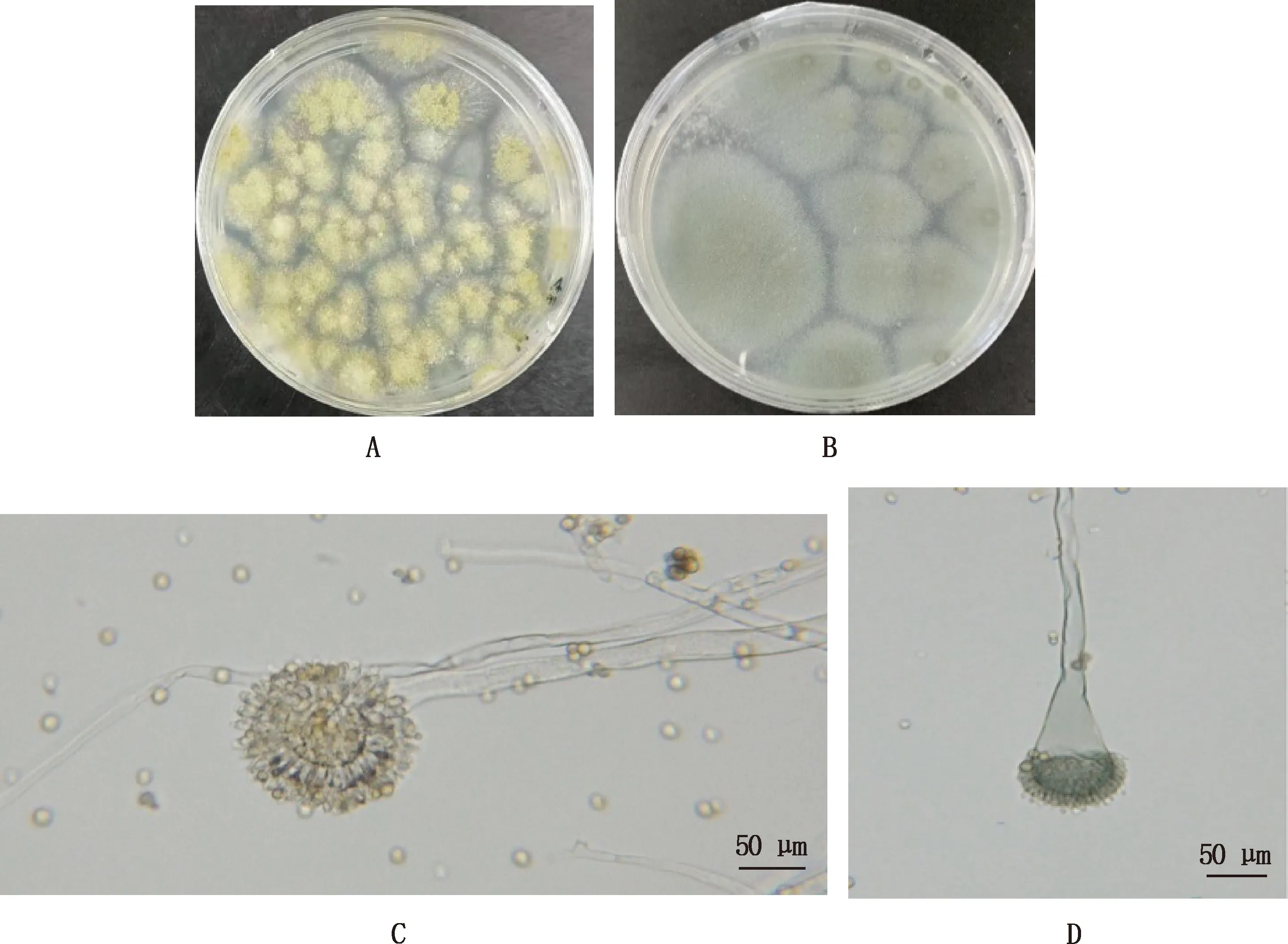
A,培养48 h时菌落1形态;B,培养48 h时菌落2形态;C,菌落1的分生孢子(40×);D,菌落2的分生孢子(40×)A,Morphology of colony 1 at 48 h;B,Morphology of colony 2 at 48 h;C,Conidia of colony 1 (40×);D,Conidia of colony 2 (40×)图1 病原真菌形态Fig.1 Morphology of pathogenic fungi
2.2 分子生物学鉴定结果
2.2.1 PCR扩增结果 目的基因扩增结果显示,经1.5%琼脂糖凝胶电泳后,扩增片段大小约为560 bp(图2),与预期大小相符。
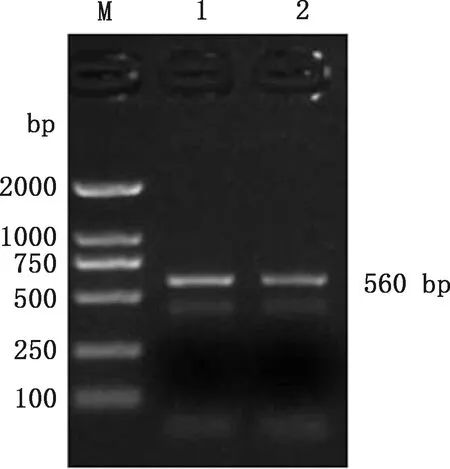
M,DL2000 DNA Marker;1,菌落1;2,菌落2M,DL2000 DNA Marker;1,Colony 1;2,Colony 2图2 目的基因PCR扩增结果Fig.2 PCR amplification results of target gene
2.2.2 菌株1系统进化树 在BLAST中比对选取黄曲霉菌MK108310、MK002477238、MK002477242、MK002477244、MK002477247、MK002477237、MK002477240、MK002477245和MK002477250,以及大卫氏菌属(Davidiellasp.) MK108394与菌株1进行系统进化树分析,结果显示,黄曲霉菌MK108310与菌株1的亲缘关系最近,相似性高达99.82%,判定菌株1属于黄曲霉菌属(图3)。
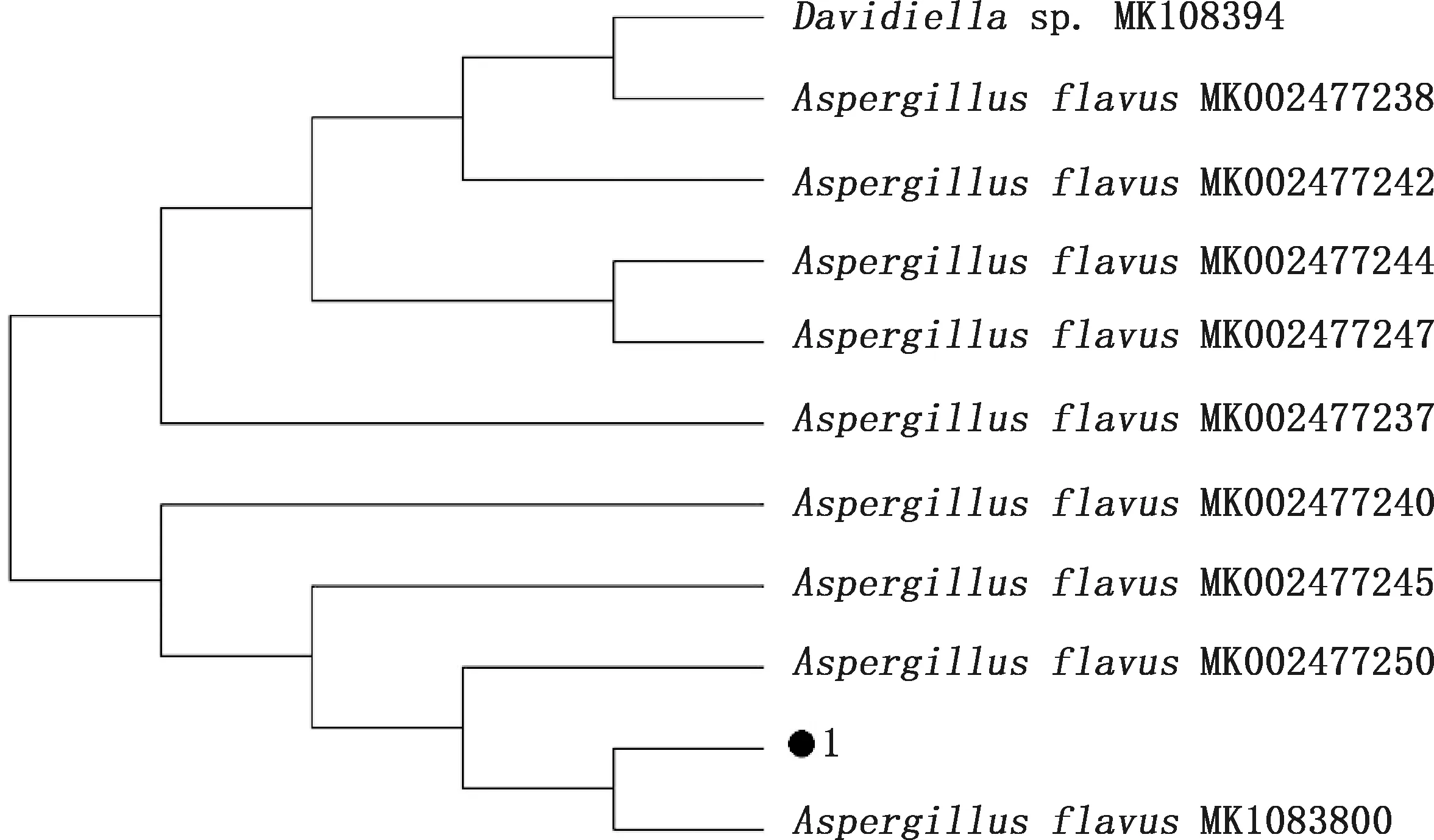
图3 菌株1系统进化树Fig.3 Phylogenetic tree of strain 1
2.2.3 菌株2系统进化树 经BLAST比对选取烟曲霉菌KY926853、NC_007201、NC_007195、NC_007196、NC_00719、NC_007200、NC_007198、NC_007196、NC_007197、NC_007194与菌株2进行系统进化树分析,其中NC_007201与菌株2亲缘关系最近,判定菌株2为烟曲霉菌属(图4)。
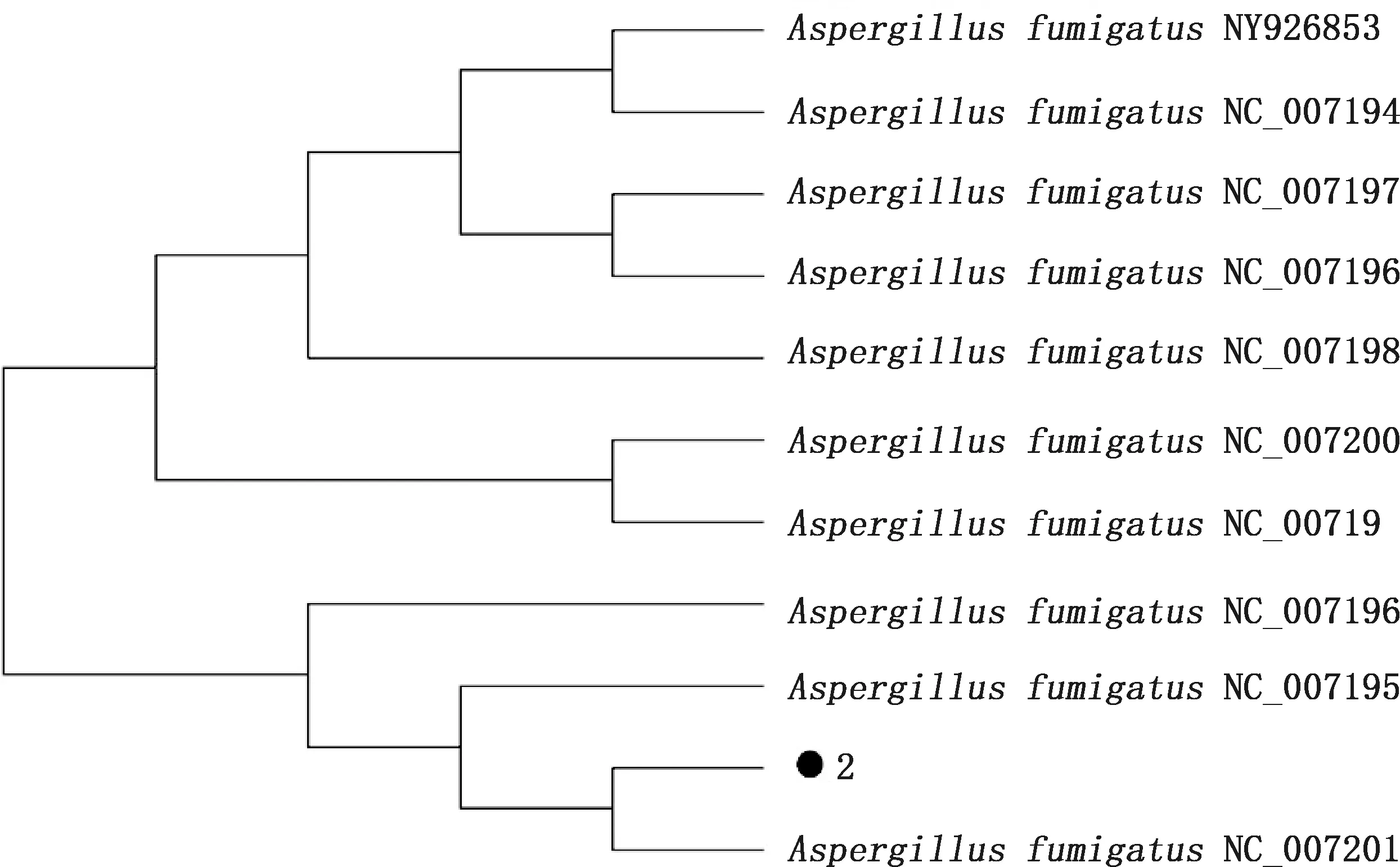
图4 菌株2系统进化树Fig.4 Phylogenetic tree of strain 2
2.3 动物回归试验结果
动物回归试验结束后对照组雏鸡反应灵敏,叫声洪亮,食欲旺盛,而试验组雏鸡呼吸困难,精神不振,站立不稳,羽毛蓬松,闭目嗜睡。剖检发现试验组雏鸡肝脏出现类似病鸭肺部灰白色结节,肝脏呈黄色,质地易碎呈豆腐渣样,肺脏肿大呈紫红色;组织学观察发现肝脏病变部位出现肉芽肿病变(图5B),在SDA培养基中将白色结节分离纯化后长出烟曲霉菌和黄曲霉菌。
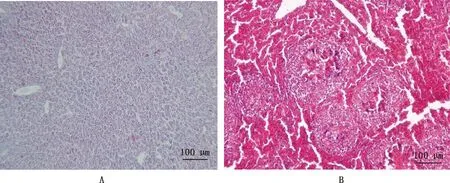
A,对照组;B,试验组A,Control group; B,Test group图5 肝脏组织病理学观察(20×)Fig.5 Histopathological observation of liver (20×)
2.4 MIC80测定结果
7种中药MIC80测定结果见表1,当石菖蒲MIC80≥8 μg/μL、黄柏MIC80≥16 μg/μL、决明子MIC80≥32 μg/μL、苦参MIC80≥64 μg/μL时测得烟曲霉菌的D630 nm值与阴性对照相比下降了80%以上,当石菖蒲MIC80≥8 μg/μL、决明子MIC80≥16 μg/μL、黄柏MIC80≥32 μg/μL、苦参和辣蓼MIC80≥64 μg/μL时测得黄曲霉菌的D630 nm0值与阴性对照相比下降了80%以上,而白头翁和蒲公英MIC80≥128 μg/μL,可见石菖蒲、黄柏和决明子对烟曲霉菌和黄曲霉菌的生长具有较强的抑制作用,而苦参、辣蓼、白头翁和蒲公英对其生长无显著抑制作用。

表1 中药MIC80测定结果
2.5 烟曲霉菌药敏试验结果
由表2和图6、7可知,中药液浓度为128 μg/μL的培养基培养72 h,石菖蒲和黄柏中无菌落长出,决明子中长出25.5个菌落,直径为4 mm;而苦参长出28.5个菌落,直径为5 mm,辣蓼长出21.0个菌落,直径为9 mm;白头翁长出24.5个菌落,直径为17 mm;蒲公英长出16.5个菌落,直径为18 mm。培养基中石菖蒲浓度为16 μg/μL时长出20.0个菌落,黄柏浓度为32 μg/μL时长出34.0个菌落。可见石菖蒲对烟曲霉菌的生长具有较强的抑制作用,其次是黄柏和决明子的抑制作用显著。
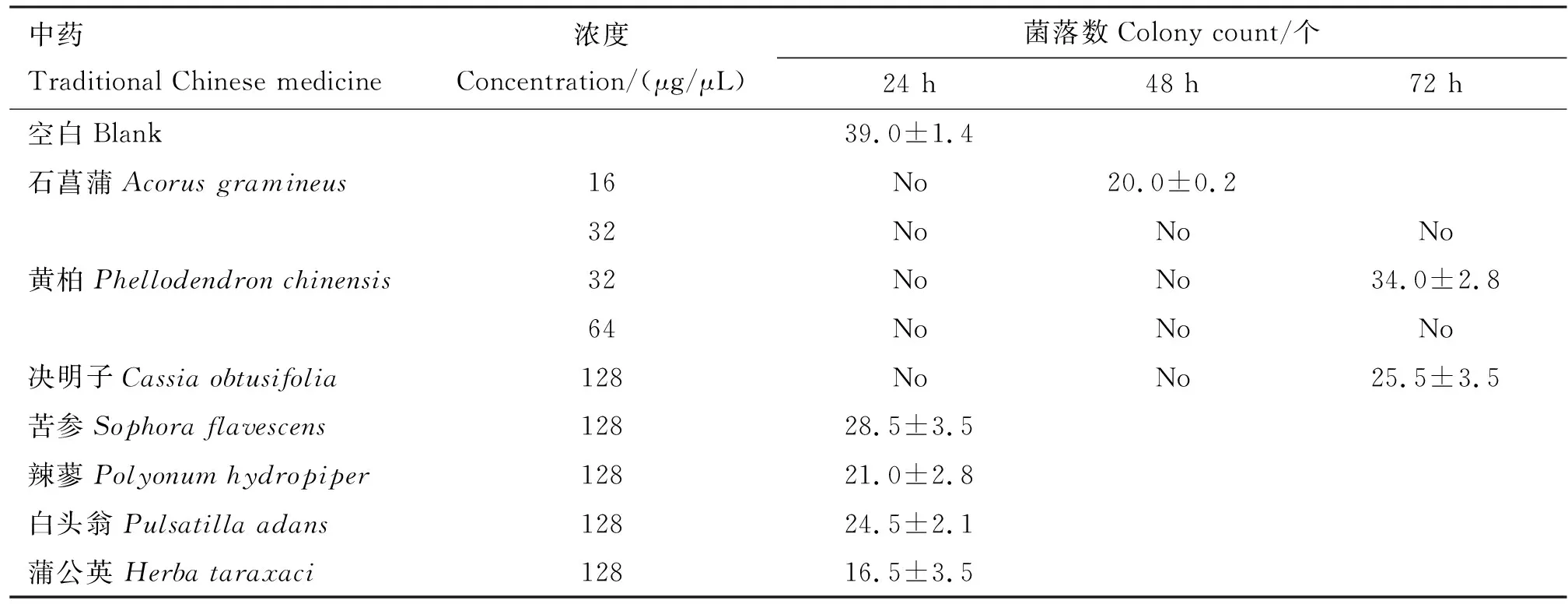
表2 不同中药浓度培养基中烟曲霉菌的生长情况
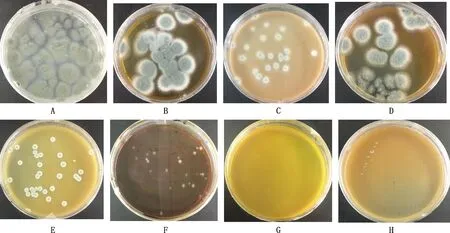
A,空白;B,蒲公英;C,辣蓼;D,白头翁;E,苦参;F,决明子;G,黄柏;H,石菖蒲A,Blank;B,Herba taraxaci;C,Polyonum hydropiper;D,Pulsatilla adans;E,Sophora flavescens;F,Cassia obtusifolia;G,Phellodendron chinensis;H,Acorus gramineus图6 烟曲霉菌在浓度为128 μg/μL的中药培养基中培养72 h的生长状态Fig.6 Growth status of Aspergillus fumigatus cultured in traditional Chinese medicine medium with a concentration of 128 μg/μL for 72 h
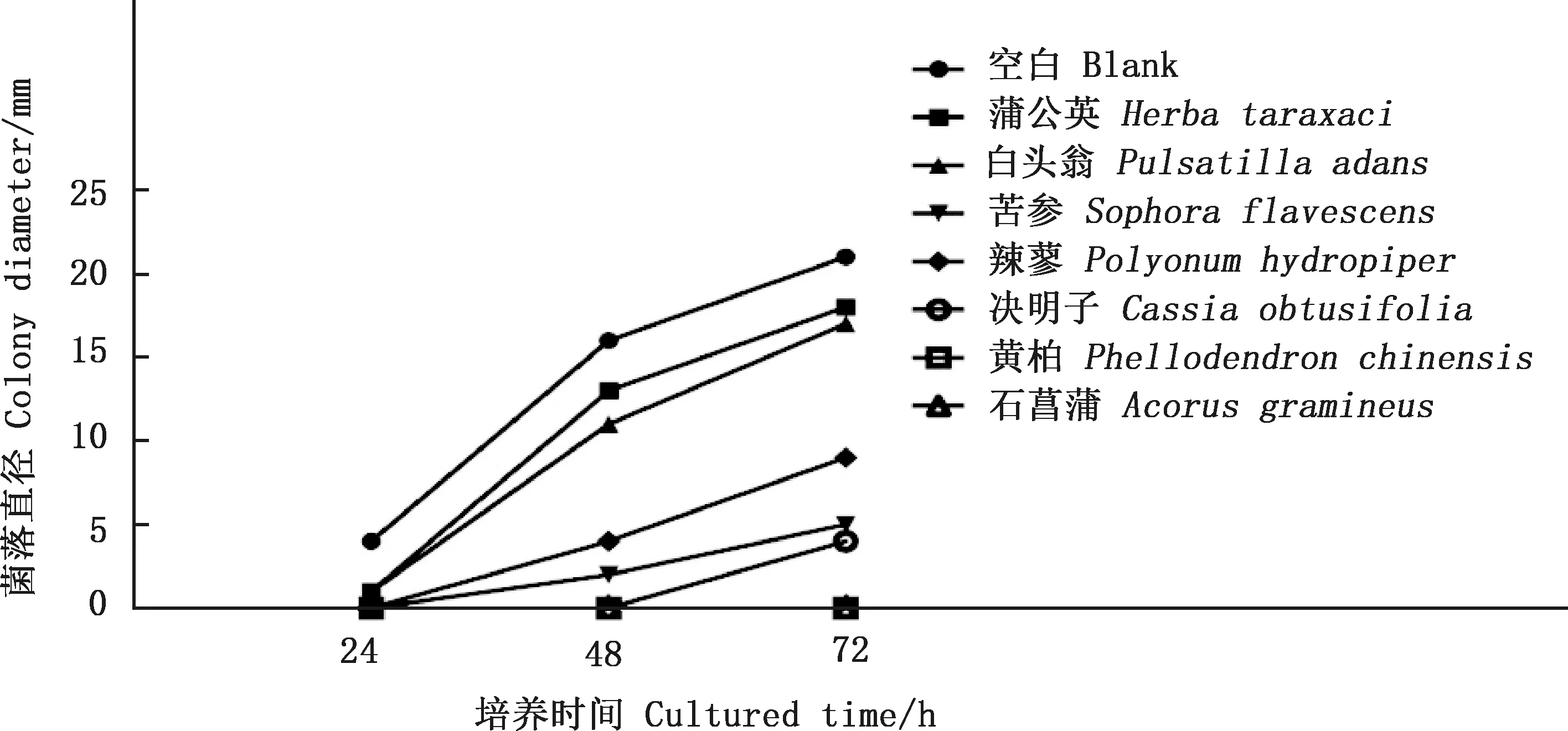
图7 烟曲霉菌在浓度为128 μg/μL的中药培养基中培养72 h的菌落直径Fig.7 Colony diameter of Aspergillus fumigatus cultured in traditional Chinese medicine medium with a concentration of 128 μg/μL for 72 h
2.6 黄曲霉菌药敏试验结果
由表3和图8、9可知,中药浓度为128 μg/μL的培养基培养72 h,石菖蒲和决明子中无菌落长出,黄柏中长出34.5个菌落,直径为2 mm;而苦参长出41.5个菌落,直径为7 mm,辣蓼长出40.0个菌落,直径为6 mm;白头翁长出44.5个菌落,直径为9 mm;蒲公英长出37.5个菌落,直径为16 mm。培养基中石菖蒲浓度为16 μg/μL时长出34个菌落,决明子浓度为32μg/μL时长出31.5个菌落。可见石菖蒲、决明子和黄柏对黄曲霉菌的生长具有较强的抑制作用,其中石菖蒲的抑制作用最为显著。
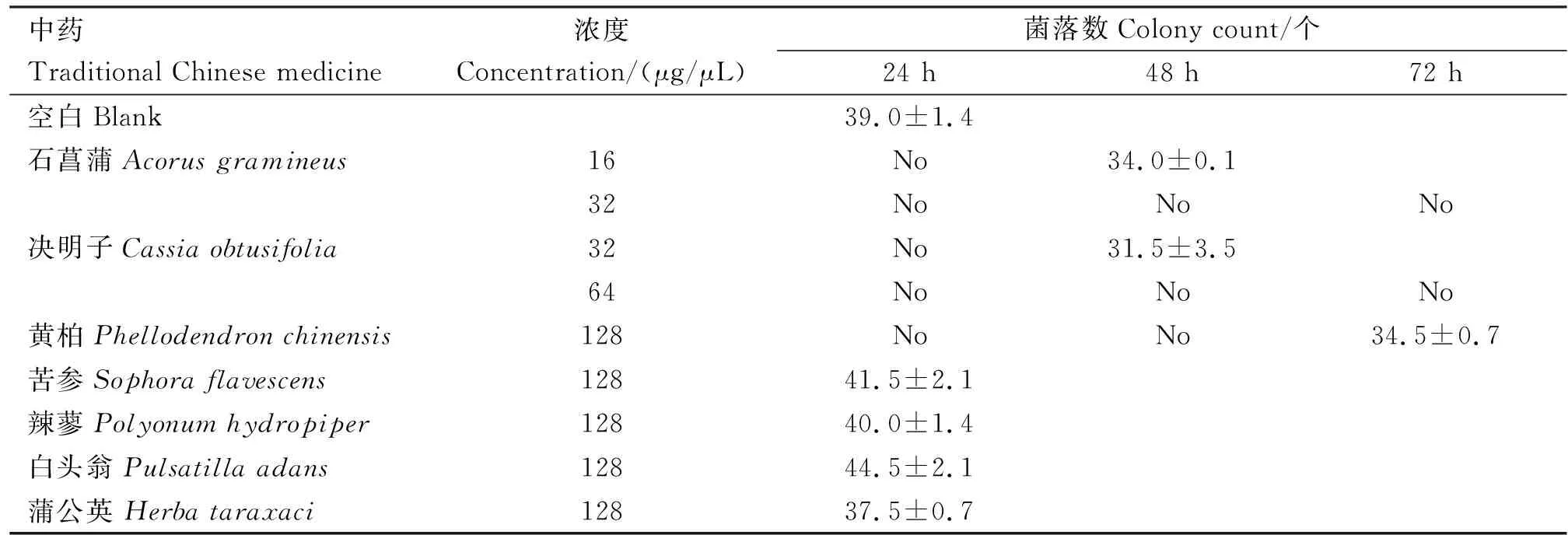
表3 不同中药浓度培养基中黄曲霉菌的生长情况
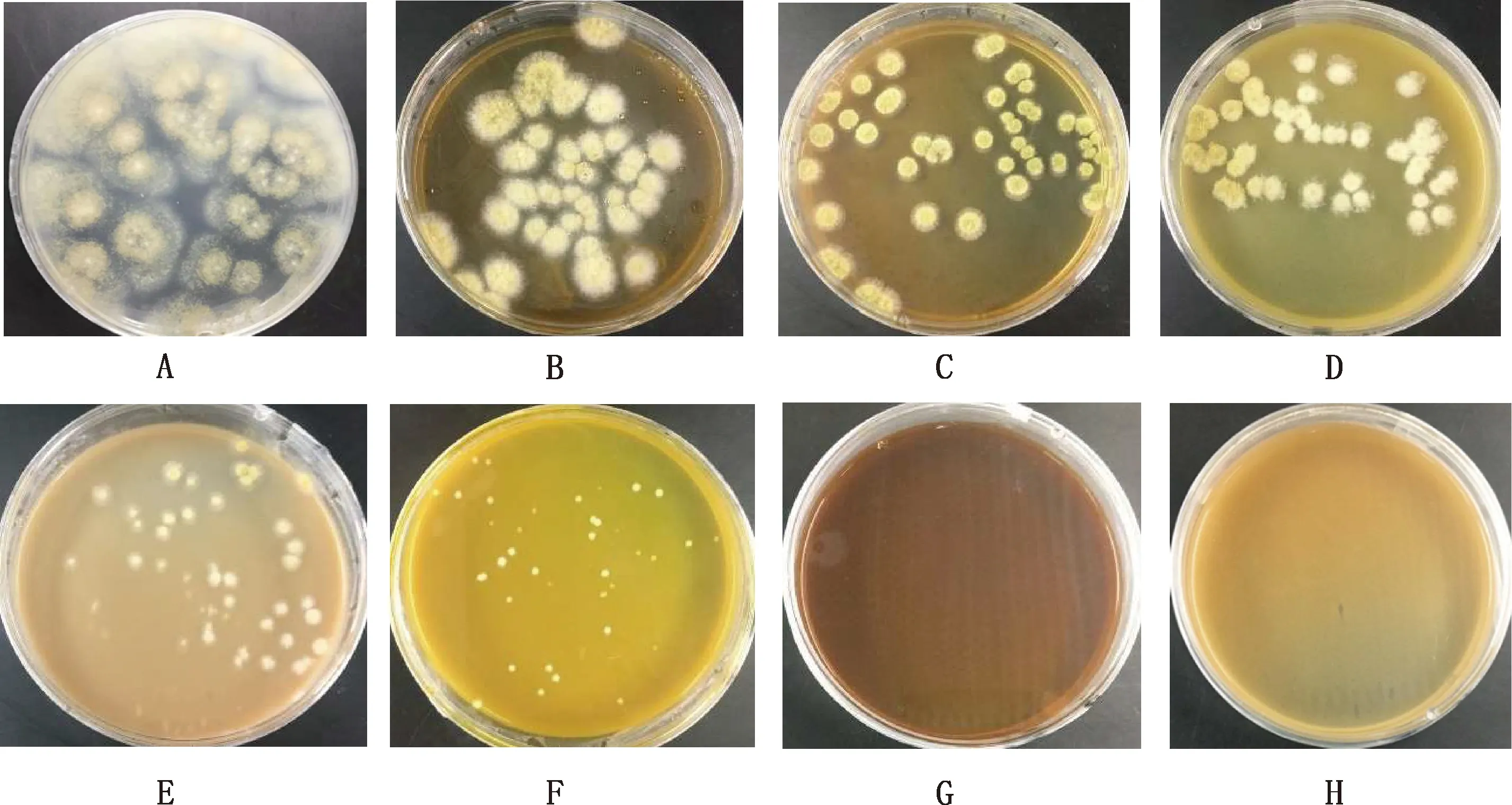
A,空白;B,蒲公英;C,白头翁;D,苦参;E,辣蓼;F,黄柏;G,决明子;H,石菖蒲A,Blank;B,Herba taraxaci;C,Pulsatilla adans;D,Sophora flavescens;E,Polyonum hydropiper;F,Phellodendron chinensis;G,Cassia obtusifolia;H,Acorus gramineus图8 黄曲霉菌在浓度为128 μg/μL的中药培养基中培养72 h的生长状态Fig.8 Growth status of Aspergillus flavus cultured in traditional Chinese medicine medium with a concentration of 128 μg/μL for 72 h
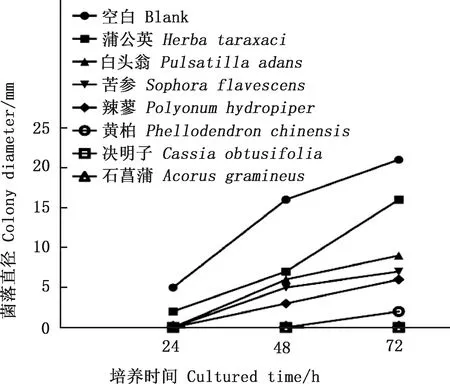
图9 黄曲霉菌在浓度为128 μg/μL的中药培养基中培养72 h的菌落直径Fig.9 Colony diameter of Aspergillus flavus cultured in traditional Chinese medicine medium with a concentration of 128 μg/μL for 72 h
3 讨 论
家禽生产受到多种真菌病的影响,包括曲霉菌病、念珠菌病、黄霉病、毛霉菌病、组织胞浆菌病和隐球菌病,在这些真菌疾病中,曲霉菌病和念珠菌病最为突出。曲霉病是由烟曲霉菌和黄曲霉菌引起的真菌感染,也是重要的空气传播腐生真菌[15]。临床上经常使用唑类和抗生素类抗真菌药物治疗曲霉菌感染,但随着上述药物长期的推广应用,不仅有副作用且易使机体易产生耐药性[16],故寻找天然无残留抗真菌药物具有重要意义。本试验从临床病鸭肺部分离出2种不同形态的霉菌,通过形态学分析发现其菌落颜色形态与黄曲霉菌和烟曲霉菌菌落形态类似,经ITS分子鉴定和相似性比对,确定2种病原菌为黄曲霉菌属和烟曲霉菌属,采用ITS片段鉴定真菌是一种简单、快速、经济有效的方法。ITS保守型在种内相对一致,不同种间差异明显,可反映种间甚至菌株之间的差异[17]。在显微镜下观察烟曲霉菌和黄曲霉菌菌丝,可观察到成熟分生孢子。现有研究表明,黄曲霉菌丝的分生孢子为两层小梗,烟曲霉菌丝的分生孢子为单层小梗[18-19]。此外,黄曲霉菌和烟曲霉菌通过分生孢子启动高度极化的生长过程,导致机体侵袭性感染[20],尤其1~3周龄雏鸭对霉菌极为敏感,常为群发,死亡率极高[21]。
在家禽养殖行业霉菌污染一直是难以避免的问题,黄曲霉菌和烟曲霉菌对不同阶段动物的致病性不同,雏鸭极为敏感,而养殖业中鸡的养殖比重远超过鸭,且黄曲霉菌和烟曲霉菌是经呼吸系统感染的急性或慢性疾病,可造成全身性感染[22],故本试验经鼻腔涂抹病原菌使雏鸡感染,探究从病鸭肺部分离的黄曲霉菌和烟曲霉菌对雏鸡是否具有致病性。结果发现雏鸡出现明显类似病鸭的症状,食欲减退,精神不佳,站立不稳,肝脏和肺脏出现病变,镜检可见病变部位有明显的肉芽肿病变。肉芽肿是由于各种病原体感染导致巨噬细胞浸润所致,是霉菌感染的典型症状[23],由此可见从病鸭肺部分离出的黄曲霉菌和烟曲霉菌对雏鸡也具有致病性。超声提取技术是近年来提取中药有效成分的新工艺之一,可瞬时破坏药材细胞壁,增强溶剂渗透至细胞内部,进而增强中药活性成分在溶剂中的溶出,可提高提取率、节省药材与溶剂、缩短提取时间,适用于绝大多数中药有效成分的提取[24],中药的有效成分为有机物,易溶于乙醇[25],因此,本研究采用超声波乙醇提取法粗提中药液,对黄曲霉菌和烟曲霉菌进行体外药敏试验。
中药毒性小,不易产生耐药性,多种活性成分共同发挥作用[26]。培养基体外药敏试验可直观探究中药液对黄曲霉菌和烟曲霉菌生长的抑制作用。黄曲霉菌和烟曲霉菌在SDA培养基中生长最快,故选用SDA培养基进行药敏试验。直至石菖蒲浓度降为16 μg/μL时,培养基才长出黄曲霉和烟曲霉菌落,决明子浓度降为32 μg/μL时才长出黄曲霉菌菌落,黄柏浓度降为32 μg/μL时才长出烟曲霉菌菌落,可见石菖蒲对黄曲霉菌和烟曲霉菌的抑制作用最强。石菖蒲中挥发油活性成分α-细辛酮和阿卡塔酮C协同抗真菌,对白色念珠菌也具有较强的抑制作用[27],且对金黄色葡萄球菌、表皮葡萄球菌、乙型溶血性链球菌、幽门螺杆菌、白假丝酵母菌、大肠埃希菌和痢疾杆菌也具有抑制作用[28],石菖蒲对黄曲霉菌和烟曲霉菌的抑制作用是否是挥发油活性成分发挥作用有待进一步研究。黄柏和决明子对烟曲霉菌和黄曲霉菌的抑制作用较为显著。研究显示,黄柏中的生物碱具有一定的抑菌作用,其中小檗碱可在一定程度上减少菌群[29],决明子对植物病原菌也具有抑制作用[30]。而在苦参、辣蓼、白头翁和蒲公英浓度为128 μg/μL的培养基中就已长出黄曲霉菌和烟曲霉菌的菌落,因此,苦参、辣蓼、白头翁和蒲公英对黄曲霉菌和烟曲霉菌的抑制作用不显著。 研究显示,苦参对白色念珠菌等有抑制作用[31],辣蓼对致病性大肠杆菌等有抑制作用[32],白头翁对大肠杆菌和金黄色葡萄球菌等有抑制作用[33],蒲公英对枯草杆菌和金黄色葡萄球菌等有抑制作用[34]。综上,石菖蒲、黄柏和决明子对黄曲霉菌和烟曲霉菌有显著的抑制作用,其中石菖蒲的抑制性最为显著,而3种中药的抑菌机制有待进一步研究。
4 结 论
石菖蒲、黄柏和决明子对禽源烟曲霉菌和黄曲霉菌有较强的抑制作用,其中石菖蒲的抑制作用最强,而苦参、辣蓼、白头翁、蒲公英对禽源烟曲霉菌和黄曲霉菌无明显抑制作用,本试验为动物健康和食品抗真菌药物的生产提供了新思路。
