基于高分辨质谱库和特征组分诊断比值法鉴别配制酒和代用茶中非法添加补骨脂
2022-02-13吴婉琴刘国姣
高 芳 吴婉琴 王 彬 刘国姣 江 丰
(1. 湖北省食品质量安全监督检验研究院,湖北 武汉 430075;2. 湖北省食品质量安全检测工程技术研究中心,湖北 武汉 430075)
补骨脂为豆科植物补骨脂的干燥成熟果实,主要产地有四川、云南、安徽、广西等地[1]。补骨脂中含有香豆素类、黄酮类、单萜酚类、拟雌内酯类等多种化学成分[2-4],是一味具有较高关注度的药材。现已发现,补骨脂中的补骨脂苷、异补骨脂苷、补骨脂素和异补骨脂素均有肝毒性,补骨脂酚具有肾毒性,其中一些补骨脂提取物还具有胚胎毒性[5-8],因此其在药物制剂和保健食品中的使用也受到一定的限制。中国《食品安全法》第三十八条明确规定“生产经营的食品中不得添加药品,但是可以添加按照传统既是食品又是中药材的物质”。2018年卫健委公布的可用于保健食品的中药名单中包含补骨脂,但未将其列入可用于食品中的中药材名单中。一些不法商家仅看到其临床的药用价值,非法在市售的酒和代用茶等普通食品中添加补骨脂。
现有的中药材非法添加鉴别手段,主要有薄层鉴别[9]、DNA条形码分子鉴定[10]、中药材特征图谱或指纹图谱鉴定[11-12]等方法,由于食品种类的多样性及其本身基质的复杂性,在食品中通过各种加工工艺掺入的中药材,其指纹图谱及特征图谱均有较大的改变,而现有的中药材鉴别手段一般只适用于中药材原料本身,对于在食品中非法加入的中药材并不能起到很好的鉴别作用。已有的补骨脂中药材研究[13-15]均只限于其药理活性、药材指纹图谱、化学组成成分及其含量的测定,尚未见有对其非法添加到食品的报道。诊断比值(Diagnostic ratio,DR)是指样品中某些特定组分之间的比值,能够表征不同样品各自的化学组成,用于判别两个样品是否一致。其特征是有独特性和差异性,基本不受外界因素影响或受外界因素影响较小。目前主要运用于化学品溯源鉴别[16-17]、医学疾病诊断[18]等领域,而在食品中中药材鉴别方面还鲜有报道。将中药材特征组分诊断比值法用于食品中非法添加中药材的鉴别,可以使分析者在不依赖特征组分指纹图谱库的情况下进行食品中中药材鉴别,极大限度地缩短鉴别时间,降低鉴别的复杂性。
为了建立一种简单易行且可靠的鉴别食品中非法添加补骨脂中药材的方法,采用高效液相色谱—四极杆—飞行时间质谱仪建立补骨脂中药材特征组分筛查库,再选取补骨脂的13种特征成分(补骨脂苷、异补骨脂苷、补骨脂素、异补骨脂素、异补骨脂二氢黄酮、补骨脂二氢黄酮、新补骨脂异黄酮、补骨脂宁、补骨脂苷二氢黄酮甲醚、补骨脂定、Corylifol A、补骨脂查尔酮和补骨脂酚)为考察对象,选取常见易非法添加中药材的配制酒和代用茶为研究对象,于高效液相色谱探索出基于特征组分的诊断比值法确证配制酒和代用茶中违法添加补骨脂中药材的鉴定技术,构建配制酒和代用茶中非法补骨脂确证技术体系,旨在为配制酒和代用茶中补骨脂中药材非法添加的科学监管提供有效的技术支撑。
1 材料与方法
1.1 材料与仪器
1.1.1 材料与试剂
补骨脂中药材(采用粉碎机进行粉碎处理后过二号筛得补骨脂粗粉,置于密封袋中,20批次补骨脂中药材编号为S1-S20,样品的具体信息见表1):市售;

表1 样品信息
20批次配制酒:市售;
10批次代用茶:市售;
补骨脂标准中药材:中国食品药品检定研究院;
补骨脂苷、异补骨脂苷、补骨脂素、异补骨脂素、异补骨脂二氢黄酮、补骨脂二氢黄酮、新补骨脂异黄酮、补骨脂宁、补骨脂苷二氢黄酮甲醚、补骨脂定、Corylifol A、补骨脂查尔酮和补骨脂酚:纯度≥98%,上海源叶生物技术有限公司;
乙腈:色谱纯,德国Merck公司;
磷酸:分析纯,国药集团化学试剂有限公司;
超纯水:电阻率为18.2 MΩ·cm(25 ℃),美国 Millipore公司。
1.1.2 主要仪器
高效液相色谱仪:Ultimate 3000型,美国Thermo公司;
串联四极杆质谱仪:AB Sciex TOF 5600+型,配备Analyst 1.6工作站、Peak View定性筛查软件、Library View数据库软件,美国SCIEX公司;
高效液相色谱仪:Waters e2695型,美国Waters公司;
光电二极管阵列检测器:Waters 2998型,美国Waters公司;
离心机:Allegra X-15R型,美国Beckman公司;
超声波清洗器:EDAA-2600T型,上海安谱科学仪器有限公司;
分析天平:ME2002E型,梅特勒—托利多国际贸易上海有限公司。
1.2 试验方法
1.2.1 仪器分析条件
(1) HPLC-TOF-MS分析条件:色谱柱为Thermo Accucore aQ色谱柱(150 mm×2.1 mm,2.6 μm);柱温35 ℃;进样量5 μL;流动相A为乙腈,流动相B为0.1%甲酸水溶液,梯度见表2。

表2 流动相梯度程序
(2) TOF/MS工作条件:离子源为电喷雾离子源;正离子扫描模式;电喷雾电压5 500 V;离子源温度550 ℃;气帘气241 kPa;雾化气379 kPa;辅助气379 kPa;去簇电压60 V;碰撞能量35 V;扫描方式采用全扫描一级质谱,质量采集范围100~1 000 Da;全扫描二级质谱,质量采集范围50~1 000 Da。质量数校正液为10 mmol/L甲酸钠溶液。
(3) TOF/MS筛查高分辨质谱库筛查条件:鉴别参数设置:化合物提取离子流响应强度>100或信噪比S/N>5,母离子精确分子量和二级碎片质量数偏差设为±0.001%,保留时间偏差±2.5%;数据库综合得分设置:质量数偏差、保留时间偏差、同位素比值、分子式匹配、数据库匹配占比均设为20%。
(4) HPLC分析条件:色谱柱为Waters Symmetry Shield C18柱(250 mm×4.6 mm,5 μm);柱温 30 ℃;检测波长246 nm;进样量10 μL;流动相 A为乙腈;流动相 B为0.05% 磷酸水溶液,梯度见表3。
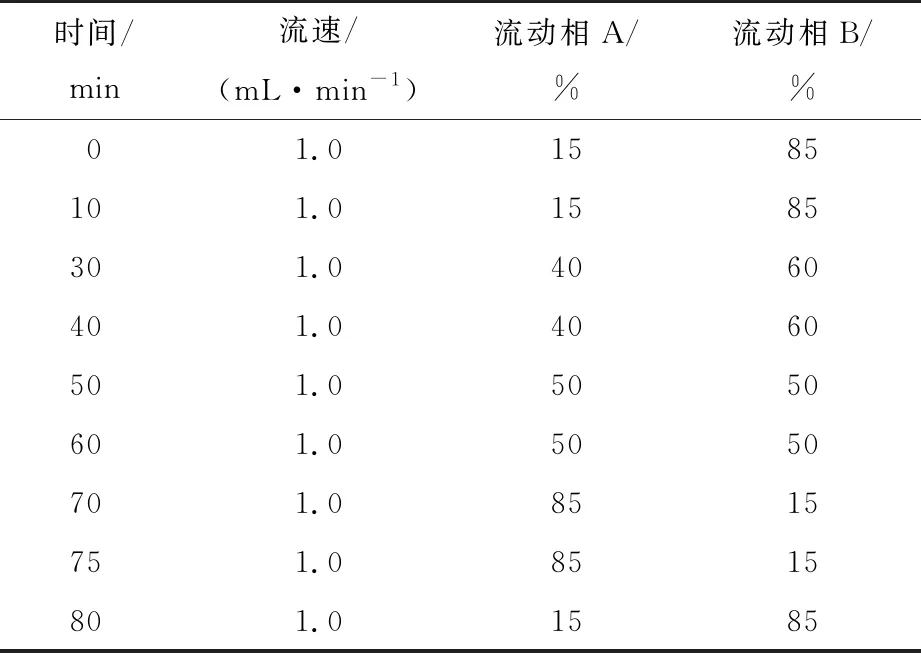
表3 流动相梯度程序
1.2.2 溶液的制备
(1) 标准储备液:准确称取补骨脂苷、异补骨脂苷、补骨脂素、异补骨脂素、异补骨脂二氢黄酮、补骨脂二氢黄酮、新补骨脂异黄酮、补骨脂宁、补骨脂苷二氢黄酮甲醚、补骨脂定、Corylifol A、补骨脂查尔酮和补骨脂酚标准品适量于10 mL容量瓶,用甲醇稀释并定容,分别得到质量浓度均为1.0 mg/mL标准储备液。
(2) 标准工作溶液:分别准确移取上述13种标准储备液,用甲醇稀释,配制成质量浓度均为0.05 mg/mL的混合标准溶液,置于4 ℃环境中冷藏避光保存。
(3) 标准中药材溶液:准确称取标准补骨脂中药材适量,用50%甲醇水溶液提取超声,浸提24 h以上,稀释后上清液过0.22 μm有机系微孔滤膜,供高效液相色谱—四极杆—飞行时间质谱仪和高效液相色谱仪检测用。
(4) 模拟补骨脂酒的制备及前处理:称取补骨脂中药材1 g(精确至0.01 g)置于棕色广口瓶中,准确加入50 mL 50%乙醇水溶液,超声30 min,取出放至室温,浸提24 h以上。取上清液过0.22 μm有机系微孔滤膜,供高效液相色谱仪检测用。
(5) 模拟补骨脂代用茶的制备及前处理:称取补骨脂中药材1 g(精确至0.01 g)置于具塞离心管中,准确加入50%甲醇水溶液,超声30 min,取出放至室温,于4 000 r/min 离心5 min。取上清液过0.22 μm有机系微孔滤膜,供高效液相色谱仪检测用。
(6) 配制酒:取适量样品,于4 000 r/min离心5 min,过0.22 μm有机系微孔滤膜,供高效液相色谱—四极杆—飞行时间质谱仪和高效液相色谱仪检测用。
(7) 代用茶:准确称取2 g(精确至0.01 g)样品置于具塞离心管中,准确加入50 mL 50%乙醇水溶液,超声30 min,取出放至室温,于4 000 r/min离心5 min。取上清液过0.22 μm有机系微孔滤膜,供高效液相色谱—四极杆—飞行时间质谱仪和高效液相色谱仪检测用。
2 结果与分析
2.1 补骨脂中特征化学组分筛查库的建立
正离子扫描模式下,比较考察了乙腈—5 mmol/L乙酸铵和乙腈—0.1%甲酸2种流动相体系,部分化合物在乙腈—5 mmol/L乙酸铵流动相体系下峰形不佳出现拖尾现象,且峰响应较差,故选择乙腈—0.1%甲酸流动相体系进行分析。为得到更全面的质谱数据信息,设定全扫描一级质谱,质量采集范围100~1 000 Da,全扫描二级质谱,质量采集范围50~1 000 Da。优化HPLC-TOF-MS条件下补骨脂标准中药材中提取得到的13种特征组分精确离子质量分数见表4,同分异构体按照对照品出峰先后顺序定位,根据分辨质谱所得到的化合物质谱参数可用于初步筛查食品中的补骨脂药材。

表4 补骨脂特征组分信息表
2.2 特征组分的选择
上述优化的HPLC色谱条件,补骨脂中13种特征组分能够得到较好的分离,其混合标准品溶液色谱图见图1(a),自采模拟的补骨脂酒和代用茶溶液色谱图见图1(b),将该色谱条件下得到的20批模拟的补骨脂酒和代用茶中13种特征组分的峰面积分别进行数据分析,根据诊断比值法的定义选择样品特征组分色谱峰的面积比值来分析,共有91种诊断比值的组合,但是由于所采购的补骨脂中药材产地和采摘时间,其掺加比例和提取过程、化合物本身性质等不同,所得到的各特征组分含量有很大的差异,优先考虑其中含量较高的特征成分,在补骨脂标准药材中补骨脂苷、异补骨脂苷、补骨脂素、异补骨脂素、新补骨脂异黄酮、补骨脂二氢黄酮甲醚、Corylifol A和补骨脂酚都是含量较高的组分,考虑特征成分的稳定性,包括受外界环境因素、时间和杂质的干扰,其中补骨脂苷和异补骨脂苷受时间影响含量变化较大,同时考虑到阳性样品中能检测出的特征成分,结果从中选出各种因素影响较小,其诊断比值数值范围较为集中的2组,即1 CoryliA/补骨脂酚(DR1)和补骨脂素/异补骨脂素(DR2),模拟酒样品中DR1数值集中在0.069~0.115,DR2数值集中在1.14~1.63,模拟代用茶样品中DR1数值集中在0.061~0.101,DR2数值集中在1.24~1.68,其数值RSD均小于20%,具体诊断比值数据结果见表5 。

1. 补骨脂苷 2. 异补骨脂苷 3. 补骨脂素 4. 异补骨脂素 5. 异补骨脂二氢黄酮 6. 补骨脂二氢黄酮 7. 新补骨脂异黄酮 8. 补骨脂宁 9. 补骨脂苷二氢黄酮甲醚 10. 补骨脂定 11. Corylifols A 12. 补骨脂查尔酮 13. 补骨脂酚
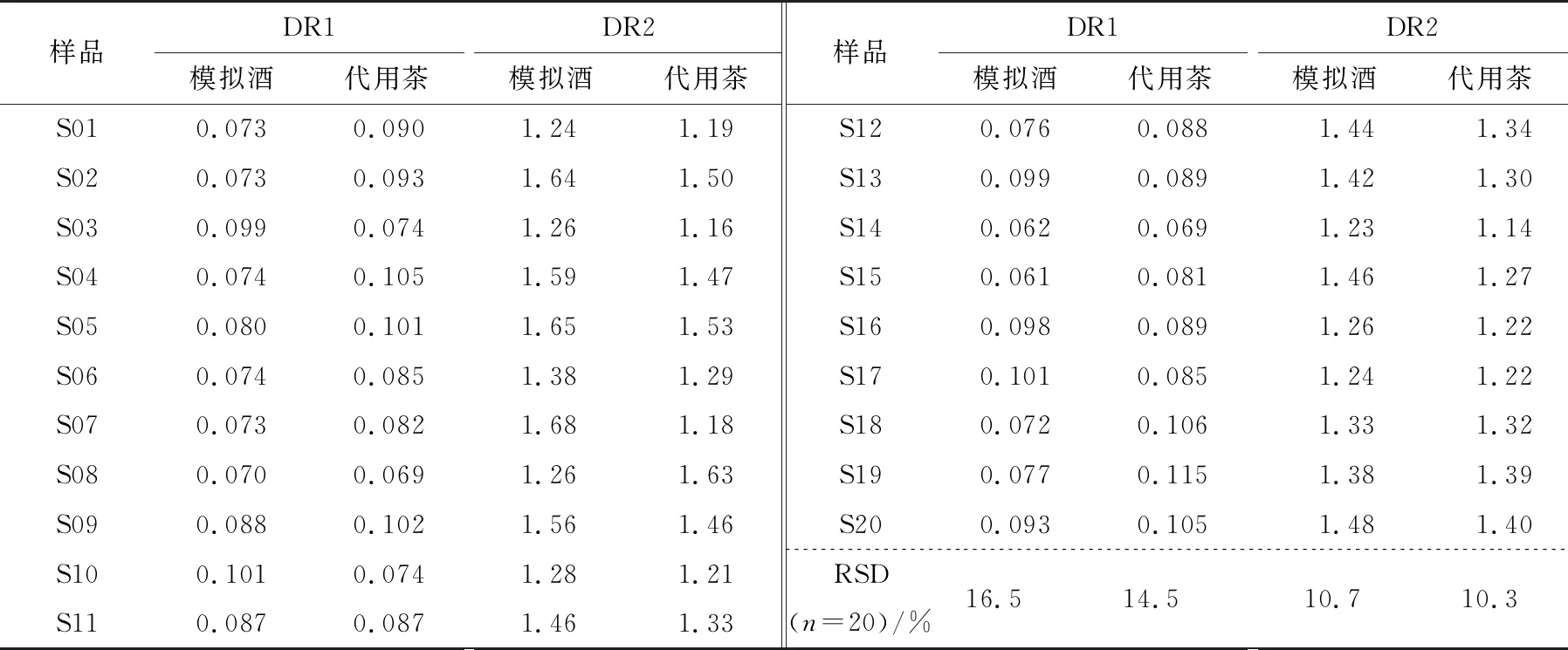
表5 20批次补骨脂中药材模拟酒和代用茶的特征组分诊断比值
2.3 不同食品基质间诊断比值显著性差异分析
采用SPSS 21.0统计学软件对选定的模拟配制酒和代用茶食品的2组诊断比值DR1和DR2进行显著性差异分析,结果显示(见表6):2种食品基质间各组诊断比值均无显著性差异(P>0.05),表明所选的2组诊断比值具有一定的稳定性,不受样品基质、加工工艺和提取溶剂的干扰,可用于不同食品基质中补骨脂中药材的鉴别。

表6 配制酒和代用茶食品的诊断比值方差分析
2.4 诊断比值非异常范围的确定
显著性差异分析显示2组诊断比值于不同基质间均无显著性差异,为更全面统一地对不同食品中补骨脂进行鉴别,使方法具有一定的通用性,考虑将2种不同基质的各诊断比值进行合并,进行箱图绘制如图2,确定各比值非异常值范围,诊断比值DR1范围为0.061~0.115,诊断比值DR2范围为1.14~1.68。
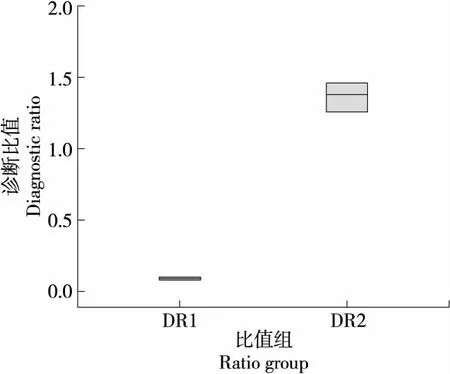
图2 食品中补骨脂中药材的诊断比值箱线图
2.5 基于诊断比值法对实际样品的检测
采用建立的方法对市售20批次配制酒和10批次代用茶样品进行高分辨质谱库分析筛查及诊断比值法鉴别,其中4批次的配制酒高分辨数据均与自建质谱库13种特征组分匹配一致,均为标签标注含补骨脂的药酒,其样品中补骨脂酚与标准品补骨脂酚碎片离子镜像图如图3所示,样品中Corylifols A与标准品Corylifols A碎片离子镜像图如图4所示,补骨脂素与标准品补骨脂素碎片离子镜像图如图5所示,异补骨脂素与标准品异补骨脂素碎片离子镜像图如图6所示,说明所建的高分辨质谱库能够快速地筛查出食品中非法添加的补骨脂,同时进液相色谱分析,采用特征组分峰面积诊断比值法对样品进行进一步确证。其色谱图见图1(c),得到的4组阳性样品诊断比值结果见表7,其诊断比值DR1和DR2均在上述绘制箱图确定的非异常值范围内,证明该4批次配制酒样品中确实含有补骨脂中药材。
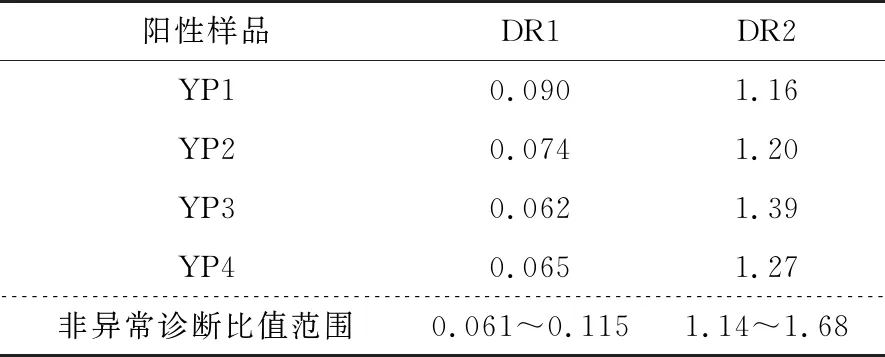
表7 阳性样品的特征组分诊断比值

上半部分为配制酒样品,下半部分为标准品
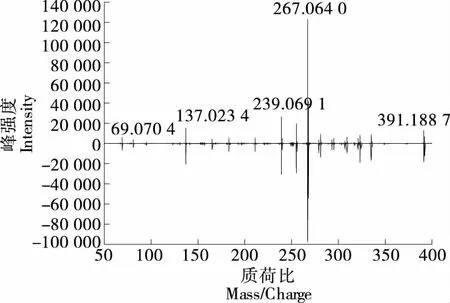
上半部分为配制酒样品,下半部分为标准品

上半部分为配制酒样品,下半部分为标准品

上半部分为配制酒样品,下半部分为标准品
3 结论
研究开发出一种基于高分辨质谱库和特征组分诊断比值法快速筛查鉴别配制酒和代用茶中非法添加补骨脂中药材的方法,选取11种特征组分构建高分辨质谱库进行初步筛查,最终确定稳定性较好的CoryliA/补骨脂酚(DR1)和补骨脂素/异补骨脂素(DR2)2组诊断比值作为鉴别依据,并考察了特征比值在配制酒、代用茶叶中的显著性差异,确定了2组诊断比值的非异常范围,构建了配制酒和代用茶中补骨脂中药材确证技术体系。该方法简单高效,适用于配制酒和代用茶中补骨脂中药材的检测。
