化学链重整制氢NiO-CeO2/γ-Al2O3复合载氧体的性能
2022-02-12韩丹华郭雪岩王志远
韩丹华,郭雪岩,王志远
(上海理工大学能源与动力工程学院,上海 200093)
目前,三分之二的世界能源需求是由石油和天然气燃料满足,这些不可再生能源正面临着枯竭,且化石燃料的燃烧对环境和健康带来了巨大的威胁,促使人们寻找合适的替代品“清洁燃料”。氢燃料作为一种新型无污染的清洁燃料以及绿色高效能源载体备受关注。但是,作为二次能源,它必须由其他能源产生。化学链技术在实现能源高效转化上具有独特优势。这种工艺主要包括空气反应器和燃料反应器,载氧体在两个反应器之间循环实现氧的转移,且燃烧温度比传统燃烧温度低,具有更高的能量利用效率。研究人员把化学链和制氢技术相结合形成一种新的制氢方法:甲烷化学链重整(chemical looping reforming,CLR)制氢,可以获得高浓度H,并且具有低成本、低能耗和流程简单等优点。CLR 制氢以甲烷为还原剂,在燃料反应中与水蒸气、氧化态载氧体(MeO)发生重整反应生成高浓度H和CO,而后失去晶格氧的载氧体(Me)在空气反应器中发生氧化反应回到氧化态(MeO),实现了燃料和空气零接触、低成本CO的收集以及氮氧化物零排放。其间发生的主要还原反应为式(1)和式(2),氧化反应为式(3)。

在化学链重整制氢过程中,载氧体起到关键的作用。化学链要实现工业领域应用,必然在高温下进行,在高温条件下载氧体参与甲烷水蒸气重整反应,产生氧离子和氧空位,并促进它们在体相中的扩散,被还原的金属在载氧体表面进一步催化甲烷和水蒸气制氢反应。目前,镍基载氧体因其高反应活性、低磨耗率而被广泛用于甲烷化学链蒸汽重整,但是有学者研究发现镍基载氧体会诱导甲烷裂解反应而产生积炭,积炭会引起反应管道压降增大,严重时会堵塞反应管从而出现局部管区过热、压力过大;积炭在空气反应器中燃烧生成CO,降低温室气体捕集效率。另外,积炭的氧化是强放热反应,会增加氧化过程载氧体表面温度,造成载氧体烧结。因此,目前镍基载氧体的性能远远不能满足大规模产氢要求,开发具有高携氧能力、高活性及稳定性、低积炭的载氧体具有十分重要的意义。
近年来,复合金属载氧体因其高晶格氧迁移率和高反应活性而受到普遍关注。有研究者研究钙钛矿型载氧体中晶格氧对化学链重整制氢的影响,通过实验发现复合载氧体中晶格氧的迁移率增大,并且载氧体在固定床实验中表现出更高的活性。具有立方结构的CeO碱性稀土材料是目前最具吸引力的氧化物之一,CeO属于等轴晶系面心立方结构,结构中有大量的八面体空位,可允许离子迅速扩散,当Ce被低价阳离子取代时,会因为电荷的不平衡,产生氧空位。并且CeO能在较宽的工作温度范围内迅速形成氧空位,具有较高的储氧能力。Zhu 等用沉淀法制备单金属CeO载氧体,通过10 个甲烷重整氧化还原实验发现,CeO本身作为活性物质,由于其活性较低,不能保持合成气和H的恒定产量。Tijani 等在载体氧化物CeO上沉积过渡金属(Cu、Co、Fe、Ni)为氧载体,探究活性位点与载体间的相互作用,发现载体氧化物的加入降低了金属的氧化和还原反应的活化能。其中Co/CeO样品在H气体还原性、氧容量和氧化还原反应活化能方面表现出较好的性能,表明在活性物质中加入CeO作为助剂在化学链实验中有进一步研究的潜力。Liu 等在化学链燃烧(chemical looping combustion,CLC)固定床装置上研究了CeO对铁基载氧体的还原和氧化过程中的反应性能的影响,结果表明CeO的加入不仅使得氧转移速率加快,而且提高了载氧体催化平均反应速率,同时发现固溶体中产生的氧空位能够通过空位扩散或空穴形成的氧通道将FeO体相氧快速转移到载氧体表面,参与非均相反应,抑制积炭产生。由此,制备复合金属载氧体时固溶体的形成可以有效增加非均相反应的进行。张军伟等用共沉淀法制备了CeO−FeO/AlO复合载氧体,通过XRD和SEM发现复合载氧体在经过多次循环后仍能保持良好的结晶度和分散度。Guerrero−Caballero 等在循环床反应器上对不同的氧化铈基氧载体进行比较研究,发现参与反应的甲烷逐渐增大时,生成碳的越多,该作者发现氧迁移率的提高并不总是有利的,增加的氧迁移率会促进甲烷的全氧化,产生大量的CO,不利于捕集,可见在制备复合载氧体时活性物质的混合比例至关重要。He 等发现掺杂过渡金属氧化物可以提高铈基载氧体的供氧能力和反应性。并且混合氧化物中双金属的比例对载氧剂的性能有明显影响,选择合适比例的载氧剂可以增加对H和CO的选择性。其中载体材料的选择对载氧体的性能起着至关重要的作用。目前用于工业的载氧体以γ−AlO载体为主,其具有一定的机械强度、几何表面积大、强吸附性等特点。Shadman−Yazdi等提出改变多孔载体内活性载氧体的分布,可改变载氧体性能。研究表明,多孔载氧体载体碱性位点是抑制碳沉积的理想载体,载氧体的碱基中心分布增加了CO的化学吸附,有利于CO和C 发生歧化反应,从而抑制碳沉积。
本文利用浸渍法制备NiO−CeO/γ−AlO复合型载氧体,考察Ni/Ce 质量比对载氧体微观结构形貌的影响。同时利用固定床反应器对复合载氧体用于化学链重整制氢过程的反应活性、稳定性及参与条件的影响进行分析研究。用XRD、SEM 对载氧体进行表征,分析载氧体表面结构与性能的关系。为开发一种高活性高性能载氧体提供理论依据。
1 材料和方法
1.1 载氧体的制备
采用浸渍法合成了不同Ni/Ce 质量比(分别为1∶0、3∶1、2∶1、1∶1、1∶2、1∶3 和0∶1) 复合载氧体NiO−CeO/γ −AlO。将计量的Ni(NO)·6HO、Ce(NO)·9HO溶于去离子水中,分别配成溶液,然后混合均匀,将γ−AlO载体放入配置好的溶液中浸渍6h,放入鼓风干燥箱中在120℃下干燥12h,最后置于马弗炉中800℃煅烧6h,多次重复上述步骤得到不同比例载氧体NiO−CeO/γ−AlO,不同Ni/Ce质量比载氧体中NiO的质量分数分别为15%、11.25%、10%、7.5%、5%、3.75%、0。
1.2 载氧体表征
采用日本理学Rigaku Ultimate Ⅳ型仪器进行载氧体的X 射线衍射(XRD)分析,测试条件Cu靶辐射(=0.154056nm),管电压40kV,管电流30mA,扫描范围10°~80°,步长0.02°,扫描速度5°/min。采用FEI Nova Nano 450型扫描电子显微镜(SEM)对载氧体样品截面内部进行形貌分析。在测试前样品经过喷金处理。
1.3 载氧体活性及稳定评价
载氧体在常压小型固定床反应器上进行测评,主要有温度控制、气流装置、集气装置等组成。反应器流程见图1。气相产物用离线气相色谱仪(NVI 2000)分析。反应管采用内径30mm、长度300mm 的不锈钢钢管。中间填充10cm 活性段,两侧填充惰性载体。反应温度设定为800℃并在N氛围下吹扫10min,待温度稳定后,通入空气预处理30min;切换气体,打开注射泵并同时通入50%CH/N混合气,用集气袋收集尾气,利用离线气相色谱(NVI2000)测定气体组成,恒温反应20min;随后N吹扫20min;切换空气吹扫20min;再次切换到N吹扫20min。上述步骤完成一次完整的循环实验。考察载氧体的循环稳定性时采用相同的实验步骤,共进行连续20次循环实验。其中,水碳比实验的方法是:甲烷的进气流量为1L/min,此刻体积空速为3442h,空气的进气流量为1L/min,通过改变注射泵水蒸气的进气流量来改变水碳比。

图1 甲烷化学链固定床反应流程
1.4 载氧体性能评价指标
本文选用CH转化率()、H选择性()、CO选择性()、CO选择性()、积炭率()评定载氧体的性能,计算如式(4)~式(8)。


2 结果与讨论
2.1 载氧体XRD表征
图2为不同比例下新鲜NiO−CeO/γ−AlO样品的XRD 图谱。谱图中载氧体的主要晶相为NiAlO(19°)、NiO (37.3°、45°)、CeO(28°、31.5°、47.4°、56°)、Ce−Ni (45.35°)、γ −AlO(34°、66.6°、76°、77°)(粉末衍射文件PDF71−1179)。从图中可以看出NiAlO衍射峰强度随着Ce 的增加变得越来越微弱,表明Ce 的加入在一定程度上可以抑制NiAlO的形成。图2(b)为40°~50°的局部XRD 图谱,其中,在45°主要晶相是NiO,随着铈的加入,在比例为3∶1 时,衍射峰角度发生了偏移,在45.35°检测到Ce−O−Ni固溶体,这表明有Ni进入到CeO中形成固溶体,并且衍射峰在衍射角度为47.4°的主要晶相为CeO时消失。通过谢乐公式计算样品的晶粒尺寸,载氧体晶粒粒径从12nm(15%∶0)下降至10.4nm(11.75%∶3.25%),后又增加到16.3nm(3.75%∶12.25%)。晶粒大小的变化和固溶体生成有关,在氧化镍中加入氧化铈,离子半径较小的Ni取代离子半径较大的Ce,产生晶格畸变,导致粒子半径减小。该结果与Gao 等研究的Ni−Co复合型载氧体的结果相似。

图2 不同Ni/Ce比载氧体的XRD图谱
2.2 固定床载氧体反应测试
CLR 反应性能评价结果见图3。可以看出氢气的体积分数和氢气的选择性随着铈的增加呈先增大后减小趋势,积炭的选择性先减小后增加,其中单金属氧化铈载氧体的制氢反应积炭选择性最高,这和氧化铈单独作为单金属载氧体时晶格氧的迁移速率低、活性不高有关。在镍铈比为3∶1 时,反应后H的体积分数和氢气的选择性最大,同时从折线图中可以看出积炭的选择性也低于其他四种载氧体,显然3∶1 复合载氧体表现出最好的综合性能。这种结果和镍铈复合载氧体形成固溶体有关,固溶体的存在增加了晶格氧的迁移速率,当表面氧被消耗时,体相氧会快速地补充氧空位,使有更多的活性物质参与化学链甲烷重整制氢反应,使反应物中氢气的体积分数增加。另一方面,足够的活性物质参与甲烷化学链重整制氢,可以抑制甲烷的裂解反应,避免了积炭引起的反应管堵塞现象。从图3也可以看出,除了低反应活性的氧化铈(0∶1载氧体),前四种载氧体的反应甲烷出口浓度差别不大,表明都可以实现较高的转化率;五种载氧体的二氧化碳产率比较接近且都很低,表明在固定床反应器中五种载氧体主要发生反应如式(1)。
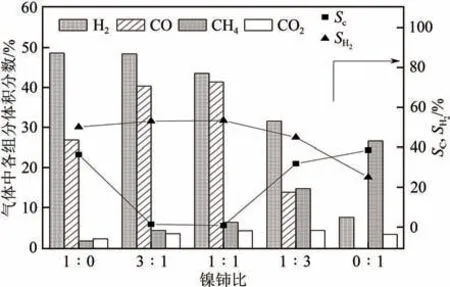
图3 不同镍铈比例载氧体活性测试
2.3 固定床载氧体稳定性测试
载氧体的再生能力是制约化学链重整制氢工艺稳定性的瓶颈,为了研究蒸汽加入对载氧体循环氧化还原活性的影响,本节在固定床实验室中对载氧体进行了评价,探究了五种载氧体在800℃下重整制氢的循环稳定性。见图4,随着循环次数的增加,单金属NiO载氧体对氢气的选择性呈下降趋势,对积炭的选择性很高,随着循环反应次数的增加,载氧体的再生能力下降,参与到反应的载氧体减少,甲烷偏向发生裂解反应产生积炭覆盖在载氧体表面,此时暴露更少的活性位点与甲烷水蒸气发生重整反应,对应的H选择性和CO选择性下降,这种结果和NiO具有较强的断裂C—C键的能力有关。比例为3∶1载氧体的循环稳定性高于其他四种,其平均H选择性和CH转化率维持在55.35%和88.38%,该比例下平均积炭率为10%,表明Ce 的加入改变了载氧体的性能,这和XRD 结果一致,一定比例的复合载氧体表现为对积炭有极大的耐受性。其中比例为1∶1和3∶1 载氧体在经过20 次循环后的H和CH转换率高于其他三种载氧体,但是比例1∶1 时经过多次循环积炭的选择性上升。Ni∶Ce比为1∶3时对CO的选择性很低,并且随着循环的进行对C的选择性呈上升趋势,可以发现过多的CeO加入会使载氧体的活性下降。在5~12 循环反应过程中,单金属CeO的H选择性呈上升趋势,此过程和CeO本身具备一定的储放氧能力有关,随着反应的进行,在发生氧化反应过程中氧气进入晶粒中,晶格氧数量提高,提高了载氧体性能,在经过12 个循环后性能开始下降;在图中可以观察到单金属CeO对CO的选择性和积炭的选择性先上升后下降。

图4 20次循环反应在不同镍铈比样品上的气体选择性
2.4 载氧体SEM结果分析
图5为不同比例载氧体反应前后在100k放大倍数下的SEM对比图像。图5(a)、(c)、(e)为反应前新鲜样品微观形貌图,(b)、(d)、(f)为20 次循环后(氧化反应后)的SEM图像。从图中可以看出,随着Ni/Ce 比的变化,载氧体的形貌也略有变化。图5(a)、(c)、(e)相比,加入Ce后,Ni/Ce比3∶1时颗粒分散程度增加,反应前有较多的孔道存在。当NiO和CeO分别成为主要成分时,颗粒的粒径明显大于3∶1,值得一提的是,从SEM图像得出的粒径变化和XRD分析与计算结果一致。从图5(b)、(d)、(f)可以看到三种颗粒均出现了不同程度的团聚或烧结现象,从NiO/γ−AlO和CeO/γ−AlO循环后的SEM图像,可以发现出现了较多的团聚,尤其CeO/γ−AlO出现了大面积的团聚堵塞通道,这和固定床循环实验甲烷转化率低的结果一致。从20 次循环后的NiO−CeO/γ−AlO载氧体的SEM 图像图5(d)中,能发现颗粒仍保持较高的分散度。

图5 不同Ni/Ce质量比的NiO−CeO2/γ−Al2O3载氧体的SEM图像
2.5 20次循环后载氧体XRD结果分析
图6 为经过20 次循环经空气再生后的XRD 图谱,从图中可知,经过20 次循环反应后的载氧体的成分变化较小,其主要晶相为NiAlO(19°)、NiO (37.3°、45°)、CeO(28°、31.5°、47.4°、56°)、Ce−Ni (45.35°)、γ −AlO(34°、66.6°、76°、77°)。从图谱中可以发现,5 种载氧体经过20 次循环后CeO(47.4°)、NiO(45°)和Ce−Ni(45.35°)的特征峰变宽且衍射峰强度有所增大,结晶化程度增大,载氧体的晶粒粒径变小。随着氧化还原反应的交替进行,在CeO与甲烷和水蒸气反应时体相晶格氧不断向表面移动,产生氧空位,Ni进入CeO结构中形成了大量的固溶体,载氧体晶粒粒径变小,且固溶体的形成增加了载氧体的储氧能力和释放速率。
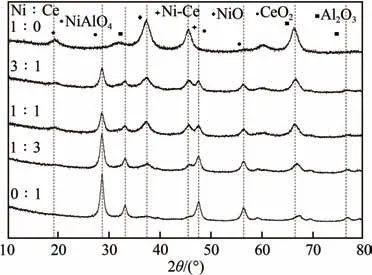
图6 不同Ni/Ce比载氧体20次循环后的XRD图谱
2.6 固定床实验
2.6.1 反应温度的影响
反应温度对重整反应有着重要影响。本节实验选用反应温度600℃、650℃、700℃、750℃、800℃、850℃和900℃,研究温度对不同镍铈比载氧体的氧化还原性能影响,试验结果见图7。通过图7 可以发现,五种载氧体在600℃时普遍表现为较低的氢气选择性和甲烷转化率,然而随着温度的升高,氢气选性增加,甲烷的转化率也呈上升的趋势,并在800~900℃时保持很小的变化趋势,这表明在600℃时并未达到重整反应所需的活化能,随着温度的升高,高温更有利于吸热重整反应的进行,并且提高了气体的分子扩散,促进了载氧体的还原,对应的氢气选择性、甲烷转化率有所提高,但是当温度达到一定临界值时,在此基础上再增加温度并未对氢气的选择性、甲烷的转化率产生明显的影响,并且过高的温度会增加所需的能耗,造成能量的浪费。因此为了提高产氢量,选择合适的温度应考虑相应的转化率和能耗。从图7中也可以发现,随着温度的升高,五种载氧体的积炭选择性都呈下降趋势,说明温度对载氧体催化甲烷化学链重整制氢有着重要影响。在温度大于750℃时虽然比例为1∶0和0∶1载氧体的氢气选择性略高于1∶1和3∶1载氧体的选择性,但是1∶0和0∶1载氧体的积炭量大于1∶1和3∶1载氧体,可见通过不同反应温度下的实验结果可以发现,单金属载氧体的性能低于复合金属载氧体,其并不适合化学链甲烷重整反应制氢。在温度大于750℃时,3∶1和1∶1载氧体的氢气选择性相近,3∶1载氧体的积炭选择性低于1∶1,由此可以发现,在相同温度下3∶1 载氧体更合适甲烷化学链重整制氢,与3∶1 载氧体颗粒尺寸较小,暴露更多的活性位点参与重整制氢的结果一致。通过这些不同温度下的实验数据对比可以判断出,Ce 的引入可以改变镍基载氧体的性能。

图7 反应温度对不同镍铈比载氧体性能的影响
2.6.2 水碳比的影响
水碳比在甲烷化学链重整制氢中起着重要作用,在本研究中,选用水碳比0、0.5、1、1.5、2、2.5和3,研究不同水碳比对不同比例载氧体的氧化还原性能的影响。实验结果见图8,随着水碳比从0 到3 的变化,五种载氧体反应产生的氢气选择性都呈单调增加趋势,积炭选择性呈递减趋势。这是因为增加的蒸汽供应有利于甲烷重整反应的平衡和水−气变换反应的进行。但是,当水碳比大于2时,五种载氧体的氢气选择性、甲烷转化率的变化趋势变小。此时可能出现蒸汽在载氧体表面上的吸附达到饱和。而且过多的蒸汽会导致额外的能耗来从产物中分离得到干燥的氢气。从图8中可以发现在水碳比小于1.5时,镍铈比例为3∶1时的氢气选择性的变化趋势虽然和1∶0 时相近,但是1∶0 载氧体的积炭选择性明显高于3∶1 载氧体,并且3∶1载氧体的积炭选择性和其他四种载氧体相比最低,由此可以推断加入一定比例的氧化铈有助于抑制积炭的形成。并且从图8中可以发现,单金属CeO的甲烷转化率低于其余四种,且积炭选择性最高,因此可以发现即使改变水碳比,单金属CeO的催化甲烷重整反应的活性也很低。通过对比3∶1、1∶1、1∶3 载氧体可以发现三种改性之后的载氧体氢气选择性相近,但是3∶1 载氧体的积炭选择性低于1∶1、1∶3 载氧体,由此可以发现3∶1 载氧体的性能最优。

图8 水碳比对不同镍铈比载氧体性能的影响
3 结论
本文采用浸渍法制备了NiO−CeO/γ−AlO复合载氧体,并通过固定床化学链重整制氢反应和表征手段,考察了不同比例镍铈载氧体的性能,通过实验结果的对比分析得出以下结论。
(1)CeO的加入在一定程度上减弱了NiO 与γ−AlO之间的相互作用,抑制了NiAlO的形成。且3∶1 复合载氧体晶粒粒径较小,更有利于化学链重整反应制氢。
(2)SEM 结果分析可知,3∶1 复合载氧体的颗粒分散度较好,反应前有较多的孔道存在,在经过20次循环实验后仍能保持较好的形貌。
(3)固定床实验发现,升高反应温度可以提高氢气选择性和甲烷转化率。但温度达到一定临界值时,载氧体的活性变化较小,在800℃时3∶1载氧体的性能表现最佳;合适的水碳比有利于提高氢气选择性,过高的水碳比在载氧体表面上吸附达到饱和。
(4)本文制备的用于化学链甲烷重整制氢的五种载氧体中,3∶1镍−铈载氧体性能最好,比较适合与甲烷化学链重整制氢。
符号说明
——反应前后进出口CH气体占总气体的摩尔分数
——产气中出口H气体的摩尔分数
——产气中出口CO气体的摩尔分数
——产气中出口CO气体的摩尔分数
in ——进气口
out ——出气口
