盐酸多西环素片在猪体内的残留消除规律研究
2022-02-11赵富华陆连寿刘自扬李思奇郭桂芳吴琴尧曹玉颖邱基程李淑媛龚晓会郭燕荧张希墨曹兴元
赵富华,陆连寿,刘自扬,李 萌,李思奇,郭桂芳,吴琴尧 ,曹玉颖, 邱基程,李淑媛,张 璐,龚晓会, 郭燕荧,张希墨*,曹兴元*
(1 中国兽医药品监察所,北京 100081; 2 中国农业大学动物医学院,北京 100193;3 国家兽药残留基准实验室,北京 100193)
多西环素为第二代半合成的四环素衍生物,为广谱、高效抗生素,对革兰氏阴性菌、革兰氏阳性菌、螺旋体、立克次体、支原体、衣原体等均有抑制作用[1]。盐酸多西环素的组织穿透力强、体内分布广和生物利用度高[2],与同类产品比较,它有价格便宜,胃肠道副作用小,静脉给药不会造成静脉炎等优点,已被广泛用于兽医临床。农业农村部、国家卫生健康委员会和国家市场监督管理总局联合发布的《食品安全国家标准 食品中兽药最大残留限量》(GB 31650-2019),多西环素在猪组织中的最高残留限量(MRL):肌肉100 μg/kg、肝300 μg/kg、肾600 μg/kg、皮+脂肪300 μg/kg[3]。同时,农业部《兽药停药期规定》规定了盐酸多西环素片的休药期为28日,但未明确动物的类型[4]。本试验的主要目的在于研究口服给予盐酸多西环素片后,多西环素在猪组织中的残留消除规律,并计算出休药期,为盐酸多西环素片在临床应用提供科学的依据,保障动物性食品安全和人民健康。
1 材料与方法
1.1 试剂与药物 盐酸多西环素片:10 mg/片,批准文号为兽药字030462604,河北远征禾木药业有限公司提供。多西环素对照品:含量≥98.7%,批号为20104,购自德国Dr. Ehrensorfer公司;Oasis HLB固相萃取柱(HLB柱):500 mg/6 mL,Waters公司;超纯水:由Milli-Q超纯水仪制取;乙腈、甲醇色谱纯;三氟乙酸、二氯甲烷、乙二胺四乙酸二钠、枸橼酸、磷酸氢二钠、草酸、硫酸、钨酸钠,均为分析纯。
1.2 仪器设备 高效液相色谱仪:Agilent 1260 高效液相色谱串联紫外检测器;分析天平,R200D,德国Sartofius公司;天平,MP2002,上海舜宇恒平科学仪器有限公司;研磨杯,SQ2119 N,上海帅佳电子科技公司;高速冷冻离心机,Centrifuge 5804R,德国Eppendorf公司;多管涡旋混合器,VX-III,北京踏锦科技有限公司;固相萃取装置:Waters 200606,美国Waters公司;氮吹仪,N-EVAP-112,美国Organomation Associate公司;无油真空泵,F-50,天津市科亿隆实验设备有限公司。
1.3 试验动物 三元杂交健康猪30头,去势雄性猪,3-4月龄,体重约50 kg,由莱西市某猪养殖厂提供。其中对照组5头,给药组25头。
1.4 给药方案 用EXCEL随机数字表法对30头猪进行随机分组,分为6组,每组5头,其中1组为不用药的空白对照组,另外5组猪以口服方式给药,每头猪给药剂量为0.5片/kg。
1.5 标准溶液的制备 标准储备液(100 μg/mL):准确称取适量的多西环素,用甲醇溶解后转移至100 mL容量瓶,再用甲醇定容。标准工作溶液:根据需要用流动相将多西环素标准储备液稀释成浓度分别为0.05、0.1、0.2、0.5、1、2、5 μg/mL的标准工作溶液。
1.6 组织采集 最后一次给药后分别在12 h、1 d、3 d、6 d和8 d,随机抽取5头猪进行屠宰,快速取其肌肉、脂肪、肝脏和肾脏等组织(每种组织样品均250 g),用滤纸吸取脏器表面血液。所取样本做好标记、包装,于-20 ℃保存。未用药猪在12 h后屠宰,采用上述方法采集相同组织作为空白对照。
1.7 样品前处理
1.7.1 提取 脂肪:称取均质试料1±0.01 g于10 mL离心管中,加ACN: H2O=1:9的溶液2 mL,涡旋混匀1 min,40 ℃超声5 min,4 ℃下12000 rpm高速离心10 min,取上清液于另一离心管。将残渣重复上述步骤重复提取一次,合并两次上清液,-80 ℃冷冻除脂5 min,4 ℃下12000 rpm离心5 min,取上清液,直接过滤膜,上机检测。
肌肉、肝脏:称取均质试料5±0.05 g于50 mL离心管中,加 EDTA·2 Na-Mcllvaine缓冲溶液20 mL,涡旋1 min,振荡10 min,加0.34 mol/L硫酸溶液5 mL、7%钨酸钠溶液5 mL,涡旋1 min,4 ℃下8500 rpm离心5 min,取上清液。残渣用EDTA·2 Na-Mcllvaine缓冲溶液20 mL、10 mL重复提取,合并三次上清液,中性滤纸过滤后,备用。
肾脏:称取均质试料2±0.02 g,于50 mL离心管中,加 EDTA·2 Na-Mcllvaine缓冲溶液10 mL,涡旋1 min,振荡10 min,加0.34 mol/L硫酸溶液2 mL、7%钨酸钠溶液2 mL,涡旋1 min,4 ℃下8500 rpm离心5 min,取上清液。残渣用EDTA·2 Na-Mcllvaine缓冲溶液10 mL、10 mL重复提取,合并三次上清液,中性滤纸过滤后,备用。
1.7.2 净化 HLB柱依次用甲醇5 mL、水5 mL和EDTA· 2 Na-Mcllvaine缓冲溶液5 mL活化,取备用液过柱,待备用液全部流出后,依次用水、5%甲醇溶液各10 mL淋洗,抽干30 s,用甲醇5 mL洗脱,收集洗脱液于刻度试管中,于40 ℃水浴氮气吹至0.5~1.0 mL,用0.01 mol/L草酸溶液定容至2.0 mL,过滤,供高效液相色谱测定。
1.8 色谱条件 色谱柱:C18(150 mm×4.6 mm,粒径5 μm);流动相:A:0.01 mol/L三氟乙酸溶液,B:乙腈;梯度洗脱;流速:1.0 mL/min;柱温:30 ℃;检测波长:350 nm;进样量:50 μL。见表1。

表1 流动相梯度洗脱条件Tab 1 Gradient elution program
2 结果与分析
2.1 方法学验证
2.1.1 线性与范围 精密量取浓度为0.05、0.1、0.2、0.5、1、2、5 μg/mL的标准液各50 μL,供高效液相色谱测定。以测得峰面积为纵坐标,对应的标准溶液浓度为横坐标,绘制标准曲线。其线性方程为Y=0.044x-0.414,R2=0.999,多西环素在50 μg/mL~5000 μg/mL范围内线性关系良好。
2.1.2 检测线与定量限 取6个空白组织样品,按照上述样品前处理的方法处理,测得基线噪音值,按照信噪比(S/N) = 3 为检测限(LOD),S/N=10 为定量限(LOQ)。本方法在猪的肌肉组织中检测限为20 μg/kg,定量限为50 μg/kg;在猪的肝脏组织、肾脏组织、皮+脂肪的检测限为50 μg/kg,定量限为100 μg/kg。
2.1.3 准确度与精密度 在空白组织中添加多西环素标准工作溶液,使肌肉组织中的浓度为50 μg/kg,100 μg/kg,200 μg/kg时,肾脏组织中的多西环素浓度为100 μg/kg,600 μg/kg,1200 μg/kg时,肝脏组织和脂肪组织中浓度为100 μg/kg,300 μg/kg,600 μg/kg时,平均回收率在60.32%~116.80%之间,批内、批间变异系数均小于15%,表明该方法符合组织中药物分析的准确度和精密度要求,见表2。盐酸多西环素标准溶液在1.8色谱条件下,待测药物盐酸多西环素在图谱中能够呈现较好的峰形,并与其他杂质峰达到良好的分离效果,详见图1。

表2 多西环素在猪肌肉和肾脏中的回收率及变异系数Tab 2 Recovery and coefficient of variation of doxycycline in pig muscle and kidney

图1 盐酸多西环素标准溶液色谱图(100 ng/mL)(a)、空白肌肉组织色谱图(b)、空白肌肉组织添加100 ng/mL色谱图(c)Fig 1 Chromatography of doxycycline hydrochloride standard solution (100 ng/mL)(a)、Chromatography of blank muscle tissue (b)、Chromatography of blank muscle with 100 ng/mL(c)
2.2 药物残留的测定 每个采样时间的每个组织的多西环素残留量如表3所示。

表3 猪组织样品中多西环素在各组织中的残留量Tab 3 Residues of doxycycline in tissues after administration

续表
2.3 休药期计算 使用WT 1.4软件按95%置信区间计算盐酸多西环素在猪肌肉、肝脏和肾脏组织中的休药期分别为2.4日、6.5日、3.5日,见图2-图4。
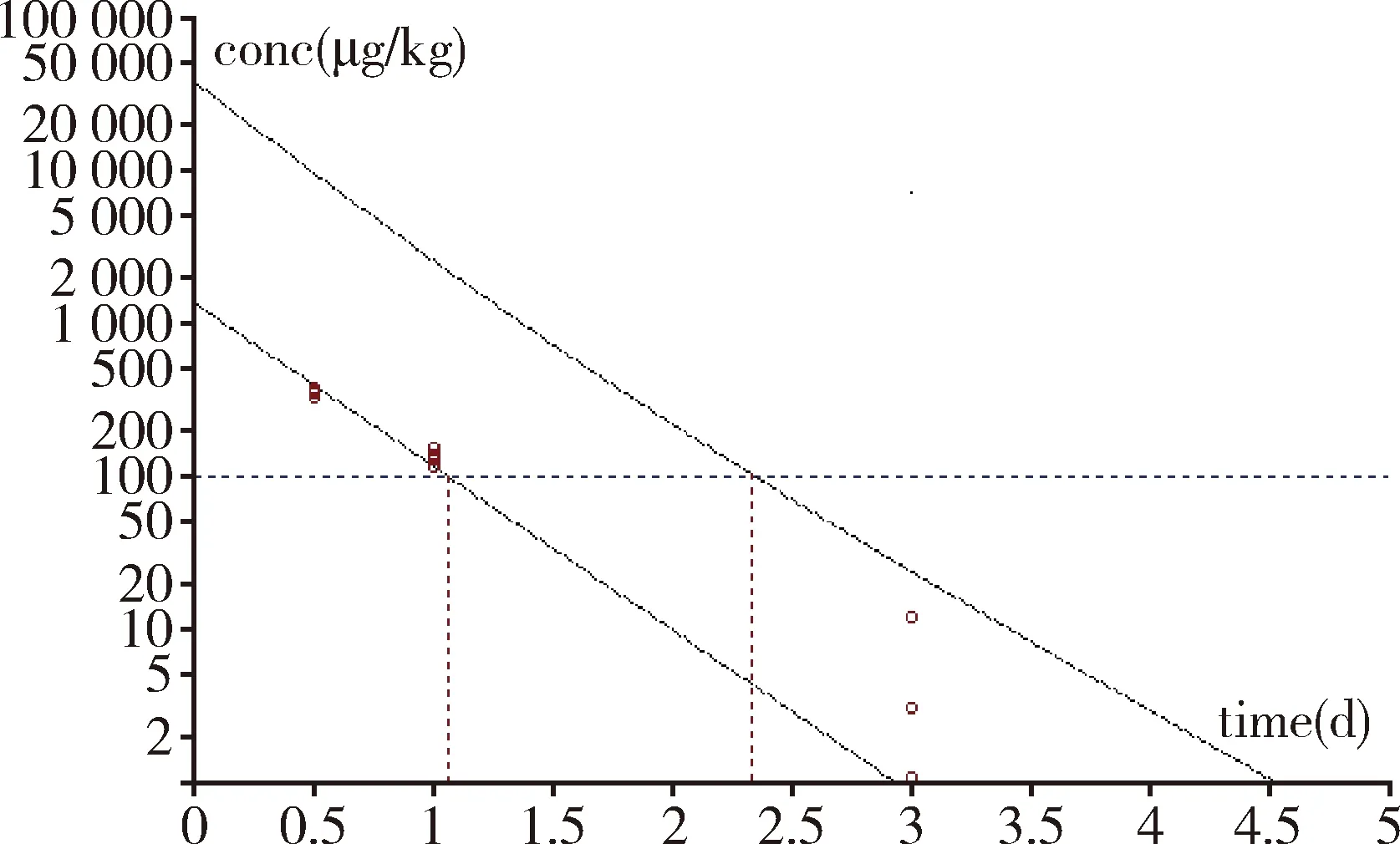
图2 盐酸多西环素片在猪肌肉中休药期计算图Fig 2 Calculation chart of drug withdrawal period of doxycycline hydrochloride tablets in pig muscle
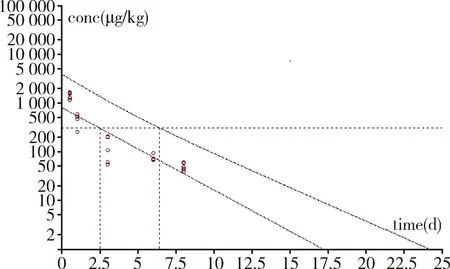
图3 盐酸多西环素片在猪肝脏中休药期计算图Fig 3 Calculation chart of drug withdrawal period ofdoxycycline hydrochloride tablets in pig liver

图4 盐酸多西环素片在猪肾脏中休药期计算图Fig 4 Calculation chart of drug withdrawal period of doxycycline hydrochloride tablets in pig kidney
3 讨论与结论
我国动物性食品生产量居世界前列,但质量与世界先进水平相比还存在差距,兽药残留超标是其中之一。因此在严格规范兽药使用原则的前提下,还要加强动物性食品中兽药残留检测技术及方法的研究。目前,抗生素已被广泛用于预防或治疗牲畜传染病[5],加大对抗生素及其代谢物检测研究力度,有助于积累其对环境持久性和生态毒性的科学证据[6-7],为兽药使用安全、食品安全与人民健康提供保障。
目前,已有研究报道了盐酸多西环素在动物体内的残留消除规律,杨秋实[8]以10 mg/kg体重剂量给猪颈部肌肉注射盐酸多西环素,隔天再次注射,发现组织中多西环素残留由高到低顺序为:肾脏>肝脏>肌肉>皮+脂肪;黄聚杰[9]以20 mg/kg的剂量给花鲈口服盐酸多西环素,发现组织中多西环素残留由高到低顺序为:血浆>肾脏>肝脏>肌肉;翟克影[10]等人给猪单次灌服5 mg/kg体重剂量连续给药4日,发现组织中多西环素残留由高到低顺序为:肾脏>肝脏>肌肉>皮+脂肪;王金花[11]等人以2.5 mg/kg单剂量肌肉注射猪,发现组织中多西环素残留由高到低的顺序为:肾脏>皮+脂肪>肌肉>肝脏;本次试验结果与上述试验结果基本一致,给药后残留浓度顺序依次为:肾脏>肝脏>肌肉>脂肪。
此外,有研究报道了不同剂型的盐酸多西环素在猪体内的休药期,黄耀凌[12]等人的试验中,自制盐酸多西环素注射液以10 mg/kg体重剂量对猪肌内注射给药,连续给药3日,建议休药期为42日,休药期较长;李媚[13]等人以10 mg/kg体重剂量于试验猪颈部肌内注射长效盐酸多西环素注射液,给药2次,给药间隔时间为48 h,建议休药期为28日;刘欣[1]等人以10 mg/kg体重剂量服用盐酸多西环素颗粒后,连续给药5日,建议休药期为12日。本文采用HPLC-VWD方法检测了猪按照5 mg/kg体重剂量口服盐酸多西环素片后在不同时间点各组织中多西环素的残留量,使用WT 1.4软件按95%置信区间计算出盐酸多西环素片的休药期为7日。上述试验中的休药期均比本试验的休药期长,但是残留结果与本试验结果基本相似,其原因可能与剂型和给药方式不同有关,盐酸多西环素在猪体内主要通过肝脏和肾脏进行代谢,且消除速度较慢,不同剂型和给药方式对其影响明显。
综上所述,建议盐酸多西环素片在猪体内的休药期为7日。
