CYP2C9和VKORC1基因检测指导心脏瓣膜置换术后华法林用药的研究
2022-01-28靳云洲
靳云洲
(重庆大学附属三峡医院 心脏大血管外科, 重庆, 404100)
心脏瓣膜病是中国常见的心脏疾病,每年接受人工瓣膜置换术的患者超过20万例,该手术的数量占成人心脏外科手术的首位[1]。人工瓣膜置换术后患者均需终身抗凝治疗,然而术后抗凝治疗不当容易导致并发症(最常见和最严重的是出血和血管栓塞,约占并发症总数的75%), 故选用较好的抗凝方案对降低人工瓣膜置换术后并发症的发生率非常重要[2]。华法林为临床一线香豆素类口服抗凝药,能有效降低中风概率,且成本相对较低,目前仍是心脏人工瓣膜置换术后的主要抗凝药物,其通过使肝脏产生羧酸化和去羧酸化蛋白失衡而达到抗凝效果[3]。但华法林用药的个体差异较大,过度抗凝会增加潜在的致命性出血风险[4], 且其达标剂量受到遗传因素及药物相互作用等非遗传因素共同决定[5-6]。影响华法林抗凝的非遗传因素包括身高、体质量、年龄、食物、药物及疾病等,还有30%~40%的用药个体差异可用影响华法林药效学的VKORC1基因多态性和影响华法林药物代谢动力学的CYP2C9基因多态性来解释[7], 且VKORC1-1639G等位基因与高华法林剂量相关[8]。本研究探讨了CYP2C9和VKORC1基因检测对心脏瓣膜置换术后患者华法林抗凝的指导意义,现报告如下。
1 资料与方法
1.1 一般资料
选取2020年5月—2021年6月在重庆大学附属三峡医院就诊的156例心脏人工瓣膜置换术后患者作为研究对象。年龄、身高、体质量、基因型、同时服用药物、基础疾病、食物等多种因素均会影响华法林的药效学与药物代谢动力学[9], 故本研究据此制订纳入标准与排除标准。纳入标准: ① 渝东北地区心脏人工瓣膜置换术后患者(饮食结构、身高、体质量差异较小); ② 年龄≥18岁者。排除标准: ① 严重肝、肾疾病患者; ② 甲状腺疾病、恶性肿瘤、活动性消化性溃疡、输血患者; ③ 血液系统疾病(如血友病、血小板缺乏症等)患者; ④ 长期口服胺碘酮、阿司匹林等影响华法林药效的药物者。156例患者中,门诊随访患者81例,住院患者75例; 男57例,女99例; 年龄33~82岁,平均(56.99±8.33)岁; 身高141~174 cm, 平均(159.12±6.58) cm; 体质量32~85 kg, 平均(58.39±8.97) kg。
1.2 方法
采用荧光定量聚合酶链反应(PCR)法进行CYP2C9和VKORC1基因检测,并根据检测结果将患者分组。156例患者CYP2C9*2(430>T)基因型均为CC型,不予分组;CYP2C9*3(1075>C)基因型分成AC型14例(占8.97%)、AA型142例(占91.03%),分别纳入CYP2C9*3 AC组、CYP2C9*3 AA组;VKORC1(-1639G>A)基因型分为GG型3例(占1.92%)、GA型22例(占14.10%)、AA型131例(占83.97%),因GG型例数较少,将其与GA型合并纳入VKORC1GA/GG组, AA型则纳入VKORC1AA组。
所有患者术后口服华法林钠片(齐鲁制药有限公司生产,规格2.5 mg/片),且长期监测凝血酶原时间-国际标准化比值(PT-INR), 医生根据PT-INR指导调整华法林用药剂量,从而使患者的抗凝治疗获得最佳收益,但大多数患者难以将PT-INR长期稳定维持在治疗范围内[10]。采集患者空腹8 h以上外周静脉血3 mL, 采用凝固法检测患者服用华法林后PT-INR。对于门诊患者,记录不同组患者PT-INR稳定在1.5~2.5时的华法林用量为实际达标剂量; 对于住院患者,记录患者出院时PT-INR稳定在1.5~2.5时的华法林用量为实际达标剂量,住院患者连续2 d的PT-INR稳定在1.5~2.5时所用时间为达标时间(因为门诊患者无法统计实际达标时间,所以本研究仅统计75例住院患者的达标时间)。
比较各组患者的体质量、年龄、身高、手术方式、干扰药物用药情况、实际达标剂量、达标时间,并进行统计学分析。
1.3 统计学分析

2 结 果
2.1 不同基因型患者年龄、体质量、身高、用药情况、手术方式及并发症比较
CYP2C9*3 AA组年龄、体质量、身高与CYP2C9*3 AC组比较,差异无统计学意义(P>0.05);VKORC1GA/GG组年龄、体质量、身高与VKORC1AA组比较,差异无统计学意义(P>0.05)。各组患者的手术方式比较,差异无统计学意义(P>0.05)。VKORC1GA/GG患者和CYP2C9*3 AC患者合计39例,发生抗凝并发症3例,并发症发生率为7.69%; 其余患者合计117例,发生抗凝并发症9例,并发症发生率为7.69%。见表1。
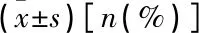
表1 不同基因型患者年龄、体质量、身高、用药情况、手术方式及并发症比较
2.2 不同基因型患者华法林用药达标剂量及达标时间比较
CYP2C9*3 AA组患者实际达标剂量高于CYP2C9*3 AC组,差异有统计学意义(t=5.730,P=0.018);VKORC1GA/GG组实际达标剂量高于VKORC1AA组,差异有统计学意义(t=17.999,P<0.001)。CYP2C9*3 AC组平均达标时间长于CYP2C9*3 AA组,VKORC1GA/GG组平均达标时间长于VKORC1AA组,但差异均无统计学意义(P>0.05)。见表2。
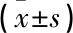
表2 不同基因型患者华法林用药达标剂量及达标时间比较
3 讨 论
影响华法林抗凝效果的非遗传因素包括年龄、身高、体质量等,其中年龄因素的影响最大[4]。研究[11]发现,儿童年龄与维生素K拮抗剂剂量呈负相关,且维生素K依赖性凝血因子和抑制剂水平在出生时显著降低,在儿童时期持续降低。相较于儿童,老年人的抗凝安全性则更加值得关注, 60岁以上患者的实际达标剂量显著降低,且达标剂量随年龄增长而逐渐降低[12]。本研究纳入患者的年龄为33~82岁,其中60岁以上患者53例,平均达标剂量为(2.43±1.08) mg, 60岁及以下患者平均达标剂量为(3.05±1.38) mg, 差异有统计学意义(P=0.015)。此外,老年患者依从性较差,很难遵医嘱定期检测PT-INR并调节华法林用量,极易发生出血、脑梗死等并发症,应引起足够重视。本研究发现,VKORC1GA/GG组年龄、体质量、身高与VKORC1AA组比较,差异无统计学意义(P>0.05), 推测华法林达标时间受体质量、身高、年龄影响较小。
华法林用药的达标剂量和达标时间受多因素共同影响,饮食、吸烟、饮酒、腹泻和发热等均可影响华法林的抗凝作用[4, 13]。本研究选择渝东北地区患者(饮食结构及生活习惯相似)作为研究对象,并排除严重肝肾疾病、甲状腺疾病、恶性肿瘤、活动性消化性溃疡、输血、血液系统疾病(如血友病、血小板缺乏症等)患者和长期口服胺碘酮、阿司匹林等药物者,旨在减少基础疾病及其他药物的干扰。心脏瓣膜置换术后常见合并用药胺碘酮对华法林的影响较大,其可通过竞争抑制华法林的代谢酶及CYP2C9的活性,减少华法林的代谢,增强华法林的抗凝作用,进而增加抗凝并发症的发生[14]。但本院患者心脏瓣膜置换术后很少会长期口服胺碘酮,常用药物多为比索洛尔。另外,华法林与阿司匹林、降脂药物联用可增加出血风险,其中联用贝特类降脂药物的出血风险显著高于他汀类降脂药物[15]。富含维生素K的食物会影响华法林的抗凝效果,而吸烟、饮酒也会影响华法林的抗凝效果[16-17], 故良好的生活饮食习惯也是保障华法林抗凝效果稳定的关键。本研究中,多数患者的手术方式为二尖瓣置换术,其中CYP2C9*3 AC组与VKORC1GA/GG组仅各有1例联合瓣膜疾病,样本量太少,故未分析手术方式对华法林的影响。
影响华法林抗凝效果的遗传因素中,目前临床研究最多的是CYP2C9基因与VKORC1基因,其中CYP2C9基因研究较多的突变位点是CYP2C9*2和CYP2C9*3。本研究患者CYP2C9*2基因均为CC型,CYP2C9*3 AC型共14例(约占8.97%), 与高伟祺等[18]提出的中国人群中CYP2C9*3突变相对更多、CYP2C9*2分布频率较低的结论一致。对于与华法林临床用量有关的VKORC1(-1639G G>A)基因,有报道[19]称中国患者的VKORCl基因型GG、AG和AA的分布频率分别为2.7%、17.6%和79.7%, 与本研究中GG、GA、AA基因型的分布频率1.92%、14.10%、83.97%接近。
本研究结果显示,CYP2C9*3 AA组患者实际达标剂量高于CYP2C9*3 AC组,VKORC1GA/GG组实际达标剂量高于VKORC1AA组,差异均有统计学意义(P<0.05);CYP2C9*3 AC组达标时间长于CYP2C9*3 AA组,VKORC1GA/GG组达标时间长于VKORC1AA组,但差异均无统计学意义(P>0.05),与单广东等[4]提出的心脏瓣膜置换术后患者进行CYP2C9和VKORC1基因分型,治疗初期能缩短INR首次达标时间的结论不同。本研究还显示,VKORC1GA/GG患者和CYP2C9*3 AC患者合计39例,抗凝并发症发生率为7.69%, 与其余患者的抗凝并发症发生率7.69%相同。由此提示,虽然不同基因型对华法林达标剂量的影响较大,但对并发症发生率并无显著影响,这可能与样本量稍小有关。
综上所述,华法林达标剂量随着年龄增长会逐渐降低,临床医生应重视老年人群的抗凝情况,并探寻更加先进、准确、方便的检测手段。排除体质量、年龄、身高、手术方式、基础疾病、联合用药、吸烟、饮酒等干扰因素后,CYP2C9*3 AC患者华法林平均达标剂量显著低于CYP2C9*3 AA患者,VKORC1GA/GG患者平均用药达标剂量显著高于VKORC1AA组,达标时间则无显著差异。CYP2C9和VKORC1基因检测有利于指导华法林初始剂量的选择,但对达标时间的影响不大,而其能否使患者更加平稳地从初始剂量到达达标剂量尚有待进一步论证。
