小而密低密度脂蛋白对急性ST段抬高型心肌梗死患者急诊PCI后对比剂肾病的预测价值
2022-01-21李雨涵马凯郑迪轩永丽李文华
李雨涵,马凯,郑迪,轩永丽,李文华
随着心血管疾病发病率的逐年上升,经皮冠状动脉介入治疗(PCI)已成为冠状动脉粥样硬化性心脏病(冠心病)治疗的常用手段,在我国每年约70万人进行PCI[1]。对比剂肾病(CIN)是患者PCI后常见且严重的并发症之一,同时也是院内获得性急性肾损伤的第3位病因[2,3]。研究表明,CIN明显提高患者的病死率及增加透析的风险且和再发心肌梗死的及靶血管的重建等事件有关[4]。小而密低密度脂蛋白(sd-LDL)是低密度脂蛋白中颗粒较小密度较大的亚组份。研究发现,sd-LDL与普通低密度脂蛋白(LDL)比较,其致动脉粥样硬化的能力更强[5]。肾脏病方面研究表明,sd-LDL与肾脏移植、慢性肾病患者的死亡风险显著相关,已成为预测肾脏病合并心血管病患者预后以及死亡的新型生化指标[6,7]。本研究旨在探讨术前血清sd-LDL水平对急性ST段抬高型心肌梗死行急诊PCI患者术后发生CIN的预测价值,从而指导临床对不同风险层次的患者制定早期个体化干预方案,降低不良事件的发生,为CIN的防治提供相关参考。
1 资料与方法
1.1 研究对象前瞻性分析徐州医科大学附属医院2019年11月至2020年8月因急性ST段抬高型心肌梗死接受急诊PCI治疗的352例患者的临床资料。STEMI诊断:具有典型缺血性胸痛,持续超过20 min,血清心肌坏死标记物浓度升高并有动态演变,心电图具有典型的ST段抬高的一类急性心肌梗死。研究方案经医院伦理委员会批准后实施,所有入选患者均签署知情同意书。排除标准:①对碘以及碘造影剂过敏史的患者;②合并恶性肿瘤、肝功能不全、甲状腺功能异常、免疫性疾病和感染性疾病;③入选前2周进行CT、磁共振或其他需要应用对比剂的检查;④术前48 h或术后72 h内使用氨基糖苷类抗生素、非甾体类抗炎药物等肾毒性药物;⑤合并严重慢性心力衰竭[纽约心脏病协会(NYHA)分级≥3 级]不能平卧24 h及以上,严重心脏瓣膜型疾病及血流动力学不稳定;⑥估算的肾小球滤过率(eGFR)<15 ml/(min·1.73 m2);⑦长期口服降脂类药物或其他可能干扰本研究的疾病。研究方案经我院伦理委员会批准,入选患者均签署知情同意书。对比剂肾病的定义:排除其他可能引起肾损害的原因,应用造影剂后48~72 h内血清肌酐水平较基线增加0.5 mg/dl(44.2 μmol/L)或相对值升高25%[8]。将患者按是否发生CIN分为CIN组(71例)和非CIN组(281例)。肾小球滤过率估算值(eGFR)采用简化MDRD公式计算:eGFR[ml/(min·1.73 m2)]=186×Scr(mg/dl)-1.154×年龄-0.203(×0.79女性)。
1.2 研究方法患者入院即刻采取静脉血3 ml,置于含有乙二胺四乙酸抗凝生化样本管内,30 min内进行离心,采用美国贝克曼AU5832及其配套试剂测定血清中sd-LDL。选择右侧桡动脉或右侧股动脉穿刺,先行冠状动脉(冠脉)造影术,根据造影结果行相关病变血管介入治疗,所有患者在行冠脉介入手术中的造影剂都选用低渗或等渗非离子型对比剂。由心内科医生根据患者病情,应用抗血小板药、β受体阻滞剂、血管紧张素转换酶抑制剂或血管紧张素Ⅱ受体拮抗剂、硝酸酯类、钙离子同道阻滞剂、低分子肝素抗凝剂等药物。术后根据患者心肾功能情况,执行个体化水化治疗,应用0.9%氯化钠溶液以1 ml/(kg·h)的速度进行,持续时间约为8~24 h。
1.3 统计学处理采用SPSS 26.0软件包进行统计学分析,计量资料用均数±标准差(±s)表示,组间比较用独立样本t检验;计数资料采用例数(构成比)表示,组间对比采用χ2检验。采用多因素Logistic回归分析PCI后发生CIN的危险因素。通过绘制ROC曲线下面积(AUC)来评估sd-LDL对诊断CIN的敏感性及特异性。以P<0.05为差异有统计学意义。
2 结果
2.1 一般资料比较352例行急诊PCI患者中,术后发生CIN者71例(20.2%)。CIN组患者的术前sd-LDL、中性粒细胞/淋巴细胞比值均高于非CIN组(P<0.05),术前eGFR低于非CIN组(P<0.05);两组间其他指标比较,差异均无统计学意义(P>0.05),表1~2。
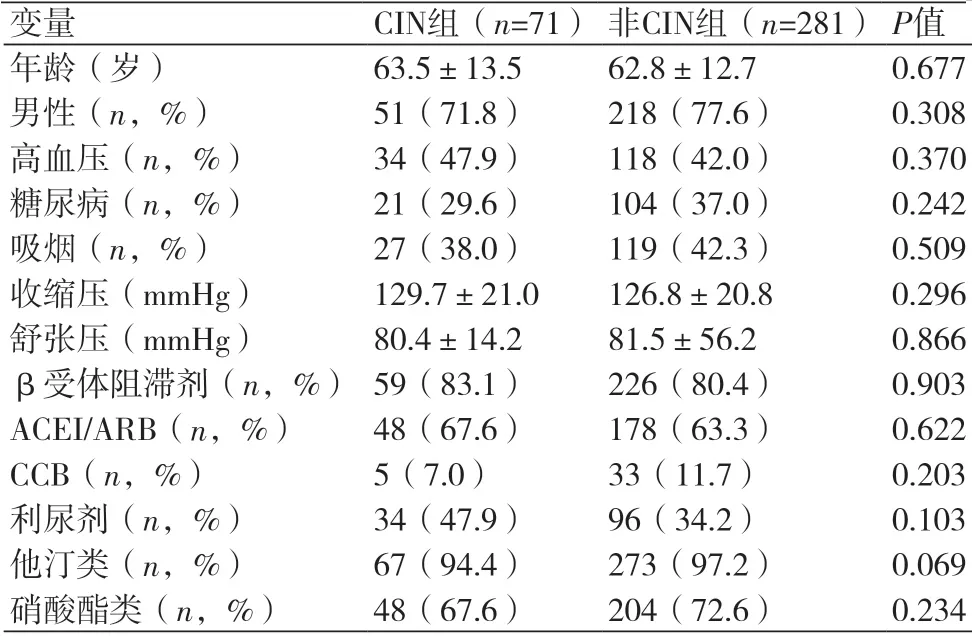
表1 研究对象的一般资料
2.2 PCI后CIN发生的影响因素分析为研究各指标与对比剂肾病发生的相关性,本研究以对比剂肾病为因变量,各相关指标为自变量进行多因素Logstic回归分析,结果显示,血清sd-LDL水平(OR=5.915,95%CI:3.254~10.752)、NRL(OR=1.081,95%CI:1.030~1.135)、血清肌酐水平(OR=1.015,95%CI:1.002~1.238)均是STEMI患者行急诊PCI后发生CIN的独立危险因素(P<0.05),表3。
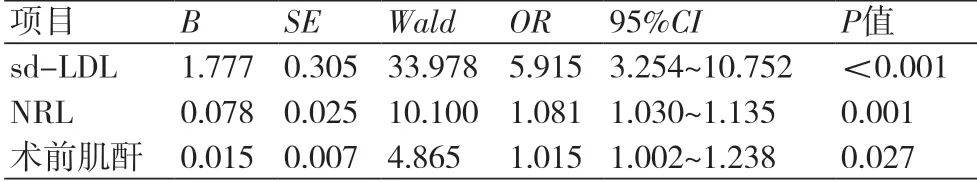
表3 对比剂肾病各指标的Logistics回归分析
2.3 不同sd-LDL水平CIN的发生率当sd-LDL<1.362 μmmol/L时,CIN的发生率为14.7%;sd-LDL≥1.362 μmol/L时,CIN的发生率为45%,两组CIN的发生率比较,P<0.001。
2.4 ROC曲线分析ROC曲线显示,sd-LDL预测急性ST段抬高心肌梗死患者急诊PCI后对比剂肾病的发生的曲线下面积为0.741,最佳截断为1.201,灵敏度为72.9%,特异性为83.5%;NLR的曲线下面积为0.612,最佳截断为4.29,灵敏度为82.9%,特异性为41.4%,图1。
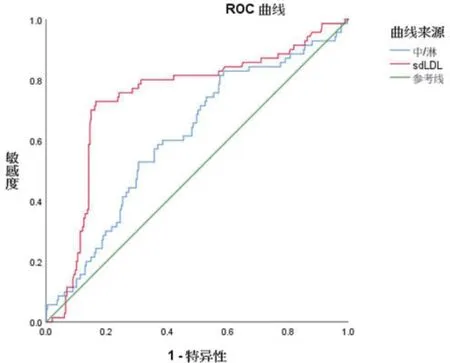
图1 sd-LDL、NLR预测急诊PCI患者CIN发生的ROC曲线
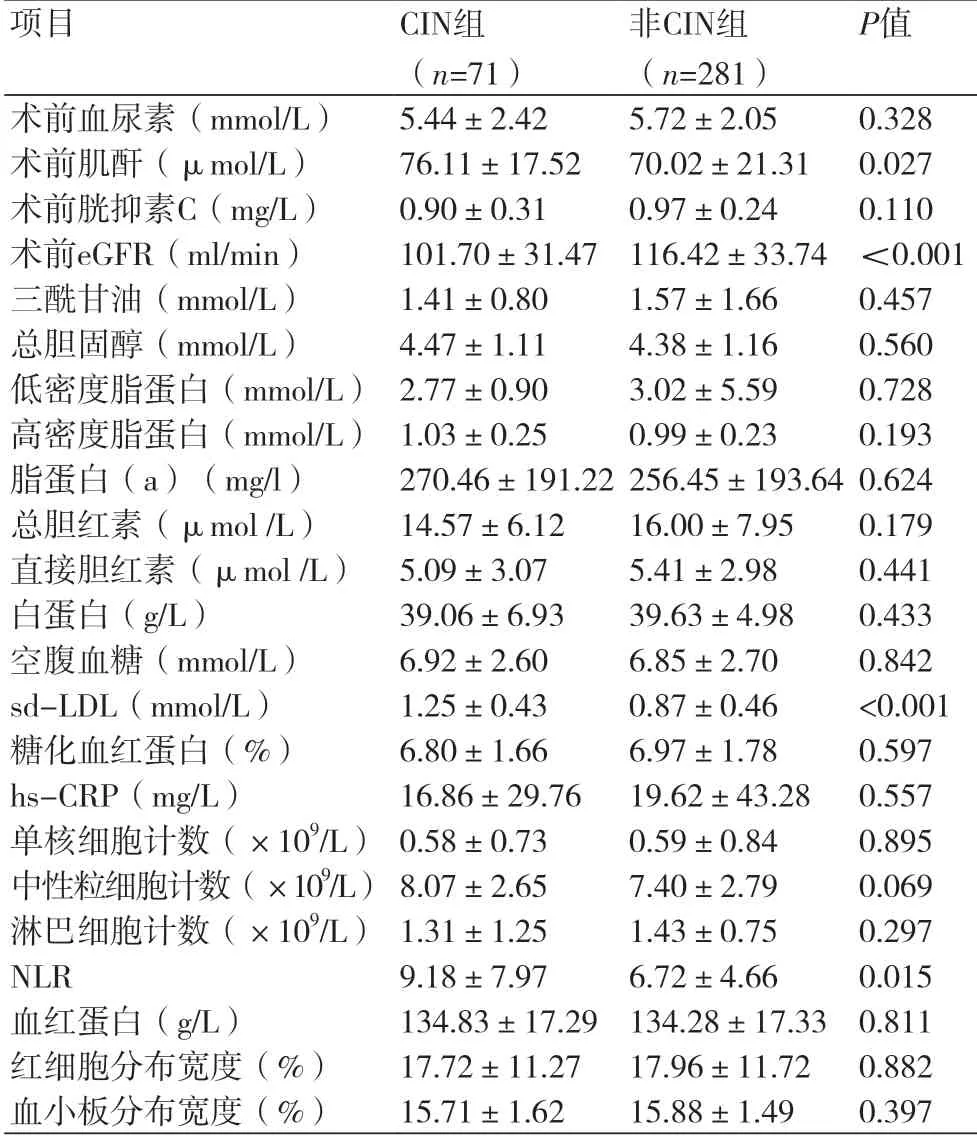
表2 CIN组与非CIN组患者术前实验室检查结果的比较
3 讨论
本研究结果显示,大部分STEMI患者在接受急诊PCI后即使术后常规进行水化预防其对比剂肾病(CIN)的发生率仍高达20.2%。研究表明,即使是轻度的肾功能损害也可能造成预后不良,如增加患者死亡率,增加心肌梗死、终末期肾病比例,延长患者的住院时间等。因此,寻找更敏感、可靠的指标来早期识别高危患者成为临床预防CIN发生的关键。
小而密低密度脂蛋白(sd-LDL)是低密度脂蛋白(LDL)中颗粒较小密度较大的亚组分,具有颗粒小、密度大、电荷少、半衰期长、易于氧化修饰、易于粘附血管壁等特点。相较于LDL,sd-LDL更易被巨噬细胞吞噬,而吞噬细胞过量的sd-LDL可导致吞噬细胞空泡化,转化成为泡沫细胞,更易造成血管内壁损伤,而内皮细胞长期反复损伤,会造成脂质不断沉积和平滑肌细胞持续增生,经过一系列恶性循环最终导致动脉粥样硬化[9]。随着国内外多项研究的深入,“脂质肾毒性”概念越来越受到重视[10]。郭晓蕙[11]认为sd-LDL与受体结合力降低,导致在血液循环中的半衰期延长,更易修饰和被巨噬细胞识别并吞噬。修饰的脂蛋白可对肾脏造成多方面的损害。一方面,其与肾小球上皮细胞及系膜表面的脂蛋白受体结合力降低,导致脂蛋白在系膜区和肾小球基底膜沉积,刺激系膜外基质(ECM)合成,可能造成肾小球的堵塞和微循环障碍,导致肾组织缺血、缺氧。另一方面,修饰的脂蛋白还易与ECM发生受体介导的结合作用。吞噬细胞以不饱和的方式大量摄取修饰的脂蛋白从而转化成泡沫细胞,进而引起肾小球系膜细胞增生和系膜外基质扩增,通过触发一系列细胞因子介导的细胞反应,导致肾小球基底膜(GBM)增厚,ECM扩张,肾小球硬化,毛细血管腔变窄甚至堵塞。研究认为,肾脏缺血是导致CIN发生的主要机制之一,因此,患者血清中高水平的sd-LDL造成的肾脏供血异常可能有意义[12,13]。本研究中经多因素Logistics回归分析显示,校正其他相关指标后,血清sd-LDL水平升高是急诊PCI后发生对比剂肾病的危险因素(OR=5.915,95%CI:3.254~10.752,P<0.001)。对于急性ST段抬高型心肌梗死同时合并高水平sd-LDL的患者术前要高度警惕CIN的发生,临床应在PCI前全面评估病情,制定个体化水化治疗方案,且高度关注PCI后肾功能变化,对早期识别和预防CIN的发生可能有积极的临床意义。
目前CIN的发生机制尚未完全阐明,已有研究表明,炎症和内皮细胞受损在致对比剂肾病损伤的发生过程中起到了不可忽略的作用[14]。中性粒细胞/淋巴细胞比值(NLR)作为近年来研究较多的全身性炎症因子,研究证实,NLR与多种心血管疾病患者的病情严重程度及预后密切相关[15]。Kurtul等[16]纳入478例因NSTEACS入院并行PCI治疗的患者,入院常规计算NLR,研究发现CIN组患者的入院NLR明显高于非CIN组患者。在多因素分析中,NLR≥3.46是NSTE-ACS患者经PCI治疗后发生CIN的危险因素。叶飘等[17]研究证实术前NLR>6.03是急诊PCI后发生CIN的独立危险因素。与已有研究结果一致,本文发现CIN组的NLR明显高于非CIN组,Logstics回归分析结果显示,NLR是急诊PCI后发生CIN的影响因素;ROC曲线显示,NLR对急性ST段抬高型心肌梗死接受PCI后CIN的发生具有一定预测价值,应密切监测NLR以便早期评估预后。
综上所述,sd-LDL升高是急性ST段抬高型心肌梗死患者接受急诊PCI治疗发生CIN的独立危险因素。在PCI前应重视sd-LDL水平异常升高患者,以便早期评估预后,提前干预治疗。但本研究样本量较小,存在一定选择偏移,有待扩大样本量进一步研究。
