肠内营养耐受性评估管理方案在重症急性胰腺炎合并腹腔高压患者中的运用
2022-01-20薛瑾周金红倪兴梅陈怡雷
薛瑾 周金红 倪兴梅 陈怡雷
重症急性胰腺炎是胰腺局部炎症疾病,患者发病急,病情进展迅速,且通常伴有腹腔高压,对患者各器官功能造成较大影响[1]。此类患者主要表现包括胃肠功能障碍等,而早期营养支持能够提供患者机体所需能量,但若直接实施肠内营养会因为患者腹腔内高压而造成腹胀、恶心、呕吐等并发症[2-3]。因此,给予患者客观、有效肠内营养指导具有重要意义。本研究对我院收治的重症急性胰腺炎合并腹腔高压患者实施肠内营养耐受性评估管理方案,并与常规早期肠内营养方案进行对比。
1 对象与方法
1.1 研究对象
选择2019年12月—2020年12月我院收治的重症急性胰腺炎合并腹腔高压患者94例作为研究对象,纳入条件:均经影像学检查、生化检查及临床症状检查确诊为重症急性胰腺炎;APACHE Ⅱ评分≥8分;腹腔内压力≥12 mmHg(1mmHg=0.133kPa);患者及家属均签署知情同意书。排除条件:精神疾病;存在无法实施早期肠内营养干预的疾病;入院48 h死亡;存在免疫功能疾病;存在血液系统疾病;恶性肿瘤;存在严重肝、肾、脑等脏器疾病。按照组间基本特征具有可比性的原则分为对照组和观察组,各47例。对照组男29例,女18例;年龄22~75岁,平均46.05±7.35岁;急性生理和慢性健康状况(APACHE Ⅱ)评分为8~24分,平均15.29±2.14分。观察组男26例,女21例;年龄24~76岁,平均46.18±7.29岁;APACHE Ⅱ评分为8~24分,平均15.44±2.21分。本研究经医院伦理委员会审核通过。两组患者一般资料比较差异无统计学意义(P>0.05)。
1.2 干预方法
1.2.1 对照组 实施早期肠内营养支持,患者进入ICU后24~48 h内用空肠法进行早期肠内营养支持。患者常规每日摄入热量115 kJ/kg,氮摄入量0.25~0.39 g/kg。第1天给予500 ml半要素膳,25 ml/h,并给予加温处理;第2天可根据患者情况加整蛋白制剂,第3天加以整蛋白为氮源的制剂。
1.2.2 观察组 实施肠内营养耐受性评估管理方案。
(1)建立营养耐受管理团队:团队成员包括科室主任医师、主任护师、营养师和专科护士,团队成员共同讨论商议并制订肠内营养耐受性评估管理方案。
(2)肠内营养耐受性评估与处理: ①呕吐。每12 h呕吐1次。干预人员检查患者空肠管,观察是否移位,并将输入速度降低50%,改为药物治疗。②腹内压/腹胀。a.腹内压在12~15 mmHg或轻度腹胀者,干预人员根据其病史及临床症状实施体格检查,此外保持原输注速度;b.腹内压在16~25 mmHg或中度腹胀者,根据其腹部平片及临床表现明确患者是否存在肠根阻,将输注速度降低至50%,6 h后复查,若仍腹胀且持续时间在24 h,则可根据其肠道蠕动、消化情况给予胃肠动力药物;c. 腹内压在25 mmHg以上或重度腹胀者,干预人员立即停止肠内营养,诊断患者是否存在肠梗阻,若无则给予肠道菌群实验或CT检查。③腹泻。a.轻度腹泻,即12 h内发作1~2次,干预人员给予患者维持原营养液输入速度;b.中度腹泻,即12 h内发作3~4次,干预人员给予患者维持原营养液输入速度,此外每隔6 h复查1次;c.重度腹泻,即12 h内发作4次以上,干预人员降低肠内营养液输入速度为原有的50%,并给予患者止泻药,每6 h 1次,并采集粪便作细菌培养,对腹泻时间在48 h以上者给予短肽类配方喂养。④胃潴留,即12 h胃潴留量在1000 ml以上,给予患者腹部X线检查喂养管位置,若为幽门后喂养则检查鼻肠管回抽物内葡萄糖,若存在葡萄糖则给予其胃肠动力药物;若非幽门后喂养则立即重新放置。⑤药物禁忌证,使用麻醉剂(机械通气的神经阻滞剂),去甲肾上腺素、肾上腺素 >0.1 μg/(kg·min)、多巴胺 >5 μg/(kg·min)则立即暂停喂养,在24 h后评估以判断是否喂养。⑥误吸。即患者呼吸道内抽吸出胃内容物。干预人员立即停止肠内营养,并实施支气管肺泡灌洗,采用X线检查喂养管位置,若正常则给予胃肠动力药物治疗,每隔6 h检查患者误吸状况。
1.3 观察指标
(1)营养状况:检测并记录两组肠内营养前、肠内营养1周后血清白蛋白、总蛋白、前白蛋白、转铁蛋白水平。
(2)免疫功能:采用流式细胞仪检测并记录两组肠内营养前、肠内营养1周后外周血T淋巴细胞亚群水平,包含 CD3+、CD4+、CD8+、CD4+/CD8+。
(3)早期肠内营养不耐受症状发生率:统计两组肠内营养期间呕吐、腹泻、胃潴留、腹胀、误吸等不耐受症状发生情况。
(4)观察并记录两组达到预期目标喂养量时间、ICU住院时间及机械通气时间。
1.4 统计学方法
采用SPSS 22.0统计学软件对数据进行统计分析,计量资料以“均数±标准差”表示,组间均数比较采用t检验;计数资料计算率,组间率的比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组肠内营养前后营养状况比较
肠内营养前两组患者营养指标比较差异均无统计学意义(P>0.05);观察组肠内营养1周后血清白蛋白、总蛋白、前白蛋白、转铁蛋白水平高于对照组,组间比较差异具有统计学意义(P<0.05),见表1。
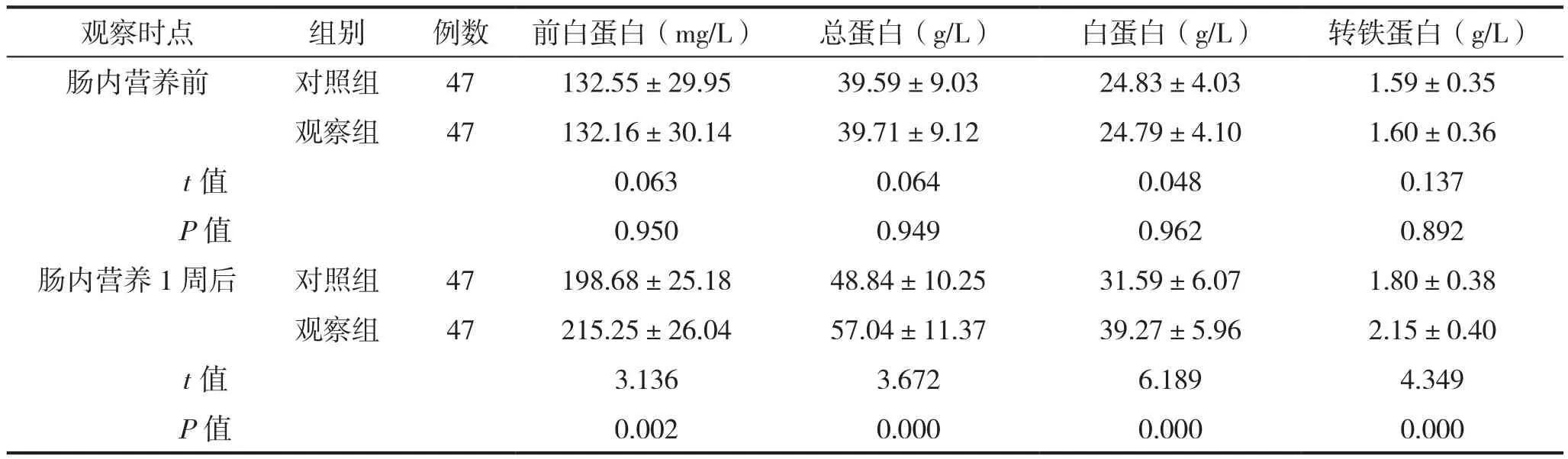
表1 两组肠内营养前后营养状况比较
2.2 两组肠内营养前后免疫功能比较
肠内营养前两组免疫功能指标比较差异均无统计学意义(P>0.05);观察组肠内营养1周后CD3+、CD4+、CD4+/CD8+水平均高于对照组(P<0.05)。见表2。
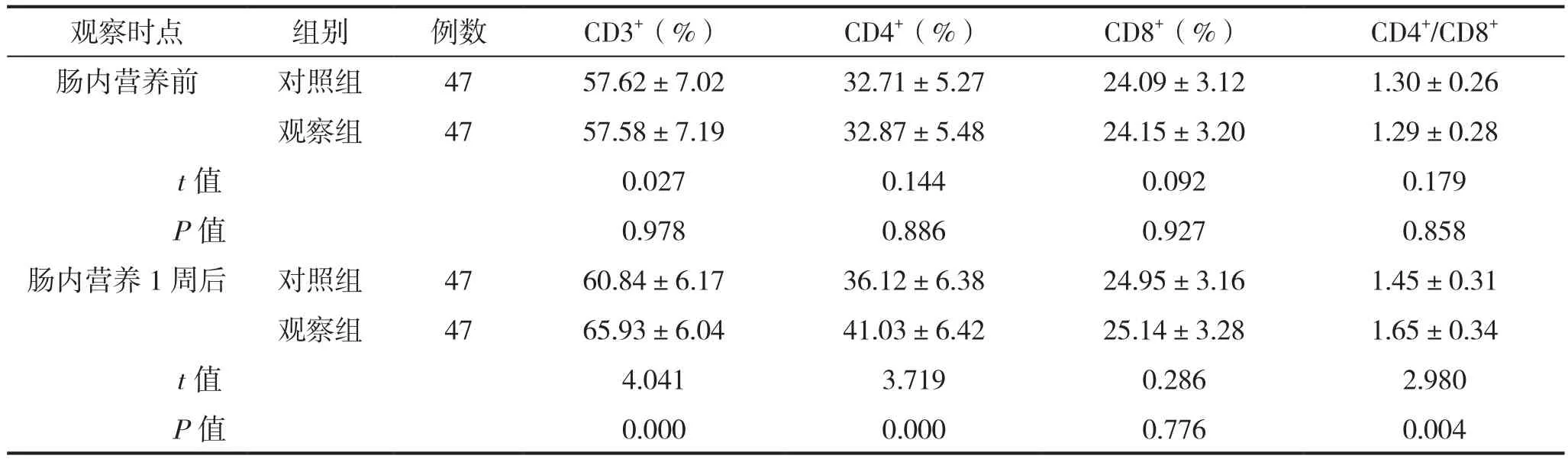
表2 两组肠内营养前后免疫功能比较
2.3 两组早期肠内营养不耐受症状发生率比较
观察组早期肠内营养不耐受症状发生率低于对照组,组间比较差异具有统计学意义(P<0.05),见表3。

表3 两组早期肠内营养不耐受症状发生率比较
2.4 两组达到预期目标喂养量时间、ICU住院时间及机械通气时间比较
观察组达到预期目标喂养量时间、ICU住院时间及机械通气时间短于对照组,组间比较差异具有统计学意义(P<0.05),见表4。
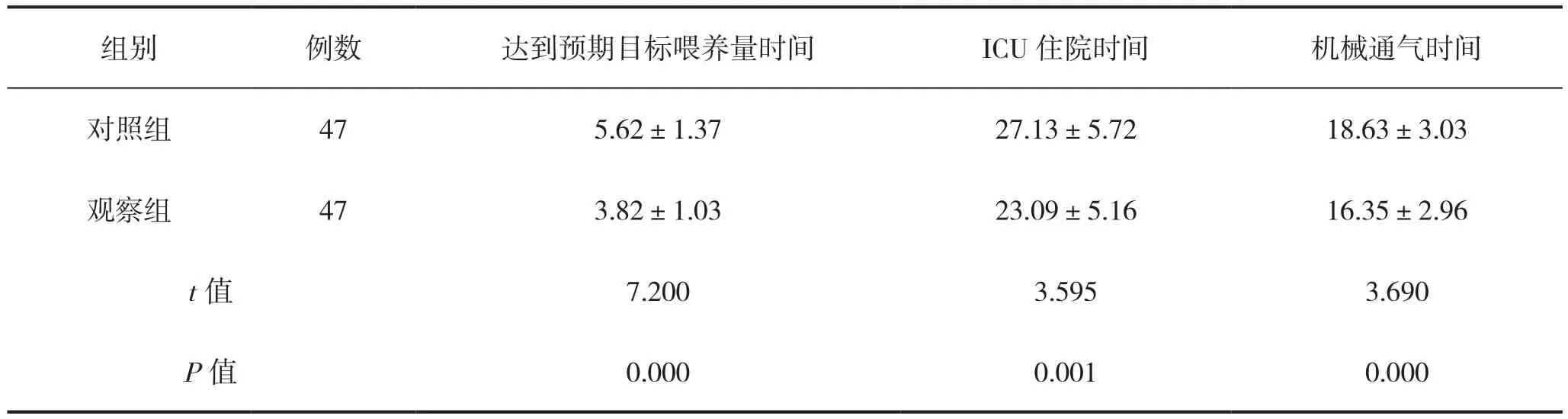
表4 两组达到预期目标喂养量时间、ICU住院时间及机械通气时间比较(d)
3 讨论
营养支持治疗对于改善重症胰腺炎患者机体内代谢状态,帮助生化指标恢复具有重要意义[4]。近年来,随着临床医学研究的进展,肠内营养已逐渐替代肠外营养成为重症胰腺炎患者的首选治疗措施,肠内营养治疗可对患者肠黏膜起到有效局部营养效果,避免肠外营养时患者长期禁食的缺陷,对肠黏膜细胞生长具有显著促进作用[5-6]。此外,肠内营养支持能够为肠道菌群正常生长起到保护作用,其安全性较高,帮助患者减轻痛苦[7]。因为重症胰腺炎患者通常存在腹腔高压的情况,其会造成胃肠功能紊乱,再加上肠内营养制剂的输入速度、时间等因素,最终可造成患者出现呕吐、腹胀等多种不耐受情况,对肠内营养支持治疗的效果造成负面影响[8-9]。本研究通过对重症胰腺炎合并腹腔高压患者实施肠内营养耐受性评估管理方案取得了显著效果。
本研究中,观察组肠内营养1周后血清白蛋白、总蛋白、前白蛋白、转铁蛋白水平均高于对照组。表明肠内营养耐受性评估管理方案可有效改善患者机体内营养水平。分析原因主要为,传统早期肠内营养治疗时,若患者出现呕吐、腹胀等不耐受症状时,干预人员会立即停止肠内营养输入,或降低输入速度,因此使早期肠内营养支持治疗效果不佳。如此反复下患者营养状况无法得到有效改善[10-11]。而肠内营养耐受性评估管理方案能够将患者不耐受症状实施分级,并对不同分级的症状实施针对性处理,从而避免盲目停止肠内营养支持治疗,提升患者早期接受治疗的耐受性,最终可提高机体营养水平[12-13]。本研究中,观察组肠内营养1周后CD3+、CD4+、CD4+/CD8+水平均高于对照组。表明肠内营养耐受性评估管理方案有效改善患者免疫功能。分析原因主要为,重症胰腺炎患者免疫功能已受损害,而机体营养不良状况又会进一步造成其免疫功能降低[14-15]。通过给予患者肠内营养支持治疗能够充分促进T淋巴细胞和免疫球蛋白的产生,调节内脏蛋白生存,从而有效改善小肠功能,使其发挥免疫调节功能[16-17]。通过肠内营养耐受性评估管理方案能够实施规范、准确评估,并采取有效措施解决患者胃肠道不耐受情况,从而确保肠内营养支持治疗的有效性,最终明显改善其机体免疫水平[18]。本研究中,观察组早期肠内营养不耐受症状发生率低于对照组,且观察组达到预期目标喂养量时间、ICU住院时间及机械通气时间短于对照组。分析原因主要为,通过评估患者不耐受症状,根据其严重程度进行分级,并给予针对性处理措施,从而转被动为主动,有效提高患者早期肠内营养耐受度,最终可有效缩短达到预期目标喂养量时间,帮助患者尽早恢复健康[19-20]。
综上所述,肠内营养耐受性评估管理方案应用于重症急性胰腺炎合并腹腔高压患者中可改善营养状况,增强免疫功能,减少不耐受症状发生,从而改善预后。
