IgG4相关性肾病2例报告
2022-01-20徐夏莲
陈 欣, 刘 红, 金 是, 徐夏莲, 林 攀*
1. 复旦大学附属中山医院肾内科,上海 200032 2. 上海市肾脏疾病临床医学中心,上海 200032
IgG4相关性疾病(IgG4-related disease,IgG4-RD)是一组以血清IgG4升高、组织内IgG4阳性浆细胞浸润及纤维化病变为特征的多系统性疾病。IgG4-RD可累及几乎所有器官,以泪腺、唾液腺、胰腺、肾脏、淋巴结、主动脉和腹膜后最多见。累及肾脏时称为IgG4相关性肾病(IgG4-related kidney disease,IgG4-RKD),主要表现为肾小管间质性肾炎(IgG4-TIN),累及肾小球时以膜性肾病(IgG4-MGN)多见[1],其他肾脏损害包括肾小球性病变(IgA 肾病、系膜增生性病变、膜增生样病变、毛细血管内增生性病变等)、肾脏炎性假瘤、慢性硬化性肾盂炎、肾动脉炎等病变[2]。
2019年复旦大学附属中山医院肾内科诊治2例IgG4-RKD,现将过程和结果报告如下。
1 病例资料
1.1 患者1入院资料 患者,男性,59岁,因“发现颈部肿物1年,血肌酐(Scr)升高1月余”于2019年6月入院。2019年5月,自行扪及颈部无痛性肿块,直径约3 cm,无红肿压痛,伴夜尿增多,无发热、关节痛、腹痛、腹泻等。尿蛋白(+),Scr 198 μmol/L,颈部超声提示双侧颌下腺回声改变伴周围淋巴结肿大。左侧颌下淋巴结活检病理示数堆腺泡上皮及导管上皮细胞,倾向腮腺炎病变。既往高血压病史12年,血压控制可。6月体格检查:血压142/92 mmHg(1 mmHg=0.133 kPa),左侧颌下可触及5 cm淋巴结肿大,质韧,活动度好,余无阳性体征。血红蛋白128 g/L,血小板295×109/L,白细胞8.42×109/L;尿蛋白(+),尿红细胞(-),尿蛋白0.82 g/d,尿β2微球蛋白24.05 mg/L(0~0.22 mg/L),N-乙酰氨基-β-D-葡萄糖苷酶(N-acetyl-β-D-glucosaminidase,NAG)12.3 U/L(0.7~11.2 U/L);粪常规及隐血阴性;Scr 229 μmol/L,估算肾小球滤过率(estimated glomerular filtration rate,eGFR)26 mL·min-1·(1.73 m2)-1,IgG 33.02 g/L,IgG4 33.40 g/L,C3 0.68 g/L,C4 0.16 g/L,肿瘤标志物、自身抗体、免疫固定电泳阴性;彩超示左/右肾长径为108 mm/113 mm,彩超及CT示双侧颌下腺、纵隔、腹股沟淋巴结肿大,无肝脾肿大;眼科会诊示无泪腺肿大,肾活检病理诊断IgG4相关小管间质炎症,全片见18个肾小球,其中2个球性硬化,余肾小球病变不明显。肾小管间质病变重度,大于90%小管结构破坏,较多蛋白管型,席纹状间质纤维化(+),大量炎细胞浸润,可见较多浆细胞、嗜酸粒细胞浸润,血管壁内膜增厚,见图1A;免疫荧光阴性。免疫组化结果示间质IgG4阳性的淋巴细胞浸润[散在少量(+),约78个/HPF],见图1B。
1.2 患者1治疗过程 患者既往外院活检示腮腺炎,血IgG4明显增高,全身多处淋巴结肿大,肾脏病理结果示IgG4-TIN诊断明确。2019年6月29日起,予注射用甲泼尼龙(500 mg,静滴,1次/d),3 d后改为甲泼尼龙片(24 mg,口服,1次/d)。治疗第2天起,患者颈部淋巴结明显缩小,复查Scr 223 μmol/L。3周后随访Scr 146 μmol/L,尿蛋白(-),IgG 18.9 g/L(治疗前33.02 g/L),IgG4 12.6 g/L(治疗前33.40 g/L),胸部CT示纵隔淋巴结较前缩小。出院后2个月甲泼尼龙片减量(20 mg,口服,1次/d),后甲泼尼龙片逐渐缓慢减量,2020年4月起,予甲泼尼龙片(4 mg,口服,1次/d)。2020年6月随访Scr 109 μmol/L,IgG4 4.76 g/L,尿蛋白阴性,复查超声未见淋巴结肿大。
1.3 患者2入院资料 患者,男性,68岁,因“大量蛋白尿、血尿3月”于2019年5月入院。2019年2月起检查发现尿蛋白()~(),血白蛋白22 g/L,Scr 100~112 μmol/L。予雷公藤(20 mg,口服,3次/d)等治疗无好转。既往高血压病史2月余,血压控制可。体格检查:血压150/81 mmHg,可触及腮腺、颈部、锁骨区、腋窝肿大淋巴结。血红蛋白135 g/L,血小板232×109/L,白细胞10.23×109/L;尿蛋白(),尿红细胞(-),尿蛋白5.64~7.22 g/d;粪常规及隐血阴性;Scr 116 μmol/L,eGFR 55.43 mL·min-1·(1.73 m2)-1,白蛋白22 g/L,IgG 42.45 g/L,IgG4 41.20 g/L,C3 0.48 g/L,C4<0.06 g/L,总补体20.0 IU/mL;免疫固定电泳IgG-κ M带阳性(浓度17.6 g/L,百分比20.0%);抗磷脂酶A2受体(PLA2R)抗体<2.0 RU/mL;彩超结果示左/右肾长径115 mm/116 mm,双侧颈部、锁骨上及腋窝淋巴结肿大;CT结果示两肺多发小结节,肺门纵隔、双侧腋窝、腹膜后、两侧髂血管旁、盆壁及腹股沟区多发肿大淋巴结;PET-CT示IgG4-RD累及双侧泪腺、多处(双侧腮腺区、颈部、锁骨区、纵隔、双肺门、双侧腋窝、肝门区、腹膜后、盆腔及双侧腹股沟)淋巴结可能。骨髓穿刺涂片示浆细胞占2.5%,形态无殊,骨髓活检示浆细胞数目稍增多,增生浆细胞约占骨髓有核细胞的6%,略呈单克隆性增生,染色体核型分析显示为46,XY[13]基因阴性;肾活检病理诊断为膜型病变伴小管间质炎症,全片可见32个肾小球,其中1个球性硬化,毛细血管袢壁增厚、走行僵硬。中度肾小管间质病变,约小于5%小管萎缩,灶性间质纤维化(+),中等量炎细胞浸润聚集成团,以小淋巴细胞为主。小动脉弹力层分层,内膜增厚,管腔狭窄,管壁增厚(图2A)。免疫荧光结果:IgG(+),IgG1()、IgG2()、IgG3(+)、IgG4()、Lambda(),THSD7A(+)呈颗粒状、团块状在血管袢弥漫分布,IgA、IgM、C3、C4、C1q、FIB、Kappa、PLA2R均阴性。肾间质部分IgG阳性细胞数目多于IgG4阳性浆细胞,IgG4阳性与IgG阳性浆细胞比<20%,见图2B。
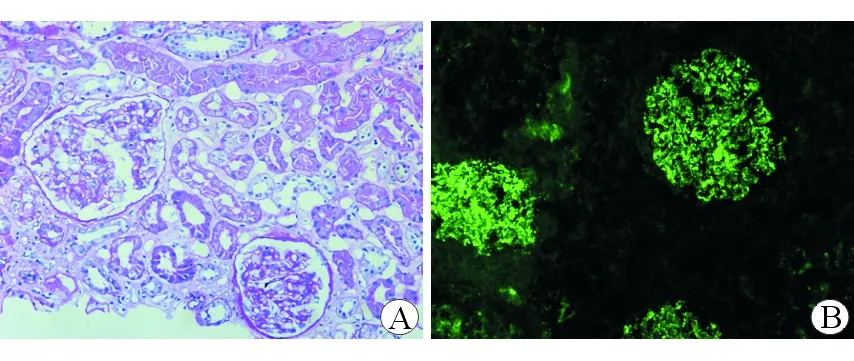
图2 患者2肾脏病理图
1.4 患者2治疗过程 患者血IgG、IgG4显著升高,双侧泪腺及多处淋巴结肿大,肾活检示PLA2R阴性膜性病变伴小管间质炎症;虽伴免疫固定电泳阳性,但无明显骨质破坏,骨髓图片及活检克隆性浆细胞<10%,可排除多发性骨髓瘤,IgG4-RKD诊断明确。2019年5月9日起,予醋酸泼尼松(40 mg,口服,1次/d)+环磷酰胺(cyclophosphamide, CTX)1 g冲击治疗。治疗第2天患者浅表淋巴结明显缩小,双下肢水肿改善。1个月后随访结果:IgG 21.01 g(治疗前42.45 g/L),IgG4 20.80 g/L(治疗前41.20 g/L),Scr 109 μmol/L,尿蛋白3.61 g/d,白蛋白35 g/L。其后每月1次CTX 1 g冲击治疗,共5次(累积剂量5 g),泼尼松逐渐减量至15 mg qd,随访尿蛋白3.39 g/d、白蛋白39 g/L、Scr 107 μmol/L。2019年11月患者出现上呼吸道感染(咽痛、咳黄色痰)后蛋白尿加重,尿蛋白6.33 g/d、白蛋白28 g/L、Scr 95 μmol/L、IgG4 14 g/L。予以抗感染治疗好转后,行第6次CTX 1 g冲击治疗(累积剂量6g),出院后予以泼尼松(15 mg,口服,1次/d)、他克莫司(1 mg,口服,1次/12 h,浓度2.5 ng/mL),2020年7月泼尼松减量至10 mg qd,他克莫司继续维持(1 mg,口服,1次/12 h)。2020年2月至10月期间随访,尿蛋白从6.33 g/d降至2.27 g/d,白蛋白从35 g/L升至38 g/L,Scr从101 μmol/L降至92 μmol/L,IgG4从5.73 g/L降至3.99 g/L。
2 讨 论
肾脏是IgG4-RD最常累及的器官之一,IgG4-RD好发于40岁以上中老年男性,平均年龄为65岁[3],其发病率和患病率尚缺乏大型临床数据资料。一项对于肾活检病理的回顾性研究[4]发现,近15年来日本40岁以上男性IgG4-RKD发病率为0.9~3.1/100万,但由于不常规进行IgG4染色,其发病率可能被低估。一项美国的研究[5]回顾了既往10年的肾活检病理,在既往82例诊断为间质性肾炎的病例中,有12例染色符合IgG4-TIN的标准。IgG4-TIN占所有肾脏活检的1%,占所有与肾小球疾病无关的活检的13%,提示原发性TIN的活检中应常规进行IgG4染色。
IgG4-RD的病因及发病机制仍不明确。IgG4抗体本身是不致病的,临床所检测到IgG4的升高可能仅代表相关免疫反应的激活[6]。血清及组织IgG4的升高并不是IgG4-RD特有表现,还可见于多种疾病,如多中心Castleman病、过敏性疾病、嗜酸性肉芽肿、多血管炎(Churg-Strauss syndrome)、结节病等[7]。越来越多证据表明该疾病与自身免疫相关,T细胞特别是细胞毒性CD4+T细胞(CD4+cytotoxic T lymphocytes,CD4+CTL)、滤泡辅助T细胞(follicular helper T cell,Tfh)起重要作用。在IgG4-RD患者的外周血及炎症组织中均可见CD4+CTL细胞克隆增殖,并可分泌促纤维化细胞因子IFN-γ和TGF-β,促进IgG4-RD受累器官的纤维化。临床使用利妥昔单抗,介导B细胞耗竭,从而诱导疾病临床缓解,与CD4+CTL数量的减少有关[8]。同样,Tfh细胞在IgG4-RD患者外周血及受累组织中显著增高,与健康人群相比,IgG4-RD患者的Tfh细胞显著促进B细胞增殖、抑制其凋亡、促进其向记忆B细胞和浆细胞转化,最终导致IgG4分泌的增加[9]。经糖皮质激素治疗后,Tfh细胞和浆母细胞显著下降,疾病复发时再次升高[10]。以上机制表明,IgG4相关疾病的组织器官损害及纤维化是T细胞和B细胞相互作用、促进多种炎症因子生成等导致的结果[11],具体发病机制还有待进一步开展基础和临床研究加以证实。
IgG4-RKD患者症状常与肾外表现有关。日本一项多中心研究[3]显示,153例IgG4-RD中15%为IgG4-RKD,其中96%存在肾外脏器受累,包括涎腺炎(83%)、淋巴结肿大(44%)、自身免疫性胰腺炎(39%)、泪腺炎(30%)、肺损害(26%)及其他表现。肾脏受累可表现为少量至中等量蛋白尿,常伴肾功能损害,偶有镜下血尿、NAG酶升高等[12]。本研究中的2例患者,患者1表现为少量蛋白尿,中重度肾功能损害,合并涎腺炎、淋巴结肿大;患者2表现为肾病综合征,轻度肾功能损害,合并淋巴结肿大、肺内结节。故可见IgG4-RKD多合并肾外表现,蛋白尿、肾功能表现因肾脏病变累及肾小球或肾小管的不同,存在较大差别。因IgG4-RD常表现为多发肿块,非常容易误诊为恶性肿瘤,必要时完善胸腹部CT或PET/CT,行鉴别诊断。
IgG和IgG4水平增高并非IgG4-RD诊断的金标准。梅奥诊所的研究[13]提示,IgG4-TIN中88%患者IgG和IgG4水平升高,56%患者补体降低,其中C3下降占43%,C4下降占46%。在日本的研究[14]中,所有IgG4-RKD患者均有IgG和IgG4的升高。尽管IgG4水平越高越支持IgG4-RD的诊断,但IgG4并非特异性指标,IgG4在其他疾病如支气管扩张、胆道疾病和胰腺恶性肿瘤中,亦会轻度升高[15]。同时,血清IgG4正常也不能排除IgG4-RD的可能。参照2011年日本肾脏学会IgG4-RKD综合诊断指南[16],诊断依据包括累及1个或多个器官的弥漫性/局限性肿大或占位性病变;血清IgG4≥1 350 mg/L;组织病理学结果示大量淋巴细胞、浆细胞浸润及纤维化,IgG4+浆细胞浸润:IgG4+/IgG+浆细胞比例>40%,且IgG4+浆细胞数>10个/高倍镜视野。同时需排除恶性肿瘤、干燥综合征、原发性硬化性胆管炎、继发性腹膜后纤维化、Wegener肉芽肿、结节病、Churg-Strauss综合征等疾病。北美肾脏病学会基于血清学、影像学、病理学提出了更加细化的诊断标准[13]。但是上述诊断标准多基于IgG4-TIN患者,且IgG4的界值定义仍不明确。本研究的2例患者IgG、IgG4均明显升高,补体降低,在排除其他疾病后,支持IgG4-RKD的诊断。
影像学对于诊断及评估IgG4-RKD的重要价值在于可协助明确IgG4-RD累积脏器及与恶性肿瘤等鉴别诊断[17]。IgG4-RKD患者常伴有肾脏相关影像学异常。超声特异性不高,部分患者可见肾脏体积增大、弥漫病变。IgG4-TIN患者增强CT多表现为双侧肾脏弥漫增大,或轮廓正常,肾实质结节状、楔形或花斑状病灶,IgG4-MGN双肾弥漫型增大不明显[1]。MRI表现为双侧肾脏T1WI呈低信号,T2WI呈稍低信号,DWI呈高信号病灶,增强扫描相对正常肾组织呈低灌注[18]。本研究2例患者由于血肌酐偏高,存在造影剂肾病风险,未行增强CT及MRI检查,肾脏超声均提示双侧肾脏偏大(110 mm+),符合IgG4-RKD影像学表现。
肾活检为确诊IgG4-RKD的金标准,肾组织中大量IgG4+浆细胞浸润是IgG4-RKD的特征性免疫组化表现。典型光镜病理特征为肾间质大量浆细胞及淋巴细胞浸润、席纹状纤维化[19],伴不同程度肾间质纤维化,也可有嗜酸性粒细胞浸润,部分小管萎缩及肾小管结构消失[20];逐步进展的间质性肾炎可导致肾纤维化、肾小球硬化,甚至进展为终末期肾病。日本肾脏病学会[21]提出,将肾组织IgG4+浆细胞计数>10个/HPF,或IgG4+/IgG+浆细胞比例>40%作为主要确诊指标之一,但这一诊断标准存在争议。梅奥诊所的学者[22]指出部分IgG4-RKD患者IgG4+/IgG+浆细胞比例<40%。有2例病例IgG4-RKD的病例报道[23-24]中,并无IgG4+浆细胞的显著升高,但患者肾活检均伴明显间质性肾炎,且有多处脏器累及,对激素反应佳。因此,日本的诊断标准特异性较高,但会造成一定程度的漏诊。肾脏活检中IgG4+细胞所占比例的界值有待更大样本的临床研究加以证实。本研究中患者1肾脏病理提示特征性席文状纤维化,间质内较多浆细胞、嗜酸性粒细胞浸润,IgG4+浆细胞>78个/HPF,肾小球IgG染色为阴性,IgG4-TIN诊断明确。
IgG4-MGN光镜符合膜性肾病的一般病理表现[3],免疫荧光可见肾小球基膜上IgG4、C3沉积,PLA2R阴性[25]。临床需要和原发膜性肾病相鉴别,原发膜性肾病存在内源性足细胞抗原,免疫复合物在上皮下沉积,多数患者肾组织PLA2R阳性。而IgG4-MGN检测PLA2R阴性,仅1/3患者肾小球内皮下及系膜区亦可见免疫复合物沉积[1],且多有其他器官累及的表现。Alexandar等[1]报道了9例IgG-MGN患者,肾脏病理均符合膜性肾病表现,平均蛋白尿8.3 g/d,白蛋白22 g/L,7例伴肾外表现,5例伴IgG4-TIN,免疫荧光PLA2R染色均阴性。随访了6例接受治疗的患者,激素联合吗替麦考酚酯或环磷酰胺(或单用激素),治疗效果佳,蛋白尿平均降低至1.2 g/d。本研究中患者2表现为肾病综合征,血清IgG、IgG4显著升高,PLA2R阴性,补体降低,累及泪腺及全身多处淋巴结,同时存在膜性肾病、间质性肾炎的病理表现,尽管病理提示IgG4+/IgG+浆细胞比例<20%(病理未报具体百分比),但考虑到病灶可能存在灶性分布,且对糖皮质激素治疗反应佳,故诊断为IgG4-RKD伴发膜性肾病。
根据2015年IgG4相关性疾病管理和治疗的国际共识指南[26],糖皮质激素是所有活动性未经治疗IgG4-RD患者诱导缓解的一线药物,除非患者存在糖皮质治疗禁忌证(2b/B级推荐)。其中IgG4-TIN属于迫切需要治疗的IgG-RD临床表现,不及时治疗可能导致患者肾功能出现不可逆损伤,进展为慢性肾脏病。通常使用泼尼松0.6 mg/(kg·d)或30~40 mg/d,治疗大多于2~4周内起效,一般表现为症状改善,包块缩小或肿大器官减小,器官功能改善,血清IgG4水平下降。一些情况下对糖皮质激素反应良好可协助诊断IgG4-RD[26]。部分患者糖皮质激素减量或停药后可能复发。指南[26]指出,单用糖皮质激素治疗无法控制病情,或长期使用糖皮质激素的不良反应不能耐受的,可以联用免疫抑制剂,但证据的有效性尚缺乏大规模前瞻性随机临床队列研究加以证实(4/C级)。一项中国的随机对照研究[27]提出,糖皮质激素联合吗替麦考酚酯较单用激素明显减少疾病复发。另一项前瞻性非随机对照研究[28]提出,糖皮质激素联合环磷酰胺短期疗效与糖皮质激素相当,但降低长期(随访1年)疾病复发率。免疫抑制剂针对IgG4-RKD的治疗尚缺乏大量文献报道。有前瞻性研究[29]发现,在30例IgG4-RKD患者中,运用利妥昔单抗1 000 mg/次(累积剂量2 000 mg),其中14例(47%)患者于6个月完全缓解,29例(97%)患者对治疗有反应,有不同程度疾病活动指标的下降。但另一回顾性研究[30]发现,运用利妥昔单抗后,37%患者病情复发。因此利妥昔单抗的疗效尚待进一步多中心、随机对照试验加以证实。对于维持治疗,指南推荐对高风险复发患者以小剂量糖皮质激素(2.5~5 mg/d泼尼松)维持治疗,但目前对于最佳维持治疗时间尚无定论。本研究2例患者使用糖皮质激素后,蛋白尿、肾功能、肿大淋巴结、IgG及IgG4水平均较前明显改善。但患者2经CTX治疗后,仍有大量蛋白尿,考虑可能与患者病程中感染相关,且病程迁延符合膜性肾病特点,出院后继续使用他克莫司,蛋白尿水平较前好转,但仍有中等量蛋白尿,因此使用小剂量糖皮质激素和免疫抑制剂维持,预防疾病复发。
IgG4-RKD患者虽对糖皮质激素反应佳,但之后其肾功能并不能完全恢复。一项超过1年的随访研究[30]提示,eGFR>60 mL·min-1·(1.73 m2)-1患者治疗后GFR没有进一步提高,eGFR<60 mL·min-1·(1.73 m2)-1患者治疗1个月后肾功能有所改善,但在长期随访中维持这一水平。部分患者甚至出现肾脏萎缩等慢性肾病表现。这表明IgG4-RKD对糖皮质激素反应佳,但仅部分肾功能恢复,长期控制可能需要运用小剂量糖皮质激素或加用免疫抑制剂[27]。本研究2例患者经过1年半的随访,糖皮质激素联合免疫抑制剂可以达到理想的疗效,患者肾功能及蛋白尿水平维持稳定,低蛋白血症完全纠正,IgG4水平基本降至正常,但需注意感染等情况可能再次诱发病情反复。
综上所述,IgG4-RKD在临床上极易漏诊及误诊。最常见的病理类型为IgG4-TIN、IgG4-MGN。本研究中2例患者共同点为血清IgG、IgG4升高,均伴肾外表现,如涎腺炎、淋巴结肿大等。不同点在于患者1为IgG4-TIN,表现为少量蛋白尿,伴夜尿增多、NAG升高等肾小管损伤表现,肾功能损害较重;患者2为膜性病变伴小管间质炎症,表现为肾病综合征,伴轻度肾功能损害。该病对于糖皮质激素治疗反应佳,表现为实验室指标好转及临床症状改善。因此,临床上对于高IgG、肾脏受累合并多发腺体或器官肿大患者,应高度警惕该病,需尽早完善血清IgG亚型分类、肾脏病理检查等,避免误诊、漏诊,以达到早诊断、早治疗的目的。
利益冲突:所有作者声明不存在利益冲突。
