钛酸亚铁材料的研究现状
2022-01-19王晓欢李胜浩史志铭新巴雅尔
王晓欢,李胜浩,史志铭,王 俊,新巴雅尔,刘 亮
(内蒙古工业大学材料科学与工程学院,呼和浩特 010051)
作为典型钛铁矿钛酸盐的FeTiO3是一种n型半导体材料,它具有与钙钛矿相同的[BO6]八面体,最大的不同之处是可变价Fe离子能够引起A位和B位离子价态变化并造成晶体缺陷,如氧空位。这些变化必然引起FeTiO3物理化学性质的改变,预示着广阔的应用前景。从晶体结构上讲,FeTiO3结构与赤铁矿相似,钛原子可以替换(001)平面上的三价铁离子。这种离子的替换进一步影响其电子结构,从而改变光学性能和电性能。此外,FeTiO3是一种含有铁和钛两种金属元素的双金属氧化物,这种结构预示着它具有很好的催化活性及离子储存性能。从能带结构上讲,没有改性的FeTiO3的带隙为2.5~2.9 eV[1-3],其光吸收范围在可见光范畴(390~760 nm),通过电子结构调控,价带电子吸收可见光容易跃迁至导带,而成为一种很好的可见光催化材料。另外,可以通过改变能带结构进而改变其导电性能,使其成为较好的离子导电材料。笔者总结了FeTiO3常见的制备方法及性能研究进展。
1 FeTiO3的制备方法
1.1 固相合成法
高温固相合成法是制备FeTiO3最早的方法,其制备基本过程是将反应物粉体按一定的比例充分混合、研磨,之后在真空下高温煅烧数小时后再经过处理,得到FeTiO3粉体。例如,NAYLOR等[4]将反应物研磨后充分混合,在1 165~1 300℃下真空煅烧30 h制备FeTiO3,反应式为Fe+Fe3O4+4TiO2=4FeTiO3。STIEKLER等[5]利用反应物在丙酮中研磨、晾干,混合物在1 000℃空气中加热24 h。研磨后在一氧化碳和二氧化碳混合气氛中1 000℃下灼烧6 h。最后放在已抽真空的硅试管中800℃煅烧14 d,并以50℃/h的速度冷却,得到FeTiO3,反应式为Fe2O3+2TiO2=2FeTiO3+1/2O2。还有研究者利用真空条件完成固相反应,加热温度为1 200℃,反应式为FeO+TiO2=FeTiO3[6]。
球磨法也是制备FeTiO3的一种常用方法。MØRUP等[7]研究了钛铁矿(FeTiO3)在惰性气氛下随着高能球磨时间的增加,其晶体结构、阳离子无序和磁性能的演变规律。钛铁矿的六方晶系结构在高能球磨128 h后仍保持不变,但中子衍射研究表明,球磨样品中Fe2+和Ti4+表现出明显的阳离子重分布现象。还有研究者将钛铁矿在室温下空气中球磨,球磨100 h后,钛铁矿完全转化为热亚稳态Fe2Ti3O9和Fe2O3相[8]。ABSALAN等[9]报道了一种利用钢球和二氧化钛纳米粒子高速球磨制备精细钛铁矿FeTiO3纳米粒子的机械化学方法。在球磨过程中,碰撞能引起局部高温,通过TiO2纳米粒子、氧气和钢球表面铁原子的反应,合成了典型的粒径为15 nm的纯FeTiO3纳米粒子。高温固相合成法制备FeTiO3耗能耗时,制备难度很高,现在应用较少。
另外,在制备过程中,焙烧气氛发挥着重要作用。它不仅决定相组成,还影响材料内部的晶体缺陷。XIAO等[10]研究了钛铁矿氧化过程的相变、形貌变化和氧化机理。FeTiO3在700~800℃氧化时转变为赤铁矿和金红石,在氧化温度达到900℃时形成假板钛矿。初始钛铁矿粉呈顺磁性,然而在中等温度(800~850℃)氧化后,产物表现出弱铁磁性。微观结构分析表明,在中等温度下,钛铁矿颗粒表面出现大量微孔,可以增强氧化过程中氧的传质。李晴宇等[11]将钛铁矿在氩气及氧化气氛中不同温度下进行煅烧。采用XRD及热分析研究了钛铁矿在不同温度下煅烧后的相组成及质量变化。在氩气气氛950℃下煅烧后,钛铁矿的物相组成没有发生变化;在空气中不同温度煅烧后,600~800℃较低温度区间,钛铁矿转变为热力学亚稳定的Fe2Ti3O9,950℃以上煅烧时,钛铁矿转化为热力学稳定的Fe2TiO5。钛铁矿的晶体结构由煅烧前的三方结构经过低温煅烧后转变为亚稳态六方晶系的Fe2Ti3O9,950℃以上煅烧后,晶体结构转变为斜方晶系的Fe2TiO5。
1.2 湿化学法
水热合成法可以制备出形貌可控、尺寸均一、结晶良好且团聚程度较轻的纳米材料。研究者们利用水热法制备出了不同形貌的纳米FeTiO3。两步连续水热法制备FeTiO3-TiO2空心球体,该空心球体具有较好的光催化效果[12]。GUAN等[13]利用水热法220℃保温10 h制备了钛酸铁纳米片,并表现出很好的催化活性和储锂性能。TAO等[14]首先将商用FeTiO3球磨后在120℃下磁力搅拌,水热处理2 h,干燥后制得FeTiO3纳米花,尺寸为厚5~20 nm、宽100~200 nm。ZHANG等[15]通过水热法,以钛酸盐纳米线前驱体为表面活性剂、FeCl2·4H2O为Fe源、硫脲为表面活性剂,成功制备了纳米圆盘、纳米立方体和纳米八面体等具有不同形态的纳米结构。WANG等[16]以MOF-Fe纳米棒为牺牲模板和前驱体,在N2气氛下进行热碳化,合成了三元TiO2@C/FeTiO3(TCF)空心纳米管。
溶胶-凝胶法因其制备工艺简单而被广泛应用。溶胶-凝胶法是制备纳米陶瓷粉体最成功的方法之一,制备的颗粒粒径分布较窄,具有明显的优越性。GU等[17]以溶胶-凝胶法为前驱体,利用静电纺丝技术制备了FeTiO3纳米纤维,其形貌如图1所示。SIVAKUMAR等[18]利用溶胶-凝胶法制备了FeTiO3/TiO2异质结,研究其光催化性能。YU等[19]利用溶胶-凝胶沉积和固态退火处理的方法制备了FeTiO3纳米棒(FTO⊂CNTs),并将其作为钠离子电池的阳极材料。MORÍN等[20]采用溶胶-凝胶法制备了几种不同比例的FeTiO3/TiO2催化剂,并研究了其光催化性能。
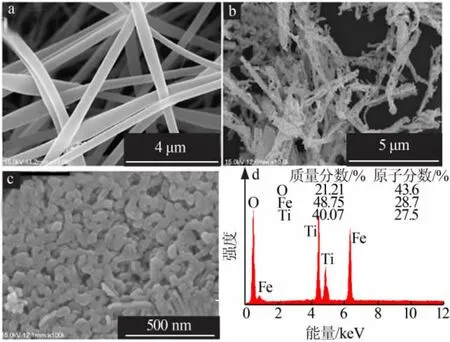
图1 FeTiO3/PVP复合纳米纤维在650℃煅烧前(a)和煅烧后(b、c)的SEM图及EDX结果(d)[17]Fig.1 SEM images of FeTiO3/PVP composite nano-fibers before(a)and after calcination at 650℃(b,c)and EDX results(d)[17]
此外,表面活性剂辅助模板法也被用来制备纳米晶FeTiO3陶瓷粉体,所得粉末在空气中以150~600℃的不同温度煅烧2 h。在600℃条件下,FeTiO3可以得到纯净的六方相[21]。微波加热,均相沉淀法合成了一系列纳米TiO2-Fe2O3复合材料[22]。利用脉冲激光沉积法在α-Al2O3(0001)衬底上制备了钛铁矿结构FeTiO3薄膜[23]。MONA等[24]采用3种不同的工艺合成FeTiO3粉体。第一种方法是在碱性条件下,用硝酸铁和氯化钛水溶液,通过铁离子和钛离子的简单共沉淀法合成FeTiO3;第二种方法是在100℃消耗氢氧根沉淀形成FeTiO3相;第三种技术是利用柠檬酸盐法制备FeTiO3粉体。共沉淀法、微波法和微波辅助煅烧法[25]也被用来制备FeTiO3纳米粉体和FeTiO3纳米花,其形貌如图2所示。

图2 水热法制备的FeTiO3-TiO2形貌图[11]Fig.2 SEM images of FeTiO3-TiO2 hollow sphere preparation by hydrothermal method[11]
2 FeTiO3的改性方法
到目前为止,对于FeTiO3的研究并不多,因此改性研究也只有半导体复合。大量研究表明半导体复合可以改善材料的光催化性能。通常,单一的半导体作为功能材料会存在一些不足,例如,单一半导体的光生电子空穴复合率较高,导致催化活性不佳。为了对半导体进行改性,研究者们会将两种半导体复合,使之形成异质结构的催化剂。这种复合一般是指将催化剂半导体与另一种禁带宽度较小的半导体进行复合。以最常用的TiO2催化剂为例,半导体复合体系 有:TiO2-ZrO2[26]、TiO2-CuO[27]、TiO2-CeO2[28]、TiO2-Ag2O[29]和TiO2-SnO2[30],由于两种半导体存在能 级差,所以复合半导体具有不同于纯半导体的能带结构。当紫外光照射时,光生电子由TiO2的价带迁移至导带,空穴聚集在窄带隙半导体的价带,实现了电子-空穴有效分离。
在此研究的基础上,研究者对FeTiO3也进行了复合改性,合成了一系列FeTiO3/TiO2复合材料,并研究其光催化性能。GAO等[31]制备了FeTiO3/TiO2异质结,研究表明由于复合之后光生空穴可以在FeTiO3和TiO2的价带(VB)之间转移,所以相比单相FeTiO3,FeTiO3/TiO2复合材料具有极高的光催化效率。SIVAKUMAR等[18]同样制备了FeTiO3/TiO2异质结,发现在紫外-可见光下FeTiO3/TiO2异质结对有机染料RY84和RB5的降解活性高于纯TiO2。原因是这种半导体间的电子空穴分离过程增加了TiO2表面空穴的寿命,因此异质结FeTiO3-TiO2比纯TiO2的光催化活性更高。ABBASI等[32]制备了FeTiO3/TiO2/Ag纳米复合材料,研究结果表明,该材料在可见光下对罗丹 明B污染物的光催化活性最高。HAN等[12]将FeTiO3和TiO2复合制备了空心球,在模拟光照条件下FeTiO3/TiO2空心球具有很好的光催化水氧化活性,原因是FeTiO3/TiO2空心球表面空间电荷区存在有效的异质界面和内建电场,对促进光致电子空穴对的分离具有积极的作用。具有适当物质的量比的FeTiO3/TiO2空心球中的光生载流子比单相FeTiO3空心球中的载流子具有更高的分离效率和更长的寿命。WANG等[16]制备了三元TiO2@C/FeTiO3(TCF)空心纳米管,包括中空的针状的框架、中间导电碳层和单分散FeTiO3纳米粒子嵌入碳层,由于这样的结构特性,空心TCF复合材料能有效地收获全频谱光能量,增强界面电荷分离和抑制复合光生电子空穴对,导致光电压增强。DADIGALA等[33]制备了太阳光驱动的C-TiO2/FeTiO3复合材料,在阳光照射下,C-TiO2/FeTiO3催化剂能有效降解甲基橙(MO),并显示出比纯FeTiO3或C-TiO2更高的光催化活性,其中含10%(质量分数)FeTiO3的C-TiO2/FeTiO3光催化剂的光催化活性最高。这是因为C-TiO2与FeTiO3之间形成了紧密接触的异质结构,使得电荷转移更容易,电子空穴对的分离更有效,从而提高了复合材料的光催化活性。ZHANG等[34]合成了α-Fe/FeTiO3/TiO2复合材料,研究表明α-Fe/FeTiO3/TiO2对 亚 甲基蓝具有较高的光催化降解效率。此外,还有研究者研究了FeTiO3/TiO2复合材料的电池性能。LI等[35]将FeTiO3和TiO2复合,制备出FeTiO3/TiO2@C柔性纤维膜,相比纯FeTiO3,该复合材料表现出较好的倍率性能和循环性能,主要归因于TiO2基体体积变化小、FeTiO3容量大和良好的3D网络导电性的协同效应。将过渡金属氧化物与TiO2混合是提高过渡金属氧化物和TiO2阳极性能的好方法,可以将过渡金属氧化物高容量的优点与TiO2的结构稳定性结合起来。
3 FeTiO3的性能研究
3.1 磁性
FeTiO3本身具有磁性,研究者对FeTiO3的磁性进行了分析。MØRUP等[7]研究了FeTiO3在惰性气氛中经过长时间高能球磨后晶体结构、阳离子无序和磁性能的演化。穆斯堡尔谱研究表明Fe2+磁超精细场,球磨前大约是5 T,经过超过4 h的球磨后,广泛分布的超精细场大约为40 T。球磨法使钛铁矿的晶体尺寸减小到20 nm左右,也导致了阳离子的无序化,但保持了六方晶体结构。由球磨引起的缺陷和阳离子无序导致了超精细场显著增加(高达约40 T),但与一些球磨铁酸盐相比,奈尔温度(TN)并不影响球磨。FUJII等[36]采用等离子溅射技术,在α-Al2O3(001)衬底上制备了外延FeTiO3+δ(001)薄膜。FeTiO3+δ薄膜的结构和磁性能在很大程度上依赖于溅射过程中的残余氧分压。低温下R3对称性薄膜具有铁磁性,而具有R3c对称性的非化学计量的FeTiO3+δ在室温下具有反铁磁性。FUJII等[37]研究发 现Fe2+和Ti4+之间的能级很接近,所以Fe2+和Ti4+之间有可能存在价间电荷转移。为了阐明FeTiO3中Ti离子的真实电子结构,在Ti2p-3d激发态上进行了共振光电发射光谱(RPES)和X射线磁圆二色性(XMCD)测试。RPES谱清晰地显示了价带Ti三维态的部分态密度。价带顶部的Ti三维态与Fe三维态重叠。此外,在Ti L2,3边的XMCD谱表明,尽管Ti4+在一般意义上具有非磁性,但FeTiO3中的Ti离子具有较大的磁极。HOJO等[38]利用脉冲激光沉积法在α-Al2O3(0001)基板上制备了0.8FeTiO3·0.2Fe2O3外延薄膜,研究了其电和磁性。有序相薄膜为p型半导体铁磁体,居里温度在270 K左右。SRINIVAS等[21]采用溶胶-凝胶自点火法制备了不同粒度分布的FeTiO3纳米粒子。将制备好的粉末在适当的温度下退火,得到纳米晶FeTiO3,并进行了微观结构和磁化表征。结果表明样品在15 K以下为弱铁磁性。所有样品在高于尼尔温度时,均完全遵守了Curie-Weiss定律。滞后曲线在峰值温度以下表现为有限矫顽力,在室温下无矫顽力。偏置磁场冷却后各样品的磁化曲线(MH曲线)均表现出TN以下的交换偏置,这是由于样品的尺寸和表面效应是有限的。交换偏置是由表面自旋无序引起的弱铁磁性和铁离子混合价态引起的铁磁性相互作用引起的。
3.2 光催化性能
快速的工业发展导致大量的有毒污染物的排放,严重破坏了环境,甚至威胁到了人类的健康。光催化是一种非常有价值和潜力的技术。尽管可见光光催化技术近年来得到了广泛的研究,但是其在废水处理中的实际应用仍然存在很多问题。1)可见光的利用率低。目前研究的催化剂材料一般对可见光的利用率较低,多在紫外区域,如果能实现对更宽的太阳光光谱响应,就可以提高光子的利用率,提高光催化效率。2)量子效率低。光生载流子形成的电子-空穴对中绝大部分都在激发后迅速复合,降低了量子效率。这在很大程度上阻碍了催化剂的实际应用。另外,较细小的光催化剂颗粒具有较大的表面能,在范德华力的作用下容易团聚,进一步降低量子效率。3)分离困难。常用的光催化剂集中于纳米尺寸,较小的纳米颗粒使得光催化反应结束后难以从水相中分离,很大程度上增加了光催化技术的成本。探究易分离的催化剂成为重要的研究方向。4)重复使用差。较细小的光催化剂具有较大的比表面积和表面能,有利于电荷的分离和污染物的吸附,然而,较小尺寸也导致了纳米颗粒易于团聚,影响光催化的性能,重复利用率低。5)光降解组分单一。大多数研究都集中于某一种污染物质的光催化降解。工程上污染物质往往存在多组分,所以单一目标物的研究与实际情况相距较远。对可见光光催化材料的结构和形貌的合理设计和构筑,能够克服上述问题,提高光催化性能。比如,无机空心球具有更大的表面积,提升了其光催化降解有机污染物的性能,有利于分离和重复使用。
到目前为止,对于钛酸亚铁性能研究较多的就是光催化。GAO等[31]发现水热法制备的FeTiO3与TiO2异质结催化剂在可见光照射下对气相2-丙醇矿化具有良好的光催化活性。ABBASI等[32]研究了FeTiO3/TiO2/Ag纳米复合材料的光催化性能,研究显示光催化剂在以罗丹明B、亚甲基蓝、甲基橙为污染物模型中表现出良好的光催化性能。DADIGALA等[33]以不同质量分数的FeTiO3为原料,合成了阳光驱动的C-TiO2/FeTiO3复合材料。在阳光照射下,C-TiO2/FeTiO3光催化剂有效降解了甲基橙,其光催化活性远远高于纯FeTiO3或碳掺杂二氧化钛(C-TiO2),其中FeTiO3质量分数为10%的C-TiO2/FeTiO3光催化剂的光催化活性最高。ZHANG等[34]还原Fe3O4@TiO2合成α-Fe/FeTiO3/二氧化钛,随后氮化处理。制得的样品对亚甲基蓝具有很好的光催化效果,降解率高达99.8%。PAN等[39]以甲基苯基亚砜为探针,在可见光辅助的FeTiO3/过硫酸盐体系中验证了Fe(Ⅳ)的存在。FeTiO3/过硫酸盐/光体系能够通过光生高价Fe(Ⅳ)选择性降解四环素和双酚A等电离势较低的芳香族化合物。分析表明,FeTiO3表面Fe(Ⅲ)与SO42-之间形成的配合物是活性差的原因。MORADI等[40]采用超声辅助法制备了FeTiO3/GO纳米复合材料,提出了FeTiO3/GO纳米复合材料可作为一种能够成功去除水溶液中酚类化合物的高稳定性催化剂。FeTiO3/GO纳米复合材料在5次循环后降解苯酚的效率仅下降了10.8%,苯酚浓度越高,降解效率越低,在最佳条件下辐照240 min,降解效果更好。清除剂的作用表明,超氧自由基和羟基自由基在光降解过程中起主要作用。
作为光催化材料,钛酸亚铁的优势在于:适当的带隙(2.5~2.9 eV),其光吸收范围在可见光范畴,可以解决可见光利用率问题;钛酸亚铁具有特有的磁性,可以很好地解决分离回收问题。针对量子效率低的问题,可以采用离子掺杂方法进行改性,力争解决其光生载流子复合问题。关于钛酸亚铁离子掺杂改性目前还没有受到关注。还原气氛下异价离子掺杂将会改变离子价态组成及氧空位浓度,从而改变催化性能。
3.3 储锂性能
锂离子电池广泛应用于手机、电脑、相机等便携式电子产品,同时在电动汽车和混合动力汽车上也表现出广阔的应用前景。目前,钛基锂离子电池负极材料的研究日渐广泛。钛基氧化物材料(如TiO2和LiTiO2)相对于传统碳负极材料具有较高的电压平台、充放电过程中体积变化小等优点,具有很好的安全性和循环稳定性,被认为是一种非常有应用前景、可替代碳的新型负极材料。钛酸锂(Li4Ti5O12)也被称为“零应变”材料,具有优异的结构稳定性,可有效避免充放电过程中因材料体积变化导致的容量衰减和循环稳定性不佳等问题,大大提高材料的循环性能和使用寿命。但是从研究现状来看,目前研究的钛基锂离子电池负极材料的电容量并不高,其主要原因是较低的理论容量、较低的电导率和低的锂离子传输速率。例如,Li4Ti5O12材料具有较低电子电导率(10-13S/cm)和锂离子传输速率(10-13~10-9cm2/s),这就造成较大的首次不可逆容量和倍率性能不佳等问题。
FeTiO3是一种典型的过渡金属钛酸盐,具有较高的理论容量(530 mA·h/g)。YU等[19]制备了FeTiO3纳米颗粒嵌入碳纳米管(FTO⊂CNTs),FTO⊂CNTs电极具有多项显著的优势,包括一个中空的内部混合纳米结构,实现了完全封装超微电活性单位、灵活的导电碳矩阵和稳定的固态电解质界面。FTO⊂CNTs电极提供了一个良好的循环稳定性(首次放电比容量为358.8 mA·h/g,200次循环后放电比容量为100 mA·h/g)和优异的电容,库仑效率高达99%。LI等[35]制备了三维网络FeTiO3/TiO2@C柔性纤维膜。直接用作阳极,该电极在750℃煅烧3 h后在电流密度为300 mA/g下经过100次循环,可逆容量为205.4 mA·h/g。GUO等[41]利用TiO2/FeTiO3@C杂化微球作为LIBs正极材料,由于TiO2基体体积变化小,FeTiO3容量大,碳涂层导电性好等协同作用,使电池具有良好的循环和速率性能,在电流密度为100 mA/g时,电池容量 可 达 到441.5 mA·h/g。BRUGNETTI等[42]利用 球磨和水热法 制 备了FeTiO3,并将其作为电池负极材料,研究结果显示第一次阳极脱渗的比容量约为150 mA·h/g,循环5次后稳定在125 mA·h/g。GUO等[43]利用溶剂热法制备了多孔TiO2-FeTiO3@C三元复合材料,电化学实验结果表明,在电流密度为100 mA/g条件下,循环150次后,所制备的多孔电极材料的可逆容量为494.5 mA·h/g。速率能力测试表明,在电流密度为100、200、400、800、1 600 mA/g时,所获得的比容量分别为374.1、248.4、189.3、158.2、116.2 mA·h/g。
从目前的研究来看,研究者们试图通过对FeTiO3进行形貌调整或复合的方法来提高其作为电极材料的循环性能和倍率性能。但是,FeTiO3作为锂离子电池负极材料在高倍率下容量衰减严重,且循环性能较差。因此,其电化学性能仍然有提升空间。例如,可以通过掺杂或复合等方法改善其导电性,从而达到提高倍率性能和循环性能的目的。
4 结论和建议
综上所述,目前对于FeTiO3的制备方法做了一些探索,制备出了不同形貌的样品,对其磁性、催化性能和储锂性能也进行了研究。从FeTiO3的晶体结构和能带结构来讲,都预示着其具有更广泛的应用前景。因此,作为功能材料其研究范围和研究深度还有待于进一步拓展和深入。例如,可以通过改变制备工艺或离子掺杂等手段调控FeTiO3的微观结构,对FeTiO3进行改性研究,以获得更优异的物理化学性能,拓宽其在功能材料领域的应用范围。
