醋酸N-正辛基吡啶离子液体在不同溶剂中的荧光光谱分析
2022-01-12肖雪松苏桂田段寒风金耀东宋杨杨
田 鹏,肖雪松,苏桂田,段寒风,金耀东,宋杨杨,黄 涛,张 航*
1.沈阳师范大学化学化工学院,辽宁 沈阳 110034 2.沈阳师范大学物理科学与技术学院,辽宁 沈阳 110034
引 言
离子液体(ILs)是熔点低于100 ℃的盐,具有低蒸气压、高热稳定性和良好的导电性等独特的性能,引起了化学工业界和基础化学界的广泛关注,有着广泛的应用前景[1]。与传统易挥发有机溶剂相比,其蒸气压几乎可以忽略,因而人们称其为“绿色溶剂”。由于这些特点,离子液体是锂离子电池和双电层电容器的替代电解质[2-3]。离子液体在气相色谱[4]、液相色谱[5]、红外光谱[6]、紫外光谱[7]、荧光光谱[8]等分析化学领域广泛应用。可以通过改变其离子的搭配来调节其性质,以产生特定用途的化合物,由于其这种可设计性,又被称为“绿色设计者溶剂”。
Wells和Coombe[9]提供了淡水生态毒性测试,结果表明离子液体的毒性与阳离子上的烷基链长度有关,由四个碳组成侧链的烷基甲基咪唑阳离子离子液体毒性温和,而十二碳、十六碳和十八碳侧链的离子液体有剧毒。由吡啶,磷,铵以及四个碳的侧链组成的离子液体毒性温和,而有六个碳以上侧链毒性显著增加。由于一些离子液体在水中的溶解度高,离子液体在不同溶剂中的检测方法非常重要。
离子液体的光谱分析法用量较少、方法简单、结果准确。光谱法包括原子发射光谱法、原子吸收光谱法、紫外吸收光谱法[10]、红外吸收光谱法和激光拉曼光谱法[11]等,文献表明,离子液体在紫外光谱分析和红外光谱分析中应用较多,离子液体在可见光范围内出现异常吸收和荧光行为已经被报道,Burrel等在合成过程中对中间体进行系统纯化后,吡咯烷离子液体的荧光强度大大降低。Singh和Kumar测量了[C8mim]BF4/乙二醇混合物的荧光,核磁共振和傅里叶变换红外光谱,紫外-可见光谱,分析表明FDH荧光强度的降低不仅仅是由于这些ILs的高光吸收所致[12]。程德红等对BmimCl离子液体以280和340 nm激发光激发以测定其荧光光谱。陈旭伟等研究[13],进一步考查了在咪唑环上取代不同长度的烷基碳链和不同卤素阴离子对其荧光光谱的影响。
已报道离子液体的色谱检测方法包括离子色谱法和离子对色谱法等。离子色谱法需采用特殊阳离子交换柱,且基线冲洗时间长;离子对色谱分析涉及特殊试剂,价格昂贵,色谱柱平衡时间长。而荧光检测法[14]具有检测快速、准确、简便等优点。不同溶剂中离子液体的荧光光谱分析报道较少[15],本工作研究了鲜有报道的醋酸N-正辛基吡啶离子液体,考察了OP-OAc离子液体在不同溶剂和混合溶液中的荧光强度,水溶液的pH值对离子液体荧光强度的影响,荧光强度与离子液体浓度的相关性。以期建立一种较快速、简单、准确的光谱检测方法。
1 实验部分
1.1 材料与试剂
实验药品:OP-OAc离子液体自制(纯度>98%),氢氧化钠(天津市恒兴化学试剂制造有限公司),盐酸(国药集团化学试剂有限公司),无水乙醇和乙腈(天津大茂化学试剂厂),甲醇(辽宁永强试剂厂),乙酸(沈阳化学试剂厂),以上试剂均为分析纯,去离子水自制。
1.2 设备与仪器
AG285型电子分析天平(精度0.1 mg,瑞士METTLER-TOLEDO公司),KQ3200型超声清洗器(昆山市超声仪器有限公司),970CRT/XP型荧光分光光度(美国VARIAN公司)。
1.3 方法
称量0.050 0 g的OP-OAc于小烧杯中,分别配制以水、无水乙醇、甲醇、乙腈,乙酸作溶剂的1 000 μg·mL-1的标准液。
从OP-OAc标准液中各取5.00 mL,分别用水、无水乙醇、乙腈、乙酸四种溶剂溶解制成500 μg·mL-1OP-OAC。设置激发狭缝10 nm,发射狭缝10 nm,扫描速度600 nm·min-1,扫描范围190~600 nm,进行荧光光谱扫描,确定不同溶剂溶解OP-OAc的最大激发波长和最大发射波长。
从OP-OAc标准液中分别移取0.25,0.50,0.75,1.00和1.25 mL于10 mL容量瓶中,用水为溶剂分别配成浓度为25,50,75和100 μg·mL-1的待测溶液,扫描并分析OP-OAc的浓度对其荧光强度的影响。
甲醇-水混合溶剂的配制:分别取1.00 mL以甲醇为溶剂的OP-OAc标准液于9个10 mL容量瓶内,用水定容后制成甲醇与水的比例为1∶9浓度为100 μg·mL-1的混合溶液;分别量取1~8 mL甲醇溶剂相应加入其中,余下体积以水定容,得到甲醇∶水=2∶8,3∶7,4∶6,5∶5以此类推的8种的混合溶液。乙醇-水、乙腈-水混合溶剂以同样的方法进行配制,通过荧光光谱扫描探究混合溶剂对离子液体荧光强度的影响。
分别配制0.2 mol·L-1的盐酸与氢氧化钠溶液,少量滴加到浓度为100 μg·mL-1的OP-OAc离子液体水溶液中,改变几种溶液的酸碱度,分别得到溶液pH值为2,4,6,8,10,12和14的溶液,进行荧光强度的测量。
2 结果与讨论
2.1 OP-OAc在不同溶剂中的荧光光谱分析
图1是四种溶剂中OP-OAc离子液体的荧光光谱。实验测得水、乙醇、乙酸、乙腈的激发波长分别为246,246,270和270 nm,由图可知发射波长分别是:369,358,326和305 nm,其最大发射波长相对于激发波长发生红移。OP-OAc离子液体在不同溶剂中的荧光强度为:I乙酸>I乙腈>I乙醇>I水;最大发射波长的大小顺序为:λem,水>λem,乙醇>λem,乙腈>λem,乙酸。
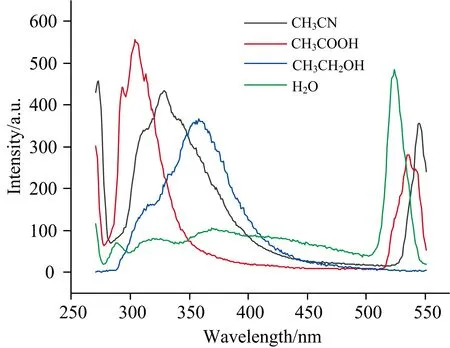
图1 四种溶剂中OP-OAc的荧光光谱Fig.1 Fluorescence spectra of OP-OAc in the four solvents
荧光物质基态与激发态的能量之间有差异,溶剂的电子运动使能级发生跃迁辐射后产生能量,因此溶剂的极化性与能级差是正比例的关系,能级差随着Δf的增大而增大,λem也会增大,荧光强度却减弱。由于水其极性较大,OP-OAc离子液体相应的发射波长较大,其荧光强度较小。而乙酸极性较小,OP-OAc离子液体相应的发射波长较小,其荧光强度较大。
2.2 OP-OAc浓度对荧光强度的影响
图2(a,b)分别是水中OP-OAc离子液体的荧光光谱和标准曲线。由图2(a)可知,随水中OP-OAc离子液体浓度的增加,OP-OAc的荧光强度呈比例增加。水中OP-OAc离子液体的荧光强度与质量浓度有很好相关性,得到线性回归方程:y=1.524x+164.2,相关系数为0.996 97。可以建立一种较快速、简单、准确的荧光检测OP-OAc离子液体的方法,同时也为其他具有类似结构的离子液体的分析检测提供参考。

图2 水中OP-OAc的荧光光谱和标准曲线(a):荧光光谱;(b):标准曲线Fig.2 Fluorescence spectra and standard curve of OP-OAc in water(a):Fluorescence spectra;(b):Standard curve
2.3 OP-OAc在混合溶剂中的的荧光强度
测量了不同比例混合溶剂中OP-OAc离子液体的荧光强度。图3(a,c,e)和(b,d,f)分别是OP-OAc离子液体于甲醇-水、乙醇-水、乙腈-水混合溶剂中激发波长为246 nm时发射波长的荧光光谱和荧光强度,由于加入的甲醇、乙醇、乙腈溶剂极性小于水,所以在同一激发波长下,混合溶剂的最大发射波长基于单一溶剂水蓝移。

图3 OP-OAc在甲醇-水,乙醇-水和乙腈-水中的荧光光谱和荧光强度(a):甲醇-水的荧光光谱;(b):甲醇-水的荧光强度;(c):乙醇-水的荧光光谱;(d):乙醇-水的荧光强度;(e):乙腈-水的荧光光谱;(f):乙腈-水的荧光强度Fig.3 Fluorescence spectra and fluorescence intensity of OP-OAc in methanol-water,ethanol-water and acetonitrile-water(a):Fluorescence spectra of methanol-water;(b):Fluorescence intensity of methanol-water;(c):Fluorescence spectra of ethanol-water;(d):Fluorescence intensity of ethanol-water;(e):Fluorescence spectra of acetonitrile-water;(f):Fluorescence intensity of acetonitrile-water
由图3可知,当加入的甲醇、乙醇、乙腈溶剂不断增加时,OP-OAc离子液体的荧光强度增加。加入量达到80%(体积分数)时,荧光强度呈现最大值;而在纯溶剂中却相对较弱,说明OP-OAc的荧光强度在混合溶剂中增强。因为单一溶剂与溶质形成的氢键,比混合溶液与溶质形成的氢键弱,使混合溶剂的离子液体结构更稳定,跃迁能量降低。而在混合溶液中,氢键作用力的减弱会破坏离子液体所具有的稳固结构,增大跃迁程度,发光效率也随之变强。当甲醇、乙醇、乙腈的比例超过80%时,OP-OAc构型的稳定性反而增强,分析认为由于OP-OAc对溶剂的氢键作用增强,导致发光效率减弱。因此OP-OAC离子液体的荧光强度随甲醇、乙醇、乙腈比例的增大而增强,溶剂与水的比例为8∶2时,荧光强度最大。
2.4 溶液pH对OP-OAc的荧光强度的影响
向100 μg·mL-1OP-OAc离子液体水溶液待测液中滴加适量的盐酸和氢氧化钠溶液,调节pH值,分别得到pH值为:2,4,6,8,10,12和14的7种溶液,进行荧光光谱扫描,探究不同溶液pH值与OP-OAc荧光强度间的关系。图4(a,b)分别是OP-OAc离子液体于不同pH值溶液的荧光光谱和荧光强度。
由图4可知,pH 10时,荧光强度最高,但pH超过10时,荧光强度开始减小;直至pH 14,荧光强度降至最低。OP-OAc离子液体由于所在溶液pH值的改变而具有不同构型,会使荧光位点发生改变,被打开或关闭。在不同pH值的溶液中,由于不同构型所占比例也存在很大的差异,综合原因导致离子液体的荧光强度出现较大的改变。

图4 OP-OAc于不同pH值溶液的荧光光谱和荧光强度(a):荧光光谱;(b):荧光强度Fig.4 Fluorescence spectra and fluorescence intensity of OP-OAc at different pH values(a):Fluorescence spectra;(b):Fluorescence intensity
3 结 论
通过OP-OAc离子液体在水、乙醇、乙腈、乙酸等4种溶剂的荧光光谱分析,得到如下结论:
(1)OP-OAc离子液体在不同溶剂中的荧光强度:I乙酸>I乙腈>I乙醇>I水;最大发射波长的大小顺序:λem,水>λem,乙醇>λem,乙腈>λem,乙酸。水中OP-OAc离子液体的荧光强度与浓度有很好相关性,得到线性回归方程:y=1.524x+164.2,相关系数为0.996 97。
(2)OP-OAC离子液体的荧光强度首先随甲醇、乙醇、乙腈比例的增大而增强,溶剂与水的比例为8∶2时,荧光强度最大;溶剂的比例超过80%时,荧光强度不再继续上升,而是突然降低。水中pH 10时,OP-OAc离子液体荧光强度最高,但pH超过10时,荧光强度开始减小;直至pH 14,荧光强度降至最低。
