氨溴索联合鼻塞式持续气道正压对肺透明膜病早产儿IL-6、IL-8水平的影响
2022-01-07王江峰陈炎炎
王江峰,陈炎炎
(1福州福兴妇产医院 新生儿科,福建 福州 350011;2福建医科大学附属福州儿童医院新生儿科,福建 福州 350005)
肺部表面活性物质(PS)匮乏是新生儿群体发生肺透明膜病(HMD)的主要因素,该疾病发病率与胎龄呈反比,是早产儿死亡的常见病因[1]。该疾病患儿的主要临床表现为出生后即出现呼吸困难、低氧血症等情况。鼻塞式持续气道正压(NCPAP)是常用的辅助通气设备,无需气管插管,即可为需氧治疗提供混合氧,有助于改善呼吸困难、呼吸衰竭等症状[2]。氨溴索是临床常用的祛痰药,具有抗氧化、抗炎的作用,有助于增加PS分泌,降低气道阻力,发挥肺保护作用。炎性因子参与了HMD的发生和发展[3]。本研究探讨氨溴索联合NCPAP治疗HMD早产儿的效果,现报道如下。
1 资料与方法
1.1 一般资料选取2018年5月至2020年5月福州福兴妇产医院和福州儿童医院收治的HMD早产儿68例。入选标准:符合HMD诊断标准[4];经肺部X线检查确诊者;伴有进行性呼吸困难、呻吟、口唇发绀等呼吸系统症状者;患儿家属同意参与本研究。排除标准:先天性器官发育不全或畸形者;基因突变者;吸入羊水、胎粪等其他原因所致呼吸窘迫者;合并其他肺部疾病者。本研究已获得我院医学伦理委员会批准。将患儿随机分为对照组和观察组,每组34例。对照组男女比例20∶14,平均胎龄(33.23±2.18)周,平均日龄(8.20±1.17)h,平均出生体重(2.10±0.18)kg;分娩方式:阴道分娩16例,剖宫产18例。观察组男女比例18∶16,平均胎龄(33.40±2.05)周,平均日龄(8.16±1.08)h,平均出生体重(2.13±0.15)kg;分娩方式:经阴道分娩15例,剖宫产19例。两组的一般资料比较,差异无统计学意义(P>0.05)。
1.2 方法两组患儿均给予保暖、呼吸道清理、营养支持、感染预防等对症支持治疗,同时实施NCPAP治疗。设置NCPAP持续气道正压通气系统(型号:NLF-200A,石家庄天行健医疗器械有限公司)参数:氧流量6~8 L/min,压力6~8 cmH2O,吸入氧浓度(FiO2)30%~60%。选取合适的鼻罩固定在患儿鼻部,实时监测血气指标,根据监测结果调整参数。待血氧饱和度(SpO2)在85%~95%范围,FiO2<30%,压力在2~3 cmH2O范围,动脉血氧分压(PaO2)>60 mm Hg且SpO2在93%以上时,改为面罩吸氧。观察组在此基础上给予盐酸氨溴索注射液(规格:4 mL∶30 mg;批准文号:国药准字H20051604;天津药物研究院药业有限责任公司)治疗,静脉给药30 mg·kg-1·d-1,每6 h给药一次。两组均连续治疗3 d。
1.3 观察指标①血气指标:采用血气分析仪(型号:PL2200,南京普朗医疗设备有限公司)测定患儿治疗前后的动脉血氧分压(PaO2)、二氧化碳分压(PaCO2)、氧合指数(PaO2/FiO2)。②炎性因子:采集患儿治疗前后的空腹肘静脉血3 mL,离心处理后取血清,低温保存,采用酶联反应分析法(ELISA)测定白介素-6(IL-6)、IL-8和肿瘤坏死因子-α(TNF-α)水平。
1.4 统计学分析应用SPSS 21.0统计软件处理数据。计量数据以±s表示,行t检验;计数数据以率表示,行χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 血气指标治疗3 d后,两组患儿的PaCO2水平均下降,PaO2和PaO2/FiO2水平均升高,且观察组的各项指标均优于对照组(P<0.05)。见表1。
表1 两组患儿治疗前后的血气指标比较(±s)
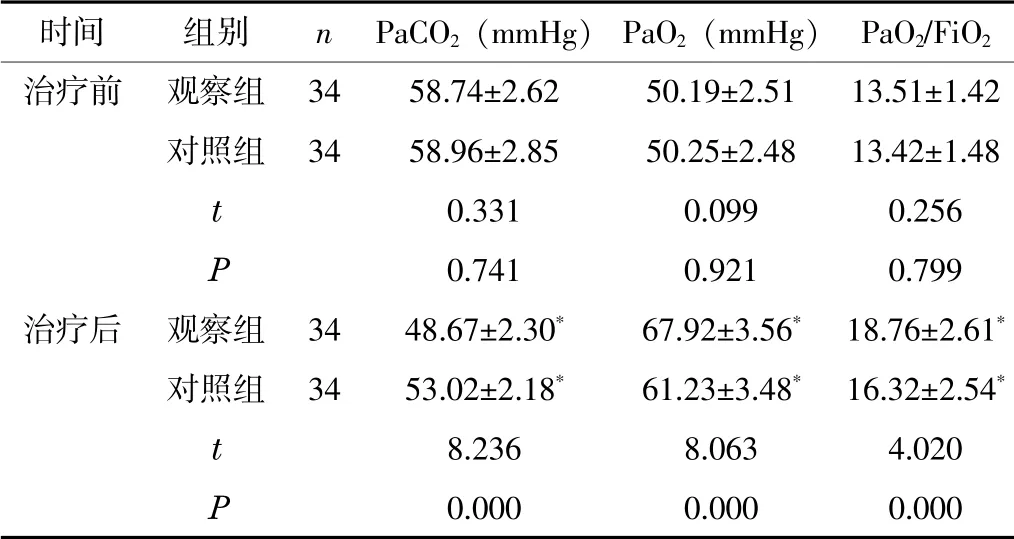
表1 两组患儿治疗前后的血气指标比较(±s)
注:与本组治疗前相比,*P<0.05。
时间 组别 n PaCO2(mmHg) PaO2(mmHg) PaO2/FiO2治疗前 观察组 34 58.74±2.62 50.19±2.51 13.51±1.42对照组 34 58.96±2.85 50.25±2.48 13.42±1.48 t 0.331 0.099 0.256 P 0.741 0.921 0.799治疗后 观察组 34 48.67±2.30* 67.92±3.56* 18.76±2.61*对照组 34 53.02±2.18* 61.23±3.48* 16.32±2.54*t 8.236 8.063 4.020 P 0.000 0.000 0.000
2.2 炎性因子水平 治疗3 d后,两组患儿的IL-6、IL-8和TNF-α水平均下降,且观察组的各指标水平均低于对照组(P<0.05)。见表2。
表2 两组患儿治疗前后的炎性因子水平比较(±s)
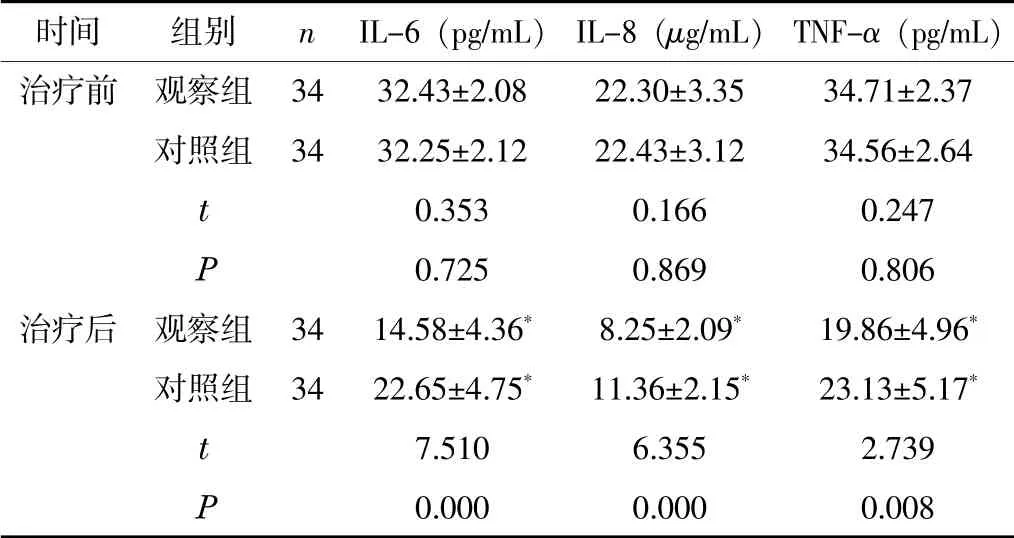
表2 两组患儿治疗前后的炎性因子水平比较(±s)
注:与本组治疗前相比,*P<0.05。
时间 组别 n IL-6(pg/mL) IL-8(μg/mL) TNF-α(pg/mL)治疗前 观察组 34 32.43±2.08 22.30±3.35 34.71±2.37对照组 34 32.25±2.12 22.43±3.12 34.56±2.64 t 0.353 0.166 0.247 P 0.725 0.869 0.806治疗后 观察组 34 14.58±4.36* 8.25±2.09* 19.86±4.96*对照组 34 22.65±4.75* 11.36±2.15* 23.13±5.17*t 7.510 6.355 2.739 P 0.000 0.000 0.008
3 讨论
HMD又称呼吸窘迫综合征,是临床早产儿的常见病症,指出生后不久内源性PS缺乏所致的进行性肺不张。HMD早产儿19~23周胎龄,出现肺泡壁上皮细胞,并在35~36周胎龄期间快速增加,造成患儿肺部器官功能发育不全,肺泡表面张力不足。加之通气和血流比例不平衡,HMD早产儿出现低氧血症和酸中毒,进一步加重病情[5]。NCPAP可提供混合氧,无需插管可有效避免对气道的伤害,降低并发症发生风险。早期应用能有效降低HMD早产儿气道阻力,促进氧合,有助于新生儿自主呼吸功能的建立。氨溴索是一种黏液溶解剂,有助于内源性PS和呼吸道黏膜浆液腺分泌,降低痰液黏度。药理实验研究[6]显示,盐酸氨溴索可刺激Ⅱ型肺泡细胞增长,有助于肺泡表面活性物质的分泌。本研究结果显示,观察组患儿治疗3 d后PaCO2下降,PaO2和PaO2/FiO2水平均上升,表明NCPAP联合氨溴索治疗的患儿血气指标改善效果显著。究其原因在于,NCPAP有助于改善患儿的肺通气功能,减少上呼吸道阻力和PS消耗,通气效果显著。联合应用氨溴索后,PS的合成和分泌增加,从而促进患儿肺功能发育,有利于病情转归。
多项临床研究[3,7]表明,抗炎因子与促炎因子在早产儿HMD的发生、发展过程中有着关键性作用。IL-6是T细胞、单核细胞、内皮细胞产生的典型促炎因子,又被称为B细胞刺激因子,具有较强的生物活性,免疫调节作用显著,其表达水平上升时,可激活C反应蛋白及补体表达,引起细胞功能受损,同时能提高黏附因子的表达,激活血管内皮细胞,活化淋巴细胞,造成机体炎性反应加剧。IL-8是一种多功能细胞因子,在机体各类炎性反应中发挥调节作用。TNF-α是巨噬细胞、单核细胞产生的早期主要炎性因子,是HMD发病的关键因子。HMD早产儿肺部损伤后,TNF-α释放量明显增加,进一步刺激IL-6等分泌,效应细胞也被快速激活,释放出溶酶体酶、氧自由基等,加重细胞损伤程度,加重病情。本研究结果显示,观察组患儿治疗3 d后的IL-6、IL-8和TNF-α水平均显著下降,表明联合氨溴索治疗后患儿炎性反应减轻。
综上所述,氨溴索联合NCPAP治疗HMD早产儿效果显著,可改善血气指标,降低炎性因子水平。
