肠溶阿司匹林的体外实验及磁控胶囊内镜人体研究
2022-01-06王茜婷焦红梅李丽陈夏欢李嘉欣刘梅林
王茜婷 ,焦红梅 ,李丽 ,陈夏欢 ,李嘉欣 ,刘梅林
阿司匹林抑制血小板聚集,是防治心血管疾病的基本药物[1-2],但在发挥抗栓疗效的同时增加消化道损伤风险[3-4],其反应性存在个体化差异。药物有效成分的释放与吸收受胃肠液pH 水平及消化道转运时间等参数影响[5]。了解阿司匹林在不同pH 水平溶液及人体消化道内的转运及崩解过程,对分析阿司匹林疗效及安全性的影响因素、探索适合我国人群的阿司匹林治疗方案具有重要临床意义。基于上述背景,我们采用磁控胶囊内镜技术[6-7],对服用肠溶阿司匹林的受试者进行胃和全小肠检查,结合体外实验观察阿司匹林肠溶片及阿司匹林肠溶缓释片在不同pH 水平溶液中及胃肠道内的转运及崩解过程,旨在探索可有效平衡心血管获益及不良反应的阿司匹林剂型及服药方式。
1 资料与方法
1.1 研究对象
选择2020 年10~12 月于北京大学第一医院老年内科住院治疗,且无明显消化道症状(腹痛、腹胀、腹泻、反酸、烧心等)的冠心病患者6 例及健康志愿者6 例,签署知情同意书并登记临床资料。排除标准:有吞咽障碍、胃肠道手术史、消化道梗阻、狭窄、憩室、瘘管及恶性肿瘤病史患者;使用心脏起搏器或其他植入式电子医疗设备的患者;患甲状腺疾病、糖尿病及自主神经功能异常患者;服用糖皮质激素及促胃肠动力药者;妊娠期妇女及病情危重、难以保证检查顺利完成者。在磁控胶囊内镜检查过程中,冠心病患者服用阿司匹林肠溶片(商品名:拜阿司匹灵,100 mg/片,德国拜耳医药保健公司),健康志愿者服用阿司匹林肠溶缓释片(商品名:介宁,50 mg/片,山东新华制药股份有限公司),根据服药剂型将两组命名为阿司匹林肠溶缓释片组及阿司匹林肠溶片组(各6 例)。本研究方案经北京大学第一医院伦理委员会批准。
1.2 体外实验
室温下将0.9%生理盐水分别与盐酸及碳酸氢钠混合,使用pH 计测定pH 值,使混合溶液分别为pH 2.0(模拟空腹胃液)、pH 7.0(模拟餐后胃液)、pH 7.5 及8.0(模拟小肠液)。将同一pH 水平的溶液分装在两支试管内(每支20 ml),分别投入阿司匹林肠溶缓释片及阿司匹林肠溶片各1 片,每15 min 观察一次直至24 h,每组PH 水平溶液均采用相同方法重复验证1 次。
1.3 磁控胶囊内镜检查
仪器:磁控胶囊内镜系统(NU-1)由安翰光电技术(武汉)有限公司生产,包括巡航胶囊内窥镜控制设备(含ESNavi 软件)、上消化道胶囊内窥镜和便携记录器(含便携记录器、检查服及数据线)。其中胶囊大小27.0 mm×11.8 mm,入瞳视场角140°,图像分辨率480ppi×480,拍摄帧数率2 帧/s。
检查方法:受试者检查前3 d 进食低渣饮食,检查前1 d 晚8 点后禁食不禁水,检查前30 min 服用西甲硅油乳剂6 ml+链霉蛋白酶颗粒20 000 IU+碳酸氢钠1 g+清水100 ml,检查前20 min 服用温水200 ml,检查时一次性饮水300~500 ml 至胃部有饱胀感。受试者穿检查服,平卧于检查台上,吞服磁控胶囊,通过操作磁控摇杆及改变体位等方法完成对食管及胃的观察后,使受试者恢复平卧位并服用1 片阿司匹林,待阿司匹林通过幽门后即操纵磁控胶囊进入十二指肠,随后嘱受试者自由活动,4 h 后进食。8 h 后受试者归还检查服,将数据导出,使用ESNavi 软件对图像进行观察分析,所有受试者磁控胶囊内镜检查均由同一人操作,图像均由2 名经验丰富的内镜医师独立阅片。
1.4 观察指标
阿司匹林开始崩解时间(以下简称开始崩解时间),定义为体外实验中药片出现肉眼可见的形态变化或上清液开始出现浑浊的时间,及胶囊内镜下阿司匹林通过幽门到出现肉眼可见形态变化的时间;阿司匹林完全崩解时间(以下简称完全崩解时间)为药片完全崩解消失的时间;阿司匹林胃通过时间(以下简称胃通过时间)为吞服阿司匹林到阿司匹林通过幽门的时间。胶囊内镜小肠检查时间(以下简称小肠检查时间)为胶囊内镜通过幽门至到达回盲部的时间或胶囊内镜尚未到达回盲部但结束检查的时间。
1.5 统计学方法
采用SPSS 23.0 统计软件进行统计分析。对连续型变量采用Kolmogorov-Smirnov 法进行正态性检验,服从正态分布的连续型变量以均数±标准差(±s)表示,两组间比较采用独立样本t检验,非正态分布的连续型变量以中位数(P25,P75)表示,两组之间的比较采用Mann-Whitney U 检验。分类变量以例数(n)表示,分析采用Fisher’s 确切概率法,以P<0.05 为差异具有统计学意义。
2 结果
2.1 体外不同pH 溶液中阿司匹林崩解情况(表1)
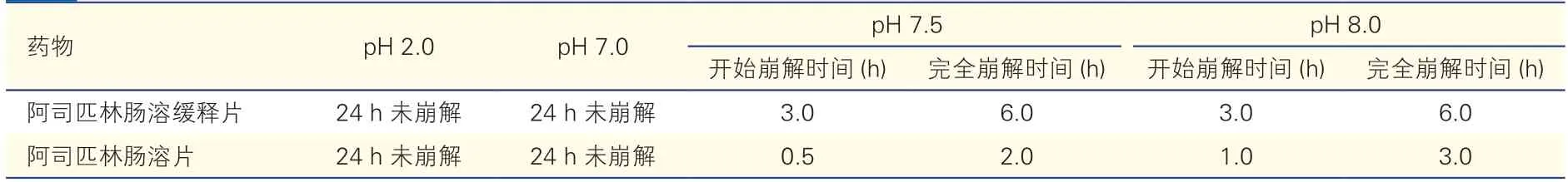
表1 体外不同pH 溶液中两种阿司匹林剂型的崩解情况
体外实验结果显示,在pH 2.0 及pH 7.0 溶液中,阿司匹林肠溶缓释片及阿司匹林肠溶片24 h 内均未崩解。在pH 7.5~8.0 溶液中,阿司匹林肠溶片0.5~1.0 h 时开始崩解,2.0~3.0 h 时完全崩解,阿司匹林肠溶缓释片3 h 时开始崩解,6 h 时完全崩解。
2.2 胶囊内镜下阿司匹林崩解情况
受试者中男性8 例,女性4 例,平均年龄64.8(45.0~84.0)岁,两组受试者性别及年龄匹配(P>0.05)。人群中肠溶阿司匹林的胃通过时间差异较大(6.0~70.0 min),阿司匹林肠溶缓释片组胃通过时间为23.0(10.0,52.0) min(9.0~70.0 min),阿司匹林肠溶片组为23.5(14.0,38.0) min(6.0~53.0 min),两组比较差异无统计学意义(P=0.720),其中3 例患者(阿司匹林肠溶片2 例,阿司匹林肠溶缓释片1例)服药后药片即嵌于胃底皱襞内(图1),22.0 min(19.0~25.0 min)后脱落至胃窦部,所有药片在胃中均未崩解。两组患者药片均于进入小肠后开始崩解(图2、图3),阿司匹林肠溶缓释片组开始崩解时间为182.5(153.0,217.0) min(132.0~266.0 min),阿司匹林肠溶片组开始崩解时间为97.5(77.0,125.0)min(72.0~145.0 min),显著低于阿司匹林肠溶缓释片组(P=0.006),见表2。两组患者均于8 h 后结束磁控胶囊内镜检查,阿司匹林肠溶缓释片组小肠检查时间为340(257,435) min(210~439 min),阿司匹林肠溶片组小肠检查时间为385(242,526) min(232~533 min),两组差异无统计学意义(P=0.598),结束检查时两组患者镜下均未见到阿司匹林药片。

表2 胶囊内镜下两组阿司匹林转运及崩解情况
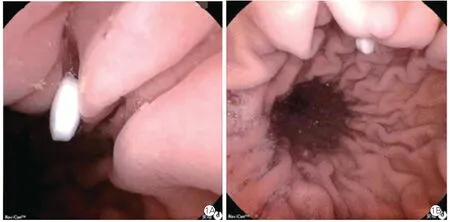
图1 阿司匹林嵌于胃底皱襞内

图2 胶囊内镜下阿司匹林肠溶片的崩解过程(空肠内,同一患者)

图3 胶囊内镜下阿司匹林肠溶缓释片的崩解过程(空肠及回肠内,同一患者)
3 讨论
阿司匹林相关消化道损伤主要包括黏膜糜烂、溃疡、出血、穿孔,临床症状可表现为恶心、呕吐、上腹不适、疼痛、腹泻、呕血、黑便等[8]。阿司匹林导致胃黏膜损伤的机制[9-10]主要包括:(1)局部作用:在胃内崩解可作用于胃黏膜磷脂层,破坏疏水保护屏障,增加白三烯等细胞毒性物质释放,进一步刺激损伤胃黏膜上皮细胞;(2)全身作用:抑制环氧化酶1(COX-1)及环氧化酶2(COX-2)活性,减少前列腺素生成,抑制胃黏膜的新生血管再生并使胃黏膜血流量下降,削弱胃黏膜的防御及修复作用,这是阿司匹林引起胃黏膜损伤的主要原因;此外,胃黏膜溃疡面的血小板聚集受抑、氧自由基的产生和胃蛋白酶的自我消化作用也参与了损伤过程。阿司匹林引起小肠黏膜损伤的机制尚不明确,有学者提出了“三次打击”假说[11]:首次打击是阿司匹林溶解了黏膜表面磷脂的脂质成分,直接损伤了上皮细胞的线粒体[12];二次打击是线粒体损伤降低细胞间的能量传递,导致钙离子外流及自由基的产生,破坏细胞间连接,增加小肠黏膜的通透性;三次打击为黏膜屏障受损后,肠腔内容物如胆汁酸、肠内细菌及其降解产物、食物大分子物质及毒素等易透过肠上皮细胞,导致黏膜损伤[13]。此外,阿司匹林抑制环氧化酶活性,导致前列腺素生成减少,也是引起小肠黏膜损伤的重要病理机制[14]。
健康成人空腹胃液pH 水平为1~3[15],进食后胃液pH 水平显著升高[16]。健康成人小肠液pH 水平为7.2~8.1(平均7.61),从十二指肠到回肠,pH水平逐渐升高[17]。肠溶阿司匹林外覆抗酸肠衣,在酸性胃液中不溶解,可避免直接刺激损伤胃黏膜上皮细胞[18],相比普通剂型可减少严重胃及十二指肠损伤[19]。目前临床中常用的肠溶阿司匹林包括阿司匹林肠溶片及阿司匹林肠溶缓释片,关于两种剂型肠溶阿司匹林有效性及安全性评估的临床研究较少。我中心前期曾进行一项关于不同剂型肠溶阿司匹林短期安全性评估的随机对照研究[20],该研究结果显示,阿司匹林肠溶缓释片可显著抑制血小板聚集,短期轻微出血事件和胃肠道不良反应的发生率均低于肠溶片,提示阿司匹林肠溶缓释片兼具疗效和安全性的优势。本研究通过观察药物在体外及消化道内的转运及崩解特点,探索肠溶缓释片更具安全性的原因。体外实验发现,阿司匹林肠溶片及肠溶缓释片在pH ≤7 的溶液中24 h 后均未出现形态变化,而在模拟小肠液的碱性环境中,两种肠溶阿司匹林均完全崩解,其中阿司匹林肠溶片在pH 相对低的碱性溶液中(pH 7.5)更早开始出现形态变化,崩解速度更快。胶囊内镜下可见两种肠溶阿司匹林在胃内均未崩解,均于进入小肠后数小时内开始出现形态变化直至完全崩解,阿司匹林肠溶片于pH水平相对更低的小肠上段即开始出现形态变化,且崩解速度显著高于肠溶缓释片,与体外实验结果一致。本研究提示,阿司匹林肠溶缓释片相比肠溶片,开始崩解时间更晚、崩解速度更慢、完全崩解所需时间更长。
临床中关于肠溶阿司匹林餐前和餐后服药时机选择仍存在争议。同为肠溶剂型,阿司匹林肠溶片(拜阿司匹灵)的药品说明书建议饭前用适量水送服,而阿司匹林肠溶缓释片(介宁)的药品说明书却建议饭后用温水送服,并强调“不可空腹服用”。本研究发现,人群中阿司匹林胃通过时间存在较大差异(6~70 min),空腹服用肠溶剂型阿司匹林后,药物在胃内虽未出现崩解,但四分之一患者服药后药片即嵌入胃底皱襞中,使阿司匹林胃通过时间明显延长,增加了药物与胃黏膜的接触时间。既往研究[21-22]表明,成人平均胃排空时间与年龄、性别、体重指数等临床参数无关,但进食可显著延长胃排空时间[23],不同饮食结构对胃排空时间的影响不同[24]。若患者餐后服用肠溶阿司匹林,一方面食物或胃潴留物升高胃内pH 水平,可能使肠溶阿司匹林在胃内提前崩解释放,增加药物相关胃肠道损伤风险,尤其阿司匹林肠溶片在pH相对低的环境中提前崩解几率更高,更易出现消化道损伤,这和文献报道一致[25],此外进食后胃肠蠕动增强,肠溶包衣在机械性挤压下更易破损,进一步增加胃黏膜损伤风险;另一方面,进食显著延长胃排空时间,可能造成肠溶阿司匹林于胃内滞留,无法快速进入小肠分解吸收,延误抗血小板聚集时机,降低抗血小板疗效。因此应建议患者空腹服用肠溶剂型阿司匹林,以最大程度兼顾抗血小板疗效及安全性。
本研究通过体外实验及磁控胶囊内镜技术,观察阿司匹林肠溶片及阿司匹林肠溶缓释片在体外不同pH 溶液及消化道内的转运及崩解过程,为探索我国人群阿司匹林疗效及安全性的影响因素提供依据。
综上,本研究结果表明,阿司匹林肠溶缓释片相对于肠溶片,开始崩解时间更晚,崩解速度更慢。为降低消化道损伤风险,保证抗血小板疗效,建议空腹服用肠溶剂型阿司匹林。胃肠动力特点与阿司匹林治疗个体化差异的相关性尚需进一步研究。
利益冲突:所有作者均声明不存在利益冲突
