累及髋臼的原发良性与交界性骨肿瘤的术式选择与预后评估
2021-12-31张珠晟鲍其远沈宇辉张伟滨
张珠晟,刘 琦,鲍其远,沈宇辉,张伟滨,万 荣
上海交通大学医学院附属瑞金医院骨科,上海 200025
骨盆是骨原发性肿瘤与转移癌的好发部位之一。根据Enneking骨盆肿瘤分区,可将其分为4个区域:Ⅰ区为髂骨,Ⅱ区为髋臼,Ⅲ区为坐骨和耻骨,Ⅳ区为骶骨翼[1]。由于髋臼的解剖结构复杂,外科手术对于髋臼区域的恶性肿瘤往往难以做到足够的边界外切除,从而导致了较高的复发率。与恶性肿瘤相比,起源于髋臼的良性与交界性骨肿瘤(benign and aggressive bone tumors,BABT)发病率不高,但却种类繁多。其生物学行为及治疗方式对患者的预后有着很大的影响,术中骨与软组织缺损的结构和功能重建也极具挑战性[2]。BABT 主要的手术方式为单纯病灶刮除或是瘤段切除;但当病变累及髋臼区域时,其手术疗效是否与同类的肢体肿瘤相同呢?本研究回顾性分析了上海交通大学医学院附属瑞金医院2004—2018 年共41 例髋臼原发BABT 的临床特征、手术方式、术后并发症及肿瘤学预后,总结了髋臼原发BABT的治疗经验,探讨其最佳治疗模式。
1 对象与方法
1.1 研究对象
对上海交通大学医学院附属瑞金医院2004—2018 年收治的以“髋臼病灶”为首诊原因的患者,根据纳入及排除标准进行筛选。纳入标准:①骨盆原发肿瘤累及髋臼,身体可耐受手术者。②经术前穿刺或术后切开活检病理证实为BABT。③无明显骨质疏松,可确保植骨或假体植入后的稳定性。④有完整的术前病史资料及术后随访资料且随访时间大于6个月。排除标准:①经活检证实为原发恶性肿瘤或转移性肿瘤。②合并2 种及以上的肿瘤。最终,本研究共纳入髋臼病灶患者88 例,其中原发性BABT 患者41 例,均经过了病理学检查证实。髋臼BABT主要表现为受累髋关节静息或行走时疼痛,部分患者伴髋关节活动受限。
1.2 治疗方式
41 例髋臼BABT 患者均接受手术治疗,根据Enneking 分区、病理类型以及影像学表现确定手术方式及范围。手术方式包括病灶刮除植骨术、病灶刮除骨水泥填充术、瘤段切除联合骨盆假体重建术以及半骨盆截肢术。手术应尽可能沿肿瘤边界进行病灶刮除;对于病灶广泛累及髋臼伴骨缺损者,行瘤段切除联合骨盆假体重建;当肿瘤巨大、神经血管束严重受累时,可选择半骨盆截肢。所有患者术后均未接受放射治疗或化学治疗。
1.3 术后处理
术后进行一般支持治疗,常规抗感染治疗3 d。对留置引流管者,静脉抗生素通常应用至引流管拔出。病灶刮除骨水泥填充患者术后3~7 d 开始下地负重行走,其余患者术后6周内以非负重功能康复为主,病灶刮除植骨术患者通常术后2个月开始部分负重功能训练,骨盆假体重建的患者术后6周开始拄拐部分负重行走训练。
1.4 术后随访及疗效评价
术后6周、12周、24周及1年门诊随访,此后良性肿瘤患者每年1 次门诊随访,交界性肿瘤患者则半年1 次门诊随访。随访内容包括患侧肢体功能、局部有无复发、术后并发症等;影像学评估采用实体肿瘤的疗效评价标准1.1 版(RECIST 1.1);患者术后髋关节功能根据世界骨与软组织肿瘤协会(Musculoskeletal Tumor Society,MSTS)评分确定。如患者死亡,死亡时间由电话确认;随访时间定义为从确诊开始至患者死亡或至最近一次随访。
1.5 统计学方法
使用SPSS 25.0 软件进行统计学处理。定性资料以频数(百分比)表示,不同组别间比较采用χ2检验。若存在任意一格频数<5,则采用Fisher 确切概率法。以P<0.05表示差异具有统计学意义。
2 结果
2.1 一般资料
在41 例髋臼BABT 患者中,男性18 例,女性23 例,年龄为6~73岁(中位年龄51岁)。其中,良性肿瘤23例,占比56.1%,包括骨囊肿/滑膜囊肿8 例、纤维结构不良7例、炎性肉芽肿4 例、软骨母细胞瘤2 例、软骨黏液样纤维瘤1 例、良性纤维组织细胞瘤1 例;交界性肿瘤18 例,占比43.9%,包括骨巨细胞瘤7例、非典型软骨肿瘤4例、多发朗格汉斯细胞组织增多症4例、骨Erdheim-Chester病1 例、骨母细胞瘤1 例、骨纤维瘤病1 例。所有患者术前常规行X 线平片、CT 及磁共振成像(MRI)检查,以确定肿瘤大小、侵犯范围、毗邻组织等情况。根据Enneking标准进行骨盆肿瘤分区,累及单纯Ⅱ区者27例、Ⅰ+Ⅱ区者4例、Ⅱ+Ⅲ区者8例、Ⅰ+Ⅱ+Ⅲ区者2例。
2.2 手术方式
良性肿瘤病例中,21 例患者行病灶刮除植骨术,仅有2 例患者(1 例纤维结构不良、1 例软骨母细胞瘤)因病灶广泛累及髋臼伴骨皮质破损,行瘤段切除联合骨盆假体重建术。交界性肿瘤病例中,9例患者行病灶刮除植骨术,2 例患者行病灶刮除骨水泥填充术,6 例患者(3例骨巨细胞瘤、3例非典型软骨肿瘤)因病灶广泛累积髋臼并伴明显软骨下骨缺损,行瘤段切除联合骨盆假体重建术;仅有1 例骨巨细胞瘤患者在外院行假体重建后约1 年2 个月复发,因肿瘤巨大伴肺转移选择了半骨盆截肢。
2.3 生存情况及并发症
所有患者均顺利完成了手术,无围手术期死亡。长期随访中失访患者1 例,随访时间为6~84 个月(中位随访时间42.6 个月)。至末次随访时,除1 例骨巨细胞瘤患者在半骨盆截肢术后2年因广泛肺转移死亡,其余患者均存活。32例行刮除术的患者MSTS评分均在25分以上。
术后,共有5 例患者出现了并发症,包括术后感染2例(假体重建术后1 例、半骨盆截肢术后1 例)、假体置换术后假体松动2 例、伤口延迟愈合1 例。至末次随访时,余36例患者均未见明显术后并发症。
2.4 骨皮质破损
41 例髋臼BABT 患者中,骨皮质完整者共19 例,均采取了病灶刮除植骨术。而伴有骨皮质破坏者22 例,其手术方法不一,包括病灶刮除植骨术11 例、病灶刮除骨水泥充填术2 例、瘤段切除联合骨盆假体重建术8 例,以及半骨盆截肢术1例。我们发现,骨皮质破损的发生率与肿瘤类型(P=0.011;Fisher 确切概率检验)、手术方式(P=0.005;χ2检验)均显著相关。与良性肿瘤相比,交界性肿瘤更具有侵袭性,因此更易发生皮质缺损,从而导致手术方式的差异。此外,相较于骨皮质完整者,伴有骨皮质破损的患者术后并发症发生率(18.2%)及肿瘤复发率(22.7%)更高,尽管这两者之间的差异并无统计学意义。19 例骨皮质完整者中,仅有1 例患者出现伤口延时愈合;而22 例骨皮质破损者中,术后感染2 例、假体松动2例,共有5例患者在手术后复发(表1)。
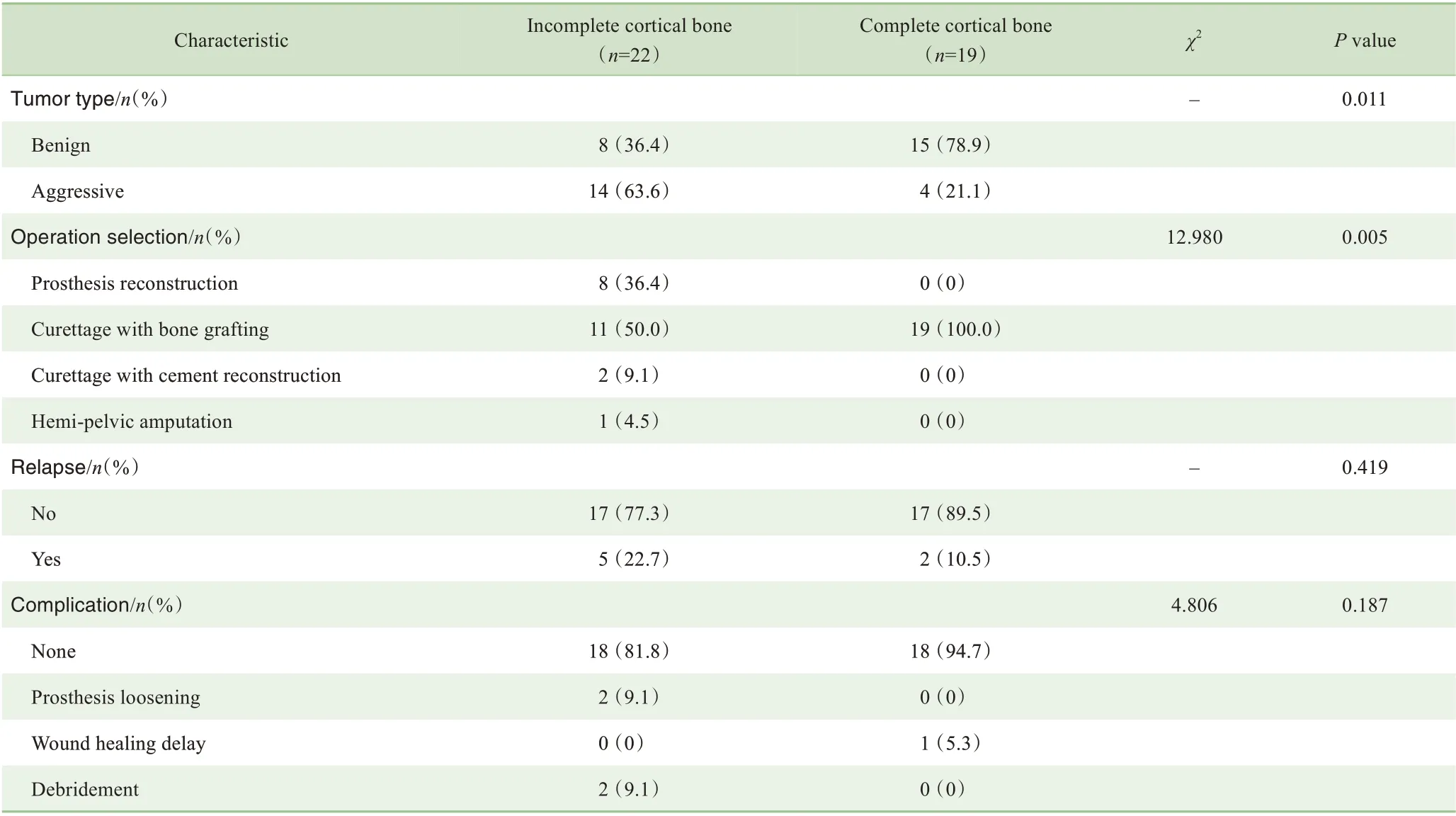
表1 41例髋臼肿瘤骨皮质表现与肿瘤类型、手术方式、肿瘤转归及术后并发症的相关性Tab 1 Correlation of bone cortical manifestations of 41 acetabular tumors with tumor types,surgical methods,tumor outcomes,and postoperative complications
2.5 临床转归
良性肿瘤病例中复发者2 例(占比8.7%),包括软骨黏液样纤维瘤1 例、骨纤维结构不良1 例,均接受了病灶刮除植骨术。多数良性肿瘤在刮除植骨术后无复发迹象,如最为常见的骨囊肿(图1)。本研究中,仅有的1 例软骨黏液样纤维瘤患者在术后9 个月复发,再次刮除后约1 年2 个月又复发,随后在第3 次术后失访;仅有的1 例骨纤维结构不良患者在术后约6 年6 个月复发。
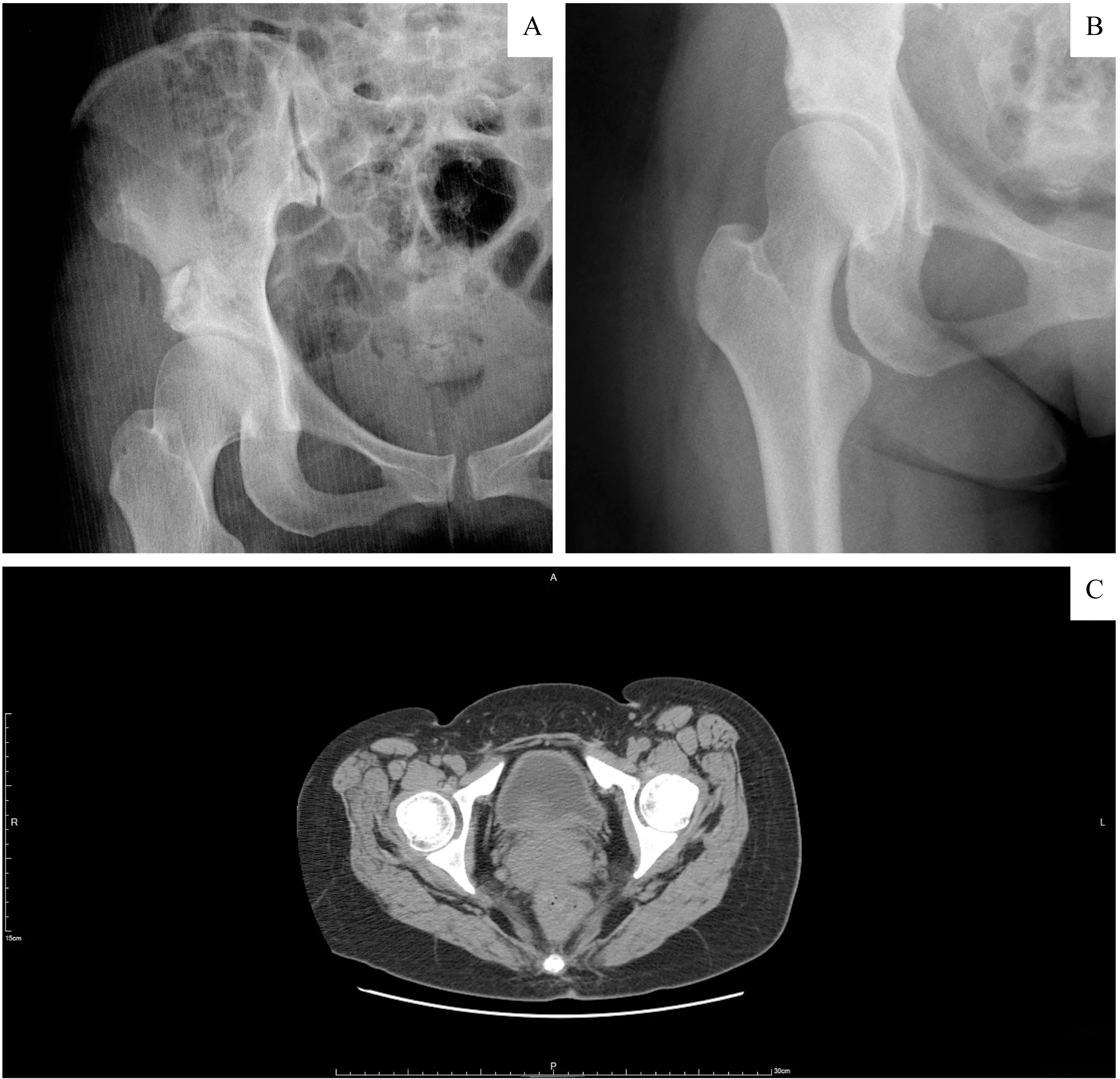
图1 1例髋臼骨囊肿刮除植骨术后X线表现Fig 1 X-ray appearance of an acetabular bone cyst after curettage with bone grafting
交界性肿瘤病例中复发者5 例(占比27.8%),包括骨巨细胞瘤1 例、非典型软骨肿瘤3 例、纤维瘤病1 例。所有的多发朗格汉斯细胞组织增生症、Erdheim-Chester病、骨母细胞瘤患者都接受了病灶刮除,术后未见复发或转移。骨巨细胞瘤患者中1 例行病灶刮除植骨术,2 例行病灶刮除骨水泥填充术(图2),3例行瘤段切除联合骨盆假体重建术,仅有1例因病灶范围较广行半骨盆截肢术后2年因广泛肺转移死亡;7例骨巨细胞瘤中,Ⅱ区1例,Ⅰ+Ⅱ区1例,Ⅱ+Ⅲ区4例,Ⅰ+Ⅱ+Ⅲ区1例(图3)。非典型软骨肿瘤病例中1例行病灶刮除植骨,术前穿刺考虑内生软骨瘤,术后病理提示软骨肉瘤Ⅰ级,且于术后约4 年7 个月复发;3 例患者行瘤段切除联合骨盆假体重建术(图4),其中2 例在术后复发(1 例在术后1 年复发后截肢,2 年后出现肺转移;另1 例在术后6 年复发)。此外,1例纤维瘤病患者行病灶刮除术后2年复发。
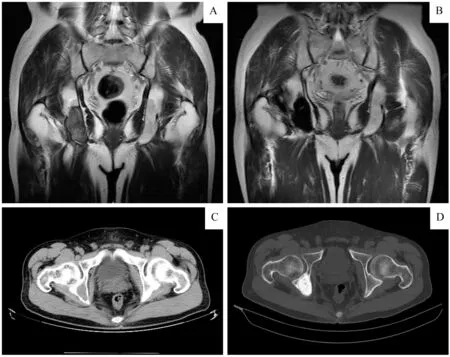
图2 1例髋臼骨巨细胞瘤行刮除骨水泥填充影像学表现Fig 2 Imaging appearance of a giant cell tumor of acetabulum after curettage with cement reconstruction
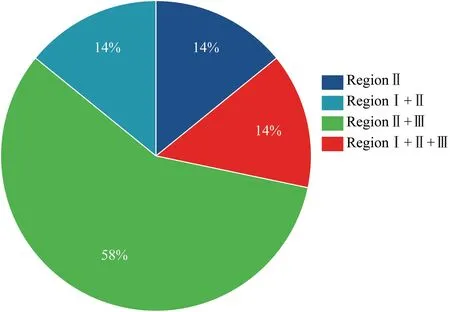
图3 7例髋臼骨巨细胞瘤骨盆累及区域分布Fig 3 Distribution of pelvic involvement in giant cell tumor of acetabulum
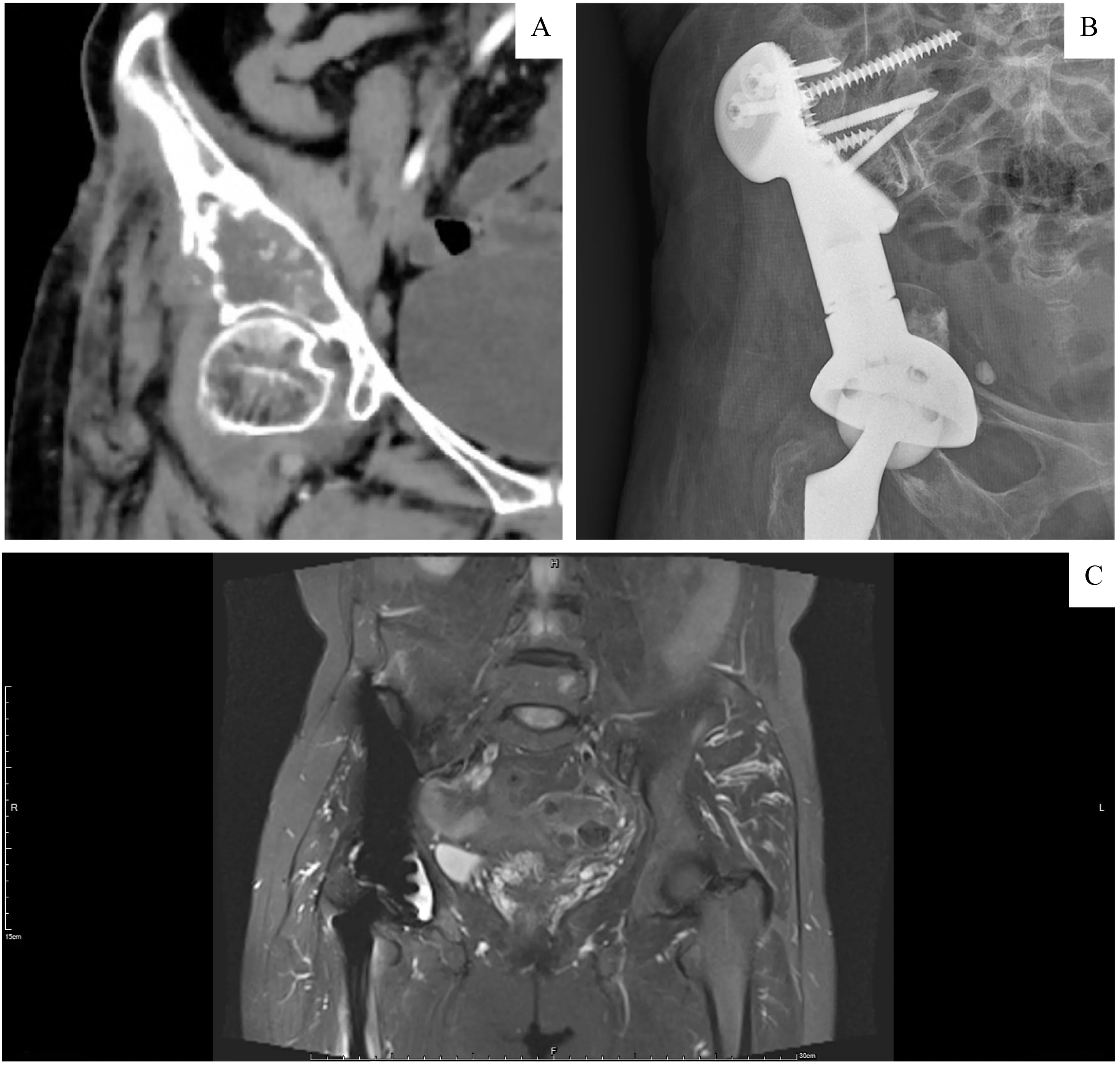
图4 1例非典型软骨肿瘤术后影像学表现Fig 4 Imaging appearance of atypical cartilage hyperplasia
如表2 结果所示,肿瘤复发风险与其大小具有相关性,差异具有统计学意义(P=0.010;Fisher 精确概率检验);但与一般情况、病理类型、手术方式以及骨皮质表现等不具有相关性(表2)。受限于本研究中不同瘤种的病例数较少,未发现手术方式与肿瘤复发/转移率之间的相关性,差异不具有统计学意义(P=0.326;Fisher 精确概率检验),见表3。
表2 41例患者肿瘤复发风险的相关因素Tab 2 Relevant factors of tumor recurrence risk in 41 patients

表3 18例交界性肿瘤手术方式与术后复发/转移的关系Tab 3 Relationship between the operation method of aggressive tumors and the progression in 18 cases

Continued Tab
3 讨论
BABT的肿瘤类型繁多,且生物学行为不一。相较于四肢,骨盆的解剖结构和生物力学复杂,手术较为困难[3]。尤其是累及髋臼的肿瘤,其术后并发症较骨盆其他区域多,目前尚无统一的治疗标准[4]。髋臼良性肿瘤虽然发病率不高,却往往缺少典型的临床症状。其症状隐匿,患者就诊较晚,导致有时肿瘤累及的范围并不小。对良性肿瘤而言,手术通常选用病灶刮除原则。然而,髋臼部位骨结构不规范,整个瘤腔显露困难,从而导致彻底刮除肿瘤困难而易致肿瘤复发。既往研究表明,当原发于髋臼部位的良性肿瘤伴有骨皮质破损或肿瘤体积较大时,往往表示肿瘤侵袭性较强,单纯刮除难以彻底根治[5-7]。Makhdom 等[8]报道了2 例髋关节骨软骨瘤伴有髋关节脱位、1例髋关节骨软骨瘤多次手术后复发的案例,通过多学科、多种模式、个体化的手术方案解决了患者的问题。因此我们认为,对于髋臼部位的良性肿瘤,当具有复发相关危险因素,如肿瘤较大、骨皮质破损以及特定瘤种等,仍要慎重选择手术方式。
交界性肿瘤一般呈低度潜在恶性,相对恶性肿瘤而言,其转移或复发风险较低;但同样由于髋臼区域解剖结构的特殊性,往往难以将肿瘤彻底刮除干净。因此,髋臼交界性肿瘤的外科治疗方式目前国际上尚未形成广泛共识[4-6]。对于一些特殊的交界性肿瘤如骨巨细胞瘤,有学者发现髋臼骨巨细胞瘤刮除后的局部复发风险,明显高于瘤段切除联合肿瘤假体重建术[5]。此外,2017 年美国国立综合癌症网络(NCCN)指南指出,髋臼的非典型软骨肿瘤相较于四肢,更易复发。因此我们建议,对于髋臼的非典型软骨肿瘤及骨巨细胞瘤,仍以瘤段切除联合肿瘤假体重建术为主。我们的研究结果表明,虽然肿瘤大小对肿瘤复发有显著影响,但肿瘤复发似乎与手术方式等其他因素并没有显著关系,甚至行瘤段切除者的复发率高于刮除植骨。另外,病理类型与肿瘤复发间并未发现统计学差异,这可能是本研究样本量较少、对瘤种的手术方式选择有偏倚等因素所导致。但根据我们的经验,还是认为病理类型会对肿瘤复发产生影响。
对于髋臼BABT 而言,伴骨皮质破损较为罕见。梅奥医学中心的学者Novais等[7]曾报道了13例骨盆动脉瘤样骨囊肿病例,其中1 例伴有髋臼骨皮质破损。Saibaba等[9]报道了1 例神经纤维瘤合并骨皮质破损,并伴有髋关节前脱位的病例。本研究中,髋臼BABT 伴骨皮质破损有22 例患者。我们发现,髋臼BABT 伴骨皮质破损较骨皮质完整者,往往肿瘤更具有侵袭性,临床症状也更为显著,从而导致手术方式复杂,术后并发症发生率及肿瘤复发率较高。该差异尚未达到统计学意义,可能与本研究样本量较少有关,尚待更多病例研究。本研究的18 例交界性肿瘤中,14 例合并骨皮质破损,其中3 例出现肿瘤复发或转移,2例无骨皮质破损者出现复发。我们认为,由于髋臼是髋关节负重的重要部分,对于髋臼交界性肿瘤出现骨皮质缺损尤其是伴软骨下骨较多吸收的患者,临床上往往有负重行走或活动后髋部不适等症状。对于这部分患者,术中往往为尽可能保留骨和关节结构,从而限制了肿瘤刮除的广度和深度,导致肿瘤容易复发。因此,交界性肿瘤合并骨皮质破损可能是复发的高危因素。对于伴有骨皮质或软骨下骨缺损的患者,术前需高度重视手术边界的界定,通过CT、MRI 等影像技术仔细界定手术范围,对于难以彻底刮除的肿瘤,建议做瘤段切除联合肿瘤假体重建术。
郭卫等[5]学者回顾分析了27 例髋臼骨巨细胞瘤患者的临床资料,认为广泛切除相比病灶刮除可以带来较低的局部复发率,可能是髋臼骨巨细胞瘤的合理手术方案。此外,髋臼合并Ⅰ区的骨巨细胞瘤由于刮除更为困难,残留肿瘤更易复发,扩大切除术成为这一类肿瘤的最佳手术方式[10]。但是,如何在降低复发率和术后髋关节的功能重建之间取得平衡,仍然是争议重重。尽管瘤段切除联合肿瘤假体重建术可降低肿瘤局部复发率,但与病灶刮除相比,其并发症的发生率更高,或许是因为植入物和更大范围的手术暴露[11]。Angelini 等[12]学者分析了270 例骨盆肿瘤患者的临床资料,与单纯切除相比,切除后重建的患者感染风险显著增加,有时患者需再进行手术将植入物取出,甚至行半骨盆切除来消除感染。Xiao 等[13]报道了7例肿瘤累积未超过髋臼上线的骨巨细胞瘤病例,术前通过计算机模拟在髋臼周围建立截骨平面,行自体骨移植联合全髋关节置换,达到了令人满意的效果。此手术方法减少了传统广泛切除手术引起的并发症,如感染、骨不连、假体松动等,是一种优化的广泛切除术,然而仍需更多病例来验证。本研究的7 例髋臼骨巨细胞瘤中,累及Ⅰ区1 例行病灶刮除骨水泥填充术,累及Ⅰ+Ⅲ区1 例行病灶刮除植骨术,术后均未见明显复发迹象。累及Ⅲ区共4例,其中1 例行病灶刮除骨水泥填充术;2 例行瘤段切除联合肿瘤假体重建术(术后1例出现假体松动);1例行半骨盆截肢后出现伤口感染,2年后局部复发伴广泛肺转移,因无法切除而死亡。因此,我们的经验表明,髋臼骨巨细胞瘤需合理甄别并酌情采用病灶刮除,或是瘤段切除联合肿瘤假体重建的治疗方式。对于合并Ⅲ区的髋臼骨巨细胞瘤,仍然建议以广泛切除为主;而单纯合并Ⅰ区的患者,可以酌情考虑单纯病灶刮除。对于考虑刮除的患者,术中应充分显露瘤腔,尤其是与髋臼相延续的髋臼后壁及坐骨支和耻骨支应充分显露,并仔细反复刮除肿瘤。结合骨水泥充填瘤腔仍是可以考虑的手术方式。
与其他交界性肿瘤相比,髋臼非典型软骨肿瘤的生物学行为可能更差,术后复发风险高。本组病例中,交界性肿瘤术后共有5 例复发,其中3 例为非典型软骨肿瘤,提示了骨盆的软骨源性肿瘤需引起临床重视。2017年NCCN 指南指出:骨盆区域的非典型软骨肿瘤,无论级别高低,均建议广泛切除;对于术后切缘阳性的患者,还需考虑辅以放射治疗或再次手术以达到切缘阴性的标准。本研究中,1 例非典型软骨肿瘤患者行刮除术后复发,再次行肿瘤假体置换手术,术后6年无复发。由此可见,对于非典型软骨肿瘤的患者,采用广泛切除相较于瘤内刮除可以明显降低复发率。此外,由于肿瘤的异质性,髋臼部位的肿瘤术前一般以穿刺活检为主,借此决定手术方案。然而,穿刺活检往往具有局限性,可能穿刺部位肿瘤是内生软骨瘤或非典型软骨肿瘤,而其他部位不排除更高级别可能(如软骨肉瘤),因此常常会出现穿刺活检结果与术后病理不符的情况。Rinas 等[14]学者报道的3 例软骨肉瘤患者的4 个样本中均出现穿刺活检结果与病理不符。此外,Ⅰ级软骨肉瘤复发后还会出现病理级别提升的情况[15]。本研究4例非典型软骨肿瘤中,1例穿刺结果提示内生软骨瘤,术后病理示软骨肉瘤Ⅰ级;1例非典型软骨肿瘤复发后提升为软骨肉瘤Ⅱ级,这也与既往研究相符[15]。因此,髋臼穿刺活检提示软骨源性肿瘤时,还需警惕病理不符或病理级别提升的问题。在其手术方案的决策上,应将穿刺活检结果与影像学资料相结合,制定个体化的手术方案,以减少术后复发及病理级别提升的问题。
综上所述,髋臼BABT 病理种类繁多,术前获得准确的病理诊断较难。对于髋臼BABT 而言,小部分具有复发相关危险因素的病例,仍需在复发风险及生活质量等多方面因素之间权衡。髋臼交界性肿瘤伴骨皮质破损者,建议以广泛切除重建为主,而单纯髋臼良性肿瘤以刮除植骨为主。对于髋臼骨巨细胞瘤,应根据其肿瘤的浸润区域和范围,权衡术后复发及患肢功能,制定个性化手术方案。髋臼软骨源性的肿瘤不同于四肢,无论级别高低,都建议广泛切除重建,严格控制手术切缘。重建技术的选择需考虑疗效的长久性以及并发症的控制。
