急性非静脉曲张性上消化道出血患者再出血预测模型和新型评分系统的构建
2021-12-31奚黎婷朱锦舟虞晨燕倪柳菁许春芳吴爱荣
奚黎婷,朱锦舟,虞晨燕,倪柳菁,许春芳,吴爱荣
苏州大学附属第一医院消化内科,苏州 215006
再出血是急性非静脉曲张性上消化道出血(acute n onvariceal upper gastrointestinal bleeding, ANVUGIB)的主要预后指标之一,发生再出血后患者的死亡风险通常显著增加。消化性溃疡是ANVUGIB 的主要原因。研究[1]显示,消化性溃疡所致ANVUGIB 的再出血率达20%~22%。随着内镜下止血技术的日趋成熟以及质子泵抑制剂的早期大剂量使用,ANVUGIB患者的再出血率明显下降[2];但国外的一项流行病学研究[3]显示,仍有10%~20%的患者经内镜下止血治疗后再次出血。
预防再出血事件的发生是ANVUGIB 治疗的根本目的,也是降低患者死亡风险的必然要求。因此,明确ANVUGIB患者再出血的高危因素至关重要。同时,对患者进行快速、有效的危险因素综合评估,以指导适时干预及分层管理,在降低患者的再出血及死亡风险方面有显著的临床意义。本研究旨在分析ANVUGIB 患者再出血的独立危险因素,构建再出血的预测模型,并对模型进行内部验证,最终将模型转换为风险评分系统并进行风险分层。
1 资料与方法
1.1 研究对象
1.1.1 纳入标准 纳入2016 年1 月1 日至2019 年12 月31日苏州大学附属第一医院收治的ANVUGIB 患者。根据《急性非静脉曲张性上消化道出血诊治指南》[4],纳入病例符合ANVUGIB 的诊断标准:①出现呕血和/或黑便症状(出血量大时也可出现血便),伴或不伴头晕、心悸、面色苍白、四肢湿冷、脉搏细速、血压下降等周围循环衰竭征象。②内镜检查发现上消化道出血病灶,但无食管胃底静脉曲张。③上消化道恶性肿瘤患者具有呕血、黑便等消化道出血表现,且有明确的影像学及血清学证据。
1.1.2 排除标准 ①年龄<18 周岁。②入院后未完善消化内镜检查。③口、鼻、咽部或呼吸道病变出血被吞入消化道而误诊为ANVUGIB。④服用铁剂、铋剂等药物或进食动物血等引起的粪便发黑,经检查排除ANVUGIB。⑤某些全身性疾病引起的上消化道出血,如血液系统疾病、结缔组织病、感染等。⑥病历资料不完整,不能用于计算内镜检查前后Baylor、 Rockall、 Glasgow Blatchford Score (GBS)、 Cedars-Sinai Medical Center Predictive Index (CSMCPI)、 AIMS65、 MAP (ASH)评分。
1.1.3 再出血定义 经药物、内镜、介入栓塞或手术治疗,上消化道出血停止(临床表现好转及血流动力学恢复)后再次出现以下1种或多种情况:呕血,黑便次数增多,粪便稀薄,伴有肠鸣音亢进;周围循环衰竭的表现经积极补液、输血后无好转,或暂时好转而又恶化;红细胞计数、血细胞比容(hematocrit,HCT)和血红蛋白(hemoglobin,Hb)浓度进行性下降,网织红细胞计数持续升高;补液和尿量足够的情况下,血尿素氮(blood urea nitrogen,BUN)再次升高。
1.2 临床资料收集
本研究为单中心回顾性研究,通过医院电子病历系统收集所有患者入院后的临床资料。患者的一般情况,如姓名、性别、年龄、住院号、服用药物史、伴随疾病及合并症;入院时的临床症状及体征,如呕血、黑便、血便、晕厥、神志改变、血压、心率等;入院首次采血检测的实验室检查结果,如Hb、HCT、国际标准化比值(international normalized ratio,INR)、白蛋白(albumin,ALB)、BUN、肌酐(creatinine,Cr)等;入院至完善胃镜检查的时间及内镜下表现,病因诊断,是否发生再出血;评估患者美国麻醉医师协会(American Society of Anesthesiologists,ASA)分级;计算患者内镜检查前后Baylor,以及Rockall、GBS、CSMCPI、AIMS65、MAP(ASH)评分。
1.3 分组、建模及验证
将收集到的686 例ANVUGIB 患者按7∶3 的比例随机分成建模组(n=481)和验证组(n=205)。使用建模组数据分析再出血的独立危险因素,建立再出血风险预测模型,并通过计算将模型转换为风险评分系统。利用验证组的数据对构建的再出血模型进行内部验证。
1.4 统计学方法
对定量资料进行Shapiro-Wilk 正态性检验及Levene's方差齐性检验。符合正态分布的定量资料以±s表示,方差齐时组间比较采用独立样本t检验,方差不齐则采用t′检验。非正态分布的定量资料采用中位数和四分位数间距表示,组间比较采用Mann-WhitneyU检验。定性资料组间比较采用χ2检验和Fisher精确概率法。将单因素分析中差异有统计学意义的变量(P<0.1)纳入Logistic回归分析(逐步向前回归法),采用Box-Tidwell方法检验连续自变量与因变量logit转换值之间是否存在线性关系,计算容忍度或方差膨胀因子检验自变量是否存在多重共线性,绘制受试者操作特征(receiver operating characteristic,ROC) 曲线。通过ROC 曲线下面积(area under the curve,AUC),即C 统计量(concordance statistics,C-statistics)评价预测模型的区分度。通过Hosmer-Lemeshow 拟合优度检验考察预测结果与实际风险的一致程度,即模型的校准度。ROC 曲线间比较采用Delong 统计法。统计学分析及绘图采用SPSS 25.0 和MedCalc 19.2.6 软件。双侧P<0.05 表示差异具有统计学意义。
2 结果
2.1 ANVUGIB患者再出血的危险因素分析及预测模型建立
在纳入的686 例ANVUGIB 患者中,发生再出血的共计35 例,其中24 例为溃疡出血(包括1 例食管溃疡、16 例胃溃疡、6 例十二指肠球部溃疡和1 例吻合口溃疡),4 例为恒径动脉瘤破裂出血,6 例为上消化道恶性肿瘤出血,1例为血管病变。发生再出血的患者中,住院期间死亡8例。
对建模组481 例数据进行单因素分析,结果见表1。再出血患者的中位年龄高于未再出血患者(P=0.006);合并肝功能衰竭、恶性肿瘤及ASA 分级>3 级的患者出现再出血的概率更高,且差异均具有统计学意义(均P<0.05);2组间脉率、收缩压、血红蛋白和白蛋白水平比较,差异均有统计学意义(均P=0.000)。再出血患者内镜下无明显出血征象的比例较低,而内镜下可见血凝块、血管裸露及活动性出血的比例较高,与未再出血患者比较,差异有统计学意义(P=0.000)。2 组间性别,心功能衰竭,肾功能衰竭,服用抗血小板药物、抗凝药物和非甾体抗炎药(nonsteroidal anti-inflammatory drugs,NSAIDs),晕厥,神志改变,INR,Cr,BUN,内镜下诊断,入院至完善胃镜时间比较,差异均无统计学意义(均P>0.05)。

表1 ANVUGIB患者再出血危险因素的单因素分析Tab 1 Univariate analysis of risk factors for rebleeding in patients with ANVUGIB

Continued Tab
将单因素分析中有意义(P<0.1)的变量纳入多因素Logistic 回归分析,向前逐步回归分析结果显示:4 个变量,包括SBP 降低(OR=0.969,95%CI0.946~0.993,P=0.011)、Hb 浓度降低(OR=0.965,95%CI0.945~0.986,P=0.001)、ASA 分级>3 级(OR=6.987,95%CI1.689~21.628,P=0.006)、内镜下高危表现(血凝块:OR=6.987,95%CI1.649~29.599,P=0.008;血管裸露:OR=7.684,95%CI2.296~25.714,P=0.001;活动性出血:OR=10.175,95%CI3.275~31.613,P=0.000)是再出血的独立危险因素,且各变量的容忍度均>0.1,方差膨胀因子均<10,不存在多重共线性(表2)。构建的Logistic 回归方程如下: logit(P)= 2.499 -0.032 × SBP -0.035×Hb+1.799×(ASA分级>3级)+1.944×有血凝块+ 2.039 ×有血管裸露+ 2.320 × 有活动性出血。

表2 ANVUGIB患者再出血危险因素的多因素Logistic分析Tab 2 Logistic regression analysis of risk factors for rebleeding in ANVUGIB patients
该预测模型ROC 曲线的AUC 为0.892 (95%CI0.838~0.946,P=0.001),提示该模型的区分能力较好;Hosmer-Lemeshow 检验χ2=3.005,P=0.934,提示该模型具有较好的校准能力。
通过验证组的205 例数据进行该模型的验证,通过Logistic回归方程计算预测值并绘制ROC曲线。AUC=0.915(P=0.001),95%CI0.851~0.980;Hosmer-Lemeshow 检验χ2=3.842,P=0.871。建模组和验证组的ROC 曲线如图1所示。

图1 建模组(A)和验证组(B)再出血预测模型的ROC曲线Fig 1 ROC curves of rebleeding prediction model for the training set(A)and the validation set(B)
2.2 再出血风险评分系统的建立
将构建的Logistic 回归模型进一步转换为风险评分系统。将此风险评分系统称为SHEA 评分(取4 个变量英文首字母), 具体评分如下: ①收缩压(S)<90 mmHg 为12 分,90 mmHg≤S<100 mmHg 为9 分,100 mmHg≤S<110 mmHg 为7 分,S≥110 mmHg 为0 分。②Hb(H)<60 g/L 为17 分,60 g/L≤H<80 g/L 为13 分,80 g/L≤H<100 g/L 为9 分,100 g/L≤H<120 g/L 为5 分,≥120 g/L 为0 分。③内镜下(E)无近期出血征象为0分,有血凝块为11 分,血管裸露为12 分,活动性出血为13 分。④ASA 分级(A)≤3 级为0 分,>3 级为10 分。总分为0~52 分。
绘制SHEA、内镜前Baylor (pBaylor)、内镜后Baylor(eBaylor)、Rockall、GBS、CSMCPI、AIMS65、MAP(ASH)评分的ROC 曲线(图2)。如表3 所示,SHEA 评分对再出血有较高的预测价值,AUC=0.882,95%CI0.823~0.942,敏感度为0.862,特异度为0.765。MAP(ASH) 评分(AUC=0.868,95%CI0.823~0.927,敏感度为0.621,特异度为0.918) 和CSMCPI 评分(AUC=0.816,95%CI0.654~0.880,敏感度为0.862,特异度为0.675)也具有较好的预测能力;而pBaylor评分对再出血的预测能力较差,AUC=0.685,95%CI0.695-0.780,敏感度为0.621,特异度为0.712。

图2 SHEA评分及各评分系统对ANVUGIB患者再出血的预测能力Fig 2 Predictive ability of SHEA score compared with other scoring systems for rebleeding in ANVUGIB patients
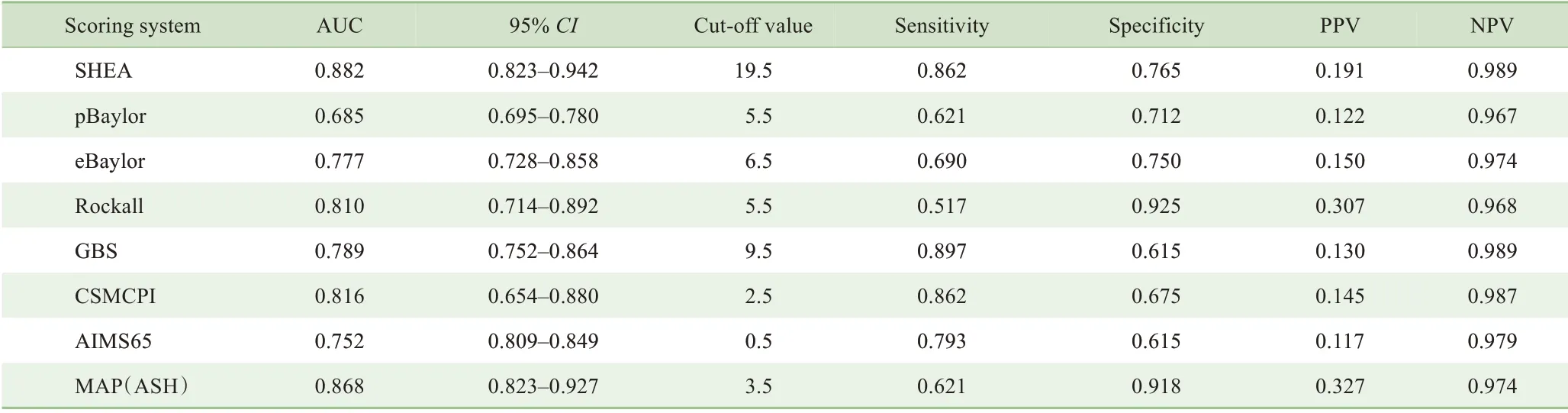
表3 建模组SHEA评分及其他评分系统对ANVUGIB患者再出血的预测价值Tab 3 Predictive value of SHEA score in the training set for rebleeding in ANVUGIB patients compared with other scoring systems
通过Delong 法比较不同ROC 曲线的效能,结果显示SHEA 评分的AUC 与pBaylor、eBaylor、Rockall、GBS、CSMCPI、AIMS65 评分的差异均有统计学意义(均P<0.05),与MAP(ASH)评分的差异无统计学意义(P=0.702),提示SHEA 评分对再出血的预测能力优于除MAP(ASH)评分以外的其余各评分。
验证组中,SHEA 评分的AUC=0.921 (P=0.000),95%CI0.876~0.954,敏感度为0.833,特异度为0.940。
根据决断值将数据划分为低危组(<20分)和高危组(≥20 分)。建模组中,低危组再出血4 例(1.14%),高危组再出血25 例(19.08%),差异具有统计学意义(P=0.000);验证组中,低危组再出血1 例(0.69%),高危组再出血5 例(8.33%),差异具有统计学意义(P=0.009)。故将SHEA 风险评分总分≥20 分的患者定义为高危患者,<20分患者为低危患者。
低危组中,进行干预的患者51 例(10.30%),死亡1例(0.20%);高危组中,干预83 例(43.46%),死亡10例(5.24%)。进行干预的患者比例和死亡患者比例的组间差异均具有统计学意义(均P=0.000),提示该评分系统对死亡和干预的风险也有一定的预测价值。
3 讨论
再出血是评估ANVUGIB 患者预后的重要因素,有报道称再出血的发生可使死亡风险增加10 倍。近几十年来,ANVUGIB的治疗策略与管理方案不断改进,特别是国内外相关指南对抑酸治疗方案不断进行总结、更新,内镜治疗快速发展,该病患者的再出血率及死亡率较前有所下降[3]。但随着人口老龄化趋势加剧,ANVUGIB患者的平均年龄增长,高龄患者往往合并多种基础疾病,器官功能较差,需要接受抗凝、抗血小板药物及NSAIDs治疗的可能性较大,因此,进一步降低ANVUGIB 的再出血率已成为当前临床上面临的一大挑战。目前,国内外指南一致推荐运用经临床验证的预后评分系统来评估患者病情,以指导适时干预。目前,临床上常见的用于判断ANVUGIB 预后的评分系统有Rockall、GBS 和AIMS65评分等,但均不是为预测再出血而设计的,更适用于对死亡的预测[5]。因此,研究影响再出血的危险因素并构建一个预测再出血的风险评分系统意义重大。
本研究回顾性分析了苏州大学附属第一医院收治的481例ANVUGIB患者的临床资料,发现SBP降低、Hb浓度降低、内镜下高危表现和ASA分级>3级是发生再出血的独立危险因素。Hb 是红细胞的主要成分,向全身组织运输氧气,可以反映机体的失血程度。消化道出血早期,由于周围血管收缩和红细胞重新分布等代偿机制,Hb 数值可无明显变化;3~4 h 后,由于大量组织液渗入血管补充血容量,Hb 被稀释;出血后约32 h,Hb 被稀释到最大程度。已有不少消化道出血的评分系统将Hb 作为判断预后的指标之一[6-7]。还有研究[8-10]显示,低Hb 是ANVUGIB内镜治疗后再出血的独立危险因素。血流动力学不稳定是再出血和死亡的重要危险因素[11],收缩压<90 mmHg、心率>100次/min和休克征象是血流动力学不稳定的表现。本研究结果显示低收缩压是再出血的独立危险因素,临床上还需注意与急性心功能不全、感染等因素所致的收缩压下降鉴别。ASA 分级是患者的身体健康状况分级,综合评估了患者的营养状况、自身疾病严重程度等[12]。ASA 分级虽为手术前麻醉评估而建立,但近年来也被不少ANVUGIB 风险评分系统纳入其中[13-14];ASA分级越高,患者的一般情况越差,往往提示预后不佳。内镜下血凝块附着、血管裸露和活动性出血(喷血及渗血)分别对应出血性消化性溃疡的Forrest 分级Ⅱb、Ⅱa、Ⅰ(Ⅰa/Ⅰb)级,其再出血率分别为22%、43%和55%[4,15]。我国一项多中心回顾性研究[16]显示,高危溃疡(ForrestⅠa~Ⅱb级)约占消化性溃疡患者的43.4%,其中仅25.2%的患者接受了内镜下止血治疗,而内镜治疗后的再出血率仍高达15.6%。本研究建立的模型及评分系统仅包括了上述4个变量,易于获得且便于计算,经过内部验证证实该模型及评分系统具有良好的效能。
高龄、合并肝功能不全、合并恶性肿瘤、脉率加快、低白蛋白血症是影响ANVUGIB 患者再出血的相关危险因素,但不是独立危险因素。血清ALB 既能体现患者的营养状况,也是一个重要的炎症生物标志物,在肿瘤等疾病的演变过程中发挥关键作用。相关研究[3,17-18]显示,低白蛋白血症是ANVUGIB 患者再出血或死亡的独立危险因素。虽然本研究未得出一致结论,但在临床上也不可忽视患者的血清ALB 水平。研究[19-20]显示,年龄是影响再出血的独立危险因素,因老年患者合并基础疾病较多,器官功能衰退,预后一般较年轻患者差。但本研究结果显示年龄不是再出血的独立预测因子,这可能与样本量不足有关。在实际临床诊疗过程中,对待高龄患者尤其是合并多种基础疾病者,仍需提高警惕,谨防再出血和死亡的发生。
近年来,国内外仍有许多学者致力于ANVUGIB 危险因素的研究。Yue 等[21]的一项单中心前瞻性队列研究显示,前白蛋白降低和D-二聚体升高是再出血的独立危险因素,单项指标对再出血的预测价值均优于GBS、Rockall 和AIMS65 评分。Lee 等[22]的回顾性研究报道,血清C-反应蛋白可作为预测ANVUGIB 患者30 d 内再出血的一项指标。但目前尚无研究进一步验证这些观点。
本研究存在一定的局限性。本研究为一项单中心回顾性研究,样本量较小且来源单一,未对构建的再出血预测模型及SHEA 风险评分进行外部验证。因而,将建立的模型及评分系统运用于所有ANVUGIB 患者,仍需进行大量多中心、前瞻性研究进一步证实其预测价值。
综上所述,SHEA 评分系统是针对ANVUGIB 患者而设计的新型再出血风险评分工具,计算简便,区分度高,同时对干预及死亡的风险分层也具有一定意义,但其在临床上的应用价值尚需进一步检验。
