肺超声联合血清NT-proBNP、sFlt-1对急性呼吸窘迫综合征患者病情严重程度及预后评估价值
2021-12-29马桂兰
马桂兰,敏 菊
(临夏市人民医院 心血管呼吸内科,甘肃 临夏 731100)
急性呼吸窘迫综合征(acute respiratory distress syndrome, ARDS)是由于肺部感染所导致的肺部严重炎症反应,临床症状主要表现为急性呼吸性窘迫、进行性呼吸困难等。该病起病急骤、病情进展迅速,ARDS急性加重期患者病情更加危急,病死率较高,早期的诊断、评估对改善预后具有十分重要的价值[1-2]。但是,目前临床尚缺乏对ARDS病情严重程度及预后预测的方法。肺部超声具有安全、快捷、无创的优点,肺部超声评分(LUS)更是临床诊断急危重症常用诊断工具[3]。有研究表明,在ARDS发生、发展过程中血清氨基末端脑钠肽前体(NT-proBNP)、可溶性血管内皮生长因子受体(sFlt-1)发挥着重要作用[4],但能否将其作为评估ARDS预后的指标仍待进一步研究。本研究旨在探讨肺部超声联合NT-proBNP、sFlt-1对ARDS患者病情严重程度及预后的评估价值,为临床诊疗提供依据及参考。
1 资料与方法
1.1病例选择 选取我院于2018年4月-2020年10月收治的ARDS患者138例,男82例,女56例。年龄39~75岁,平均(56.14±8.02)岁,体质量指数(BMI)19.76~27.46 kg/m2,平均(22.45±2.68) kg/m2。其中发病原因:脓毒血症52例,脑血管事件31例,外伤28例,开胸术后27例。纳入标准:①符合2012年ARDS柏林会议诊断标准[5];②签署知情同意书。排除标准:①临床诊断不明确;②发病时间超过24小时;③合并恶性肿瘤;④合并自身免疫疾病或血液系统疾病;⑤合并心源性肺水肿、肺纤维化、弥漫性肺出血等疾病;⑥合并肺结核;⑦严重精神障碍。本研究经我院医学伦理委员会批准同意。
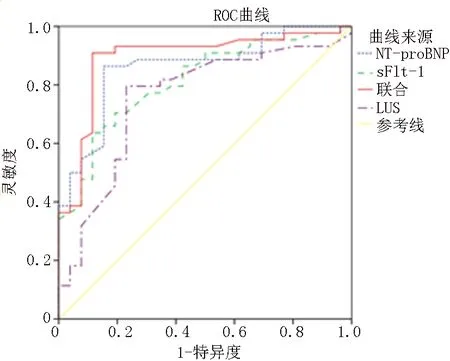
1.2方法 收集患者一般临床资料,进行肺部超声检查,计算LUS,测定血清NT-proBNP、sFlt-1。按照氧合指数(OI)将ARDS患者分为重度组[OI≤100 mmHg(1 mmHg=0.133 kPa),58例]、中度组(100 mmHg 1.3观察指标 1.3.1一般临床资料 记录年龄、性别、BMI、合并基础疾病、发病原因,测定平均动脉压(MAP)、心率、呼气末正压(PEEP)、动脉血二氧化碳分压(PaCO2)和动脉血氧分压(PaO2),计算OI。 1.3.2肺部超声及LUS 仪器:便携式彩色多普勒超声诊断仪(型号:开立S8 Exp,深圳开立生物医疗科技股份有限公司),参数:相控阵凸面探头,频率3.5~10.0 MHz。进行肺部超声检查者经专门超声训练。患者取仰卧位,检查患者后胸壁上下部、两侧前胸壁及侧胸壁,共将两侧肺部划分为12个区域。LUS标准:依次检查所有患者肺前区域、肺侧区域及肺后区域,每一分区以最高评分进行记录。超声图像显示通气区正常为0分;超声检查切面出现1~2个彗星尾症,肺通气减少为1分;一个超声检查切面出现彗星尾症≥3个,重度肺通气减少为2分;超声检查切面可见肺实变(肺出现组织样结构,有动态支气管充气征)或肺不张(肺出现组织样结构,有静态支气管充气征)为3分。12个肺区评分综合即为LUS,为0~36分,分数越高表明肺部损伤越严重。 1.3.3血清NT-proBNP、sFlt-1 采集患者空腹肘静脉血5 ml,4 500 r/min离心10 min,分离血清,采用电化学发光法测定血清NT-proBNP,试剂盒购自美国罗氏公司。采用酶联免疫吸附实验(ELISA)法检测sFlt-1,试剂盒由上海力勤生物科技有限公司生产,严格遵循说明书进行检测。 2.1LUS、血清NT-proBNP、sFlt-1比较 3组LUS、血清NT-proBNP、sFlt-1比较,差异有统计学意义(均P<0.05)。重度组LUS、血清NT-proBNP、sFlt-1高于中度组和轻度组(均P<0.05)。中度组LUS、血清NT-proBNP、sFlt-1高于轻度组(均P<0.05)。见表1。 表1 3组LUS、血清NT-proBNP、sFlt-1比较 2.2预后亚组临床资料比较 138例ARDS患者中有预后不良41例(29.7%),预后良好97例(70.3%)。预后不良组入住ICU时间、LUS、NT-proBNP、sFlt-1显著高于预后良好组(均P<0.05),PaCO2、PaO2、OI显著低于预后良好组(均P<0.05),见表2。 表2 各预后亚组临床资料比较 2.3预后的回归分析 以ARDS患者预后是否良好为因变量,以入住ICU时间、PaCO2、PaO2、OI、LUS、NT-proBNP、sFlt-1为自变量,进行Logistic回归分析。结果显示,入住ICU时间、LUS、NT-proBNP水平、sFlt-1均为ARDS预后的影响因素(均P<0.05),见表3。 2.4LUS联合血清NT-proBNP、sFlt-1对ARDS预后评估效能 ROC曲线显示,LUS、NT-proBNP、sFlt-1预测ARDS预后的最佳截断点分别为18.12分、598.36 ng/L、487.52 ng/L,三者联合的特异度为84.54%,高于LUS、NT-proBNP、sFlt-1单独评估的特异度。三者联合预测ARDS预后的AUC为0.896,高于LUS、NT-proBNP、sFlt-1单独的AUC(0.751、0.844、0.773)。见表4、图1。 图1 LUS联合血清NT-proBNP、sFlt-1预测ARDS预后不良的ROC曲线 表4 LUS联合血清NT-proBNP、sFlt-1对ARDS预后的预测价值 ARDS患者影像学表现为肺组织不同区域的肺通气改变和不同程度的实变,起病急骤、病情进展迅速,发病率和病死率较高[6]。肺部超声具有安全、快捷、无辐射、无创、可重复性强等优点,是一种非侵入性检查,临床在评估呼吸系统疾病患者病情方面广泛应用[7]。依据超声征象评估的LUS能很好地反映肺部局灶性病变,评估患者肺损伤程度[8]。NT-proBNP主要来源于心室分泌的脑利钠肽前体裂解,其水平对脓毒症的发生具有一定预测价值,而脓毒症是ARDS急性加重期患者的重要诱发因素[9-10]。sFlt-1是一种糖蛋白,其水平升高可导致内皮细胞受损,降低免疫功能,促进疾病恶化[11]。 本研究重度组LUS、血清NT-proBNP、sFlt-1均高于中度组和轻度组,中度组LUS、血清NT-proBNP、sFlt-1均高于轻度组。表明LUS、血清NT-proBNP、sFlt-1越高,患者病情可能越严重。与Karge等[12]研究结果一致。本研究预后不良发生率29.7%,预后不良组入住 ICU时间、LUS、NT-proBNP、sFlt-1均显著高于预后良好组,而PaCO2、PaO2、OI显著低于预后良好组。回归分析显示,入住ICU时间、LUS、NT-proBNP、sFlt-1均为ARDS预后的影响因素。提示临床医师在诊治过程中需对上述影响因素逐一控制,以降低ARDS预后不良率。曾天星等[13]比较了ARDS不同预后患者早期NT-proBNP,发现预后不良组各时间点NT-proBNP均高于预后良好组,提出NT-proBNP与ARDS患者预后可能存在一定相关性。本研究证实了NT-proBNP为ARDS预后的影响因素,与其结果相印证。sFlt-1在抗血管生成中发挥重要作用,通过减弱巨噬细胞和单核细胞的活化及迁移产生抗炎作用。有研究发现,sFlt-1的变化是对肺部疾病的代偿保护,能够提示病情严重程度,sFlt-1过高时表明机体处于高激活状态[14],可作为患者重要的预后评估指标。有研究表明,LUS在ARDS急性加重期患者中具有较高诊断效能,可作为临床诊断的重要参考指标[15]。ROC曲线显示,LUS、NT-proBNP、sFlt-1单一及联合检测预测ARDS预后的AUC分别为0.751、0.844、0.773、0.896,提示LUS联合NT-proBNP、sFlt-1对ARDS预后具有较高预测效能,可将其作为临床重要参考指标。临床医师可结合LUS、NT-proBNP、sFlt-1在疾病早期对患者病情进行预测,提前发现、控制和治疗。 综上,肺部超声联合NT-proBNP、sFlt-1对ARDS预后的预测效能较高,建议在临床中采用肺部超声联合NT-proBNP、sFlt-1对ARDS进行诊断,以提高对ARDS预后判断的准确性,降低患者死亡风险。
2 结 果


3 讨 论
