CS/CMC/HAP/TCP复合PGMA材料的合成研究*
2021-12-29黄俊潮张光学
张 鹏,黄俊潮,屈 亮,张光学
(湖北科技学院核技术与化学生物学院,湖北 咸宁 437100)
随着全球人口数量增加及人均寿命的提升,每年因骨折、患病造成骨坏损需要进行骨矫正与骨移植手术的病例呈上升之势,需要大量的骨修复材料,常用的材料有自体骨、异体骨、异种骨及人工骨材料4种[1]。从生物学角度考虑,自体骨是理想的骨移植材料,但从骨来源、手术给患者造成痛苦的角度考虑也存在不足;虽然异体骨与异种骨可以解决骨来源问题,却因其存在免疫排异反应或传染疾病的风险也受到了限制。因此,骨移植材料来源就落在人工骨材料方面。
羟基磷灰石(HAP)与磷酸三钙(β-TCP)都是骨组织的主要成分和骨组织修复的良好材料,已在临床医学上得到了广泛的应用[2]。壳聚糖(CS)具有良好的生物相容性、生物可降解性且降解产物可被人体完全吸收,明显改善材料的力学性能,促进骨细胞的黏附、增值作用[3]。羧甲基纤维素钠(CMC)具有可降解、生物相容性及较强的粘结性[4]。聚甲基丙烯酸缩水甘油酯(PGMA)具有较好力学性能,但由于表面光滑,骨细胞附着性、骨传导性及骨再生修复功能存在缺陷,所以寻找具有良好的力学性能、再生修复作用强的人工骨材料一直是科研工作者追求的目标。我们采用CMC、CS、HAP、β-TCP与甲基丙烯酸缩水甘油酯(GMA)经辐照聚合制备人工材料,现将过程总结报告如下。
1 材料与方法
1.1 材料
骨水泥材料采用钴源辐照方法,于湖北省农业科学院完成。
主要试剂与仪器:壳聚糖,脱乙酰度90%,BR,国药集团化学设计有限公司;纳米HAP:AR,β-TCP:AR,GMA:98%,AR,以上皆购于上海阿拉丁有限公司;人骨肉瘤细胞(U2OS),ATCC;1640培养液、缓冲液FBS、青霉素、链霉素,皆为Gibco,USA。
X射线衍射仪(X’Pert Pro MPD,Philips,Ducth);Inspect-F扫描电子显微镜(FEI,USA);万能材料试验机(AG10TA,JEOL,Japan);倒置相差显微镜(Olympus,USA)。
1.2 实验方法
1.2.1 复合骨水泥材料的制备
分别配制20% CS与20% CMC凝胶,取混合凝胶(各50%)1g数份,依次加入0.0、0.1、0.2、0.3、0.4g质量(HAP/TCP=1)粉体,与混合凝胶充分搅拌混匀后,置于模具中定型。定型的固体先在50℃真空中48h干燥至恒重,然后让固体材料整体浸泡液体GMA中;数天直至恒重取出,将其置于钴源中辐照,辐照总剂量为14kGy,制成复合材料,见图1(封三)。
1.2.2 扫描电镜观察
将复合材料烘干后真空喷金,用扫描电镜扫描试样表面,观察样品表面形貌,记录并照相。
1.2.3 X射线衍射分析
采用X射线衍射仪对HAP、β-TCP、PGMA复合材料分别进行了物相组成分析,分析条件为:电压35kV,电流25mA,衍射起始角10°,衍射终止角80°,步宽0.06°,波长1.5406 nm。
1.2.4 复合材料的力学性能测试
使用万用材料试验机对不同质量比复合材料进行抗压强度测试,于室温以1mm/min的速度等速加载压缩,直至样品破裂或者厚度减少60%。按照公式计算强度[5],抗压强度(MPa)=4Fmax÷πd2,其中Fmax为最大加载力(kg),d为试件的直径(mm)。每种样品测3次,取平均值。
1.2.5 复合材料细胞增殖实验
将材料切成2mm厚,直径10mm的小块,置于EP管中121℃高压灭菌20min;将灭完菌的材料置于12孔板上预湿,每空一块材料,每种材料置3孔,并设3孔为不加材料的空白对照组;将第三代U2OS细胞以1×105/孔定量接种在材料上,每孔2mL培养液,于37℃、5%CO2、饱和湿度下培养,每天换一次液;培养一周后,用胰蛋白酶EDTA消化吸收细胞,将细胞计数后求平均值;增值率=(平均细胞数-初始细胞数)/初始细胞数。
2 结 果
2.1 X射线衍射分析结果
从图2可知,复合材料中HAP(2θ=32.1°的主峰和33°的次强峰)与β-TCP(2θ=31°的主峰和33.2°的次强峰)的特征衍射峰清晰可见,材料的复合并没有改变HAP与β-TCP的结构,其与混合凝胶、PGMA之间的复合应为物理结合。
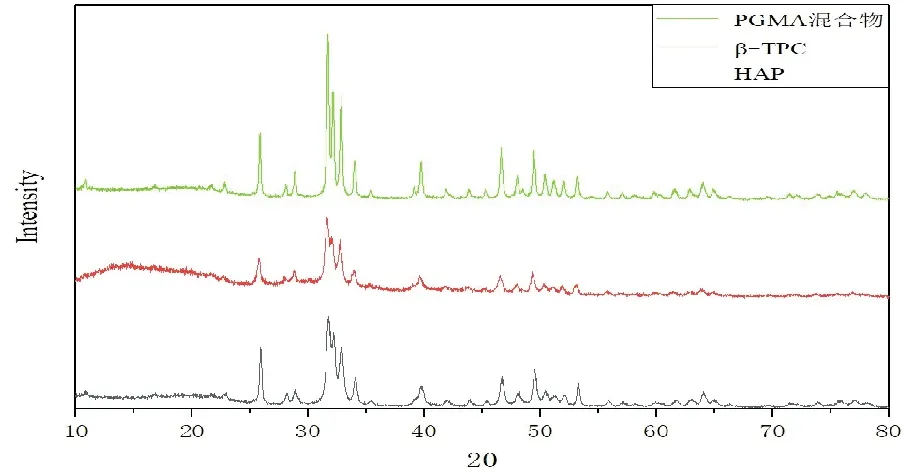
图2 复合材料的X射线衍射图谱
2.2 抗压强度检测结果
表1是1.0g混合凝胶中加不同质量的粉体(HAP/β-TCP=1∶1),不加GMA未辐照时所测定的复合材料的压缩强度;1.0g混合凝胶中加不同质量的粉体(HAP/β-TCP=1∶1),浸泡GMA辐照聚合后所测定的复合材料的压缩强度,所得结果明显高于不加GMA未辐照的复合材料。

表1 添加不同质量粉体复合材料的力学性能表
2.3 扫描电镜观察结果
1g质量混合凝胶中加0.3g粉体(HAP/β-TCP=1∶1)扫描电镜观察。图3a为放大10k倍,未加GMA不辐照,材料中空隙较大,其原因是材料干燥过程中凝胶中的溶剂挥发所致。图3b放大10k倍,加GMA辐照的材料中可以看见缝隙明显降低,其原因是材料浸泡了一定量的GMA,经钴源辐照生成了聚合物PGMA,降低了材料中的空隙。

图3 复合材料的扫描电镜观察图(10k倍)
2.4 U2OS细胞形态学观察结果
表2是人肉瘤骨细胞培养7d的细胞增殖情况。从表中可知,复合材料有利于细胞增殖。图4(封三)为倒置显微镜观察U2OS细胞形态,A-C为壳聚糖与HAP和β-TCP比例为0.1、0.2、0.3复合材料浸提液中的细胞,D为阴性对照组,细胞在不同比例的复合材料浸提液中生长良好,与阴性对照组没有差别。

表2 细胞相对增值率对照表
3 讨 论
上述复合材料经真空干燥后,材料中的溶剂分子将会逸出一部分留下空隙,将其放于GMA中浸泡,GMA慢慢渗透到材料空隙中。将浸泡的材料于60Coγ射线辐照,GMA转化生成PGMA凝胶,进一步降低材料中的空隙,因而复合材料压缩强度得到了进一步的提高。
由于混合凝胶为CS与CMC,CS与CMC在组织体液中长时间浸泡,CS与CMC就会发生降解和溶解,导致材料的力学性能迅速下降;而骨组织再生修复过程是一个比较缓慢的过程,所需时间要达数月甚至更长。为充分保证复合材料高强度力学性能,避免给患者二次手术造成痛苦;将材料添加GMA进行辐照,增加疏水性的PGMA高分子聚合物。一方面可以进一步提高材料的压缩强度,另一方面可以延缓CS与CMC降解和溶解的速度,骨组织进行再生修复时,骨材料的力学性能不会迅速下降。
由于HAP具有良好的生物相容性,与骨组织成分相似,目前骨外科矫形材料应用较多,HAP的强度不高且难以降解,不利于骨组织的再生与修复。为寻找优异性能的骨移植材料,很多学者[2-6]采用CS、CMC复合的方法。TCP强度不高,在体内代谢生成Ca2+、 PO43-,被骨组织吸收,促进骨组织的再生与修复。CS是天然高分子聚合物,具有消炎、杀菌、生物体内易降解及良好的生物相容性而广泛用于生物复合材料。图4的生物学实验进一步说明,复合材料有利于细胞的附着与增殖;利用CS、CMC易于降解之特性,其降解所留下来的孔隙,将有利于骨细胞体液的传导,更好地促进骨组织再生与修复。
为解决骨外科矫形材料力学性能不足,目前较多的是用高分子聚合物聚甲基丙烯酸甲酯(PMMA)进行复合[7],而PGMA的结构与PMMA非常相似,用作生物材料也未见文献报道;采用辐照法合成PGMA高分子聚合物,操作简便易行,可以根据所需矫正骨的形状设计相应的模具,再将复合材料加到模具中即可制成不同形状骨组织材料。本次抗压强度实验结果说明,随着粉体量的增加,复合材料的力学性能呈先增后降趋势,实验中加入0.2、0.3g粉体所制备的复合材料皆在180MPa以上,完全可以满足骨组织替代材料力学性能的要求。U2OS为人骨肉瘤组织中分离的细胞,对化合物及病毒极其敏感,已广泛用于体外生物医学实验[8];表2与图4的细胞形态学实验表明,所制备的复合材料具有良好的生物相容性。
总之,采用辐照方法合成PGMA高分子聚合物,能将CS、CMC、HAP/β-TCP粉体很好的融合为一体,方法简便、生物相容性好,既满足了骨材料力学性能的要求,又兼顾了骨组织再生修复,有望成为骨外科矫形材料一种新的合成方法。
