含吡唑-4-甲酰胺的嗜球果伞素类化合物的设计、合成及杀虫活性
2021-12-23楼佳明郝树林方佳琪杜晓华
楼佳明, 郝树林, 方佳琪, 杜晓华
(浙江工业大学 催化加氢中心,浙江省绿色农药清洁生产技术研究重点实验室,浙江省绿色农药协同创新中心,杭州 310014)
嗜球果伞素 (Strobilurin) 类化合物自1969 年Musílek 等[1]发现其具有杀菌活性以来,已开发出嘧菌酯、肟菌酯、吡唑醚菌酯等20 余种农用杀菌剂,形成了一个重要的杀菌剂类别。此外,经过不断的结构改造,部分Strobilurin 类化合物在除草[2]、杀螨[3]、抗病毒[4]及抗癌[5]等方面也具有很好的活性。本课题组设计合成了一系列含嘧啶硫醚的Strobilurin 类化合物,表现出了良好的杀螨活性,其中化合物 L1(图式1) 对朱砂叶螨Tetranychus cinnabarinus幼虫和卵的活性约为嘧螨酯的2 倍[6]
吡唑酰胺类杀菌剂是近年来迅速发展起来的一类琥珀酸脱氢酶抑制剂 (SDHI),如氟唑环菌胺、苯并烯氟菌唑、联苯吡菌胺、氟唑菌酰胺、氟茚唑菌胺和吡噻菌胺等。
本文以含嘧啶硫醚的Strobilurin 类化合物L1为基础,通过活性亚结构拼接,将吡唑-4-甲酰胺通过苯环与嘧啶环连接,设计并合成了16 个结构新颖的Strobilurin 类化合物,并进行了生物活性测试。目标化合物的设计和合成路线分别见图式1和图式2。
1 实验部分
1.1 仪器与试剂
Bruker Avance Ⅲ 500 MHz 核磁共振波谱仪(CDCl3或者DMSO-d6为溶剂,TMS 作为内标)。全部试剂均为市售分析纯化学试剂。柱层析硅胶(筛孔径为45~75 μm) 产自青岛海洋化工厂;5-氟-1, 3-二甲基-1H-吡唑-4-酰氟,纯度98%,由绍兴好润有限公司提供。
1.2 化合物合成
1.2.1 中间体2 的合成通法 参考文献[7-8]方法进行。在50 mL 三口烧瓶中依次加入5.24 g(30 mmol) 1c 和15 mL 甲苯,在室温搅拌下缓慢滴加17.8 g (150 mmol) 氯化亚砜和0.1 mL DMF,升温回流4 h。待烧瓶内再无气泡产生时,减压蒸馏出甲苯和过量氯化亚砜,得到4.7 g 2c 中间体。同法合成2a 和2b。2a~2c 均为棕色液体。
1.2.2 中间体5 的合成通法 参考文献[9]方法进行。在1 L 三颈烧瓶中依次加入84 g (0.5 mol) 对硝基苯甲酸和500 mL 乙腈,在25 ℃下机械搅拌0.5 h 后,分批加入97 g (0.6 mol) 羰基二咪唑(CDI),继续室温搅拌2 h,作为反应液A 备用。
在另一个2 L 三颈烧瓶中依次加入119 g(0.7 mol)丙二酸单乙酯钾盐和500 mL 乙腈,于25 ℃下机械搅拌0.5 h,依次加入73 g (0.725 mol)三乙胺和69 g (0.725 mol) 无水氯化镁,继续室温搅拌2 h 后,冷却到0 ℃。将反应液A 缓慢滴加入上述反应体系,通过薄层色谱监测至硝基苯甲酸原料点消失时,用盐酸调节pH 值为6~7,减压蒸馏脱去大部分乙腈后,加入700 mL 水和1 L 乙酸乙酯进行萃取,依次用饱和碳酸氢钠溶液和饱和氯化钠溶液洗涤有机层,减压蒸馏脱去溶剂,得到117.16 g 对硝基苯甲酰乙酸乙酯 (化合物5),黄色固体,收率为99 %,熔点72.5~73.8 ℃ (文献[10]71~73 ℃)。
1.2.3 中间体6 的合成通法 参考文献[11-13]方法进行。在500 mL 三颈瓶中依次加入65 g (0.96 mol)乙醇钠和270 mL 无水乙醇,在25 ℃下搅拌0.5 h,加入95 g (0.4 mol) 化合物5 和90 g (0.8 mol) 硫脲,加热升温至回流,通过薄层色谱 (V(乙酸乙酯) :V(石油醚) = 2 : 1) 监测至反应结束。减压蒸馏脱去乙醇。加入1 000 mL 水溶解反应液,用盐酸调节 pH=2~3,析出固体,抽滤,滤饼用500 mL水洗涤3 次,收集并烘干得到81 g 化合物6,黄色固体,粗产品未进行提纯投入下一步反应。
1.2.4 中间体7 的合成通法 参考文献[14-15]方法进行。在250 mL 三颈瓶中依次加入20.0 g(80 mmol) 化合物6、15.5 g (112 mmol) 碳酸钾和100 mLN,N-二甲基甲酰胺 (DMF),室温下搅拌0.5 h 后,加入11.6 g (96 mmol) 3-溴丙烯,继续室温搅拌4 h。冷却至室温,向反应液中加入200 mL水,滴加盐酸调节至中性,抽滤,将滤饼用100 mL 水洗涤3 次后烘干,得到21.8 g 化合物7a,不经提纯投入下一步反应。
7a 和7b 表征数据如下。
7a:淡黄色固体,m.p. 191.1~192.5 ℃。1H NMR(600 MHz, DMSO),δ: 12.86 (s, 1H), 8.35 – 8.28 (m, 4H), 6.87(s, 1H), 6.05−5.95 (m,1H), 5.37(dd,J= 17.0, 1.4 Hz, 1H), 5.15(dd,J= 10.0, 1.4 Hz, 1H), 3.94 (d,J= 6.9 Hz, 2H)。HRMS:C13H11N3O3S[M−H+],计算值288.044 8,测试值288.044 2。
7b:白色固体,m.p. 195.5~196.7 ℃。1H NMR(600 MHz, DMSO),δ: 12.82 (s, 1H), 8.37–8.28 (m, 4H), 6.91(s, 1H), 6.43 (t,J= 7.5 Hz, 1H), 4.02 (t,J=7.5 Hz, 2H)。HRMS: C13H9Cl2N3O3S[M−H+],计算值355.966 9,测试值355.966 1。
1.2.5 中间体8 的合成通法 参考文献[16]方法进行。在2 5 0 m L 三颈瓶中依次加入1 7.4 g(60 mmol) 化合物7a、16.8 g (300 mmol) 铁粉、100.8 g (0.6 mol) 六氟异丙醇、60 mL 盐酸和540 mL 水,室温下反应30 min,向反应液中加入饱和碳酸钠溶液调节pH 值为中性,用50 mL乙酸乙酯萃取3 次,合并有机相,用无水硫酸镁干燥,抽滤除去固体残渣,滤液减压脱除溶剂,得到的粗产品,再经硅胶柱层析 (V(乙酸乙酯) :V(石油醚) = 1 : 1) 分离纯化后得到15.6 g 化合物8a,收率98 %。
8a 和8b 表征数据如下。
8a:黄色固体,m.p. 201.4~201.8 ℃.1H NMR (500 MHz, DMSO),δ: 12.44 (s, 1H), 7.80 (d,J= 8.0 Hz, 2H),6.63 (d,J= 8.1 Hz, 2H), 6.40 (s, 1H), 5.98 (dd,J= 16.8,9.5 Hz, 1H), 5.96 (s, 2H), 5.34 (d,J= 17.1 Hz, 1H), 5.14 (d,J= 9.9 Hz, 1H), 3.91 (d,J= 6.2 Hz, 2H)。HRMS: C13H13N3OS[M−H+],计算值258.070 7,测试值258.070 4。
8b:黄色固体,m.p. 190.2~192.4 ℃.1H NMR (600 MHz,DMSO),δ: 12.42 (s, 1H), 7.79 (d,J= 8.2 Hz, 2H), 6.62 (d,J=8.3 Hz, 2H), 6.46 (s, 1H), 6.39 (t,J= 7.3 Hz, 1H), 5.74 (s, 2H),3.96 (d,J= 7.3 Hz, 2H)。HRMS: C13H11Cl2N3OS[M−H+],计算值325.992 7,测试值325.991 1。
1.2.6 中间体9 的合成通法 参考文献[17-18]方法进行。在50 mL 三颈瓶中依次加入2.6 g (10 mmol)化合物8a、2.1 g (15 mmol) 碳酸钾和10 mL DMF,在25 ℃下搅拌15 min 后,加入3.4 g (12 mmol)2 -溴甲基-α-甲氧基亚氨基苯乙酸甲酯,于85 ℃下搅拌8 h。向反应液中加入30 mL 水,用乙酸乙酯 (30 mL × 3) 萃取,合并有机相,用50 mL 饱和氯化钠溶液洗涤3 次,无水硫酸镁干燥,抽滤除去固体残渣,滤液减压脱除溶剂,得到粗产品,通过硅胶柱层析 (V(乙酸乙酯) :V(石油醚) = 2 : 1)分离纯化,得到2.5 g 化合物9b,收率55 %。
9a~9d 表征数据如下。
9a:黄色油状物,1H NMR (600 MHz, DMSO),δ: 7.89(d,J= 8.7 Hz, 2H), 7.66 (s, 1H), 7.53 – 7.47 (m, 1H), 7.37 –7.31 (m, 2H), 7.17 – 7.12 (m, 1H), 6.87 (s, 1H), 6.67 (d,J=8.7 Hz, 2H), 6.07 – 5.95 (m, 1H), 5.76 (s, 2H), 5.32 (dd,J=17.0, 1.4 Hz, 1H), 5.29 (s, 2H), 5.14 – 5.10 (m, 1H), 3.85 (d,J= 6.8 Hz, 2H), 3.80 (s, 3H), 3.61 (s, 3H)。HRMS:C25H25N3O4S[M+H+],计算值464.163 9,测试值464.164 6。
9b:黄色油状物,1H NMR (500 MHz, CDCl3),δ: 7.90 –7.80 (m, 2H), 7.53 (d,J= 7.4 Hz, 1H), 7.46 – 7.38 (m, 2H),7.21 (dd,J= 7.5, 1.2 Hz, 1H), 6.68 (d,J= 8.6 Hz, 2H), 6.63 (s,1H), 6.08 − 6.02 (m, 1H), 5.32 (s, 2H), 5.31 (dd,J= 16.95, 1.4 Hz, 1H),5.12 (dd,J= 10.0, 1.0 Hz, 1H), 4.02 (s, 3H), 3.86 (d,J= 6.9 Hz, 2H), 3.83 (s, 3H)。HRMS: C24H24N4O4S[M+H+],计算值465.159 1,测试值465.157 4。
9c:淡黄色油状物,1H NMR (600 MHz, DMSO),δ:7.86 (d,J= 8.7 Hz, 2H), 7.65 (s, 1H), 7.48 – 7.44 (m, 1H),7.36 – 7.29 (m, 2H), 7.16 – 7.10 (m, 1H), 6.89 (s, 1H), 6.62 (d,J= 8.7 Hz, 2H), 6.31 (t,J= 7.5 Hz, 1H), 5.78 (s, 2H), 5.26 (s,2H), 3.90 (d,J= 7.5 Hz, 2H), 3.81 (s, 3H), 3.59 (s, 3H)。HRMS: C25H23Cl2N3O4S[M+H+],计算值532.085 9,测试值532.085 8。
9d:黄色油状物,1H NMR (600 MHz, DMSO),δ: 7.85(d,J= 8.7 Hz, 2H), 7.54 (d,J= 7.2 Hz, 1H), 7.49 – 7.39 (m,2H), 7.24 (dd,J= 7.5, 1.0 Hz, 1H), 6.81 (s, 1H), 6.62 (d,J=8.7 Hz, 2H), 6.32 (t,J= 7.5 Hz, 1H), 5.79 (s, 2H), 5.25 (s, 2H),3.91 (s, 3H),3.90 (d,J= 7.5 Hz, 2H), 3.72 (s, 3H)。HRMS:C24H22Cl2N4O4S[M+H+],计算值533.081 2,测试值533.081 2。
1.2.7 目标化合物10 的合成通法 目标化合物的合成采用了两种反应方式:一种是吡唑-4-甲酰氯中间体与胺反应;另一种是吡唑-4-甲酰氟与胺反应。其中10a~10h 和10m~10p 由吡唑-4-酰氯与胺反应得到,10i~10l 由吡唑-4-酰氟与胺反应得到。
1.2.7.1 吡唑-4-甲酰氯与胺反应 参考文献[19-20]方法进行。以目标化合物 (E) -2-甲氧基亚甲基-2-(6- (4- (5-氯-1, 3-二甲基-1H-吡唑-4-羰基氨基) -苯基) -2-烯丙硫基-4-氧基甲基) 苯乙酸甲酯 (10m) 的合成为例:将0.20 g (0.43 mmol)9a、0.12 g (0.65 mmol) 2c 和4 mL 乙腈加入到25 mL 三颈瓶中,加入0.07 g (0.86 mmol) 三乙胺作缚酸剂,在室温下搅拌,通过薄层色谱 (V(乙酸乙酯) :V(石油醚) =1 : 1) 监测,待原料点消失时向反应液中加入30 mL 水,用乙酸乙酯 (30 mL × 3) 萃取。合并有机相,用50 mL 饱和氯化钠溶液洗涤3 次,无水硫酸镁干燥,抽滤除去固体残渣,滤液减压脱除溶剂,得到粗产品,通过硅胶柱层析 (V(乙酸乙酯) :V(石油醚) = 1 : 1) 分离纯化得到0.25 g 目标化合物10m,收率92 %。
1.2.7.2 吡唑-4-甲酰氟和胺反应[21]以目标化合物 (E) -2-甲氧基亚甲基-2- (6- (4-(5-氟-1,3-二甲基-1H-吡唑-4-羰基胺基)-苯基) -2-烯丙硫基-4-氧基甲基) 苯乙酸甲酯 (10j) 的合成为例:将0.20 g (0.43 mmol) 9a、0.11 g (65 mmol) 5-氟-1, 3-二甲基-1H-吡唑-4-酰氟和4 mL 氯苯加入到25 mL 三颈瓶中,加入0.07 g (0.86 mmol) 三乙胺作缚酸剂,在140 ℃下搅拌8 h。向反应液中加入30 mL 水,用乙酸乙酯 (30 mL × 3) 萃取。合并有机相,用50 mL 饱和氯化钠溶液洗涤3 次,无水硫酸镁干燥,抽滤除去固体残渣,滤液减压脱除溶剂,得到粗产品,通过硅胶柱层析 (V(乙酸乙酯) :V(石油醚) = 1 : 1)分离纯化得到0.20 g 目标化合物10j,收率79 %。
1.3 生物活性测试
1.3.1 供试药液的配制 将供试化合物用含0.1 %吐温80 的蒸馏水溶液稀释至试验所需的剂量(200 和500 mg/L),备用。以蒸馏水为对照(CK)。
1.3.2 试验方法
1.3.2.1 浸叶法 采用文献[22]的方法测定。供试靶标为黏虫Mythimna separata。将适量玉米叶在配好的药液中充分浸润后自然阴干,放入垫有滤纸的培养皿中,接入黏虫3 龄中期幼虫,10 头/皿,置于24~27 ℃观察室内培养,2 d 后调查结果。以毛笔触动虫体,无反应视为死虫。
1.3.2.2 喷雾法 采用文献[22]的方法测定。供试靶标为朱砂叶螨Tetranychus cinnabarinus和苜蓿蚜Aphis craccivoraKoch。分别将接有朱砂叶螨和苜蓿蚜的蚕豆叶片置于Potter 喷雾塔下喷雾处理,处理后将朱砂叶螨置于24~27 ℃观察室内培养,苜蓿蚜置于20~22 ℃观察室内培养,48 h 后调查结果。以毛笔触动虫体,无反应视为死虫。
2 结果与分析
2.1 目标化合物的合成
所有目标化合物都是通过吡唑羧酸 (或酰氟)、对硝基苯甲酸和2-溴甲基-α-甲氧基亚甲基苯乙酸甲酯经过多步反应得到。首先对硝基苯甲酸经过羰基二咪唑活化和丙二酸单乙酯钾盐反应得到对硝基苯甲酰乙酸乙酯,然后与硫脲在碱性条件下缩合得到6- (4-硝基苯基) -2-硫代-2, 3-二氢嘧啶-4(1H) -酮,室温下与不同的卤代溴丙烯进行亲核取代反应,再经过铁粉还原得到对氨基苯基嘧啶中间体;另一中间体吡唑酰氯则是通过吡唑羧酸氯化得到。然后将对氨基苯基嘧啶中间体与2-溴甲基-α-甲氧基亚甲基苯乙酸甲酯经过亲核取代,再与吡唑酰氯 (或酰氟) 缩合得到目标化合物。其结构表征数据见表1 和表2。
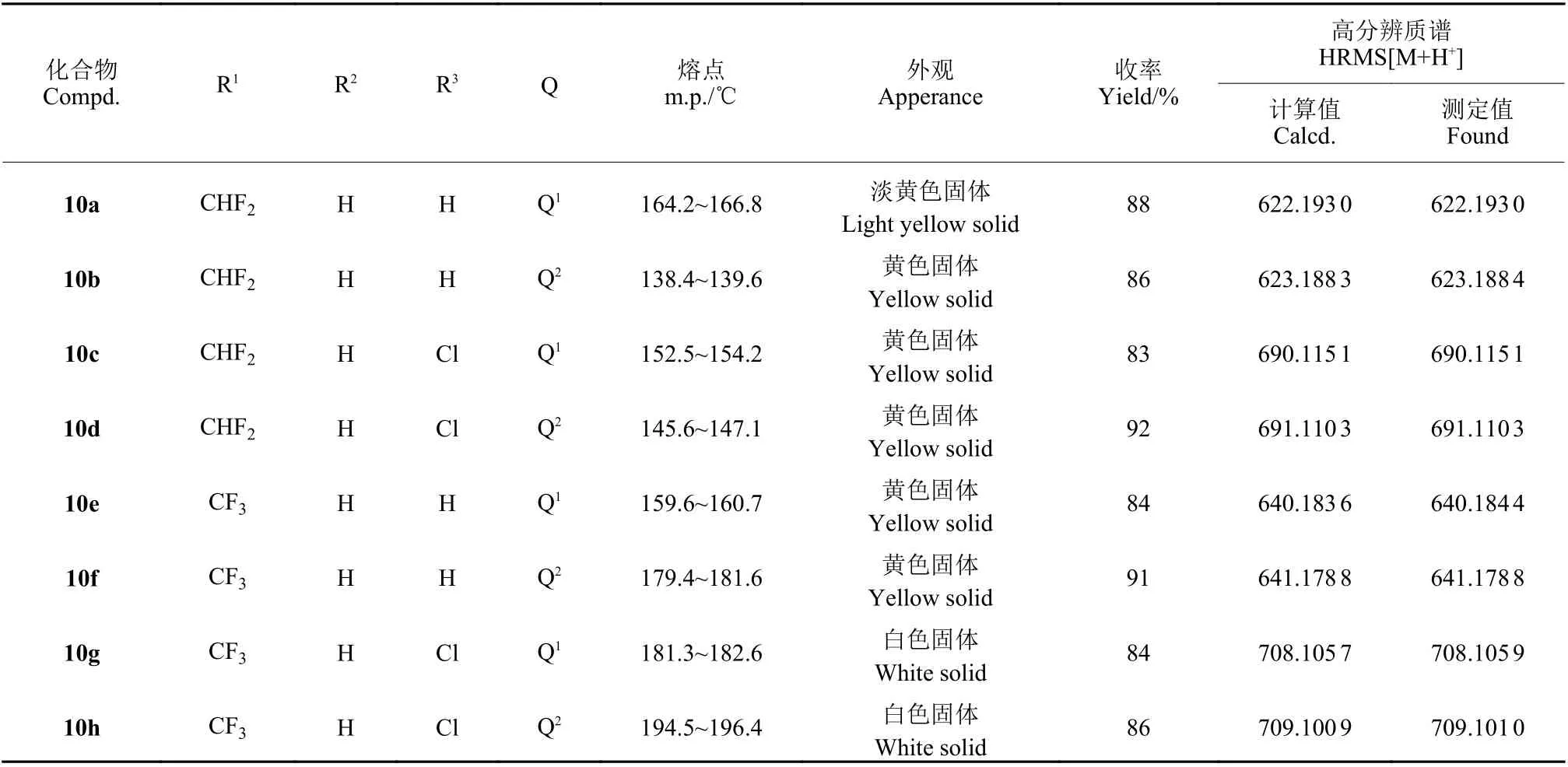
表1 目标10a~10p 的理化性质及高分辨质谱数据Table 1 Physico-chemical properties and HRMS data of compounds 10a-10p

续表1Table 1 (Continued)
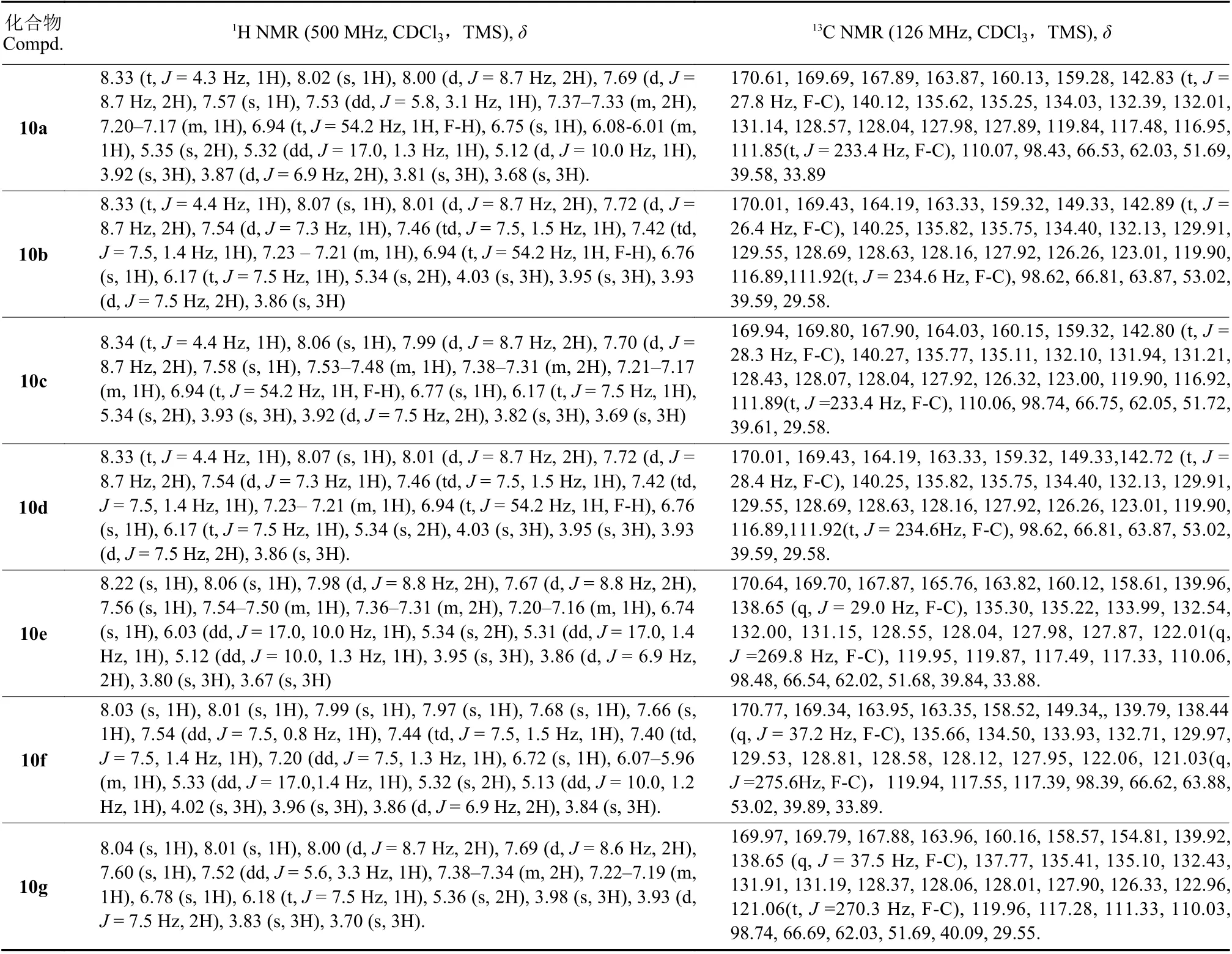
表2 目标化合物10a~10p 的 1H NMR 和 13C NMR 数据Table 2 The 1H NMR and 13C NMR data of compounds 10a-10p

续表2Table 2 (Continued)
在合成中间体7 时,对于SH 和OH 两个基团之间的选择性,根据硫原子和氧原子亲核能力的差异,会与不饱和卤代烃发生选择性取代,通过文献报道[15]和反应条件的探索,最终选择以DMF为溶剂、碳酸钾为缚酸剂,室温搅拌反应,高选择地得到了中间体7,但若反应温度高于60 ℃,则嘧啶4 号位上氧原子与卤代物的副反应产物会明显增加。
2.2 生物活性
生物活性普筛结果发现,所有目标化合物均没有表现出预期的杀菌和杀螨活性,在200 mg/L下其对黄瓜白粉病、黄瓜灰霉病、玉米锈病与水稻纹枯病的抑菌活性均小于50% (数据见附加材料电子版);在500 mg/L 下对朱砂叶螨T. cinnabarinus和苜蓿蚜A. craccivora的杀虫活性均为0。值得注意的是,所有目标化合物对黏虫均表现出一定的杀虫活性,其中10h~10k 和10m~10p 在500 mg/L下的致死率达100 % (表3)。初步构效关系表明:R1为甲基、R2为氟和氯时,对黏虫的杀虫活性较好;R1为三氟甲基和二氟甲基、R2为氢时,杀虫活性有不同程度的减弱;多数情况下,R3为氢的活性高于R3为氯的活性,而Q 为肟醚乙酸酯 (Q2)时的活性高于Q 为甲氧基丙烯酸甲酯 (Q1) 时的活性。

表3 目标化合物10a~10p 在500 mg/L 下对黏虫杀虫活性Table 3 Insecticidal activity of target compound 10a-10p against Mythimna separata at 500 mg/L
近年的研究发现,在嗜球果伞素类化合物中引入不同的结构片段,所得化合物会具有一定的杀虫活性[23-25],如引入苄基腙片段会对黏虫Mythimna separata、桃蚜Myzus persicae、小菜蛾Plutella xylostella和朱砂叶螨Tetranychus cinnabarinus表现出一定的杀虫活性[26],说明了嗜球果伞素类化合物在杀虫活性方面也具有研究价值。本文设计并合成的目标化合物对黏虫具有杀虫活性,可能是由于化合物的分子质量增大使其物理化学性质发生了变化,从而导致其对靶标活性出现差异。
3 结论
本文以含嘧啶硫醚的Strobilurin 类化合物L1为先导,通过活性亚结构拼接,合成了既含有SDHI 类药效片段,又含有先导化合物Strobilurin结构的新化合物,期望发现具有两种作用机制的新的先导或高活性化合物,然而生物活性测定结果表明,目标化合物并未表现出预期的杀菌、杀螨活性,但表现出一定的杀虫活性,其中8 个化合物在500 mg/L 下对黏虫的致死率达100 %,具有进一步研究的价值。
