白藜芦醇调控金属蛋白酶9抑制宫颈癌细胞增殖和迁移的作用及机制*
2021-12-20南文庆范学锋王勤学方彩霞付卫东
南文庆,范学锋,宋 涛,王勤学,方彩霞,付卫东
(甘肃省庆阳市人民医院 1.药剂科,2.肿瘤科,甘肃 745000)
宫颈癌是全世界女性中第四大最常见的恶性肿瘤,也是肿瘤相关死亡的第四大主要原因,仅在2018年就报告了约57万例宫颈癌病例和31万例死亡病例[1]。据估计,全世界宫颈癌死亡的85%左右发生在低收入和中等收入的发展中国家中,包括我国在内,宫颈癌死亡率是发达国家的18 倍[2]。由于诊断和治疗的进步,早期宫颈癌患者的临床结局得到了改善,而晚期和转移性宫颈癌的预后仍然不尽人意[3]。研究报道天然化合物是抗宫颈癌晚期治疗的潜在有效治疗剂[4]。白藜芦醇(resveratrol,RSV)是一种天然的多酚化合物,其在包括宫颈癌在内的多种肿瘤中的抗肿瘤作用逐渐被报道[5-6]。研究显示,RSV 通过抑制HPV E6 蛋白、STAT3 磷酸化、自噬信号通路等抑制宫颈癌的恶性进展,但是RSV在宫颈癌发挥抗肿瘤的具体作用机制未完全明确[6-8]。金属蛋白酶9(a disintegrin and metalloproteinase 9,ADAM9)属于ADAM 家族,该家族与包括血管生成、细胞间相互作用和迁移等多种生物学过程相关[9]。ADAM9在宫颈癌组织中高表达,其高表达与宫颈癌患者预后不良相关[10]。Lin 等[11]报道RSV 通过蛋白—蛋白酶体途径抑制肿瘤细胞中ADAM9蛋白的表达以抑制肺癌和食管癌细胞迁移和生存能力。本研究通过探讨RSV调控ADAM9抑制宫颈癌的恶性进展,获得RSV抗宫颈癌治疗的新分子机制及ADAM9作为RSV潜在抗癌靶点的实验室依据。
1 材料与方法
1.1 主要试剂材料
宫颈癌细胞系HeLa,购自中国科学院细胞库;DMEM细胞培养基和FBS,购自北京清大天一生物技术有限公司;DMSO 和RSV 试剂购自美国sigma公司;细胞计数试剂盒-8(CCK8),购自英国Abcam公司;Transwell小室,购自美国Coring公司;活性氧ROS检测试剂盒,购自上海碧云天生物技术有限公司;ADAM9敲减质粒(sh-ADAM9)和ADAM9过表达质粒(oe-ADAM9),由上海吉凯基因生物技术有限公司构建;高效蛋白裂解液,购自上海贝博生物科技公司;BCA 蛋白浓度检测试剂,购自美国Thermo公司;上样缓冲液,购自上海碧云天试剂有限公司;SDS-PAGE 凝胶配制试剂盒,购自北京索莱宝试剂公司;PVDF膜,购自美国Promega公司;ECL化学发光试剂盒,购自中国大连Meilunbio®飞克特试剂有限公司;ADAM9 和GAPDH 抗体,购自英国Abcam公司。
1.2 细胞培养
将宫颈癌细胞HeLa 培养在含有10% FBS 的DMEM 培养基中,并在5%CO2的37 ℃全湿度培养箱中培养。细胞长满时,弃掉培养基,PBS 洗两次后,加入胰酶消化细胞,终止消化后进行细胞传代。
1.3 CCK8检测RSV对宫颈癌细胞增殖的影响
HeLa 细胞胰酶消化计数后,以每孔1 500 个细胞接种于96 孔板内,设置0 µmol/L、5 µmol/L、10 µmol/L、20 µmol/L、40 µmol/L 和80 µmol/L 浓度RSV 的细胞,每个浓度设置6 个平行复孔。细胞接种10 h后,分别采用相应浓度的RSV处理细胞。药物处理48 h 后,更换100 µL 培养基和20 µL 的CCK8 试剂,混匀后在37 ℃全湿度培养箱中继续培养1 h。采用酶标仪450 nm检测细胞吸光度值(OD值)。细胞增殖抑制率=(1-相应浓度RSV平均细胞OD值/0浓度RSV平均细胞OD值)×100%。
1.4 细胞分组及细胞转染
HeLa 细胞胰酶消化计数后,以每孔2×105个细胞接种于6孔板内,分为DMSO组和RSV组。细胞接种10 h时,采用20µmol/L的RSV处理RSV组,采用相对应体积的DMSO处理DMSO组,放置培养箱中处理48 h。
HeLa 细胞胰酶消化计数后,以每孔2×105个细胞接种于6孔板内,分为RSV组、RSV+NC组、RSV+sh-ADAM9 组和RSV+oe-ADAM9 组。细胞接种10 h后,RSV组采用20µmol/L的RSV处理细胞,RSV+NC 组采用20µmol/L 的RSV 处理细胞并采用脂质体2000 转染无关序列,RSV+sh-ADAM9 组采用20µmol/L的RSV处理细胞并采用脂质体2000转染ADAM9敲减质粒,RSV+oe-ADAM9组采用20µmol/L的RSV处理细胞并采用脂质体2000转染ADAM9过表达质粒。
1.5 Transwell检测细胞迁移能力
各组HeLa 细胞胰酶消化并洗涤细胞两次后,计数,以1×106个细胞重悬至100µL 无血清培养基中,铺在Transwell 小室的上腔室中的聚碳酸酯膜上。600µL 完全培养基(含有10%FBS)放入Transwell 小室的下室中,放至37 ℃全湿度培养箱中培养12 h。将穿过膜的细胞于甲醇溶液中固定10 min,吉姆萨染色30 min。采用显微镜计数细胞穿过的数目。
1.6 Western blotting检测蛋白表达
各组HeLa 细胞胰酶消化并洗涤细胞两次后,加入高效蛋白裂解液。细胞裂解后4 ℃、14 000 r/min 离心30 min,获得蛋白上清液。BCA 蛋白浓度检测试剂检测蛋白的浓度,水煮变性。50µg 等量蛋白加至SDS-PAGE 凝胶中80 V 电泳2 h 后,采用350 mA、1.5 h 将蛋白条带转移至PVDF 膜上。PVDF 膜与8%脱脂牛奶室温孵育1 h,封闭非特异性抗原。TBST 洗3 次后,与ADAM9 一抗稀释液(稀释倍数1∶500)、GAPDH 一抗稀释液(稀释倍数1∶1 000)4 ℃孵育过夜。TBST 洗3 次后,与兔二抗稀释液(稀释倍数1∶10 000)常温孵育1 h,TBST 摇床洗3 次后,采用ECL 化学发光法显示蛋白条带。Image J软件分析蛋白条带灰度值。
1.7 流式细胞仪检测ROS
各组HeLa 细胞弃掉旧培养基后,加入含有10µmol/L DCFH-DA 的无血清培养基放置37 ℃全湿度培养箱中孵育30 min进行探针装载。PBS洗3次后,采用流式细胞仪,在488 nm激发波长,525 nm发射波长,获得样品荧光强度。
1.8 统计学方法
采用SPSS 17.0 软件进行数据分析,计量资料以均数±标准差()表示,两组比较采用t检验,多组比较采用单因素方差分析。以P<0.05为差异有统计学意义。
2 结果
2.1 RSV抑制宫颈癌细胞HeLa增殖
HeLa 细胞经不同浓度的RSV 处理48 h 后,CCK8结果显示RSV呈浓度依赖性抑制宫颈癌细胞HeLa的增殖能力,见图1。
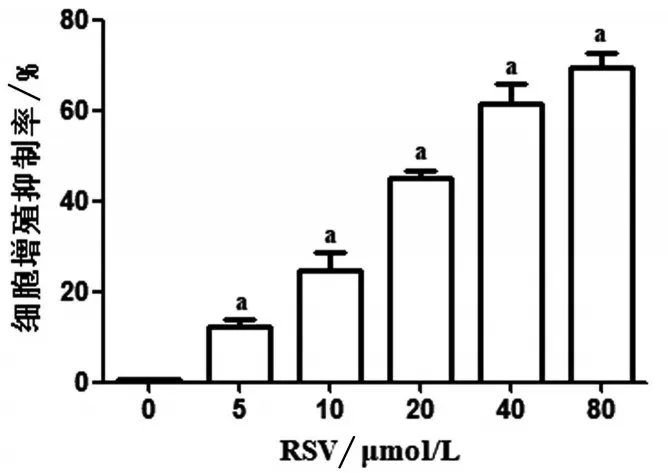
图1 RSV对HeLa细胞增殖能力的影响
2.2 RSV抑制宫颈癌细胞迁移能力
20 µmol/L 的RSV 处理宫颈癌细胞HeLa 48 h后,Transwell 小室实验检测结果显示,DMSO 组穿膜细胞数为(74.33±16.09)个,RSV组穿膜细胞数为(30.67±3.79)个。与DMSO 组比较,RSV 组宫颈癌细胞迁移能力显著降低(t=4.582,P=0.006),见图2。
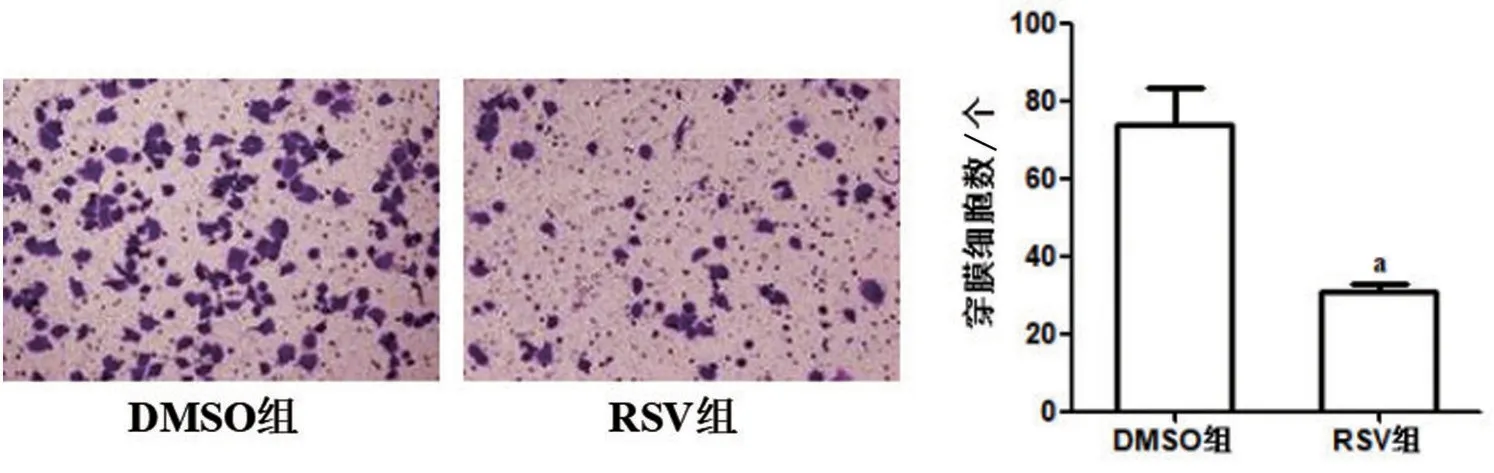
图2 RSV对HeLa细胞迁移能力的影响
2.3 RSV抑制宫颈癌细胞中ADAM9蛋白的表达
20 µmol/L 的RSV 处理宫颈癌细胞HeLa 48 h后,western blotting实验检测结果显示,DMSO组细胞中ADAM9 蛋白的表达为0.98±0.09,RSV 组细胞中ADAM9蛋白的表达为0.13±0.04,与DMSO组相比,RSV 组宫颈癌细胞中ADAM9 蛋白的表达显著降低(t=14.945,P=0.000),见图3。

图3 RSV对HeLa细胞中ADAM9蛋白表达的影响
2.4 RSV抑制宫颈癌细胞中ROS的产生
20 µmol/L 的RSV 处理宫颈癌细胞HeLa 48 h后,流式细胞仪检测结果显示,DMSO 组细胞中ROS相对荧光强度为1.00±0.02,RSV组细胞中ROS相对荧光强度为0.44±0.08,与DMSO 组相比,RSV组宫颈癌细胞中ROS 产生显著降低(t=11.760,P=0.000),见图4。

图4 RSV对HeLa细胞中ROS产生的影响
2.5 RSV 调控ADAM9 基因对宫颈癌细胞增殖能力的影响
与RSV 组和RSV+NC 组比较,RSV+sh-ADAM9 组细胞增殖能力降低,RSV+oe-ADAM9 组细胞增殖能力增加,差异均有统计学意义(P<0.05),见图5。
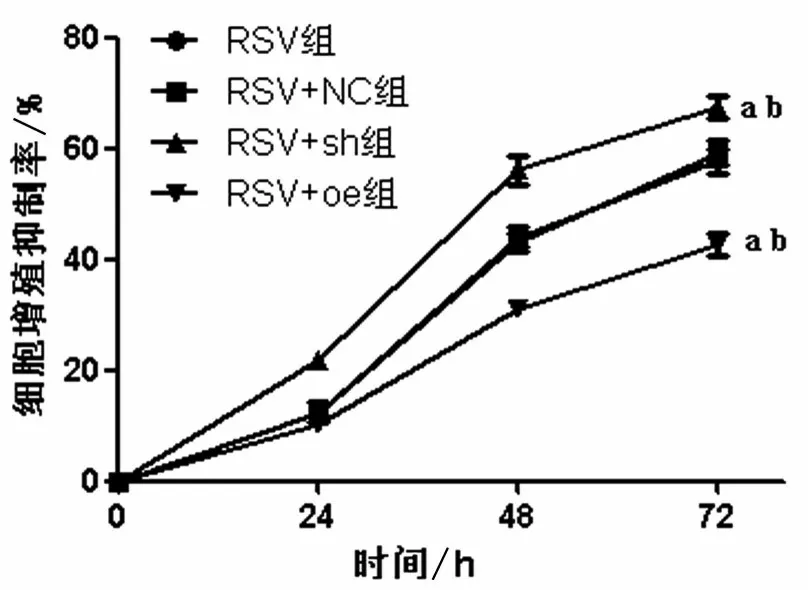
图5 RSV调控ADAM9基因对宫颈癌细胞增殖能力的影响
2.6 RSV 调控ADAM9 基因对宫颈癌细胞迁移能力的影响
RSV 组、RSV+NC 组、RSV+sh-ADAM9 组和RSV+oe-ADAM9组穿膜细胞数分别为55.67±6.28、53.33±7.81、26.33±5.96、80.33±7.04,与RSV 组和RSV+NC组相比,RSV+sh-ADAM9组细胞迁移能力明显降低,RSV+oe-ADAM9 组细胞迁移能力明显升高(均P<0.05),见图6。

图6 Transwell检测RSV调控ADAM9基因对宫颈癌细胞迁移能力的影响
2.7 RSV 调控ADAM9 基因对宫颈癌细胞HeLa ROS的影响
RSV 组、RSV+NC 组、RSV+sh-ADAM9 组和RSV+oe-ADAM9 组ROS 相对荧光强度分别为1.00±0.02、0.98±0.03、0.41±0.05、2.31±0.19,与RSV组 和RSV+NC 组相 比,RSV+sh-ADAM9 组 细 胞ROS 产生明显降低,RSV+oe-ADAM9 组细胞ROS产生明显增加(均P<0.05),见图7。
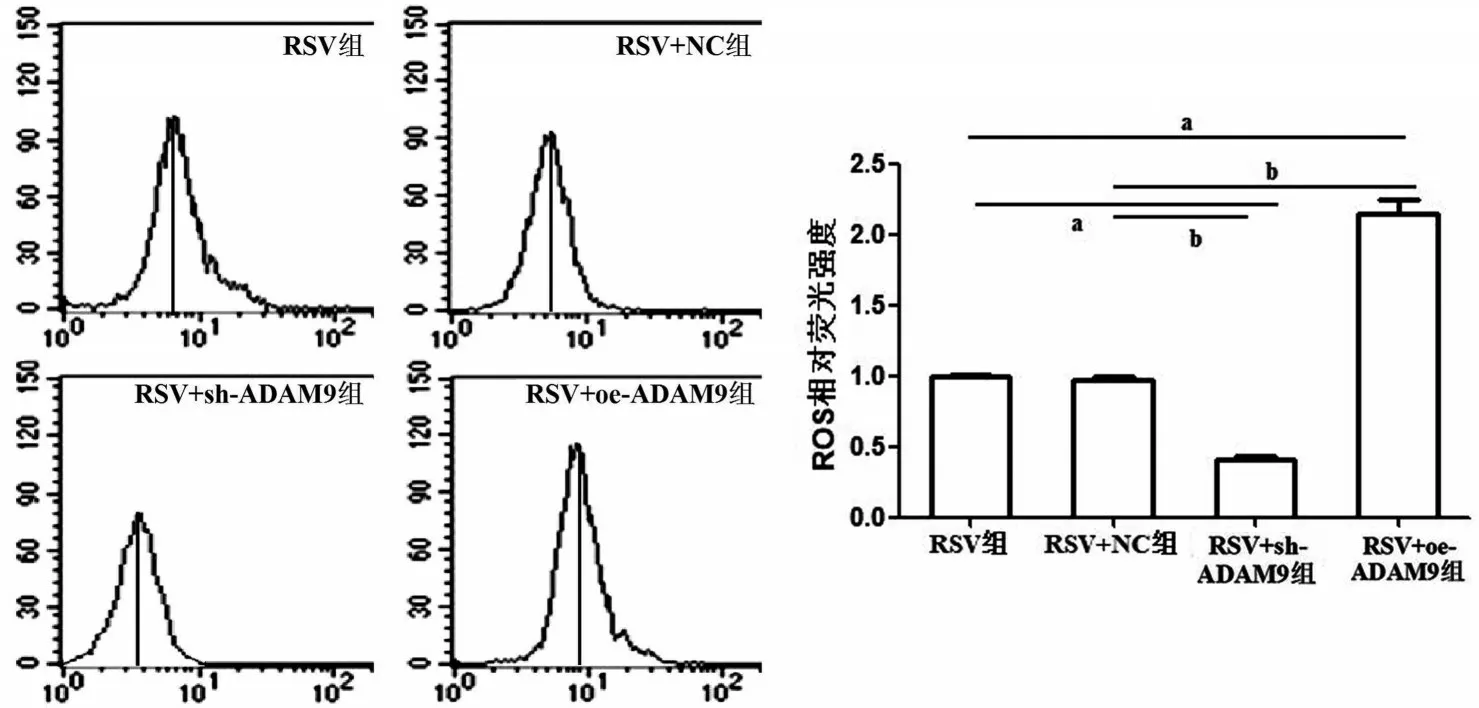
图7 流式细胞仪检测RSV调控ADAM9基因对宫颈癌细胞ROS产生的影响
3 讨论
研究显示,双氢青蒿素、三氧化二砷等为代表的传统中药具有来源广泛、毒副作用较小及疗效显著等优势在抗肿瘤中日益显现,为改善肿瘤患者临床效果和延长患者寿命带来了新希望[4,12]。RSV(3、4、5-三羟基-反式-二苯乙烯)是一种天然的多酚化合物,广泛存在于葡萄、蔓越莓、花生和红酒中,由于其抗氧化剂的特性,RSV具有多种有价值的药理作用,包括抗氧化、抗炎、抗癌、抗菌和心血管保护作用[13]。RSV 的抗肿瘤作用也逐渐被发现,目前RSV 在实体肿瘤和血液系统肿瘤中的抑癌作用均被报道,能显著抑制肿瘤细胞的增殖、侵袭转移、化疗耐药及诱导细胞凋亡等肿瘤生物学过程[5,14]。Sun等[5]研究发现,RSV通过抑制HeLa和Ca Ski细胞中HPV E6 蛋白和视网膜母细胞瘤蛋白诱导细胞凋亡和细胞周期阻滞抑制宫颈癌进展。
本研究通过CCK8 实验和Transwell 实验发现,RSV 显著抑制宫颈癌HeLa 细胞增殖和迁移能力,表明RSV 能抑制宫颈癌的恶性进展,与Sun 等[7]的报道相一致。同时,Sun 等[7]报道RSV 通过调控STAT3 信号通路降低STAT3 磷酸化状态、上皮—间质转化分子标记蛋白质水平和细胞外基质降解酶,以抑制宫颈癌细胞的增殖和转移能力。细胞外基质降解酶通过降解细胞外基质以促使血管生成是肿瘤侵袭和转移的关键步骤之一,研究显示,金属蛋白酶(ADAM)家族是细胞外基质降解酶的重要蛋白,其通过将膜锚定的蛋白质在胞外域脱落的过程中将其胞外域分离,而在细胞增殖、粘附、迁移和侵袭中起关键作用[10]。Lin 等[11]发现RSV 通过抑制ADAM9蛋白的表达在肺癌和食管癌中发挥抗癌作用。
ADAM9 是一种Ⅰ型跨膜蛋白,其结构包含一个用于脱落的金属蛋白酶域和一个用于粘附的双整合蛋白域。ADAM9在多种类型的恶性肿瘤中过表达,增强包括乳腺癌、肺癌和食管癌等细胞的生长、迁移和转移能力,因此ADAM9 是候选癌基因,是抗肿瘤治疗的潜在靶标[15]。在宫颈癌中ADAM9同样被发现高表达,并与患者预后差相关[10]。本研究发现,RSV 能显著抑制宫颈癌细胞中ADAM9 蛋白的表达。为了进一步验证RSV 是通过调控ADAM9抑制宫颈癌细胞的增殖和迁移能力,我们构建ADAM9 过表达和敲减质粒,结果显示,ADAM9 敲减增强了RSV 对宫颈癌细胞增殖和迁移的抑制作用,ADAM9 过表达减弱了RSV 对宫颈癌细胞增殖和迁移的抑制作用,表明ADAM9 能促进宫颈癌细胞增殖和迁移能力,且RSV 通过抑制ADAM9 的表达在宫颈癌中发挥抗癌作用。
ROS是由氧气形成的几种活性物质的总称,是由一些氧分子以单价还原形式产生的。ROS 是重要的信号分子,通过调节血管的结构和功能,影响细胞的蛋白质、脂质和核酸在调节细胞增殖、迁移和分化中发挥重要作用[16]。在胰腺癌中,RSV 抑制ROS 诱导的肿瘤细胞活化、侵袭、迁移和糖酵解[17]。同时,Dong等[18]报道ADAM9通过增加ROS的产生促使白介素6诱导的肝细胞癌细胞迁移和侵袭。本研究结果发现,RSV能显著抑制宫颈癌细胞中ROS的产生,且ADAM9 敲减增强了RSV 对宫颈癌细胞ROS 产生的抑制作用,ADAM9 过表达减弱了RSV对宫颈癌细胞ROS产生的抑制作用,表明RSV通过抑制ADAM9 蛋白的表达减少ROS 的产生进而抑制宫颈癌细胞的恶性进展。
综上所述,RSV显著抑制宫颈癌细胞的增殖和迁移能力,可能是通过抑制ADAM9 蛋白的表达减少ROS 的产生发挥作用。ADAM9 可能是RSV 抗宫颈癌治疗的潜在分子靶点。
