食品中单核细胞增生李斯特氏菌检测分析
2021-12-16王晓英
王晓英
(福建省产品质量检验研究院,福建 福州 350002)
1 引言
李斯特氏菌为革兰氏阳性菌,呈圆尾带状,是一种非芽孢兼性厌氧菌[1],有6个种:单核细胞增生李斯特氏菌(L.monocytogenes,LM)、(绵羊)伊氏李斯特氏菌(L.ivanovii)、斯氏李斯特氏菌(L.seeligeri)、格氏李斯特氏菌(L.grayi)、威氏李斯特氏菌(L.welshimeri)、英诺克李斯特氏菌(L.innocua)[2]。这些菌中,只有单核细胞增生李斯特氏菌能引起人畜共患病[3]。单核细胞增生李斯特氏菌,简称“单增李斯特氏菌”,常见于乳制品、肉类、禽类等食品中,易引起新生儿脑膜炎、孕妇流产、成人败血症等疾病,多发于免疫缺陷患者、妊娠妇女、老人和新生儿[4]。其中孕妇感染比健康成年人高达20倍,2001年,美国将其列为法定上报疾病[5]。国内感染单增李斯特氏菌报告数量呈上升趋势,主要以新生儿和孕妇为主[6]。GB 29921—2013《食品安全国家标准 食品中致病菌限量》规定熟肉制品和即食生肉制品中不得检出单增李斯特氏菌[7],因此,单增李斯特氏菌快速、精准检测显得尤为重要。
本文从单增李斯特氏菌国标检测方法和VITEK 2 Compact 30全自动微生物鉴定系统应用两方面对食品中单增李斯特氏菌检测展开分析,找出检测关键点并提出单增李斯特氏菌快速、精准检测的对策建议。
2 国标检测法分析
2.1 LB1和LB2选择性增菌
LB 1和LB2均为选择性增菌液体培养基,含有萘啶酮酸,广谱抗菌,尤其对革兰氏阴性杆菌的抑制生长能力明显。多数情况下,可疑菌经LB1增菌培养后进行选择性分离即可被检测到,但LB2增菌必不可少,因为样品中如果可疑菌含量低而竞争菌含量高,且可疑菌活力很低,需要通过LB2二次增菌培养以提高单增李斯特氏菌的检出率。
2.2 选择性平板分离
2.2.1 PALCAM琼脂培养基
PALCAM 琼脂除提供必要营养外,七叶苷经李斯特氏菌水解后,与Fe2+反应形成黑色的6,7-二羟基香豆素;氯化锂和其他的抗生素能抑制G-和大多数G+。李斯特氏菌属均可水解七叶苷(表1),在PALCAM琼脂培养基上均为圆形、灰绿色菌落,周围有棕黑色水解圈。因此,当样品中混杂除单增李斯特氏菌以外的李斯特氏菌属菌种时,PALCAM琼脂培养基无法快速筛选出单增李斯特氏菌。
2.2.2 显色培养基
李斯特氏菌显色培养基,均含有一些细菌特异性酶的显色底物,检验人员可根据菌落颜色或是否有乳白色晕环等对可疑菌做出快速筛选,可极大提高单增李斯特氏菌的检出率和准确性。HKListeria和CHROMagar Listeria对单增李斯特氏菌基本无抑制作用,可根据菌落颜色和形态直接对单增李斯特氏菌进行分离筛选。其具有较高灵敏度、特异性和选择性,是非常有效的选择性分离培养基。一般情况下,单增李斯特氏菌在HKListeria呈现蓝绿色菌落,在CHROMagar Listeria有明显的白色晕环(图1)。为避免出现假阳性,检测人员可将可疑菌分离纯化后辅以木糖、鼠李糖试验初步确证。

图1 单增李斯特氏菌显色培养基菌落形态
2.3 木糖、鼠李糖试验
从显色平板上选取可疑菌进行木糖、鼠李糖试验,单增李斯特氏菌木糖阴性、鼠李糖阳性,英诺克李斯特氏菌木糖阴性、鼠李糖反应不定。因此,通常情况下,除英诺克李斯特氏菌外,其它李斯特氏菌均可与单增李斯特氏菌快速区分(表1)。选择木糖阴性、鼠李糖阳性的纯培养物继续进行后续的生化鉴定。
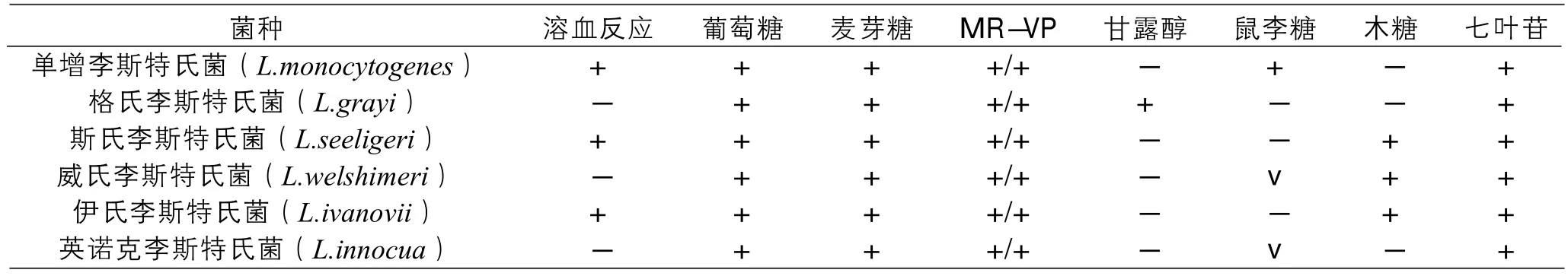
表1 单增李斯特氏菌生化特征与其他李斯特氏菌的区别
3 VITEK 2 Compact 30鉴定分析
目前,VITEK 2 Compact 30已成为食品微生物检验检测可疑菌鉴定的“金标准”,检测人员在可疑菌的鉴定环节普遍采用VITEK 2 Compact 30全自动微生物鉴定系统代替传统生化实验。然而,当前测试卡反应底物下,单增李斯特氏菌和英诺克李斯特氏菌反应类型极为相似,仅PIPLC反应存在差别(表2)。因此,显色培养基上的单增李斯特氏菌可疑菌落经VITEK 2 Compact 30鉴定后,结果有可能被误定为英诺克李斯特氏菌,且可信度达到可接受水平(≥85%),严重影响了检测人员对可疑菌的准确检出。类似情况,国内的多家检测机构在参加检验机构能力验证中均有遇到。笔者咨询仪器售后服务工程师后,认为可能是VITEK 2 Compact 30分析软件版本的影响,也可能是菌株生长状态的差异。

表2 单增李斯特氏菌VITEK 2 COMPACT反应情况
4 检测关键点和对策建议
综上,食品中单增李斯特氏菌检测关键在于区分英诺克李斯特氏菌和单增李斯特氏菌。国标法虽然操作复杂、耗时长,但仍是目前公认的最可靠的方法。为了准确区分英诺克李斯特氏菌和单增李斯特氏菌,本文在传统国标法基础上进行改进(图2)。检测人员可用SN/T 5224—2019《出口食品中单核细胞增生李斯特氏菌检验方法 实时荧光PCR内标法》[8]对LB2增菌液进行快速筛查以初步判断是否含单增李斯特氏菌。显色平板上分离所得可疑菌接种木糖和鼠李糖并进行溶血试验,同时划线TSA-YE平板充分纯化。一般情况下,单增李斯特氏菌在新鲜血平板上具有清晰、狭窄、明亮的溶血圈。选择具有明显溶血的TSA-YE培养纯菌落通过VITEK 2 Compact 30全自动微生物鉴定系统和API Listeria测试卡鉴定。在VITEK 2 Compact 30鉴定结果与显色培养基菌落形态、溶血实验和荧光PCR检测结果均不一致的情况下,以API Listeria测试卡补充鉴定实验结果为最终判断标准。

图2 单核细胞增生李斯特氏菌定性检验程序
5 讨论
单增李斯特氏菌是一种重要的食源性致病菌,广泛分布于自然界中,当人食用污染有单增李斯特氏菌的食物后,极易发病,尤其对新生儿、老年人、孕妇等免疫力低下者。WHO已将单增李斯特氏菌列为四大食源性致病菌之一[9]。国标检测法对样品进行选择性增菌,然后根据显色平板上的特征性菌落分离单增李斯特氏菌,再经过一系列生化试验进行确证,所需设备要求、成本低,但操作性强,对检验人员检测法的掌握程度要求高。笔者认为,在传统国标检测法基础上辅以一些快速检测设备如荧光PCR进行初筛是单增李斯特氏菌检测的有效手段。另外,国标检测法中显色培养基的应用至关重要,国产的有HKListeria,进口的有CHROMagar Listeria,单增李斯特氏菌菌落特征明显,可有效分离出可疑菌。单增李斯特氏菌具有独特的溶血特征,对于显色培养基上的可疑菌落先做溶血实验,综合溶血、木糖、鼠李糖反应结果进行可疑菌落的后续鉴定,可大大增强目标菌选择的准确性。API Listeria测试卡中的DIM孔是梅里埃的专利,用于检测房基酰胺酶,专门用于区分单增李斯特氏菌和英诺克李斯特氏菌,可等同或替代VITEK 2 Compact 30的鉴定结果[10]。再者,表1中所列是李斯特氏菌属典型菌株的生化反应特征,但有些菌株某些反应类型具有差异,如少数单增李斯特菌溶血实验为阴性(ATCC 15313),少数英诺克李斯特菌木糖发酵实验结果为阳性(CICC 10416)等,检验人员不能单纯通过表1或某个生化实验结果来确认或排除某一种李斯特氏菌,需同时采用多种方法进行综合判断。
