公民逝世后器官捐献原位肝移植后早期肝功能不全的危险因素分析
2021-12-14张贯启巫爽齐浩龙
张贯启,巫爽,齐浩龙
(武汉大学人民医院 肝胆外科,湖北 武汉 430060)
目前,肝移植是终末期肝病最有效、最彻底的治疗方案。我国公民逝世后器官捐献(donation after citizens death,DCD)供肝逐步成为供体肝源的重要来源,在一定程度上缓解了供体紧缺的窘况。但是,研究表明,与脑死亡供肝(donation after brain death,DBD)和司法途径来源的供肝相比,DCD肝移植术后早期发生肝功能不全(early allograft dysfunction,EAD)的发生率较高,可能造成受体肝功能损伤[1-2]。因此,本研究通过分析武汉大学人民医院65 例原位肝移植患者的供体、受体及术中相关因素,探讨DCD原位肝移植术后EAD的危险因素,为降低肝移植术后EAD的发生率,提高受体生活及生存质量提供依据。
1 资料与方法
1.1 一般资料
受体资料:选取2017年1月至2019年12月间在我院肝胆外科行原位肝移植的65例患者,其中男45例,女20例,平均年龄为(52.4±11.3)岁。排除一周内死亡、二次肝移植及供受体资料不全患者。术后EAD诊断标准:(1)术后第7 天总胆红素≥171 μmol/L;(2)术后第7 天国际标准化比率≥1.6;(3)术后第7 天内天冬氨酸转氨酶(aspartate aminotransferase,AST)或丙氨酸转氨酶(alanine aminotransferase,ALT)>2 000 U/L,符合以上1 项即诊断为EAD[3]。所有患者或代理人均签署知情同意书,符合医学伦理学要求。
供体资料:按照中国器官捐献分类标准,所有65例DCD供者均为中国二类。65例受体中,男60例,女5例;年龄(40.1±9.6)岁。原发疾病分别为:乙型肝炎后肝硬化15 例,酒精性肝硬化4 例,原发性胆汁性肝硬化1例,爆发性肝衰竭2例,原发性肝癌38例,胆管细胞癌4例,肝豆状核变性1例。
1.2 手术方式和免疫抑制剂应用
采用4 ℃德国克勒HTK溶液灌注腹主动脉、门静脉快速供肝切取法获得供肝,取小部分供肝组织行组织病理学检测及肝脂肪变性分级[4]:其中,S0 20例,肝细胞大泡型脂肪变为0;S1 18例,肝细胞大泡型脂肪变<30%;S2 23例,肝细胞大泡型脂肪变30%~60%;S3 4例,肝细胞大泡型脂肪变>60%。
所有患者均行原位肝移植术,受体手术时采用巴利昔单抗诱导,术中及术后第4天各使用1次(20 mg);术后均采用由他克莫司、吗替麦考酚酯、糖皮质激素组成的三联免疫抑制方案抗术后排斥。术后第3天开始服用他克莫司胶囊,并定期复查他克莫司血药浓度,早期将其血药浓度值控制在8~12 mg/L。
1.3 统计学分析
采用SPSS 17.0统计软件进行数据处理,计量资料以()表示,采用t检验;计数资料采用χ2检验;肝功能不全的影响因素分析采用多因素Logistic回归分析。以P<0.05为差异有统计学意义。
2 结果
2.1 原位肝移植患者术后早期肝功能不全的单因素分析
65 例患者中,有29 例发生EAD,发生率为44.6%。将供体及受体的相关治疗进行单因素分析,供体血清钠水平、热缺血时间、冷缺血时间、住院时间及受体的无肝期时间组间差异有统计学意义(P<0.05),见表1、2。

表1 术后早期肝功能不全的供体相关变量单因素分析

表2 术后早期肝功能不全的受体相关变量单因素分析
2.2 原位肝移植患者术后早期肝功能不全的多因素Logistic回归模型分析
将供体血清钠水平、热缺血时间、冷缺血时间、住院时间及受体的无肝期时间等具有统计学意义的变量进行多因素分析发现,影响术后早期肝功能不全的独立危险因素是供体血清钠水平(OR18.372,95%CI1.846~24.173,P=0.019)及热缺血时间(OR8.105,95%CI1.513~37.205,P=0.013),见表3。
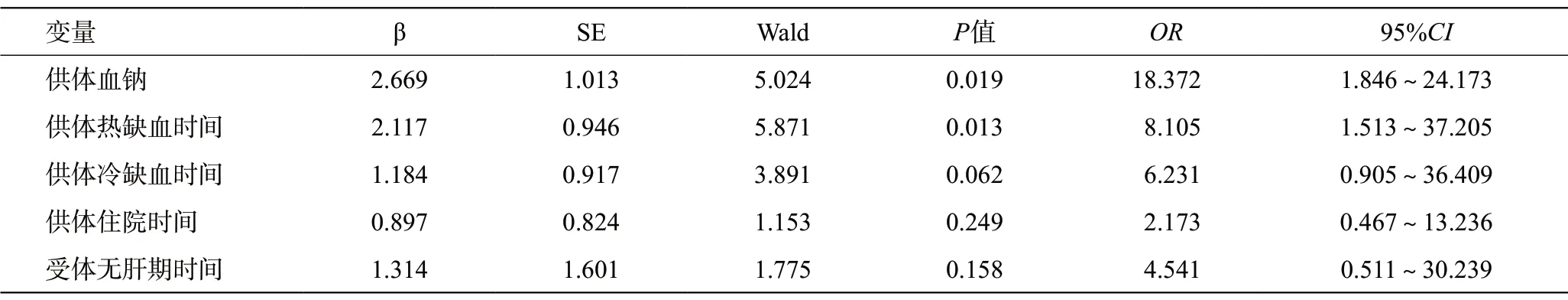
表3 术后早期肝功能不全的多因素Logistic回归分析
3 讨论
自2015年1月1日起,司法途径来源的供肝被明令禁止后,DCD成为肝移植供肝的最为主要获取途径之一。随着肝移植外科技术的不断优化和提高,器官保存液的不断生理化,抗免疫抑制剂的升级换代,特别是EAD的发生被足够重视以来,终末期肝病患者取得比较理想的预后。EAD是供体肝细胞缺血-再灌注损伤的外在表现,是判断肝移植术后肝功能预后的有效影响因素[5]。赵强等[6]研究表明,EAD组术后6个月、12个月、18个月及24个月的受者累积存活率明显低于非EAD组患者。明确EAD发生的危险因素,及早进行预防和干预对提高肝移植患者的长期生存率具有重要的意义。本研究表明,供体血清钠水平及供肝的热缺血时间是EAD发生的独立危险因素。
研究表明,高钠血症不仅能够引起供体肝细胞内呈高渗状态,从而造成肝细胞肿胀、受损,而且肿胀的肝细胞在缺血-再灌注时更容易损伤、死亡,导致移植物功能障碍,甚至无功能。王博等[7]研究表明,与非高钠血症组相比,高钠血症组不仅肝功能明显较差,护肝药物的使用时间长,而且患者的ICU的住院时间明显延长。Saab等[8]研究发现,对于高钠血症供肝患者,可行肠系膜下静脉输注5%葡萄糖液以降低DCD供者血钠水平,降低术后EAD的发生率,而未经5%葡萄糖液输注组移植后肝功能衰竭的发生率为高达60%。本研究也表明,EAD组供体高血清钠水平能够明显高于非EAD组,且是EAD的独立危险因素之一。因此,术前有效地降低供体血钠水平对供体的术后恢复具有重要的意义。
热缺血发生的时间指的是当供者动脉压<50 mmHg(1 mmHg=0.133 kPa)和(或)氧饱和度<70%开始直至进行器官保存液冷灌注结束。缺血-再灌注损伤是不可避免的重要过程,尽可能缩短热缺血时间,可达到与脑死亡器官捐献(donation after brain death,DBD)肝移植相似的存活率,当缺血时间>15 min时,多提示肝移植预后不良[9]。许蜂蜂等[10]研究认为,热缺血时间是EAD发生的独立危险因素,能够准确预测移植术后肝功能状态,当缺血时间>8 min时,EAD的发生率明显增加。曾庆兵等[11]通过首创常温机械灌注系统不中断血流技术完成6 例肝移植手术,对消除肝移植术中热-冷缺血带来肝细胞的损伤具有一定的临床效果。
Lee等[12]研究表明当冷缺血时间超过6 h后,时间每增加1 h,受体术后肝功能衰竭发生率约增加8%。本研究中,受体中EAD组中,冷缺血时间最长的时间超过了10 h,平均时间为(8.32±1.15)h,远远高于非EAD组。术前充分评估患者病情,积极纠正凝血功能异常、低蛋白血症、贫血等不利因素,合理优化手术步骤,最大可能减少冷缺血时间,对降低术后EAD的发生率具有显著的作用。
除此之外,有研究表明当供体ICU住院时间>72 h,ALT>80 U/L以及血管活性药物的使用均是DCD肝移植术后EAD的危险因素[10,13]。我们应予以重视,结合患者自身病情,尽可能地规避危险因素,保障移植后肝脏的功能,提高受体术后的生活质量。
综上所述,DCD肝移植术是涉及到两个个体间庞大、复杂的工程,其中任何一个因素的变化均在一定程度上影响着手术的顺利及患者的预后。本中心研究表明供体血清钠水平及热缺血时间是原位肝移植术后EAD的独立危险因素。随着中国肝移植注册网中心样本量的不断增加,多中心、大样本的研究定会为临床工作提供更能够全面、科学的依据,提前预防、及时干预,将EAD的发生率控制在更低的水平。
