云南哥纳香抗肿瘤化学成分研究
2021-12-13季泓源张建英张新渐左爱学王洪云
季泓源,张建英,王 巧,张新渐,左爱学*,王洪云*
1云南中医药大学中药学院暨云南省南药可持续利用重点实验室,昆明 650500;2保山中医药高等专科学校,保山 678000
番荔枝科哥纳香属(Goniothalamus)植物约160种,分布于亚洲热带、亚热带地区。该属植物在南亚多个国家民间作为风湿、水肿及堕胎药使用[1],在我国南方省区用作镇痛、解毒、杀虫、止痢、抗疟药物使用[2]。哥纳香属植物我国产10种,主要分布在广西,云南,海南,台湾等省区[3]。目前国内外学者已从哥纳香属植物中发现苯乙烯内酯、生物碱、萜类、黄酮、番荔枝内酯等成分,其中番荔枝内酯和苯乙烯内酯为哥纳香属植物的特征成分,具有较强的抗肿瘤活性,被喻为“明日抗癌之星”[4]。
云南哥纳香(G.yunnanensis)为番荔枝科哥纳香属植物,是中国特有品种。生长于海拔350 m的地区,多生长于山地林下,主要分布于中国的云南等地。目前还未见云南哥纳香的化学成分及生物活性的研究报道,为了探索云南哥纳香中生物活性物质,课题组开展了云南哥纳香的化学成分及体外抗肿瘤作用研究,以期为利用我国宝贵的野生植物资源以及抗肿瘤药物的开发提供科学依据。
1 材料与方法
1.1 仪器和试剂
Bruker Avance III 400 MHz、Bruker DRX 500 MHz超导核磁共振仪(德国Bruker公司,四甲基硅烷(TMS)为内标);半制备液相(北京赛普锐思),半制备液相所用试剂为色谱纯;旋转蒸发仪(上海豫康科教仪器设备有限司);SHZ-D(III)循环水式多用真空泵(巩义市予华仪器有限公司);FA2004分析天平(上海舜宇恒平科学仪器有限公司);YRT-3(硅油)熔点仪(天津市精拓仪器科技有限公司)。
硅胶(200~300目)和GF254薄层层析硅胶板(青岛海洋化工有限公司);凝胶SephadexLH-20(瑞典Pharmacia公司);YMC-PackOSD-A半制备色谱柱(250 mm×20 mm,5 μm)为YMC有限责任公司产品;95%乙醇(云南杨林工业开发区汕滇药业有限公司);显色剂:10%硫酸乙醇溶液。层析用试剂甲醇、丙酮、乙酸乙酯、三氯甲烷、二氯甲烷、石油醚等试剂为工业纯或化学纯;乙醇、正丁醇为分析纯;水为纯化水。
1.2 植物
云南哥纳香样品采自云南省金平县,经云南中医药大学中药鉴定教研室杨竹雅副教授鉴定为番荔枝科哥纳香属云南哥纳香(G.yunnanensis)的茎叶,原植物标本(NO.20190407)现存于云南中医药大学中药学院科研实验室。
1.3 实验方法
1.3.1 提取与分离
云南哥纳香茎叶(12 kg)粉碎后以95%乙醇浸提3次,每次浸泡7天,回收溶剂得浸膏658 g。浸膏加适量的水混悬,依次用石油醚、乙酸乙酯萃取,回收各部分溶剂。取乙酸乙酯部位浸膏(400 g),硅胶柱色谱分离,以石油醚-丙酮梯度洗脱,合并相同组分,得到7个组分Fr.1~Fr.7。
Fr.3(44.2 g)部分经硅胶柱层析,用氯仿∶丙酮(10∶1→1∶1,V/V)梯度洗脱,合并成6个部分Fr.3A~Fr.4F。Fr.3D部分经硅胶柱层析,用环己烷-氯仿-丙酮混合溶剂梯度洗脱,重结晶得到化合物1(134 mg)和化合物4(10 mg)。Fr.3E经Sephadex-LH20(氯仿∶甲醇=1∶1,V/V)纯化,得到化合物12(45 mg)。Fr.3F部分经硅胶柱分离,用环己烷∶乙酸乙酯(25∶1→15∶1)体系梯度洗脱,合并薄层色谱相同部分,重结晶得到化合物14(20 mg)和化合物10(144.2 mg)。
Fr.4(14.7 g)部分经硅胶柱层析,用环己烷∶丙酮(30∶1→5∶1,V/V)梯度洗脱,收集洗脱剂,薄层色谱检查,合并色点相同流分得到9个部分Fr.4A~Fr.4I。将Fr.4C部分经ODS半制备色谱柱层析,以甲醇∶水(40%~100%)梯度洗脱,再经硅胶柱色谱,以石油醚∶丙酮(15∶1→10∶1,V/V)体系梯度洗脱,重结晶得到化合物6(17.7 mg)。Fr.4D经Sephadex-LH20(氯仿∶甲醇=1∶1,V/V)纯化,重结晶得到化合物13(26.9 mg)。Fr.4D经ODS半制备色谱(30%~100%甲醇-水)纯化得到化合物5(49.1 mg)和化合物2(10 mg)。
Fr.5(32.4 g)部分经硅胶柱层析,用环己烷∶乙酸乙酯(7∶1→3∶1,V/V)体系梯度洗脱,合并色点相同流分得到3个部分Fr.5A~Fr.5C。Fr.5A经Sephadex-LH20(氯仿∶甲醇=1∶1,V/V)纯化,重结晶得到化合物7(5.6 mg)。Fr.5 B部分经硅胶柱分离,用氯仿∶丙酮(5∶1,V/V)进行洗脱,重结晶得到化合物8(12.6 mg)和19(7.2 mg)。Fr.5C经Sephadex-LH20(氯仿∶甲醇=1∶1,V/V)纯化,重结晶得到化合物9(7.1 mg)和化合物18(24.2 mg)。
Fr.7(22.6g)部分经硅胶柱层析,用氯仿∶甲醇(15∶1→5∶1,V/V)体系梯度洗脱,合并色点相同流分得到4个流分Fr.7A~Fr.7D。Fr.7A经Sephadex-LH20(氯仿∶甲醇=1∶1,V/V)纯化,重结晶得到化合物11(99 mg)。Fr.7B经ODS半制备色谱(60%~100%甲醇-水)纯化得到化合物3(43 mg)和化合物15(24.2 mg)。Fr.7C部分经硅胶柱层析,氯仿∶丙酮(5∶1,V/V)洗脱,纯化得到化合物16(185.2 mg)和化合物17(15.4 mg)。
1.3.2 抗肿瘤活性测试
选取3种常见的肿瘤细胞株,对其中9个单体化合物进行了抗肿瘤活性测试。取对数生长期的三阴性乳腺癌HCC1806、结直肠癌HCT116、宫颈癌Hela细胞,用磺酰罗丹明B蛋白染色法(sulforhodamine B,SRB)进行测试。
根据预实验测定细胞生长速率的结果,调整细胞密度为3×104个/mL,吸取100 μL接种于96孔培养板中,细胞培养过夜后,加入合物,将各化合物以一定浓度梯度(50、25、12.5、6.2、3.125、1.563 μM)生理盐水稀释,按每孔10 μL加入96孔板培养板中,每个浓度3个复孔。5%CO2、37 ℃条件下培养细胞72h后,倒去培养液,用预冷的10%TCA在4 ℃固定细胞1h后用自来水洗涤5次,在空气中自然干燥。然后每孔加入由1%冰醋酸配制的SRB(4mg/mL)溶液60 μL,室温染色20 min,弃染色液,1%酸酸洗涤5次,空气中自然干燥。最后每孔加入非缓冲溶液Tris-base碱液(10 mmol/L,pH=10.5)150 μL溶解,在酶标仪上均匀振荡混匀,以560 nm波长测定吸光度OD值,计算抑制率,公式为抑制率=[1-(对照组OD值-给药组OD值)/对照组OD值]×100%,根据抑制率,计算出IC50。
2 实验结果
2.1 结构鉴定
化合物1黄色粉末;EI-MS:m/z265 [M]+,C16H11NO3;1H NMR(400 MHz,DMSO-d6)δ:10.81(1H,br s,NH),10.30(1H,s,3-OH),9.10(1H,J= 7.5 Hz,H-5),7.91(1H,d,J= 7.3 Hz,H-8),7.60(1H,s,H-2),7.51~7.58(2H,m,H-6,7),7.09(1H,s,H-9),4.01(3H,s,4-OCH3);13C NMR(100 MHz,DMSO-d6)δ:168.5(C=O),122.4(C-1),113.4(C-2),152.2(C-3),148.9(C-4),121.8(C-4a),125.9(C-4b),126.0(C-5),125.3(C-6),127.3(C-7),129.0(C-8),134.9(C-8a),104.0(C-9),135.3(C-10),120.4(C-10a),59.5(4-OCH3)。以上数据与文献[5]对照基本一致,故鉴定该化合物为aristolactam AII,结构见图1。

图1 云南哥纳香中化合物结构Fig.1 Compounds from G.yunnanensis
化合物2黄色粉末;EI-MS:m/z295 [M]+,C17H13NO4;1H NMR(400 MHz,DMSO-d6)δ:10.79(1H,s,NH),10.12(1H,s,3-OH),8.61(1H,d,J= 8.2 Hz,H-5),7.83(1H,s,H-9),7.40(1H,s,H-2),7.32(1H,t,J= 7.9 Hz,H-6),7.04(1H,d,J= 5.1 Hz,H-7),4.03(3H,s,4-OCH3),3.99(3H,s,8-OCH3);13C NMR(100 MHz,DMSO-d6)δ:168.4(C=O),125.8(C-1),109.9(C-2),154.2(C-3),150.6(C-4),124.0(C-4a),118.0(C-5a),121.6(C-5),123.3(C-6),112.2(C-7),153.8(C-8),127.1(C-8a),98.7(C-9),133.9(C-10),120.2(C-10a),59.9(4-OCH3),57.2(8-OCH3);以上数据与文献[6]对照基本一致,故鉴定该化合物为enterocarpam II。
化合物3黄色粉末;ESI-MS:m/z282 [M+H]+,C16H11NO4;1H NMR(400 MHz,DMSO-d6)δ:10.67(1H,s,NH),10.22(1H,s,OH-3),9.75(1H,s,OH-6),8.55(1H,d,J= 2.4 Hz,H-5),7.74(1H,d,J= 8.6 Hz,H-8),7.59(1H,s,H-2),7.07(1H,dd,J= 8.5,2.4 Hz,H-7),6.99(1H,s,H-9),3.98(3H,s,4-OCH3);13C NMR(100 MHz,DMSO-d6)δ:168.3(C=O),122.6(C-1),119.6(C-2),155.2(C-3),151.3(C-4),111.7(C-4a),127.3(C-4b),116.9(C-5),157.7(C-6),121.8(C-7),120.1(C-8),127.6(C-8a),104.2(C-9),132.5(C-10),113.2(C-10a),59.5(4-OCH3)。以上数据与文献[7]对照基本一致,故鉴定该化合物为aristolactam AIIIa。
化合物4黄色粉末;ESI-MS:m/z280 [M+H]+,C17H13NO3;1H NMR(400 MHz,CDCl3)δ:10.82(1H,s,NH),9.14(1H,d,J= 8.2,1.7 Hz,H-5),7.92(1H,dd,J= 7.9,1.9 Hz,H-8),7.63(1H,s,H-2),7.62(1H,s,H-9),7.51~7.58(2H,m,H-6,7),4.01(3H,s,4-OCH3),3.87(3H,s,3-OCH3);13C NMR(100 MHz,CDCl3)δ:170.4(C=O),125.9(C-1),109.6(C-2),154.4(C-3),151.9(C-4),124.2(C-4a),127.0(C-4b),127.7(C-5),126.9(C-6),128.8(C-7),129.0(C-8),133.6(C-8a),106.3(C-9),134.8(C-10),122.5(C-10a),60.3(4-OCH3),57.1(3-OCH3)。以上数据与文献[8]对照基本一致,故鉴定该化合物为aristolactam BII。
化合物5淡黄色粉末;EI-MS:m/z295 [M]+,C17H13NO4;1H NMR(400 MHz,DMSO-d6)δ:10.63(1H,s,NH),10.62(1H,s,4-OH),8.88(1H,d,J= 8.5 Hz,H-5),7.72(1H,s,H-2),7.48(1H,t,J= 7.8 Hz,H-6),7.42(1H,s,H-9),7.16(1H,d,J= 8.0 Hz,H-7),4.03(3H,s,8-OCH3),3.98(3H,s,3-OCH3);13C NMR(100 MHz,DMSO-d6)δ:168.4(C=O),125.1(C-1),107.4(C-2),155.1(C-3),149.6(C-4),124.1(C-4a),115.8(C-4b),120.3(C-5),124.1(C-6),114.4(C-7),155.1(C-8),127.5(C-8a),97.7(C-9),134.7(C-10),120.3(C-10a),57.2(3-OCH3),55.8(8-OCH3)。以上数据与文献[9]对照基本一致,故鉴定该化合物为griffithinam。
化合物6黄色粉末;EI-MS:m/z295 [M]+,C17H13NO4;1H NMR(400 MHz,DMSO-d6)δ:10.10(1H,s,NH),8.23(1H,d,J= 8.0 Hz,H-5),7.58(1H,dd,J= 8.2,2.1 Hz,H-7),7.50(1H,m,H-6),7.20(1H,s,H-9),4.50(3H,s,2-OCH3),4.02(3H,s,5-OCH3);13C NMR(100 MHz,DMSO-d6)δ:168.6(C=O),125.6(C-1),105.6(C-1),154.3(C-2),141.1(C-3),156.1(C-4),113.5(C-4a),128.9(C-4b),126.5(C-5),125.9(C-7),128.8(C-8),125.4(C-8a),105.3(C-9),133.4(C-10),125.1(C-10a),61.4(2-OCH3),60.8(5-OCH3)。以上数据与文献[10]对照基本一致,故鉴定该化合物为胡椒内酰胺B。
化合物7黄色针晶体;EI-MS:m/z291 [M]+,C18H13NO3;1H NMR(400 MHz,CDCl3)δ:9.20(1H,m,H-11),8.92(1H,d,J= 5.3 Hz,H-5),8.60(1H,m,H-8),7.82(1H,d,J= 5.3 Hz,H-4),7.78(1H,m,H-9),7.60(1H,m,H-10),7.24(1H,s,H-3),4.13(3H,s,1-OCH3),4.05(3H,s,2-OCH3);13C NMR(100 MHz,CDCl3)δ:145.1(C-1),119.8(C-1a),121.8(C-3b),152.5(C-2),106.7(C-3),135.9(C-3a),122.3(C-4),144.6(C-5),157.2(C-6a),182.9(C-7),132.0(C-7a),128.8(C-8),128.7(C-9),134.7(C-10),129.0(C-11),124.2(C-11a),60.8(1-OCH3),56.3(2-OCH3)。以上数据与文献对照[11]基本一致,故鉴定该化合物为观音莲明碱。
化合物8白色粉末;ESI-MS:m/z282 [M-H]-,C17H17NO3;1H NMR(400 MHz,DMSO-d6)δ:7.37(2H,d,J= 8.4 Hz,H-2,6),7.28(1H,d,J= 16.0 Hz,H-7),7.00(2H,d,J= 8.4 Hz,H-2′,6′),6.70(2H,d,J= 8.4 Hz,H-3′,5′),6.38(2H,d,J= 8.4 Hz,H-3,5),6.36(1H,d,J= 16.0 Hz,H-8),3.30(2H,dd,J= 6.5,6.8 Hz,H-8′),2.63(2H,t,J= 7.2 Hz,H-7′);13C NMR(100 MHz,DMSO-d6)δ:130.0(C-1),129.2(C-2,C-6),115.8(C-3,C-5),157.7(C-4),139.6(C-7),118.7(C-8),165.3(C-9),129.6(C-1′),129.5(C-2′,6′),115.1(C-3′,5′),155.7(C-4′),34.5(C-7′),40.7(C-8′)。以上数据与文献对照[12]基本一致,故鉴定该化合物为N-对香豆酰酪胺。
化合物9黄色粉末;EI-MS:m/z283 [M]+,C16H13NO4;1H NMR(400 MHz,DMSO-d6)δ:8.24(1H,dd,J= 7.6,0.8 Hz,H-8),8.07(1H,dd,J= 7.6,0.8 Hz,H-5),7.87(1H,ddd,J= 7.6,7.6,1.2 Hz,H-7),7.73(1H,ddd,J= 7.6,7.6,1.2 Hz,H-6),4.01(1H,s,3-OCH3),3.96(1H,s,N-CH3);13C NMR(100 MHz,DMSO-d6)δ:157.8(C-2),149.4(C-3),135.5(C-4),118.7(C-4a),126.2(C-5),133.7(C-6),134.2(C-7),125.7(C-8),132.2(C-8a),182.5(C-9),140.5(C-9a),179.9(C-10),132.0(C-10a),59.1(3-OCH3),34.7(N-CH3),13.96(CH3-4)。以上数据与文献[13]对照基本一致,故鉴定该化合物为marcanine B。
化合物10白色块状结晶;ESI-MS:m/z257 [M+Na]+,C13H14O4;1H NMR(400 MHz,DMSO-d6)δ:7.20~7.57(5H,m,Ph),5.02(1H,br s,H-7),4.87(1H,m,H-1),2.98(1H,d,J= 19.5 Hz,H-4b),4.54(1H,m,H-5),4.24(1H,m,H-8),2.86(1H,dd,J= 19.5,5.2 Hz,H-4a),1.86(1H,dd,J= 14.0,3.9 Hz,H-9a),2.81(1H,m,H-9b),1.82(1H,d,J= 3.9 Hz,OH-8);13C NMR(100 MHz,DMSO-d6)δ:76.0(C-1),169.7(C-3),36.9(C-4),66.8(C-5),71.8(C-7),68.4(C-8),24.4(C-9),137.9(C-1′),127.5(C-2′,6′),128.2(C-3′,5′),127.6(C-4′)。以上数据与文[14]对照基本一致,故鉴定该化合物为9-deoxygoniopypyrone。
化合物11白色块状结晶;ESI-MS:m/z251 [M+H]+,C13H15O5;1H NMR(400 MHz,DMSO-d6)δ:7.23~7.46(5H,m,Ph),4.99(1H,dd,J= 4.8,2.7 Hz,H-7),4.91(1H,d,J= 4.8 Hz,H-8),4.90(1H,m,H-4),4.46(1H,m,H-6),4.01(1H,m,H-5),3.99(1H,d,J= 2.7 Hz,OH-6),2.78(1H,dd,J= 18.5,6.2 Hz,H-3a),2.70(1H,m,H-3b);13C NMR(100 MHz,DMSO-d6)δ:176.2(C-2),36.5(C-3),78.0(C-4),88.9(C-5),74.8(C-6),88.5(C-7),72.3(C-8),143.5(C-1′),127.7(C-2′,6′),128.2(C-3′,5′),128.8(C-4′)。以上数据与文献[14]对照基本一致,故鉴定该化合物为goniofufurone。
化合物12无色块状结晶;EI-MS:m/z200 [M]+,C13H12O2;1H NMR(400 MHz,CDCl3)δ:7.15~7.55(5H,m,Ph),7.06(m,1H,H-4),6.77(1H,d,J= 15.7 Hz,H-8),6.42(1H,dd,J= 15.7,6.6 Hz,H-7),6.92(1H,m,H-1),6.20(1H,m,H-3),5.03(1H,m,H-6),2.36(2H,m,H-5);13C NMR(100 MHz,CDCl3)δ:164.21(C-2),123.3(C-3),145.9(C-4),30.27(C-5),78.2(C-6),127.0(C-7),131.4(C-8),135.7(C-9),129.1(C-10,14),127.2(C-11,13),128.6(C-12)。以上数据与文献对照[15]基本一致,故鉴定该化合物为goniothalamin。
化合物13黄色粉末;ESI-MS:m/z257 [M+H]+,C15H14O4;1H NMR(400 MHz CDCl3)δ:12.10(1H,s,OH-5),10.80(1H,s,OH-7),7.36~7.52(5H,m,Ph),5.91(1H,d,J= 2.0 Hz,H-8),5.55(1H,d,J= 2.0 Hz,H-6),5.58(1H,dd,J= 12.6,2.8 Hz,H-2),3.25(1H,dd,J= 17.1,12.6 Hz,H-3a),2.78(1H,dd,J= 17.1,3.1 Hz,H-3b);13C NMR(100MHz,CDCl3)δ:79.9(C-2),43.5(C-3),193.8(C-4),163.1(C-5),95.2(C-6),166.9(C-7),96.5(C-8),162.5(C-9),100.1(C-10),138.7(C-1′),127.3(C-2′,6′),129.4(C-3′,5′),127.5(C-4′)。以上数据与文献[16]对照基本一致,故鉴定该化合物为pinocembrin。
化合物14白色片状晶体;EI-MS:m/z414 [M]+,C29H50O;1H NMR(400 MHz,DMSO-d6)δ:5.32(1H,d,J= 5.0 Hz,H-6),3.50(1H,m,H-3),0.92(3H,s,H-19),0.88(3H,d,J= 6.6 Hz,H-21),0.80(3H,t,J= 7.5 Hz,H-29),0.76(3H,d,J= 6.8 Hz,H-27),0.75(3H,d,J= 6.8 Hz,H-26),0.61(3H,s,H-18);13C NMR(100 MHz,DMSO-d6)δ:37.3(C-1),31.5(C-2),71.5(C-3),42.2(C-4),140.6(C-5),121.5(C-6),32.6(C-7),32.6(C-8),50.5(C-9),36.8(C-10),21.0(C-11),39.7(C-12),42.8(C-13),56.6(C-14),24.4(C-15),28.0(C-16),56.2(C-17),12.6(C-18),19.0(C-19),36.3(C-20),18.7(C-21),33.5(C-22),26.9(C-23),44.7(C-24),29.2(C-25),18.7(C-26),19.2(C-27),23.8(C-28),11.9(C-29)。以上数据与文献[17]对照基本一致,故鉴定该化合物为β-谷甾醇。
化合物15白色粉末;ESI-MS:m/z575 [M-H]-,C35H60O6;1H NMR(400 MHz,DMSO-d6)δ:5.39(1H,m,H-5),5.08(1H,d,J= 7.7 Hz,H-1′),4.61(1H,dd,J= 11.7,2.5 Hz,H-6),4.42(1H,dd,J= 11.7,5.5 Hz,H-6′),2.24~2.38(2H,m,H-3′,4′),4.07(1H,dd,J= 8.0 Hz,H-2′),3.94~3.98(2H,m,H-3,5′),2.24~2.38(1H,m,H-4),1.02(3H,d,J= 6.2 Hz,H-21),0.96(3H,s,H-19),0.91(3H,m,H-29),0.88(6H,d,J= 6.8 Hz,H-26,27),0.65(3H,s,H-18);13C NMR(100 MHz,DMSO-d6)δ:37.8(C-1),30.2(C-2),78.1(C-3),39.3(C-4),140.6(C-5),121.6(C-6),32.1(C-7,C-8),50.6(C-9),36.2(C-10),21.3(C-11),19.8(C-12),41.4(C-13),56.8(C-14),24.3(C-15),28.5(C-16),56.0(C-17),12.3(C-18),19.1(C-19),36.7(C-20),19.0(C-21),34.0(C-22),26.2(C-23),46.0(C-24),29.3(C-25),19.2(C-26),20.1(C-27),23.4(C-28),12.2(C-29),102.5(C-1′),75.2(C-2′),78.2(C-3′),71.5(C-4′),78.3(C-5′),62.6(C-6′)。以上数据与文献[18]对照基本一致,故鉴定该化合物为胡萝卜苷。
化合物16白色针晶;EI-MS:m/z154 [M]+,C4H10O2S2;1H NMR(400 MHz,DMSO-d6)δ:3.26(4H,q,J= 7.2 Hz,H-2,2′),1.26(6H,t,J= 7.2 Hz,H-1,1′);13C NMR(100 MHz,DMSO-d6)δ:8.3(C-1,1′),46.6(C-2,2′)。以上数据与文献[19]报道相一致,故将其鉴定为diethyl disulfoxide。
化合物17白色无定形粉末;ESI-MS:m/z597 [M+Na]+,C35H58O6;1H NMR(400 MHz,C5D5N)δ:5.24(1H,s,H-6),5.14(2H,m,H-23),5.06(1H,m,H-22),4.56(1H,d,J= 8.0 Hz,H-1′),4.31(1H,m,H-3),4.27(1H,m,H-6′),3.97(1H,t,H-4′,5′),3.93(1H,m,H-3′),2.74(1H,m,H-2′),0.94(3H,s,H-19),0.92(3H,s,H-27),0.90(3H,s,H-21),0.86(3H,t,J= 6.5 Hz,H-29),0.65(3H,s,H-26);13C NMR(100 MHz,C5D5N)δ:37.9(C-1),30.6(C-2),78.5(C-3),39.7(C-4),141.3(C-5),123.3(C-6),32.5(C-7),32.4(C-8),50.0(C-9),37.3(C-10),21.6(C-11),38.4(C-12),42.7(C-13),57.3(C-14),24.9(C-15),28.9(C-16),56.5(C-17),40.8(C-18),19.8(C-19),21.1(C-20),21.8(C-21),139.1(C-22),129.9(C-23),50.7(C-24),29.6(C-25),19.5(C-26),21.3(C-27),26.0(C-28),12.5(C-29),102.9(C-1′),75.7(C-2′),78.8(C-3′),72.2(C-4′),79.0(C-5′),63.2(C-6′)。以上数据与文献[20]报道相一致,故将其鉴定为豆甾醇-3-O-β-D-吡喃葡萄糖苷。
化合物18黄色针晶;EI-MS:m/z231 [M]+,C12H9NO4;1H NMR(400 MHz,DMSO-d6)δ:11.28(1H,s,OH-7),10.55(1H,s,NH-10),8.84(1H,s,NH-10),7.80(1H,t,J= 8.2 Hz,H-5),7.56(1H,dd,J= 8.4,0.9 Hz,H-4),7.25(1H,dd,J= 8.4,0.9 Hz,H-6),2.55(3H,s,H-12);13C NMR(100 MHz,DMSO-d6)δ:184.7(C-1),152.8(C-2),180.7(C-3),119.7(C-4),139.0(C-5),122.1(C-6),161.7(C-7),114.0(C-8),133.7(C-9),109.1(C-10),202.3(C-11),33.0(C-12)。以上数据与文献[21]报道相一致,故将其鉴定为景洪哥纳香胺。
化合物19白色粉末;ESI-MS:m/z455 [M(H](,C30H48O3;1H NMR(400 MHz,CDCl3)δ:5.52(1H,t,J= 2.3 Hz,H-12),3.46(1H,dd,J= 10.2,5.7 Hz,H-3),2.68(1H,d,J= 11.3 Hz,H-18),1.24(3H,s,H-27),1.22(3H,s,H-25),1.05(3H,s,H-24),1.02(3H,s,H-23),0.99(3H,d,J= 6.3 Hz,H-30),0.98(3H,d,J= 5.7 Hz,H-29),0.88(3H,s,H-26);13C NMR(100 MHz,CDCl3)δ:38.8(C-1),27.0(C-2),79.0(C-3),38.8(C-4),55.3(C-5),18.4(C-6),33.1(C-7),39.6(C-8),47.7(C-9),37.8(C-10),23.4(C-11),125.6(C-12),138.3(C-13),42.2(C-14),28.1(C-15),24.3(C-16),47.9(C-17),52.9(C-18),39.0(C-19),39.0(C-20),30.8(C-21),36.9(C-22),27.0(C-23),15.6(C-24),15.5(C-25),16.2(C-26),23.0(C-27),180.7(C-28),17.0(C-29),21.2(C-30)。以上数据与文献[22]报道相一致,故将其鉴定为乌苏酸。
2.2 抗肿瘤活性
以顺铂为阳性对照,用SRB法对从云南哥纳香种分离得到的9个化合物进行体外抗肿瘤活性筛选,结果见表1~3。结果表明化合物7、12、13在50 μM浓度下,对HCC1806、HCT116、Hela肿瘤细胞的增殖具有一定的抑制作用,其中苯乙烯内酯类化合物12的抑制作用表现最明显,对HCC1806、HCT116、Hela肿瘤细胞株活性IC50分别为5.2±0.7、3.1±0.5和10.5±1.0 μM(见表4)。

表1 9个化合物对HCC1806肿瘤增殖抑制活性Table 1 Inhibitory activity of nine compounds on HCC1806 tumor proliferation
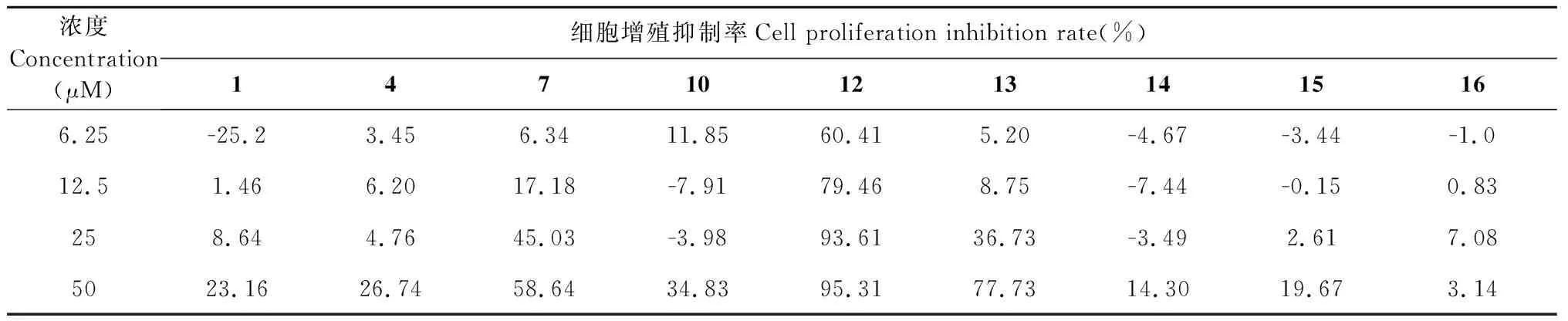
续表1(Continued Tab.1)

表2 9个化合物对HCT116肿瘤增殖抑制活性Table 2 Inhibitory activity of nine compounds on HCT116 tumor proliferation

表3 9个化合物对Hela肿瘤增殖抑制活性Table 3 Inhibitory activities of nine compounds on Hela tumor proliferation
3 结论
本实验对云南哥纳香乙醇提取物的化学成分及其体外抗肿瘤活性进行了研究,从中分离鉴定了19个化合物,化合物的主要类型包括生物碱类(1~9、18)、苯乙烯内酯(10~12)、黄酮(13)、三萜类(19),所有化合物均为首次从该植物中分离得到,并采用SRB法对其中9个化合物进行了人肿瘤细胞株HCC1806、HCT116、Hela的细胞毒活性测试。结果表明:化合物7和12对3种人肿瘤细胞株均显示较为明显的细胞毒活性,苯乙烯内酯化合物12对3种人肿瘤细胞毒活性优于阿朴菲型生物碱类化合物7和黄烷类化合物13。并且首次发现化合物12对HCC1806和HCT116两株癌细胞的增殖具有较明显的抑制作用,IC50分别为5.2±0.7和3.1±0.5 μM。
苯乙烯内酯类化合物是番荔枝科哥纳香属植物的特征成分,在哥纳香属植物中广泛存在。Goniothalamin是由Hlubucek和Robertson首次从Cryptocaryacaloneura树皮中分离得到的苯乙烯内酯类化合物,也是哥纳香属植物中分离出的第一个苯乙烯型内酯类化合物[23]。Goniothalamin最早是以一种胚胎毒性化合物被发现,但后面的研究发现该化合物具有良好的抗肿瘤活性和细胞毒作用,对胃癌(HGC-27)、乳腺癌(MCF-7、T47D、MDA-MB-231)、白血病(HL-60)、卵巢癌(Caov-3)等多种癌细胞具有显著的抑制增殖作用[24],并且,对荷有埃利希氏肿瘤的小鼠给药goniothalamin后,未观察到毒性证据,表明goniothalamin具有良好的生物相容性,即在抑制肿瘤生长的同时没有副作用[25];Goniothalamin主要通过氧化应激反应和caspases激活介导调节癌细胞周期和诱导癌细胞凋亡[26]。本文也首次发现化合物goniothalamin(12)对HCC1806和HCT116癌细胞株的增殖具有较明显的抑制作用,为抗肿瘤药物的设计和开发提供一定的实验依据。
综上,本研究首次开展了云南哥纳香化学成分和抗肿瘤活性研究,初步阐明了云南哥纳香的抗肿瘤活性药效物质基础,为云南哥纳香在抗肿瘤方面的开发利用提供了一定的实验依据。
