腹壁子宫内膜异位症47例临床特点分析
2021-12-02马兰芳曹莉莉吴章颖汪俊涛
马兰芳, 曹莉莉, 吴章颖, 汪俊涛
子宫内膜异位症(endometriosis,EMs)好发于育龄期女性,是一种较常见的慢性妇科疾病,发病率约为11%[1]。EMs病理特点表现为子宫内膜(腺体及间质)生长于子宫腔以外的部位,其发病机制尚不清楚。异位内膜可累及全身任何部位,包括膀胱、肾、输尿管、脐、肺、乳腺、胸膜,甚至大腿及手臂等,但大部分位于盆腔内,以卵巢和宫骶韧带最常见,其次为子宫[2]。腹壁子宫内膜异位症(abdominal wall endometriosis,AWE)是一种特殊类型的盆腔外子宫内膜异位症,是指EMs发生于腹膜表面,多数继发于妇产科手术,如剖宫产术[3-4]。其发病机制不明,多偏向种植学说,即手术过程中将子宫内膜种植于腹壁切口,内膜组织在激素作用下增生,促使周围筋膜组织化生为腺瘤样病灶。近年来随着剖宫产率的升高,AWE的发病率也呈上升趋势,发病率为0.03%~0.45%[5-6]。本研究回顾性分析我院47例AWE患者的临床资料,总结其临床特点、诊治方法、预后因素及术后管理,为有效预防AWE的发生以及AWE的临床管理提供参考。
1 资料与方法
1.1一般资料 收集2015年1月至2020年12月贵阳市妇幼保健院妇科病区收治的47例AWE患者的临床资料。纳入标准[7]:既往有腹部手术史,腹壁切口处可触及结节或包块,肿块出现周期性疼痛或触痛,与月经周期相关(经前期或经期加重,月经干净后好转);超声检查提示腹壁切口处低回声结节,怀疑子宫内膜异位结节;经手术病理证实为AWE;病历资料及随访资料完整。排除有严重心、肺、肝或肾脏疾病及炎症活动期患者。
1.2资料收集 通过医院电子病历系统查阅患者住院病历,收集患者年龄、月经史、孕产史、既往手术史、症状与体征、发病位置与原切口关系、辅助检查结果、手术麻醉方式、术中探查包块大小、病灶侵犯深度、术中出血量、手术时间、术后补充治疗等临床资料及随访资料。
2 结果
2.147例AWE患者的一般情况 患者年龄20~43(32.17±4.45)岁,以30~34岁占比最高(46.81%)。均有剖宫产手术史,患者初次发病距离上次剖宫产手术时间为2~120个月,中位时间为27.00个月。剖宫产1次者占比最高,达68.09%。腹部手术切口以横形占比最高,达91.49%。见表1。
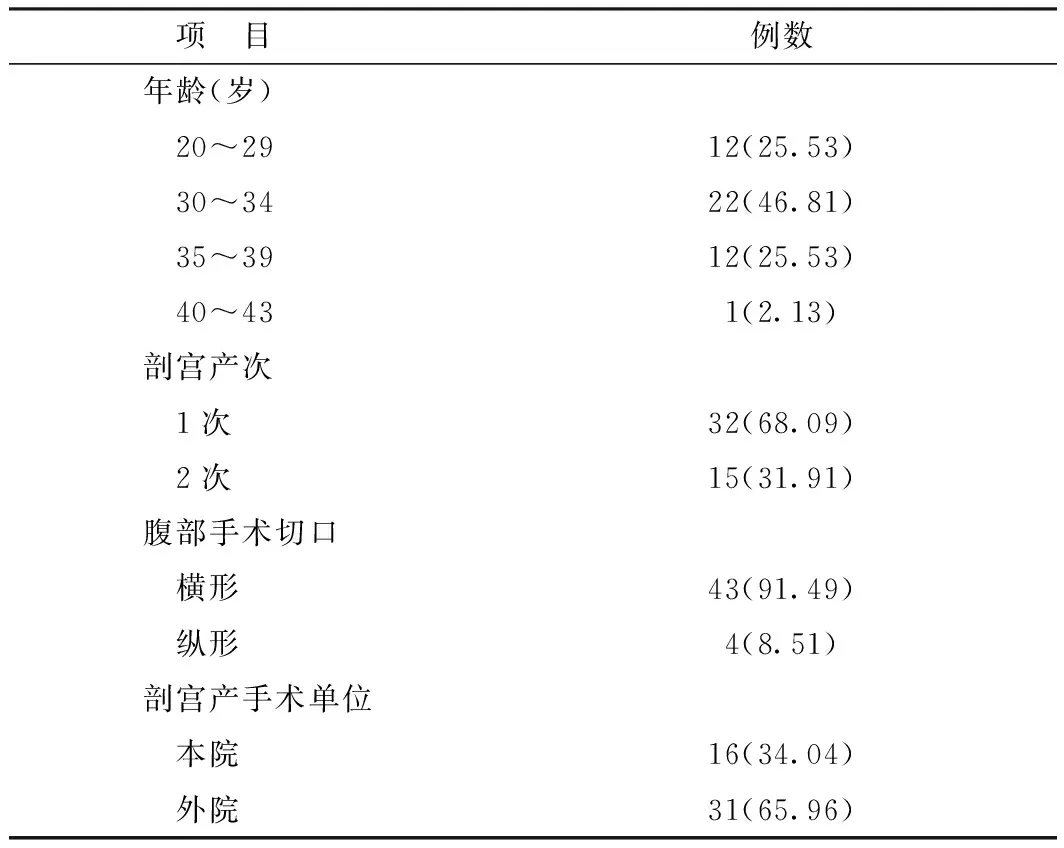
表1 47例AWE患者的一般情况[n(%)]
2.247例AWE患者的症状及体征情况 1例(2.13%)无临床症状及体征,于经腹子宫肌瘤剔除术中意外发现,关腹过程中腹直肌前鞘瘢痕处扪及一3 cm×2.5 cm×2.5 cm包块,有咖啡色液体流出,术后证实为AWE。37例(78.72%)以经期腹壁包块疼痛为首发症状,其中有2例同时出现瘢痕处伴随月经的周期性出血。9例(19.15%)查体于腹壁瘢痕处触及结节,活动欠佳,与周围组织分界不清。包块于剖宫产手术横切口以右侧多见,4例纵形切口均见于切口下部。见表2。

表2 47例AWE患者的症状及体征情况[n(%)]
2.347例AWE患者辅助检查结果 47例AWE患者均行腹壁B超检查,其中5例(10.64%)未探及病灶,42例(89.36%)提示腹壁切口处不规则的低回声肿块,边界不清,部分包块内可见血流信号;其中41例为单发,1例为多发。47例AWE患者中有29例行CA125检测,结果显示为9.0~56.8(23.52±12.81)U/ml。
2.447例AWE患者治疗情况 47例患者均行手术切除病灶,采取全身麻醉41例(87.23%),硬膜外麻醉4例(8.51%),局部麻醉2例(4.26%)。其中1例进入盆腔并发现卵巢子宫内膜异位囊肿,行切除术;2例发现盆腔子宫内膜异位病灶行病灶电凝术。术中切除病灶直径为0.75~4.50(2.55±0.85)cm。病灶位于脂肪层9例(19.15%),筋膜层23例(48.94%),肌层11例(23.40%);病灶达腹膜层4例(8.51%)。手术时长为10~105(47.43±21.94)min,术中出血量为5~100 ml,平均为31.70 ml。
2.547例AWE患者的随访及复发情况 随访6~73个月,中位随访时间为43.00个月。期间有6例(12.77%)复发,复发时长为术后6~24个月。6例复发患者中有2例于术后补充了促性腺激素释放激素激动剂(gonadotropin releasing hormone agonist,GnRH-a)治疗,另4例术后未行补充治疗。2例复发患者因症状较重于外院再次手术,另4例复发患者症状较轻,仍在密切随访中。
3 讨论
3.1目前EMs发病机制尚未完全清楚,存在多种学说,普遍认为有异位种植学说、体腔上皮化生学说、诱导学说、遗传因素学说、免疫与炎症因素学说和在位内膜决定论等,但均存在各自的局限性,并不能全面阐释EMs的发病机制[8]。AWE作为常见的盆腔外子宫内膜异位症,多数学者认为医源性播散是AWE发生的主要原因。本研究中所有AWE患者均有剖宫产史,提示医源性手术与AWE的发生相关。剖宫产术后AWE的发生支持子宫内膜种植学说,推测可能的原因与手术操作相关,术中将子宫内膜直接带到切口的筋膜层、肌层等,随后这些内膜在雌激素的刺激下生长,从而导致AWE发生[9]。但是有些病灶可以出现在远离剖宫产瘢痕部位,种植学说对此难以完全解释[10],淋巴脉管播散学说可以进行补充解释。近年来,黄佳明和姚书忠[11]研究提出AWE是一种复杂的慢性疾病,是多种发病机制共同作用的结果。
3.2AWE好发于育龄期女性,本研究显示患者的平均年龄为(32.17±4.45)岁,与相关文献报道的32.54岁相近[12]。从本研究结果来看,产次增加并未提高AWE的发生率。另外,本研究发现,AWE患者的剖宫产手术单位为外院的占比明显大于本院。本院是三级甲等医院,剖宫产技术处于贵州省内较高水平,由此推测,剖宫产技术可能是影响AWE的发病率的重要因素。虽然AWE多见于剖宫产手术横形切口左右两侧,但横形切口本身就是剖宫产常采用的切口方式,因此也难以说明AWE的发生与切口形状有关联。
3.3对于AWE的诊断目前尚缺乏统一标准,但AWE患者大多有典型的临床表现及体征,经期腹壁包块疼痛及瘢痕旁包块常为首发症状。本研究结果显示,经期腹壁包块疼痛为最常见的首发症状,占78.72%。其中2例患者内异病灶穿透皮肤出现破溃,表现为周期性病灶出血。大多病例可根据上述症状和体征诊断,但仍需注意与其他疾病鉴别。目前国内多采用国外学者提出的AWE诊断标准[13],需符合以下三点:(1)与月经相关的周期性疼痛;(2)有妇产科或下腹部手术史;(3)靠近瘢痕或瘢痕处查见包块。本研究中有42例(89.36%)术前经B超检查发现并诊断,提示B超可作为AWE诊断的便捷检查方法,可作为首选。有学者提出,对于B超探查的包块直径>4 cm者,建议行核磁共振进行充分评估,明确浸润范围及深度,避免术中损伤到盆腔器官,判断病灶切除后的腹壁缺损是否需要补片或皮瓣修补治疗[11]。另外本研究中29例AWE患者CA125检测未见明显升高,提示CA125对于AWE的诊断价值有限。有研究显示,若将CA125的截断值定为35 U/ml时,其诊断AWE诊断的敏感度为21.43%[14]。可能是由于病灶局限,AWE对全身的生物因子影响不大。细针穿刺细胞学检查虽是最精准的检查方法,但其为有创操作,建议在排除恶变时使用。
3.4本组患者均行手术治疗,部分患者术后补充GnRH-a治疗,用药期间病情缓解,但停药后有患者复发,并需再次手术。目前尚无循证医学证据表明药物治疗对AWE有效,手术治疗仍是AWE的首选治疗方案[15]。亦有研究提出术后予孕三烯酮口服补充治疗,患者在术后随访6个月至1年期间无复发情况[16],但该研究仅有16例病例,尚需大样本临床研究提供更有力证据。随着病程迁延,AWE的病灶会逐渐增大并且侵犯周围组织,增加手术难度,必要时需皮瓣移植或使用补片修补。因此,AWE一经确诊应尽早手术。本研究发现AWE病灶多侵及筋膜层和肌层,少数侵及脂肪和腹膜层,多数与周围组织形成粘连,界限不清。多数学者认为,手术切缘距离病灶至少1 cm[17]。
3.5AWE多继发于剖宫产术后,为降低其发生率,应严格掌握剖宫产手术指征[18-19]。剖宫产过程中应注意规范操作[20],取胎时用纱垫保护好子宫切口周围术野,防止宫腔内容物溢入腹腔和腹壁切口。缝合子宫时,避免缝针穿透子宫内膜。缝合子宫切口后对使用的手术器械、缝针线、手套等应用盐水冲洗等,预防剖宫产术后AWE的发生。此外,产后建议母乳喂养可推迟月经复潮,这对预防AWE有益。
综上所述,AWE为少见的EMs,临床医师应防止医源性种植。结合临床症状体征及B超检查可对AWE作出较准确的诊断。治疗以手术为首选,术后药物治疗可以控制残留病灶和微小病变,进而控制疼痛复发,若近绝经期可选择药物保守治疗。因术后存在一定的复发率,故术后应对患者予以密切的随访观察,制定规范的管理模式,减轻疾病给患者身心健康带来的影响。
