ZIF-12在检测抗坏血酸和L-色氨酸中的应用
2021-12-02李改花刘爽冯桂荣
李改花,刘爽,冯桂荣
(唐山师范学院化学系,唐山市绿色专用化学品重点实验室,河北唐山063000)
分子筛咪唑框架(ZIFs)是由二价金属离子(Zn2+,Co2+等)与咪唑基配位体通过络合作用,以四配位方式组装形成的纳米多孔晶体材料[1-2]。由于其具有优异的热稳定性、化学稳定性、可调节性以及化学多样性而受到广泛关注[3-4]。更重要的是,ZIFs的超高表面积和高孔隙率也引起了科研工作者对其在电化学领域应用的极大兴趣[5-6]。ZIFs作为多孔材料载体具有大的比表面积,可以为电化学传感器的检测提供优良的基底材料;其次,ZIFs材料中具有裸露的骨架结构,可以为化学传感器提供活性位点[7]。
抗坏血酸(Ascorbic acid.A)又称为维生素C,是一种常见的水溶性维生素,对其在生物体内的检测尤为重要[8-9]。L-氨基酸是一种存在于生物体的有机小分子,是构成生物体所需蛋白质的基准物质。L-氨基酸和抗坏血酸常常共存于生物体内,它们的区分和同步检测也是化学检测的难题之一[10]。本实验以ZIF-12作为电化学传感器基底材料,采用循环伏安法分别对抗坏血酸和L-色氨酸进行了检测,并实现了两者的同步检测。
1 实验部分
1.1 试剂与仪器
苯并咪唑,甲苯,甲醇,氨水,四水乙酸钴,硫酸,硝酸钾,铁氰化钾,抗坏血酸,L-色氨酸,磷酸二氢钾,磷酸氢二钾,以上试剂均为分析纯。
HJ-2A恒温磁力搅拌器,YXJ-2高速离心机,VER⁃TEX70傅里叶红外光谱仪,LK98A微机电化学分析系统,SIGMA300场发射扫描电镜,D/Max-2500 X射线衍射仪。
1.2 实验方法
1.2.1 ZIF-12的合成
称量0.48 g的苯并咪唑溶于19.19 g甲醇,室温下搅拌,加入18.32 g甲苯和0.07 g氨水,接着加入0.125 g四水合乙酸钴,室温下连续搅拌3 h,完成结晶。采用离心法收集ZIF-12,并用甲醇洗涤3次,室温下干燥过夜。
1.2.2 基底电极的预处理
(1)物理活化:用湿润的镜头纸轻轻擦拭玻碳电极(GCE)表面,除去电极表面污物,确保电极表面光滑。取少许0.3 μm的Al2O3于麂皮上,然后滴加少许去离子水,用玻碳电极上绝缘部分稍微搅匀,之后竖直地握住玻碳电极,用力均匀,呈圆形打磨2~3 min。用去离子水冲洗掉电极表面残留的氧化铝,再依次用超纯水,1∶1 HNO3,1∶1乙醇和超纯水超声清洗2~3 min,除去电极表面的污物。
(2)化学活化:将玻碳电极作为工作电极,甘汞电极作为参比电极,铂电极为辅助电极组成电解池,在0.5~1.0 mol/L H2SO4溶液中,在电位扫描范围-1.0~1.0 V,扫描速度为100 mV/s的条件下,用循环伏安法扫描到标准稳定的循环伏安图为止,消除化学残留物对电极的影响。
1.2.3 ZIF-12修饰电极的制备
用微量取样器移取10 μL的ZIF-12膜溶液,滴加在已经处理好的玻碳电极的电极表面,覆盖住玻碳电极中间的黑色部分,在烘烤灯下烘烤至成膜覆盖在电极上,制得ZIF-12修饰电极。
2 结果与讨论
2.1 ZIF-12的结构与表征(图1)
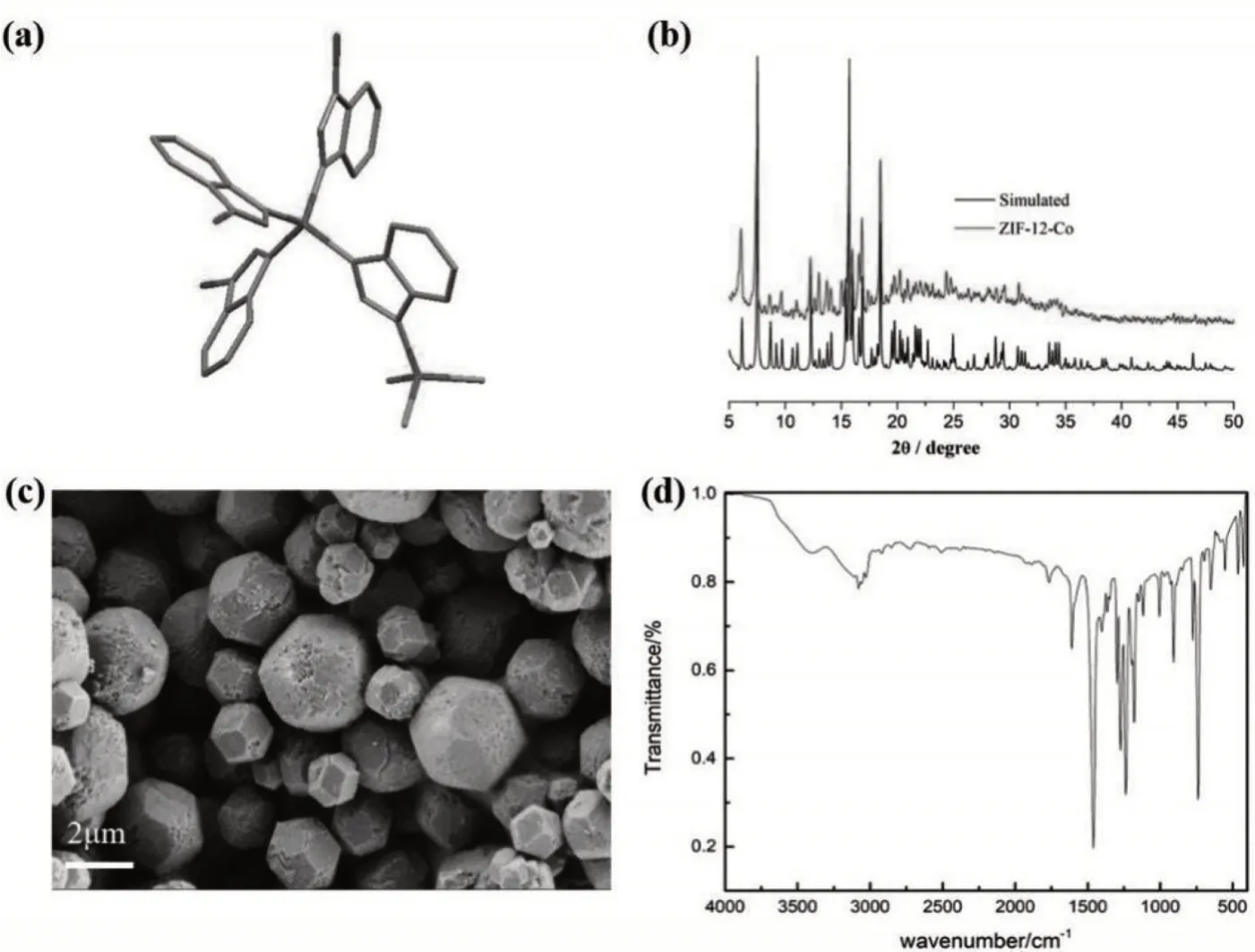
图1 (a)ZIF-12的结构;(b)X-粉末衍射图;(c)扫描电镜图;(d)红外光谱图
以X-粉末衍射、电镜扫描、红外光谱表征ZIF-12样品。由图1b可见,合成产品衍射峰与ZIF-12单晶数据模拟的XRD相比,其特征衍射峰的位置一致,说明该配合物具有较高的相纯度。从扫描电镜中可以看出,ZIF-12是规则的多面体结构,粒径分布约1~3 μm(图1c)。
2.2 pH对检测的影响
为了实现更好的检测效果,以玻碳电极为工作电极,甘汞电极为参比电极,铂电极为辅助电极组成电解池,分别对不同pH的缓冲液(pH=6.00,6.50,7.00,7.50,8.00)进行CV扫描。由图2可知,随着缓冲溶液pH的增加,峰电流逐渐增大,达到某一点之后开始下降。选取最高点的峰电流所在pH的缓冲溶液作为电解液,即pH=6.80。
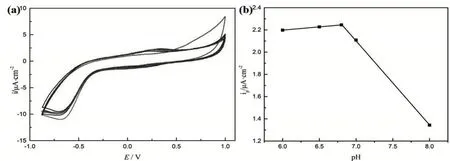
图2 (a)工作电极在不同pH缓冲溶液中的CV图;(b)峰电流(ip)与电解液pH的关系
2.3 ZIF-12/gelatin/GCE电化学稳定测试
以ZIF-12/gelatin/GCE电极为工作电极,饱和甘汞电极为参比电极,铂电极为辅助电极组成三电极体系。用磷酸盐缓冲液(PBS)(磷酸二氢钾和磷酸氢二钾的浓度均为0.2 mol/L)作为电解液(pH=6.80),电位扫描范围为-1.0~1.0 V,扫描速度为100 mV/s的条件下进行CV扫描20圈。由图3可见,在多次扫描过程中氧化还原特征峰的峰形良好,峰电流没有明显下降,说明ZIF-12在玻碳电极上的耐受性良好,在水体中可以稳定存在[11-12]。
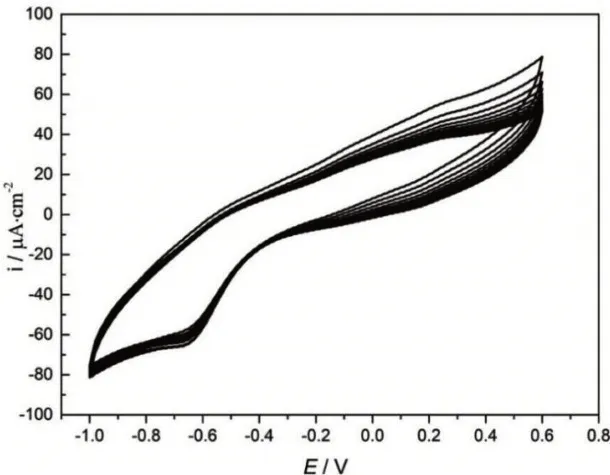
图3 以ZIF-12/gelatin/GCE为工作电极,磷酸盐缓冲溶液为电解液,电位范围-1.0~1.0 V,扫描速度为100 mV/s条件下扫描20圈的CV图
2.4 ZIF-12/gelatin/GCE的CV扫速影响
在以ZIF-12/gelatin/GCE电极为工作电极的三电极体系中,用磷酸盐缓冲液作为电解液(pH=6.80),电位扫描范围为-1.0~1.0 V,扫描速度为20~140 mV/s的条件下进行CV扫描。
从图4a可见,氧化峰和还原峰的电流密度都随着扫速的增加而增加。根据氧化还原峰电流(ip)与扫速的平方根(ν1/2)的关系图4b可以看出,峰电流和扫速的平方根存在线性关系,这说明ZIF-12与玻碳电极之间的电子传导受扩散过程的影响[13-14]。
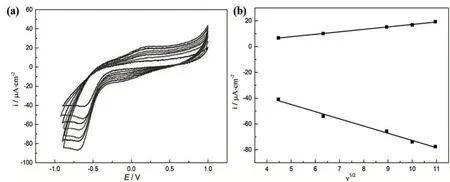
图4 (a)ZIF-12/gelatin/GCE在PBS中扫速变化的CV图(扫速20~140 mV/s);(b)峰电流(ip)与扫速平方根(ν1/2)的关系图
2.5 ZIF-12/gelatin/GCE对抗坏血酸的检测
以ZIF-12/gelatin/GCE电极为工作电极,饱和甘汞电极为参比电极,铂电极为辅助电极组成三电极体系,电位扫描范围为-1.0~1.0 V,扫描速度为100 mV/s,在磷酸盐缓冲液(pH=6.80)中加入不同浓度的抗坏血酸(浓度分别为0.25 mM,0.50 mM,0.75 mM,1.00 mM,1.25 mM,1.50 mM)。
由图5可见,随着加入的抗坏血酸浓度的增加,峰电流也呈现逐渐递增的趋势。以峰电流(ip)对抗坏血酸浓度(cAA)作图得到ip~cAA的线性关系图,线性方程为ip=10.810cAA+6.713,R2=0.995,灵敏度为10.810 μA·cm-2。
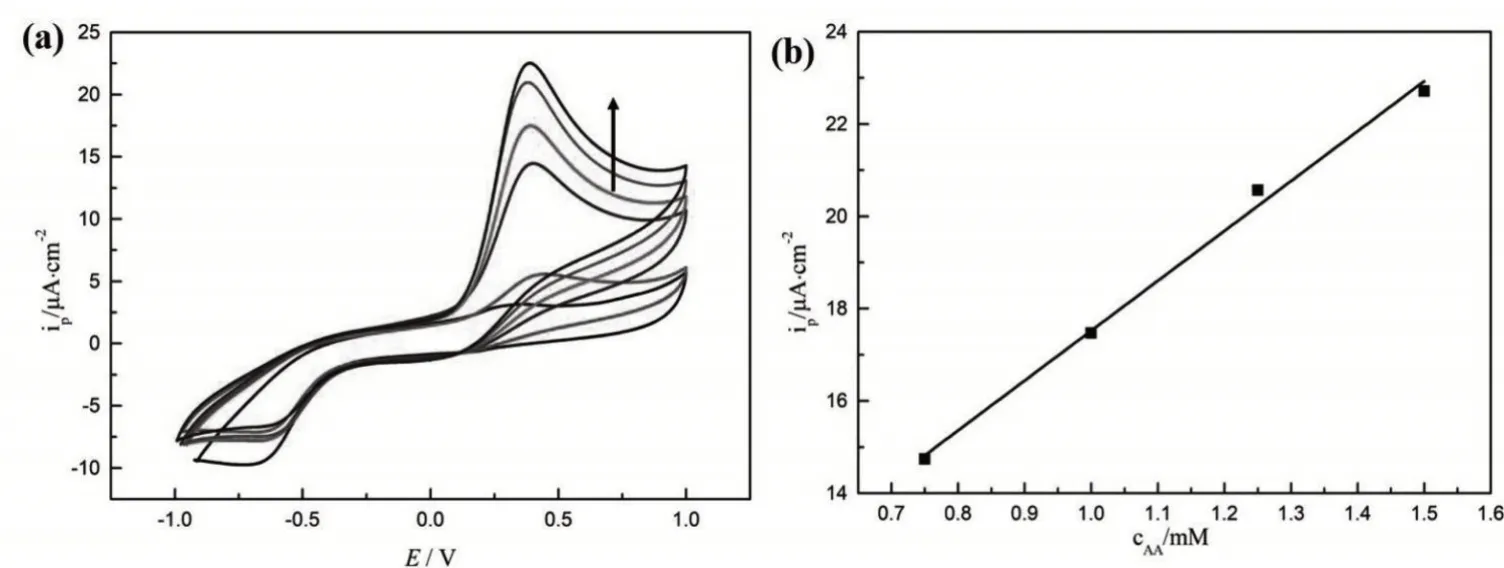
图5 (a)ZIF-12/gelatin/GCE在PBS中加入不同浓度抗坏血酸的CV图;(b)峰电流(ip)与抗坏血酸浓度(cAA)的关系图
2.6 ZIF-12/gelatin/GCE对L-色氨酸的检测
以ZIF-12/gelatin/GCE电极为工作电极,饱和甘汞电极为参比电极,铂电极为辅助电极组成三电极体系,电位扫描范围为-1.0~1.0 V,扫描速度为100 mV/s,在磷酸缓冲液(pH=6.80)中加入不同浓度的L-色氨酸(浓度分别为0.1 mM,0.2 mM,0.3 mM,0.4 mM,0.5 mM)。
从图6中可以看出,随着L-色氨酸浓度的增加,峰电流也呈现逐渐递增的趋势。以峰电流(ip)对L-色氨酸浓度(cL-Trp)作图得到ip~cL-Trp的线性关系图,线性方程为ip=32.287cL-Trp+3.894,R2=0.994,灵敏度为32.287 μA·cm-2。

图6 (a)ZIF-12/gelatin/GCE在PBS中加入不同浓度的L-色氨酸的CV图;(b)峰电流(ip)与L-色氨酸浓度(cL-Trp)的关系图
2.7 ZIF-12/gelatin/GCE对抗坏血酸和L-色氨酸的同步检测
以ZIF-12/gelatin/GCE电极为工作电极,饱和甘汞电极为参比电极,铂电极为辅助电极组成三电极体系,电位扫描范围为-1.0~1.0 V,扫描速度为100 mV/s,在磷酸缓冲溶液(pH=6.80)中加入1.5 mM的抗坏血酸,然后依次加入0.1 mM,0.2 mM,0.3 mM,0.4 mM,0.5 mM的L-色氨酸。
从图7可以看出,在抗坏血酸的存在下,随着L-色氨酸浓度的增加,峰电流逐渐增大,这说明,在抗坏血酸存在的条件下,ZIF-12/gelatin/GCE可以稳定地检测L-色氨酸而不受抗坏血酸的干扰。以峰电流(ip)对L-色氨酸浓度对数(logcL-Trp)作图得到ip~cL-Trp的线性关系图,线性方程为ip=18.884 log cL-Trp+37.160,R2=0.991,灵敏度为18.884 μA·cm-2。
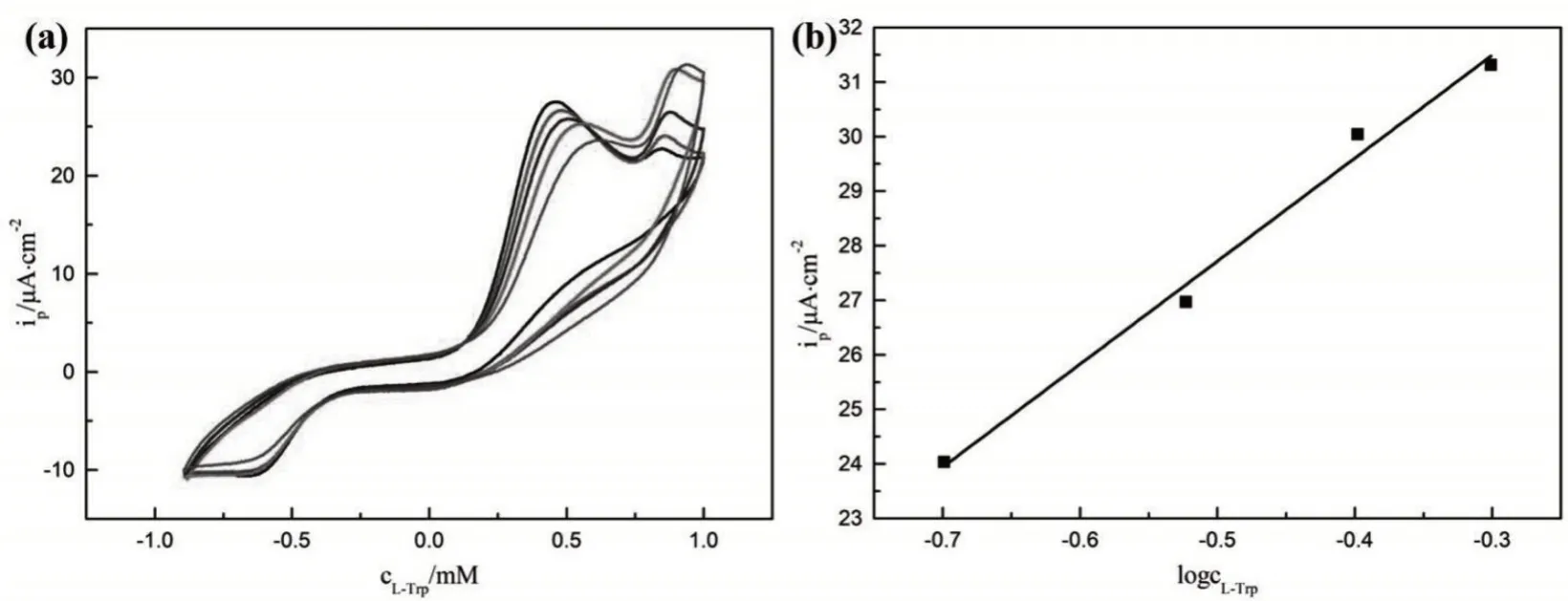
图7 (a)ZIF-12/gelatin/GCE在含有1.5 mM抗坏血酸的PBS中加入不同浓度的L-色氨酸的CV图;(b)峰电流(ip)与L-色氨酸浓度对数(logcL-Trp)的关系图
3 结论
以苯并咪唑和乙酸钴为原料,采用室温搅拌法合成分子筛咪唑骨架-12(ZIF-12),并对其进行了XRD、红外和扫描电镜表征。ZIF-12作为生物电化学传感器材料应用于对抗坏血酸、L-色氨酸、抗坏血酸和L-色氨酸的同步检测,具有准确度高、稳定性强、快速简便的优点。
