HPLC法与化学发光微粒子免疫法测定癫痫患者血浆中卡马西平浓度的一致性评价
2021-11-30白建海牟红云郑丹庞苗菜丁晓敏张敏丽王时力王毅超
白建海 牟红云 郑丹 庞苗菜 丁晓敏 张敏丽 王时力 王毅超


[关键词] 高效液相色谱法; 化学发光微粒子免疫法;卡马西平;血药浓度;一致性
[中图分类号] R969.4 [文献标识码] B [文章编号] 1673-9701(2021)18-0109-05
Consistency evaluation of HPLC and chemiluminescence microparticle immunoassay in determination of plasma carbamazepine concentration in patients with epilepsy
BAI Jianhai1 MOU Hongyun1 ZHENG Dan1 PANG Miaocai1 DING Xiaomin2 ZHANG Minli2 WANG Shili1
WANG Yichao3
1.Department of Ophthalmology, Taizhou Central Hospital (Taizhou University Hospital) in Zhejiang Province, Taizhou 318000, China; 2.Operating room, Taizhou Central Hospital (Taizhou University Hospital) in Zhejiang Province, Taizhou 318000, China; 3.Department of Laboratory Medicine and Precision Laboratory, Taizhou Central Hospital (Taizhou University Hospital) in Zhejiang Province, Taizhou 318000, China
[Abstract] Objective To evaluate the consistency of the two methods (high performance liquid chromatography (HPLC method) and chemiluminescence microparticle immunoassay (CMIA method)) in the determination of plasma carbamazepine concentration in patients. Methods The Bland-Altman method and Passing-Bablok regression method were used to analyze the measured values of the two detection methods, and the consistency of the two methods was further analyzed. Results The Bland-Altman analysis showed that the two methods (HPLC method and CMIC method) had good consistency in the determination of plasma carbamazepine concentration in patients. The regression equation of the two methods was Y=0.9912X-0.1083(R2=0.970, n=117), indicating a good correlation between the two methods. Conclusion The two methods (HPLC method and CMIA method) have good correlation and consistency in the determination of plasma carbamazepine concentration in patients. The two methods can substitute each other.
[Key words] High performance liquid chromatography; Chemiluminescence microparticle immunoassay; Carbamazepine; Plasma concentration; Consistency
卡馬西平通常用于治疗癫痫或眼科神经病理性疼痛,也被用于双相情感障碍的二线治疗药物,特别是在治疗全身强直痉挛性癫痫和混合型癫痫、视神经痛、青光眼、躁狂等疾病疗效明显。同时,卡马西平通过诱导药物代谢酶可以影响药物与药物之间的临床药效相互作用。卡马西平的大多数口服制剂都能够很好的吸收,具有较高的生物利用度。但是其治疗范围较窄[癫痫:4~12 μg/mL;情感障碍(青光眼):4~10 μg/mL],在给药剂量间隔期间血浆药物浓度波动明显,药物代谢动力学个体差异大,且与情志因素相关疾病(癫痫、青光眼)副作用及病情变化密切相关,且毒副反应不易于症状加重区分[1-2],因此临床使用过程中,须对其血药浓度进行监测。
测定卡马西平血浆浓度的检测方法较多,精密度及评价标准参差不齐。高效液相色谱(High-performance liquid chromatographic,HPLC)[3-5],荧光偏振免疫分析方法(Fluorescence polarization immunoassay,FPIA)[6-7],液相色谱串联质谱法(Liquid chromatography tandem mass spectrometry,LC-MS/MS)[8-10]等方法,其中有报道HPLC法不仅可以测定卡马西平浓度,还可以用于评价其生产品的质量,也可以用于检测其稳定性[3-5]。化学发光微粒子免疫法(Chemiluminescence microparticle immune assay,CMIA)检测技术以自动、定量、随机加载和宽线性范围检测的优点,逐步取代人工定性检测方法[11-12]。上述各种检测手段在技术原理,操作程序,性能参数,客观评价等方面都有很大的区别。本研究选取发病较为常见的癫痫患者作为研究对象,通过对比分析CMIA法和HPLC法测定患者血浆中卡马西平浓度,通过运用Bland-Altman plot评价两者相关性及一致性,为神经科及眼科药物应用提供参考。
1 材料与方法
1.1 仪器与试药
高效液相色谱(waters 600,美国),全自动化学发光免疫分析仪(ARCHITECT i2000SR,美国ABBOTT公司),超纯水通过微孔净水装置(Bedford,美国)生成(电阻率大于18.2 MΩ×CM),化学品和实验试剂(Highest grades,sigma,美国),卡马西平标准对照品(中国药品检验总所,批号:100142-201004),甲醇(Waltham,美国)为色谱纯。
1.2 样本收集
项目经过台州市中心医院(台州学院附属医院)医学伦理委员会批准(2021L-03-06),收集2019年2月至2021年3月台州市中心医院(台州学院附属医院)服用卡马西平的117例癫痫患者(10~69岁)药物浓度血样(服药前取空腹全血)3 mL,高速离心机(D-37520,美国ABBOTT公司)离心血样5 min(1 min,6000 r/min)分离出血浆并取样,标本血浆分成2份,其中一份采用CMIA法检测(当天);另外一份冰箱封存(-40℃),待采样完毕后进行HPLC检测。
1.3 RP-HPLC法测定血浆中卡马西平药物浓度
1.3.1 样品的处理 用甲醇将精密称定卡马西平标准对照品(100142-201004)配成储备液(520 μg/mL)备用,按照梯度浓度将标准品储备液稀释成为520、390、260、130、65、32.5、16.25 μg/mL标准对照品液。移液枪(Eppendorf公司)精密取甲醇标准对照液25 μL,精密加入空白血浆(450 μL)并用漩涡混合器(Votex Genius 3,德国IKA公司)漩涡混匀得对照标准品血浆系列样品。上述同种方法配制质量浓度(400.0 μg/mL)质量控制储备液(Quality control stock solution,QC),分别置于4℃条件下冷藏。取上述血浆系列标准对照品样品100 μL,加入甲醇(300 μL),漩涡混合器(Votex Genius 3,德国 IKA公司)漩涡混匀120 s,高速离心机(D-37520,美国 ABBOTT 公司)离心5 min(15000 r/min,4℃),取上清液进样分析。
1.3.2 色谱条件 色谱柱条件(4.6 mm×250 mm,5 μm,35℃);流动相条件:甲醇和水的混合物(50∶48 v/v),检测波长为285 nm,流速:1.0 mL/min。
1.3.3 专属性考察 按照(1.3.1)方法分别制备血浆(空白),血浆(空白+标准品),患者血浆(服用卡马西平)并进样,绘制色谱图。
1.3.4 标准曲线的绘制 制备系列标准血浆样品,按上述方法处理分析。
1.3.5 回收率试验
1.3.5.1 提取回收率 用血浆(空白)和卡马西平QC储备液制成浓度分别为2.5、10.0、20.0 μg/mL的样品各5份,按上述方法处理分析,卡马西平平均峰面积为A1;另取空白血浆加3倍量甲醇,涡旋120 s,离心5 min(15 000 r/min,4℃),取上清液,与卡马西平QC储备液制成同浓度的樣品各5份,同法处理分析,卡马西平平均峰面积为A2,按A1/ A2×100%计算提取回收率。
1.3.5.2 方法回收率 用血浆(空白)和卡马西平标准对照品溶液精密配制成体积浓度分别为2.5、10.0、20.0 μg/mL的样品各5份,同法操作后,进样分析,将所得的峰面积相应的回归方程计算浓度值,计算方法是测得值和实际值的比值。
1.3.6 稳定性试验 用血浆(空白)和卡马西平标准品溶液精密配制成体积浓度为2.5、10.0、20.0μg/mL的样品,按上述方法处理。室温稳定性:温度为25℃条件下放置样品4 h后,按上述方法处理分析。冻融稳定性:温度为-40℃条件下放置样品24 h,取出静待样品完全融化,反复3次(3 d),按上述方法处理计算。长期稳定性:温度-40℃条件下样品于静置7、14、21、28、35 d后,同法处理,计算。
1.3.7 精密度试验 批内精密度:用血浆(空白)与卡马西平标准品溶液精密配制成体积浓度为2.5、10.0、20.0 μg/mL的同一批样品各5份,按上述方法进样并计算。批间精密度:同法配制浓度分别为2.5、10.0、20.0 μg/mL的样品,按上述方法测定处理不同批的样品,连续测定5批,同法计算。
1.3.8 质量控制 待测血浆的样品与按照上述方法处理所得高、中、低3种浓度空白血浆和卡马西平QC储备液配制成的样品平行测定。
1.3.9 患者血浆测定 按照上述方法分析待测血浆,按照上述标准曲线计算患者样品中卡马西平含量。
1.4 CMIA法
1.4.1 CMAI法原理 详细内容见ARCHITECT 卡马西平测定试剂盒说明书[13]。为了控制分析质量,校准器和质量控制样品通常按照制造商的要求进行。
1.4.2 标准曲线的制备 卡马西平标准曲线制备按照Abbott ARCHITECT i2000SR系统操作手册应用原装的标准定标液进行。自动拟出标准曲线,系列校准样品浓度分别为2.0、4.0、8.0、12.0、24 μg/mL。
1.4.3 性能指标的评估 按照Abbott ARCHITECT i2000SR系统操作手册进行精密度、回收率、线性、专属性等指标验证。
1.4.4 CMIA法测定患者血浆中卡马西平浓度 按照标准操作规范流程检测血浆,定时平行测定质控样品。
1.5 两种检测方法比较
1.5.1 方法 通过Passing-Bablok回归和Pearson检验,对CMIA法(检测系统)和HPLC法(待评价系统)回归方程和相关系数进行评价,应用Bland-Altman偏差图评价CMIA和HPLC一致性。两种测量平均值根据数据分布采用配对样本t检验或者Wilcoxon检验。
1.5.2 相关性分析 按照Passing-Bablok回归方法对上述测定的结果进行相关性分析。
1.5.3 一致性分析 按照Bland-Altman方法对上述两种方法的测定结果进行一致性分析。
1.6 统计学方法
前提条件是比较的检测系统(CMIA法)和待评价系统(HPLC法)可重复性优,测定结果相关性分析采用Passing-Bablok回归法进行分析;测定结果的一致性采用Bland-Altman偏差图进行分析;测定结果(CMIA法和HPLC法)进行配对样本t检验,以检验系统误差,P<0.05为差异有统计学意义。统计学处理软件为Med Calc医学统计软件(第15.8版,比利时)。卡马西平浓度以(x±s)表示。
2 结果
2.1 HPLC法测定血浆中卡马西平药物浓度
2.1.1 专属性考察 图1示峰形及分离度良好,卡马西平定量分析不被内源性杂质所干扰。
2.1.2 标准曲线的绘制 峰面积和峰浓度线性关系良好,线性范围0.8125~26.0 μg/mL(R2=0.9997,n=6),峰面积(Y)对浓度(X)回归方程为Y=1.53×104X+4.9×103。
2.1.3 回收率考察
2.1.3.1 提取回收率 低、中、高三浓度的提取回收率分别为(100.86±8.69)%(RSD 8.61%)、(104.56±9.99)%(RSD 9.56%)、(97.93±3.46)%(RSD 3.54%),符合样品分析的要求。
2.1.3.2方法回收率 低、中、高3浓度的方法回收率分别为(90.57±9.00)%(RSD 9.94%)、(84.30±5.21)%(RSD 6.19%)、(98.83±4.77)%(RSD 4.82%),符合样品分析的要求。
2.1.4稳定性及精密度考察 结果表明,卡马西平样品稳定性较好,精密度符合样品分析的要求。
2.1.5 质量控制 结果表明,低浓度偏差均<20%,中、高浓度偏差<15%,因此样品测定结果有效。
2.1.6 患者血浆测定 HPLC法测定癫痫患者血浆中卡马西平的平均浓度为(7.7±3.2)μg/mL。
2.2 CMIA法测定血浆中卡马西平浓度
2.2.1 性能指标的评估 精密度、回收率、线性、专属性等指标均符合操作手册要求。
2.2.2 患者血样测定 CMAI法测定的癫痫患者血浆中卡马西平的平均浓度为(8.0±3.1)μg/mL。
2.3 两种检测方法比较
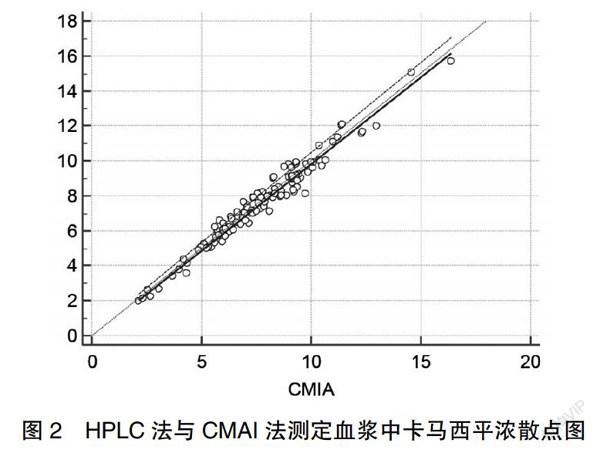
2.3.1 相关性分析 对上述两种测定方法测定的癫痫患者血浆中卡马西平浓度结果按照Passing-Bablok回归方法进行分析(图2),典型线性回归方程得Y=0.9912X-0.1083(X,CMAI法测定的癫痫患者血浆中卡马西平的浓度结果;Y,HPLC法测定癫痫患者血浆中卡马西平的浓度结果;R2=0.970;n=117),方程的斜率为0.9912(95%CI:0.9548~1.0314,P<0.0001),截距为-0.1083(95%CI:-0.3975~0.1623,P=0.0003),线性有效性(Cusum)检验可知无显著性线性偏差(P=0.37)。结果示CMAI法测定癫痫患者血浆中卡马西平的浓度结果和HPLC法测定癫痫患者血浆中卡马西平的浓度结果存在线性相关性(R2>0.95),检测方法可以相互替代。同时结果显示回归率和矩阵结果符合统计要求[14]。
2.3.2 两种测定方法测定结果的一致性分析 上述两种测定癫痫患者血浆中卡马西平浓度结果进行Bland-Altman分析,图3示对数变换测量的平均偏差和95%的一致性極限(95%LOA)分别为0.19和0.18~0.45,HPLC法为0.17,CMIA法为0.18~0.35。为得到一个可以接受的结果,进行反向变换,以获得这两个测量值的比值。图3示4.3%(5/117)的点在95%LOA以外,符合要求;在95%LOA以内,HPLC法测定癫痫患者血浆中卡马西平的浓度结果与CMAI法测定癫痫患者血浆中卡马西平的浓度结果比较,绝对值(差值百分比)的最大值为14.5%(1.05 μg/mL)。因此上述两种方法可以互换。
2.3.3 系统误差分析[14] 上述结果显示,HPLC法和CMIA法测定血浆中卡马西平浓度时可以互换,但还需考察他们之间测定卡马西平时是否存在系统误差。运用回归方程法进行分析,其中因变量设为两种检测手段得出的每个样本的每次测定值;自变量设为两种检测手段得出的每个样本的平均值;公式为Y=0.1429X-0.0029(R2=0.053,n=117,P>0.05),其斜率差异无统计学意义,不存在比例误差,说明不存在比例误差。对HPLC法和CMIA法两种方法测定的血浆中卡马西平浓度结果进行配对样本t检验,结果P=0.0044,提示两种检测方法存在固定误差(P<0.05)。
3 讨论
本研究建立了HPLC法测定癫痫患者血浆中卡马西平的浓度,并收集临床应用卡马西平治疗的癫痫患者血液样本(n=117),采用HPLC法及CMIA法测定血浆样本中卡马西平浓度,同时两种方法均考察精密度、准确度、线性及范围等等方法学效能指标,结果显示两种方法均符合重复性、准确性等测定要求。
参考文献运用Passing-Bablok Regression对两种测定结果的相关性进行分析[7,15-16],并进行相应差异的比较。结果表明HPLC法测定癫痫患者卡马西平血浆药物浓度和CMIA法测定癫痫患者卡马西平血浆药物浓度两种方法相关性较好,具有可比性(图2)。
Bland-Altman Plot是评价比较两种临床定量测量方法的金标准,应用近30年历史[17-18]。本项研究中两种测量方法一致性密切线性相关,如果以图形作为参考,则获得95%LOA将比小值所需的间距更宽,比两者间距更窄的实为大值[15]。因此,在做Bland-Altman Plot分析前,两种方法测量值均应进行对数转换,从而消除差值和波动之间的关系,得到合适的95%LOA。经过对数转换以后,结果还需要再进行反向转换才比较容易理解。另外,本研究以图形作为参考在分析结果时可以兼顾考虑系统误差和比例误差,使分析结果更加客观和精确。
系统误差分析可以使上述HPLC法测定癫痫患者卡马西平血浆药物浓度和CMIA法测定癫痫患者卡马西平血浆药物浓度对结果的一致性误差减小[19-20],所以实际操作过程中本项目以两系统实测值之差为因变量,以两系统实测值之平均值为自变量再次进行回归分析。如果分析结果存在比例误差,则回归分析图示中有一条斜率不为零的趋势线,那么固定误差是回归方程y=ax+b中的截距(b),比率误差是回归方程y=ax+b中的斜率(a)。如果回归分析图示中趋势线为零,则两种方法的偏差主要是固定误差,可以用置信区间法或配对t检验来检测[14]。本研究综合考虑上述各方面因素对结果分析的影响,运用多种分析方法消除HPLC法测定癫痫患者卡马西平血浆药物浓度和CMIA法测定癫痫患者卡马西平血浆药物浓度结果分析过程中一致性的差异,结论客观真实。
本研究采用Bland-Altman法评价两种方法的一致性,结果显示,区间内差异百分比的最大值为14.5%(1.05 μg/mL),临床上可接受。结果表明,HPLC法测定癫痫患者卡马西平血浆药物浓度和CMIA法测定癫痫患者卡马西平血浆药物浓度结果一致性较好,但HPLC法测定值比CMIA法低2.1%(图3)。系统误差分析的结果也表明这两种方法都有一定的系统误差(固定误差)。这就决定了这两种方法的区别。分析误差来源最可能的原因是卡马西平代谢产物10,11环氧卡马西平与卡马西平结构相似,干扰卡马西平的测定。虽然这两种方法都不是金标准,但与CMIA法相比,HPLC法准确、可靠、快速,技术要求较低,能更好地反映真实值。
本项研究尚存在如下缺陷:①两种检测方法重复性限制了纳入研究患者数量,由于患者标本通常只能测试一次,因此,在临床应用样本中缺乏HPLC法和CMIA法重复性。②未评价药物代谢对于两种方法检测患者血浆中卡马西平含量的影响。③95%LOA是否能够被临床医生接受尚不得而知。
综上所述,本项研究建立一种准确、可靠、快速、简单的HPLC法测定癫痫患者血浆中卡马西平浓度,并与CMIA进行比较和验证,研究表明,HPLC法是测定卡马西平浓度比较可靠的方法。该方法可以提供更大的特异性,预后价值和成本效率,可以为精神科或者眼科用药监测提供理论依据。
[参考文献]
[1] Hiemke C,Bergemann N,Clement HW,et al. Consensus guidelines for therapeutic drug monitoring in neuropsychopharmacology:Update 2017[J]. Pharmacopsychiatry,2018,51(1-2):e1.
[2] 张相林.治疗药物监测临床应用手册[M].北京:人民卫生出版社,2020.
[3] 武晓玉,王荣,谢华,等.柱切换-高效液相色谱法快速监测癫痫患者卡马西平血药浓度[J].药物分析杂志,2013,33(10):1715-1719.
[4] 王强,库丽.反相高效液相色谱外标法测定卡马西平和茶碱的血药浓度[J].中国药业,2012,21(18):35-36.
[5] 熊友健,涂琼,卢庆红,等.高效液相色谱法同时测定拉莫三嗪、卡马西平、苯巴比妥的血药浓度[J].儿科药学杂志,2014,20(4):42-45.
[6] 周素琴,张鸿燕,果茵茵.荧光偏振免疫法与高效液相色谱法测定人血清中卡马西平、苯巴比妥浓度的比较[J].中国医院药学杂志,2010,30(14):1242-1244.
[7] 焦正,赵志刚,施孝金,等.比较HPLC和FPIA法测定人血清中卡马西平的血药浓度[J].中国临床药理学杂志,2004,20(4):291-294.
[8] 陈凯云,骆利,谢文毅,等.高效液相色谱-质谱串联法同时测定人血清中拉莫三嗪及卡马西平的含量[J].中国医院用药评价与分析,2012,12(12):1108-1110.
[9] 张静,袁宇琳,熊雯.UPLC-MS/MS法测定人血浆中卡马西平浓度[J].中国药物应用与监测,2020,17(2):86-89.
[10] 陈晓,朱斌,杨阳,等.UPLC-MS/MS法同时检测人血浆中拉莫三嗪和卡马西平浓度[J].实用药物与临床,2019, 22(10):1083-1086.
[11] Bazin C,Guinedor A,Barau C,et al. Evaluation of the architect tacrolimus assay in kidney,liver,and heart transplant recipients[J].J Pharm Biomed Anal,2010,53(4):997-1002.
[12] Li ZY,Yan CL,Yan R,et al. Analytical performance of the Abbott Architect i2000 tacrolimus assay in Chinese patients after renal transplantation[J]. Transplantation Proceedings,2010,42:4534-4537.
[13] 雅培贸易有限公司.ARCHITECT卡马西平测定试剂盒说明书.2012.
[14] 倪平,陳卉,涂娇,等.基于Bland-Altman法对定量资料的一致性评价及其SAS宏实现[J].中国临床药理学与治疗学2014,19(8):898-894.
[15] 周金玉,孙增先,许静,等.酶放大免疫分析法与高效液相色谱法检测人血浆中丙戊酸浓度比较[J].中国新药与临床杂志,2012,31(12):748-752.
[16] 萨建,刘桂芬.定量测量结果的一致性评价及Bland-Altman法的应用[J].中国卫生统计,2011,28(4):409-411.
[17] 李镒冲,李晓松.两种测量方法定量测量结果的一致性评价[J].现代预防医学,2007,34(17):3263-3266.
[18] Ludbrook J. Confidence in Altman-Bland plots: a critical review of the method of differences[J]. Clin Exp Pharmacol Physiol,2010,37(2):143-149.
[19] 陈卉. Bland Altman分析在临床测量方法一致性评价中的应用[J]. 中国卫生统计,2007,24(3):308-310.
[20] 张剑波,江泽友,房俊,等. Kappa统计量和Bland-Altman分析法在HbA1c试剂盒一致性评价中的应用[J].数学的实践与认识,2019,49(20):167-175.
(收稿日期:2020-12-05)
