CEUS对乳腺癌前哨淋巴结术前指导价值
2021-11-29刘艳超刘郭坤王巍巍张宁张迎舟
刘艳超 刘郭坤 王巍巍 张宁 张迎舟
前哨淋巴结是最先接受来自肿瘤淋巴引流的淋巴结,约89.9%的乳腺癌前哨淋巴结位于患侧腋窝[1]。针对乳腺癌患者,前哨淋巴结活检和腋窝淋巴结清扫结果是评估患者肿瘤分期、预后的重要组成部分,乳腺癌患者腋窝淋巴结是否转移是影响患者预后的重要因素,无淋巴结转移患者5年生存率达90.5%,而存在淋巴结转移患者的5年生存率下降至53.6%,准确鉴定前哨淋巴结转移情况对乳腺癌治疗具有重要意义[2-4]。目前,临床常用前哨淋巴结活检进行前哨淋巴结的定位、定性诊断,而随着超声造影(contrast-enhanced ultrasound,CEUS)技术的不断发展完善,CEUS有望成为乳腺癌术前前哨淋巴结定位、定性诊断的有效检查方法,指导手术治疗[5,6]。本研究分析80例乳腺癌患者前哨淋巴结术前CEUS诊断结果与临床病理结果,分析CEUS的应用价值,报道如下。
1 资料与方法
1.1 一般资料 选择2017年1月至2020年1月我院收治的80例女性乳腺癌患者,年龄32~68岁,平均年龄(47.62±8.54)岁;平均乳腺肿物直径(4.52±0.64)cm;病理类型:浸润性导管癌60例,浸润性原位癌12例,浸润性小叶癌2例,其他6例;肿瘤分期:T1s 12例,T1 46例,T2 15例,T3 3例,T4或多灶 4例;免疫组化:Luminal A 2例,Luminal B-HER2(+)9例,Luminal B-HER2(-)52例,HER2过表达13例,基底型4例。
1.2 纳入与排除标准
1.2.1 纳入标准:经病理组织学确诊为乳腺癌;乳腺癌首次确诊;术前接受经皮CEUS检查识别前哨淋巴结;临床治疗及影像学资料完整。
1.2.2 排除标准:合并其他恶性肿瘤;有放化疗史;患侧乳房或腋窝曾行较大手术而破坏此区域的淋巴引流;对超声造影剂过敏。
1.3 方法 超声仪器为西门子Acuson Sequoia 512彩色超声仪,探头频率7.0 MHz,L8-S线阵探头。
1.3.1 常规超声检查:患者造影前常规进行患侧腋窝淋巴结二维超声检查,取仰卧位,充分暴露腋窝,观察淋巴结大小、形态、内部回声、血流形态分布等情况,初步确定前哨淋巴结。
1.3.2 CEUS检查:常规消毒乳腺及腋窝皮肤,采用1%利多卡因局部浸润麻醉,用2 ml注射器抽取1.5 ml造影剂声诺维(SonoVue)皮内注射,轻轻抚摸患者注射部位10~30 s,在造影模式下沿淋巴管进入淋巴结的路径实时连续前哨淋巴结状态,记录淋巴结的造影增强模式、前哨淋巴结的性质、增强时间等。探头扫清病灶后用1 ml注射器抽取1%亚甲蓝注射液0.5 ml,定位于造影所示前哨淋巴结内并进行标记。
1.3.3 图像分析:前哨淋巴结增强模式分为Ⅰ型(均匀增强)、Ⅱ型(不均匀增强)、Ⅲ型(无增强);Ⅰ型为良性淋巴结(阴性),Ⅱ、Ⅲ型为转移性淋巴结(阳性)。
1.3.4 病理检查:超声造影检查后4 h内行前哨淋巴结活检,完成乳腺癌改良根治术,术中前哨淋巴结单独送病理检查。

2 结果
2.1 前哨淋巴结CEUS增强模式与病理结果比较 80例患者经术前CEUS检查检出前哨淋巴结97枚,经术中蓝染法证实为前哨淋巴结,3例患者经术前CEUS未探及明确前哨淋巴结,术前CEUS前哨淋巴结定位率96.25%(77/80)。见表1。

表1 前哨淋巴结CEUS增强类型与病理结果比较 枚
2.2 前哨淋巴结CEUS特征分析 CEUS检出阳性前哨淋巴结最大径大于阴性前哨淋巴结(P<0.05),存在周边声晕、血流Ⅱ~Ⅲ级枚数均多于阴性结果(P<0.05)。见表2。

表2 前哨淋巴结CEUS增强类型与病理结果比较
2.3 前哨淋巴结CEUS诊断结果与病理结果比较 CEUS诊断97枚前哨淋巴结中良性淋巴结37枚,转移性淋巴结60枚,病理检查诊断良性淋巴结61枚,阴性淋巴结26枚。CEUS诊断前哨淋巴结转移的灵敏度为100%,特异度为60.66%,准确率为75.26%,阳性预测值60.00%,阴性预测值100%。见表3。
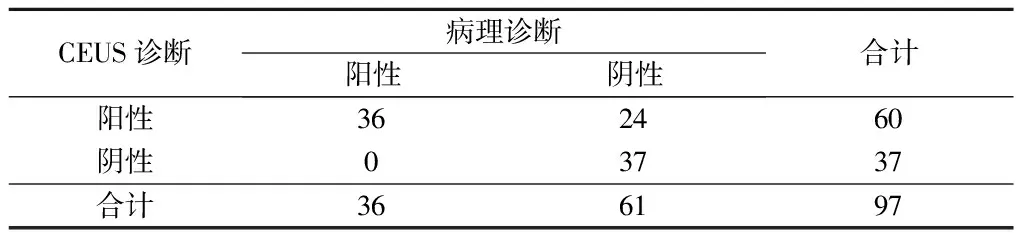
表3 前哨淋巴结CEUS诊断结果与病理结果比较 枚
2.4 图像典型病例分析 女性,46岁,浸润性乳腺癌;前哨淋巴结CEUS图像示无明显增强,Ⅲ型。女性,54岁,浸润性乳腺癌;彩色血流图Ⅲ级;前哨淋巴结CEUS图像示无明显增强,Ⅲ型。见图1~4。

图1 前哨淋巴结CEUS图像 图2 前哨淋巴结CEUS图像及二维图像 图3 超声彩色血流图像 图4 前哨淋巴结CEUS图像及二维图像
3 讨论
临床试验公布的10年随访结果证实,腋窝前哨淋巴结确诊1~2阳性的保乳术后患者可避免腋窝淋巴结清扫,这使得对乳腺癌患者进行前哨淋巴结的定位、定性诊断成为临床关注热点[7,8]。根据示踪剂的不同,前哨淋巴结活检可分为蓝染法和核素法,其中蓝染法因简便易行、无放射性污染且对定位乳腺癌前哨淋巴结有一定优势而应用更为广泛[9,10],但前哨淋巴结活检对手术操作者技术要求较高,术前存在盲目性,操作时间较长,国际专家共识认为早期乳腺癌患者进行盲目的前哨淋巴结活检并不符合伦理[11,12]。
乳腺癌患者术前可通过超声、CT、MRI、PET等影像学手段进行前哨淋巴结的定位和定性诊断,有助于术中准确定位[13]。其中,近年CEUS技术不断发展和完善,CEUS通过经皮注射超声造影剂能够显示引流区域淋巴管及前哨淋巴结,实时动态观察淋巴管走行情况及淋巴结增强模式,可显示二维超声、CT和MRI等检查方法不能显示的影像特征,成为临床关注的前哨淋巴结定位和定性诊断检查手段[14,15]。超声造影检查时,造影剂能够通过细胞间隙的胞饮或胞吐作用而被吸收,并使造影剂被限制在淋巴管内而不流入淋巴结,从而进行淋巴管显像,超声可快速从注射部位发出线状增强的淋巴管及与之相连的圆形或椭圆形增强淋巴结,造影持续时间较长,有利于检查者对注射部分至淋巴管、淋巴结进行往返观察,清晰描绘造影剂的流动路线,检测最先显像增强的前哨淋巴结对其进行诊断,乳腺癌前哨淋巴结病理性质与CEUS增强模式有关,临床普遍将均匀性增强淋巴结诊断为良性,不均匀性增强及无增强淋巴结诊断为恶性。本研究80例患者经术前CEUS检查检出前哨淋巴结97枚,术前CEUS前哨淋巴结定位率96.25%,与既往研究[16]结果相符,表明CEUS术前定位前哨淋巴结是有效、可行的。CEUS诊断97枚前哨淋巴结中良性淋巴结37枚,转移性淋巴结60枚,且转移性淋巴结表现为最大径更大、周边有声晕、血流分级Ⅱ~Ⅲ级;以病理结果为金标准,CEUS诊断前哨淋巴结转移的灵敏度为100%,特异度为60.66%,准确率为72.41%,与胥桐等[17]研究显示的90.9%敏感度、83.3%特异度、70.2%准确率比较,本研究特异度较低,假阳性较高,分析原因:淋巴结不均匀性增强与肿瘤浸润显著相关,癌细胞增殖在前哨淋巴结内堆积、阻塞、破坏细小淋巴管及慢性炎症等良性病变也可导致淋巴引流不畅,形成充盈缺损区,使得CEUS表现为不均性增强,因此造成本研究中的假阳性;而癌栓阻塞淋巴管使造影剂不能顺利通过但癌组织尚未侵及前哨淋巴结也表现为假阳性。此外,目前许多未转移性前哨淋巴结因淋巴回流、淋巴结结构等原因也表现为不均匀性增强,具体机制仍有待临床深入研究,无增强的前哨淋巴结也应结合常规超声表现进行综合诊断,进一步提高诊断准确性。
综上所述,CEUS在乳腺癌术前行前哨淋巴结定位、定性诊断有良好效能,可指导手术探测淋巴管及前哨淋巴结,但特异度较低,Ⅱ型增强模式良恶性重叠,仍需考虑结合其他影像特征综合判断,提高诊断效能。
