CoFe2O4/CoFe2S4活化PMS性能及机理
2021-11-29赵缘园,张国权,杨凤林
赵 缘 园, 张 国 权, 杨 凤 林
( 大连理工大学 环境学院 工业生态与环境工程教育部重点实验室, 辽宁 大连 116024 )
0 引 言
抗生素,是指由微生物(包括细菌、真菌、放线菌属)或高等动植物在生活过程中所产生的具有抗病原体或其他活性的一类次级代谢产物,能干扰其他生活细胞发育功能的化学物质[1].其中,黄连素是一种常见的抗生素,又称盐酸小檗碱(berberine),分子式C20H18NO4,是一种具有多种药理学和生物学作用的异喹啉天然生物碱[2].黄连素对革兰氏阳性和阴性菌均有抑制作用,因此作为一种广谱抗菌性的抗生素被广泛使用,通常从草本植物中提取或通过化学方式合成[3].然而,生产或使用黄连素时会产生大量含残留黄连素的废水,如果直接排放,会杀死或抑制水体、土壤、沉积物中的有益微生物[4],导致环境的生态平衡遭到破坏,因此,从废水中去除这类生物难降解污染物具有重要的现实意义和紧迫性.

本文采用简单而温和的两步水热法制备尖晶石型钴铁复合硫化物催化剂(CoFe2O4/CoFe2S4).通过扫描电子显微镜(SEM)、透射电子显微镜(TEM)、X射线衍射(XRD)及X射线光电子能谱(XPS)等技术手段对催化材料的表观形貌、晶体结构和元素组成等进行表征.以黄连素为目标污染物,探究不同条件下CoFe2O4/CoFe2S4与PMS体系氧化降解黄连素的效果及动力学,考察CoFe2O4/CoFe2S4催化剂的重复利用性能,分析体系中产生的活性物种,揭示CoFe2O4/CoFe2S4活化PMS的机理.
1 实验部分
1.1 材料的制备
1.1.1 CoFe2O4的制备 取60 mL去离子水加入100 mL烧杯中,依次加入2 mmolCo(NO3)2·6H2O、4 mmol Fe(NO3)3·9H2O、17 mmol尿素和4 mmol NH4F,搅拌至均匀后,将烧杯中的溶液转入清洁干燥的100 mL反应釜,超声分散30 min后将反应釜转移至鼓风干燥箱中于120 ℃水热反应12 h.待温度降至室温后将材料取出,使用去离子水和无水乙醇将材料清洗干净,最后在60 ℃下干燥8 h,即可得到CoFe2O4.
1.1.2 CoFe2O4/CoFe2S4的制备 取配制的60 mL 10 mmol/L Na2S溶液至清洁干燥的反应釜中,然后加入1.0 g CoFe2O4,将反应釜转移至鼓风干燥箱于120 ℃水热反应8 h,降至室温后将材料取出,用去离子水和无水乙醇将材料清洗干净,60 ℃下干燥2 h,即可得到CoFe2O4/CoFe2S4.
1.2 表征分析
对CoFe2O4和CoFe2O4/CoFe2S4分别进行表征.用美国FEI公司的Quanta 450型场发射扫描电子显微镜(SEM)、Tecnai F30高分辨率透射电子显微镜(HRTEM)对材料的形貌进行表征,材料的晶体结构和物相组成分析采用日本理学制作所的D/max-2400 X射线粉末衍射仪,材料的元素组成和价态采用美国Thermo VG公司的ESCALAB 250 X射线光电子能谱仪,AlKα(1 486.6 eV)为电子辐射源,XPS谱图以C1s谱线(284.8 eV)为基准进行荷电效应校正.利用Gaussian/Lorentzian函数对XPS谱线进行分峰拟合.
1.3 黄连素的测定方法
黄连素的浓度采用紫外分光光度法进行测定[23].首先配制10 mmol/L黄连素溶液,使用紫外可见分光光度计在波长190~800 nm进行全波分析,确定黄连素的最大吸收波长.配制浓度分别为2、3、4、5、8、10、15、16和20 mmol/L的黄连素溶液,在最大吸收波长下测定不同浓度黄连素的吸光度,根据测定结果绘制标准曲线;在实验过程中每隔5 min取一次样,测定吸光度,根据已绘制的标准曲线,计算黄连素的去除率.采用准一级动力学模型来描述黄连素的氧化降解速率,其方程为
(1)
其中kobs为黄连素降解的表观速率常数,t为时间,c和c0分别为t时刻和初始时刻黄连素浓度.
1.4 反应条件优化实验
取200 mL初始浓度为10 mg/L的黄连素溶液放入烧杯中,在恒温水浴锅中进行恒温反应,分别投加PMS和制备的催化材料,每隔5 min取一次样,利用紫外可见分光光度计测定其吸光度.考察CoFe2O4/CoFe2S4投加量、PMS浓度、温度以及pH对黄连素降解效果的影响.
2 结果与讨论
2.1 材料的形貌及化学组成表征
图1(a)、(b)分别为CoFe2O4和CoFe2O4/CoFe2S4的SEM图.由图可见,CoFe2O4样品呈现片状交错排布的蜂窝形貌,而CoFe2O4/CoFe2S4显示出纳米片和纳米花颗粒混杂的形貌,这可能是由于硫化作用导致了第二相粒子偏析[21],在片层间隙形成了纳米颗粒.表1与表2是经EDS测出的元素种类(图1(c)、(d))及各元素的百分比,CoFe2O4中Co、Fe、O的元素比接近1∶2∶4,CoFe2O4/CoFe2S4中存在Co、Fe、O、S等元素且Co、Fe的元素比接近1∶2,表明在温和条件的硫化处理后成功合成出CoFe2O4/CoFe2S4催化材料.

(a) CoFe2O4的SEM图
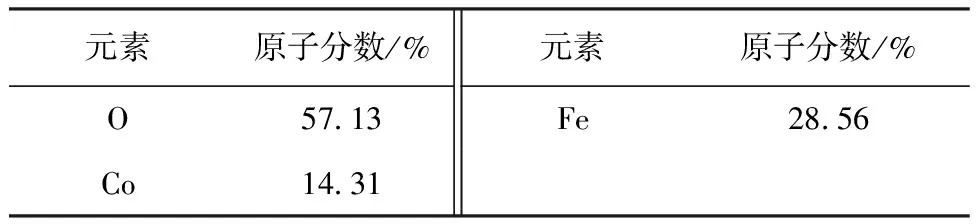
表1 CoFe2O4中EDS测出的元素比Tab.1 EDS measured element ratio in CoFe2O4

表2 CoFe2O4/CoFe2S4中EDS测出的元素比Tab.2 EDS measured element ratio in CoFe2O4/CoFe2S4
通过TEM进一步分析测试CoFe2O4和CoFe2O4/CoFe2S4样品的微观结构.由图2(a)、(b)可见,CoFe2O4呈形态不规则的纳米粒子形貌,而CoFe2O4/CoFe2S4由不规则的近似六边形多面体和四方形纳米片混合而成,内部CoFe2O4与外层CoFe2S4之间存在明显的边界.从图2(c)可以看出,CoFe2O4的晶格条纹间距为0.161、0.241 和0.297 nm,分别归属于CoFe2O4的(511)、(222)和(220)晶面[20].CoFe2O4/CoFe2S4样品HRTEM图(图2(d))中,CoFe2O4(220)晶面中心附近的晶格条纹间距为0.297 nm,而在纳米片的边缘部分,0.266 nm的晶格条纹间距[CoFe2S4(311)晶面]大于CoFe2O4(311)晶面的标准晶格间距(0.253 nm),这可能是由于经过硫化反应,原子半径较大的S原子取代了部分O原子而生成CoFe2S4,导致晶面间距增大.此外,CoFe2O4和CoFe2O4/CoFe2S4的选区电子衍射(SAED)图(图2(c)、(d)插图)呈现连续的衍射环,这与样品的多晶面特性一致.

(a) CoFe2O4的TEM图
图3是CoFe2O4和CoFe2O4/CoFe2S4的XRD谱图.CoFe2O4在18.32°、30.14°、35.44°、37.14°、43.12°、53.62°、57.06°、62.64°和74.23°显示出较强衍射峰,对应CoFe2O4(JCPDS #22-1086)的(111)、(220)、(311)、(222)、(400)、(422)、(511)、(440)、(533)晶面[19].CoFe2O4/CoFe2S4的XRD衍射峰为18.30°、30.14°、35.46°、37.10°、43.10°、53.54°、57.00°、62.62°和74.08°,与CoFe2O4的谱图基本一致,但衍射峰位置略向低角度偏移.这一结果表明,在CoFe2O4/CoFe2S4硫化过程中,尽管部分半径较小的O原子被半径较大的S原子替换,但产物中没有形成杂质相(如Fe或Co的硫化物),这种取代只轻微影响晶格参数,但未改变产物的晶体结构[20-21].为了进一步进行验证,将CoFe2O4/CoFe2S4的XRD谱图与标准卡片FeS2(JCPDS #42-1340)
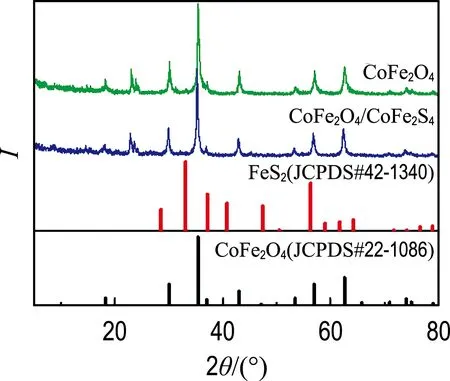
图3 CoFe2O4和 CoFe2O4/CoFe2S4的XRD谱图Fig.3 XRD patterns of CoFe2O4 and CoFe2O4/CoFe2S4
进行比对,发现CoFe2O4/CoFe2S4特征峰的位置较FeS2特征峰的位置向高角度偏移,这可能是由于半径较小的Co原子取代Fe原子而产生了CoFe2S4[21]。
材料表面的化学性质对其催化性能有显著影响,为此,进行XPS分析以了解CoFe2O4和CoFe2O4/CoFe2S4催化剂的元素组成和化学键合状态.如图4(a)所示,通过高斯拟合,Co2p的高分辨率XPS谱图在结合能为797.3、781.6 eV处呈现Co2p1/2和Co2p3/2峰,而在结合能为804.0、787.4 eV处出现两个卫星峰,归因于微量的Co3+[21,24-25].此外,Co2p1/2与Co2p3/2的自旋轨道分裂(两峰的结合能差)约为15.7 eV,表明两催化剂中Co2+和Co3+同时存在.Fe2p的XPS谱图(图4(b))中,结合能为712.1和725.1 eV的两个主峰分别对应于Fe2p3/2和Fe2p1/2,表明存在Fe3+及少量的Fe2+[20,25-26].以上结果证实两催化剂中存在以Fe3+和Co2+为主的不同价态的Fe(Fe2+/Fe3+)和Co(Co3+/Co2+)元素.O1s的XPS谱图(图4(c))中,OA表示吸附在催化剂表面上的水分子所形成的表面氧基团(OH-),OB表示催化剂中存在的金属-氧键(O2-)[24,27].图4(d)中CoFe2O4/CoFe2S4的S2p1/2峰位于162.2 eV处,表现为金属-硫键(S2-),S2p3/2峰位于161.1 eV处,这可能与低配位硫离子的存在有关[16-17,22-23].综上表征结果可知,CoFe2O4/CoFe2S4催化剂中含有Co2+/Co3+、Fe2+/Fe3+、O2-和S2-,证实CoFe2O4/CoFe2S4的成功合成.
2.2 CoFe2O4/CoFe2S4对PMS的活化性能及条件优化
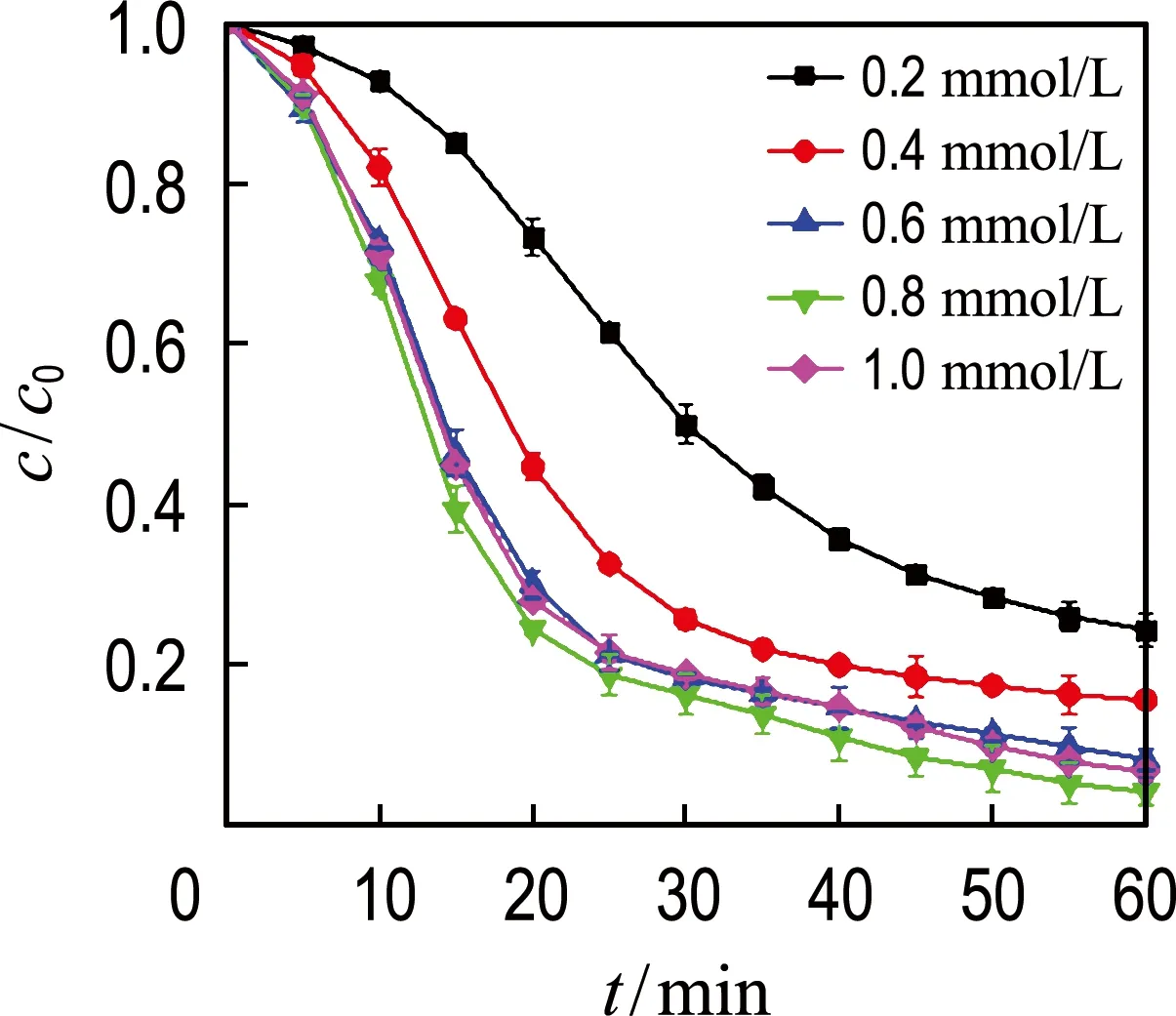
为评估CoFe2O4与CoFe2O4/CoFe2S4活化PMS的性能,首先考察PMS、CoFe2O4@PMS、CoFe2O4/FeS2@PMS与CoFe2O4/CoFe2S4@PMS不同体系对黄连素的降解效果.如图5所示,在pH为7.0、PMS浓度为1.0 mmol/L、催化剂投加量为1.0 mg/L的条件下,单PMS体系60 min 内对黄连素(10 mg/L)的去除率为7.6%,对比之下,CoFe2O4@PMS、CoFe2O4/FeS2@PMS和CoFe2O4/CoFe2S4@PMS体系降解黄连素的效果明显,CoFe2O4/CoFe2S4@PMS体系在60 min 内对黄连素的去除率最高,为98.4%.从表观速率常数来看,kobs分别为0.054 9、0.053 4和0.067 6 min-1,说明上述催化剂均能有效活化PMS,且降解速率较快.硫化后所得CoFe2O4/CoFe2S4的催化性能高于CoFe2O4的原因可能是:①O2-具有较大的电负性,而半径较大的S2-取代部分O2-后,可通过改变电荷密度和引入不对称的电子分布来增强CoFe2O4/CoFe2S4的催化活性[16,28];②S的d轨道很容易被极化,易与PMS分子吸附和相互作用[16],从而增强了CoFe2O4/CoFe2S4@PMS体系的氧化降解能力.

(a) Co2p

(a) 降解效率


(a) 降解效率
CoFe2O4/CoFe2S4@PMS体系的催化剂投加量(0.2~2.0 mg/L)在pH为7.0、温度为40 ℃、PMS浓度为0.8 mmol/L的条件下对黄连素去除率的影响如图7所示.随着CoFe2O4/CoFe2S4用量从0.2 mg/L增加到1.0 mg/L,黄连素的去除率不断提高,表明CoFe2O4/CoFe2S4能够有效激活PMS去除黄连素,这是由于提高催化剂用量不仅增加体系中的表面催化活性位点,而且会直接增加CoFe2O4/CoFe2S4与PMS之间的接触,产生更多的活性物种[19,27].当CoFe2O4/CoFe2S4的用量增加到1.5和2.0 mg/L时,黄连素的去除率并无明显增加,说明1.0 mg/L CoFe2O4/CoFe2S4催化剂表面的活性位点足以满足活化0.8 mmol/L PMS的需要.

(a) 降解效率
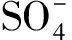
(a) 降解效率
溶液温度强烈影响CoFe2O4/CoFe2S4@PMS体系氧化降解黄连素的效果.在pH为7.0、PMS浓度为0.8 mmol/L、催化剂用量为1.0 mg/L 条件下,溶液温度对氧化降解黄连素的影响如图9所示,随着温度从20 ℃升高到40 ℃,降解效率不断增强,kobs从0.031 2 min-1升高到0.068 1 min-1,而当温度为40 ℃时,在不添加CoFe2O4/CoFe2S4催化剂的情况下,黄连素几乎无降解,说明40 ℃温度下不能有效地活化PMS,因此,CoFe2O4/CoFe2S4@PMS体系起主要活化作用的是活性组分CoFe2O4/CoFe2S4,温度对反应的影响可能主要来源于高温有利于PMS中O—O键的断裂[31].这里,用Arrhenius方程描述准一级反应表观速率常数kobs与温度的关系[32]:
(2)
式中:Ea为活化能,R为通用气体常数(8.314 J·mol-1·K-1),A为常数.通过绘制lnkobs-1 000/T图,可以得到CoFe2O4/CoFe2S4@PMS体系氧化降解黄连素的活化能.利用图10的斜率值可计算得到Ea=33.73 kJ/mol,低于在黄连素浓度为10 mg/L、CoFe2O4/CoFe2S4投加量为1.0 mg/L、PMS浓度为0.8 mmol/L、pH为7.0、温度为40 ℃条件下,通过连续氧化降解黄连素实验来评价CoFe2O4/CoFe2S4催化剂的可循环性和稳定性.为了减少催化剂的质量损失,将使用过的催化剂用蒸馏水和乙醇洗涤,然后在80 ℃烘箱中干燥1 h,以相同的用量加入下一个循环.如图11所示,在60 min的处理过程中,3个循环的去除率从98.4%下降到91.1%.反应60 min后,3次实验后溶液中可检测到溶出Fe离子浓度分别为0.025、0.022、0.017 mg/L,溶出Co离子浓度分别为0.021、0.018、0.016 mg/L,在降解实验中Fe、Co溶出率不高.而黄连素去除率降低的原因可能是在反应过程中,由于机械搅拌作用,部分CoFe2O4/CoFe2S4损失以及催化剂的一部分反应位点被黄连素占据,降低了CoFe2O4/CoFe2S4催化PMS的活性.

(a) 降解效率
Fe2O3[33]、负载型钴氧化物[34-35]和CuCo2S4[15]活化PMS的活化能,表明CoFe2O4/CoFe2S4在温和的环境温度下是一种优异的PMS催化剂.
2.3 CoFe2O4/CoFe2S4稳定性测试
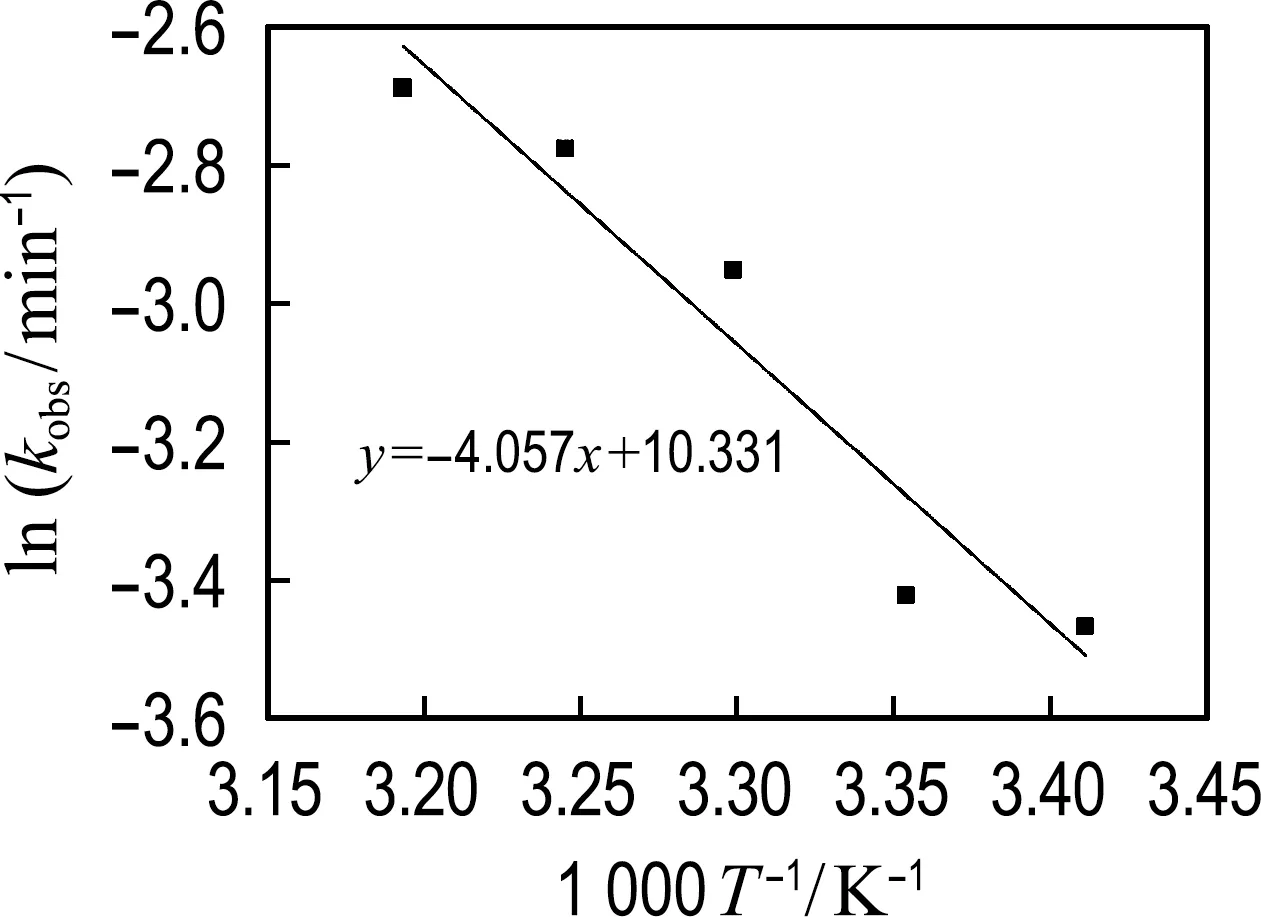
图10 ln kobs-1 000/T图Fig.10 Graph of ln kobs vs. 1 000/T

图11 CoFe2O4/CoFe2S4 @PMS体系去除黄连素可循环性实验Fig.11 Recyclability test of CoFe2O4/CoFe2S4@PMSsystem for berberine removal
2.4 CoFe2O4/CoFe2S4@PMS体系中活性物种的鉴定及活化机理


图12 以DMPO为捕获剂的PMS体系和CoFe2O4/CoFe2S4@PMS体系的EPR谱图

图13 叔丁醇和乙醇自由基淬灭剂对CoFe2O4/CoFe2S4@PMS体系中黄连素降解的影响
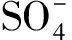
(3)
(4)
(5)

(6)
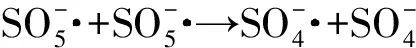
(7)
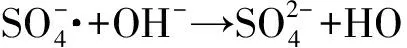
(8)
(9)
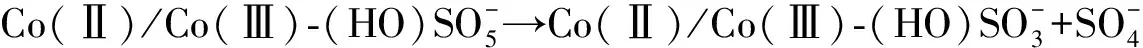
(10)
(11)
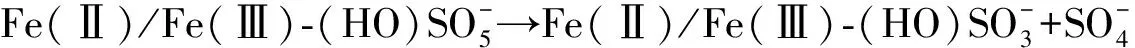
(12)
3 结 语
本文通过简单而温和的两步水热法成功制备出尖晶石型钴铁复合硫化物催化剂CoFe2O4/CoFe2S4,通过SEM、TEM、XRD及XPS等技术手段对催化材料的表观形貌、晶体结构和元素组成等进行表征,证实了CoFe2O4/CoFe2S4的成功合成.
构建CoFe2O4/CoFe2S4与PMS体系用以氧化降解黄连素,考察体系降解黄连素效果及动力学,得出最优降解条件.另外,本文考察了CoFe2O4/CoFe2S4催化剂的重复利用性能;利用EPR分析体系中产生的活性物种,确定自由基种类,进行自由基抑制剂实验进一步确定体系中的自由基及自由基的贡献.
经过实验探究及思考,本研究还存在不足之处.本文所用的黄连素废水是实验室模拟黄连素废水,而在实际抗生素废水中,成分多样,污染物种类繁多,对降解效果有一定的影响,希望可以对实际抗生素废水进行降解并进行探究.
