牛乳蛋白与淀粉相互作用的研究进展
2021-11-23侯佳曼李丹丹韩永斌
侯佳曼,李丹丹,*,崔 波,陶 阳,韩永斌
(1.南京农业大学食品科技学院,江苏南京 210095;2.齐鲁工业大学(山东省科学院)生物基材料及绿色造纸国家重点实验室,山东济南 250353)
淀粉是人类膳食的主要营养成分和能量来源[1]。淀粉基食品的感官品质和营养价值主要取决于淀粉在加工过程中其结构包括分子结构和颗粒结构以及理化性质包括糊化性质、流变学特性和消化性质等的变化。蛋白质作为食品中的主要成分,一方面可与淀粉分子交缠形成凝胶或相分离,改变食品质构和口感;另一方面,可覆盖于淀粉表面,限制淀粉酶降解淀粉,从而减缓人体餐后的血糖上升速率[2−4]。添加牛乳蛋白可以改善淀粉基食品如面包、馒头等的感官品质[5]。淀粉作为一种低成本的添加剂如增稠剂、稳定剂等亦被广泛用于改善干酪、酸奶等乳制品的质构和稳定性等[3,6−7]。因此,明晰淀粉和牛乳蛋白之间的相互作用机制,对改善两种成分共存食品品质的意义重大。
刘晓明等[8]于2012 年对淀粉和牛乳蛋白相互作用的研究进行了初步的归纳总结,综述了国内外学者关于牛乳蛋白/淀粉混合物的糊化和流变学特性的研究。但是,其报道未涉及淀粉与牛乳蛋白之间的相互作用机制以及牛乳蛋白对淀粉消化性质影响的报道。近5 年来,随着科学技术的进步、研究手段的增加以及人们健康意识的提高,国内外研究者们对淀粉与牛乳蛋白间的相互作用力以及蛋白与淀粉消化性质的相关性进行了深入而广泛的研究[9−11]。因此,重新对淀粉和牛乳蛋白相互作用的研究进展进行综述具有必要性。本文综述了淀粉和牛乳蛋白之间相互作用机制、牛乳蛋白对淀粉的热性质、流变学特性和消化性质影响规律的研究进展,旨在为食品品质的改良以及新型功能型食品的开发提供理论指导。
1 牛乳蛋白和淀粉相互作用方式的研究进展
天然淀粉是由支链淀粉分子和直链淀粉分子通过氢键相互作用有序排列形成的,呈不溶于冷水的颗粒态结构[12]。颗粒态淀粉在加热过程中会吸水溶胀,颗粒结构被破坏,支链淀粉和直链淀粉分子溶出,分子间氢键被打断,呈无序的分子态形式[12]。牛乳蛋白的主要成分是酪蛋白和乳清蛋白,其中酪蛋白占总蛋白含量的80%[13]。牛乳蛋白在氢键、静电相互作用、疏水相互作用和范德华力的共同作用下可吸附在淀粉颗粒的表面、与淀粉分子链缠结,或由于生物大分子的热不兼容性与淀粉分子发生相分离现象,从而改变淀粉的糊化、回生和流变学性质[3,14−15]。
1.1 牛乳蛋白与淀粉颗粒的吸附作用
牛乳蛋白可吸附于淀粉颗粒表面,且研究者们普遍认为淀粉颗粒和蛋白之间的主要作用力为疏水相互作用,氢键与范德华力亦参与其中(图1a)。Noisuwan 等[9]利用激光共聚焦显微镜观察到酪蛋白酸钠和乳清分离蛋白可吸附在普通和蜡质大米淀粉颗粒表面。Xu 等[16]利用色谱法和分子模拟研究发现,大米蛋白和直链淀粉间可自发地结合,且主要驱动力为疏水相互作用。淀粉颗粒在加热膨胀过程中,表面吸附的蛋白分子一方面限制水分进入颗粒内部,另一方面可能与淀粉颗粒糊化过程中泄露的直链淀粉分子竞争水分或发生相互作用,从而改变淀粉的糊化和回生性质[3,9]。此外,蛋白覆盖在淀粉颗粒的表面,可限制口腔中淀粉酶与淀粉的接触,减慢淀粉消化速率[17]。随着人们生活节奏的加快、膳食构成的改变,糖尿病、肥胖症、高血压等胰岛素抵抗相关的代谢综合症比例不断提升。慢消化淀粉不仅可维持餐后血糖稳态,改善葡萄糖耐量,而且可降低餐后胰岛素分泌,提高机体对胰岛素的敏感性[18]。因而,利用淀粉和蛋白间的相互作用制备慢消化淀粉已成为近年来的研究热点。
1.2 牛乳蛋白与淀粉分子的凝胶作用
蛋白和淀粉分子可在一定条件下相互作用形成混合凝胶(图1b),从而赋予共混体系一些独特的性质,如改善产品的流变学特性等。刘晓明[7]研究发现,酸奶中的酪蛋白可通过静电作用吸附于羟丙基二淀粉磷酸酯表面,形成表面带正电荷的大聚集体,该聚集体可与酪蛋白聚集体通过静电排斥维持酸奶体系的稳定。实际上,羧甲基淀粉、辛烯基琥珀酸淀粉酯、淀粉磷酸酯和乙酰化二淀粉己二酸等带电荷的变性淀粉分子,均可通过静电力、氢键和范德华力的共同作用与蛋白分子相互缠连,形成稳定的凝胶,从而改善产品的冻融稳定性和流变学特性[6−7,14,19]。其中,静电相互作用是形成稳定凝胶的关键[4,20]。但是,天然的淀粉分子通常不带电,与蛋白分子间主要通过氢键形成不稳定的凝胶,二者间无共价键形成[21]。Zeng 等[22]利用红外光谱仪研究玉米醇溶蛋白、面筋蛋白、大豆蛋白和菜籽蛋白等与天然玉米淀粉分子间的相互作用时发现,红外谱图中没有新的特征峰出现但羟基峰的位置向低波数方向移动,说明不带电淀粉与蛋白间的主要作用力为氢键,二者间没有形成新的化学键。蛋白与天然淀粉分子间的相互作用会影响淀粉分子链的重排,改变淀粉的回生性质[23]。
1.3 牛乳蛋白与淀粉分子的相分离现象
相分离是属于物理学、化学及工程学中的基本概念,即同类物质间存在相互聚集或分离的“力”,有助于同类物质的快速聚集或解离[24]。对于牛乳蛋白和淀粉分子的混合体系而言,Noisuwan 等[25]研究发现,在淀粉糊化的后期,随着淀粉颗粒的破碎,直链淀粉逐渐溶出,牛乳蛋白首先与淀粉分子相互缠结,形成不稳定的凝胶,之后随着温度的降低,蛋白分子聚集,与淀粉分子间发生相分离。图1c 显示了淀粉和牛乳蛋白的相分离现象,亮光部分为蛋白质聚集体,黑暗部分为淀粉聚集体。淀粉分子和蛋白之间的相分离现象通常认为是大分子间的结构不一致性导致的。Vu Dang 等[26]在研究乳清蛋白/天然蜡质玉米淀粉混合物过程中观察到的蛋白质聚集体直接证实了相分离现象的存在。与其它多糖/蛋白体系相比,淀粉/牛乳蛋白体系发生相分离所需浓度通常更高。Olsson 等[27−28]发现,当β-乳球蛋白浓度为6%时,只有马铃薯支链淀粉浓度超过0.75%后,蛋白/淀粉凝胶网络才会发生相分离。变性淀粉通常可通过静电相互作用与牛乳蛋白形成稳定的凝胶,但在不合适的加工和贮藏条件下,凝胶的稳定性会降低,亦可能发生相分离[6]。

图1 淀粉与牛乳蛋白相互作用示意图[9,29]Fig.1 Schematic diagram of interactions between starch and milk protein[9,29]
2 牛乳蛋白对淀粉流变学特性影响的研究进展
2.1 酪蛋白对淀粉流变学特性的影响
淀粉悬浮液的流变学特性取决于溶胀淀粉颗粒所占的体积分数[3]。淀粉糊化是淀粉和水的悬浮液加热到一定程度淀粉颗粒吸水溶胀、破裂形成淀粉糊的过程。因此,淀粉糊化性质与流变学特性紧密相关。淀粉的糊化一般包括三个阶段,即可逆吸水阶段、不可逆吸水阶段和颗粒解体阶段[1]。酪蛋白通过疏水相互作用吸附于淀粉颗粒表面后,淀粉膨胀受限、糊化起始温度增加[9],但依然包括三个阶段(图2):第一阶段即可逆吸水阶段,淀粉颗粒分散于牛乳蛋白溶液中并发生轻微的膨胀,且此时的膨胀是可逆的。此阶段,由于淀粉颗粒表面和牛乳蛋白之间的疏水相互作用和氢键的存在,部分牛乳蛋白吸附于淀粉颗粒表面[9]。第二阶段即不可逆吸水阶段,随着温度的继续升高,大量的水分渗入淀粉颗粒内部,导致淀粉颗粒的剧烈膨胀。然而此阶段,体系中的部分淀粉颗粒在吸水膨胀过程中被牛乳蛋白或者牛乳蛋白-淀粉分子缠结物粘附甚至包裹住,覆盖于淀粉颗粒表面的这一层聚合物与淀粉竞争水分,并造成这部分淀粉颗粒的膨胀和糊化受到抑制,起始糊化温度增加[3−4]。第三阶段即颗粒解体阶段,牛乳蛋白一部分通过氢键吸附在淀粉颗粒的外表面,一部分则与渗漏出来的可溶性淀粉分子缠结在一起并逐步包裹在淀粉表面,在抑制淀粉颗粒吸水膨胀的同时,也阻止了淀粉颗粒的破裂,从而导致淀粉糊的峰值黏度发生变化,且黏度的变化与牛乳蛋白的添加量以及淀粉的来源有关[30]。淀粉完全糊化后,从膨胀淀粉颗粒中溶出的淀粉分子可与牛乳蛋白相互作用首先形成均匀的混合物,但之后由于生物大分子间的热不兼容性,牛乳蛋白相互聚集发生相分离,亦会影响体系的流变学特性。酪蛋白对淀粉糊化过程的影响与亲水胶体类似[31]。
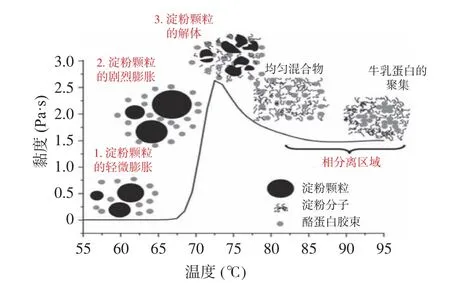
图2 酪蛋白对淀粉糊化过程的作用示意图[25]Fig.2 Schematic diagram of the effects of casein on starch pasting[25]
酪蛋白可吸附于淀粉颗粒表面或与糊化淀粉分子发生相分离,从而影响淀粉的流变学特性,但该影响与蛋白的添加量以及淀粉的来源相关。即使添加极少量的酪蛋白酸钠(<0.1%)也会影响淀粉悬浮液的糊化行为[9]。但是,酪蛋白添加量不同,对淀粉的流变学特性尤其是淀粉糊黏度有显著不同的影响[3,25]。一般地,低浓度酪蛋白会引起淀粉糊黏度的降低,而高浓度会导致黏度的增加。例如,添加10%的酪蛋白酸钠会引起普通大米淀粉峰值黏度的增加,但低浓度添加量(2.5%)时,淀粉糊的黏度降低[32]。淀粉来源不同,其分子结构以及磷酸基团含量不同,与酪蛋白间的相互作用力存在差异。蜡质淀粉中直链淀粉含量较少,与蛋白作用形成凝胶的强度比普通淀粉和高直链淀粉小,因而酪蛋白对蜡质淀粉流变学性质的影响通常更小[25]。对于玉米淀粉、小麦淀粉、木薯淀粉等磷酸基团含量较少的天然淀粉而言,添加酪蛋白酸钠会显著降低淀粉糊中溶胀颗粒的体积分数以及连续相中溶解的淀粉分子,从而导致淀粉的膨胀和溶解受限[9,33]。然而,马铃薯淀粉颗粒中含有的大量磷酸基团可与酪蛋白酸钠发生静电相互作用,该作用的影响远大于淀粉与酪蛋白之间的相互作用,导致酪蛋白对其流变学特性的影响与其他淀粉存在差异。Bertolini 等[30]研究发现添加酪蛋白酸钠会导致木薯、玉米和小麦淀粉凝胶存储模量和黏度的提高,但马铃薯淀粉呈相反变化。通过光学显微镜观察发现马铃薯淀粉和酪蛋白酸钠形成的复合物体系较其他淀粉来说分布更均匀。Kelly 等[34]比较了酪蛋白酸钠对马铃薯淀粉和玉米淀粉流变学性质的影响,结果表明少量酪蛋白酸钠的吸附即可显著降低淀粉糊的黏度;但在低水平电解质的情况下,由于马铃薯淀粉中磷酸基团含量较高,其黏度的降低主要是由非特异性离子效应导致的。对于带电的变性淀粉来说,与马铃薯淀粉类似,可与酪蛋白通过静电相互作用力形成稳定的凝胶,从而改善酸奶的贮藏稳定性和稠度[6−7]。
2.2 乳清蛋白对淀粉流变学特性的影响
虽然乳清蛋白也可通过疏水相互作用吸附于淀粉颗粒的表面,从而限制水分进去颗粒内部,抑制其膨胀[9],但是乳清蛋白往往是通过影响淀粉-蛋白凝胶网络的形成来进一步影响淀粉基食品的流变学特性的[3]。乳清蛋白和淀粉经加热处理后可形成凝胶。两者混合物形成的凝胶连续相,既可以是单独的蛋白质网络、淀粉网络,也可以是由淀粉和乳清蛋白相互穿插形成的混合网络[3]。图3 为乳清蛋白与木薯淀粉形成凝胶的过程示意图。加热前淀粉颗粒分散在乳清蛋白溶液中(图3a)。随着温度的增加,淀粉颗粒糊化,乳清蛋白发生热变性,之后两者通过疏水相互作用和静电相互作用形成混合凝胶,体系弹性模量增加(图3b)。乳清蛋白-天然木薯淀粉(WPINTS)混合凝胶由不连续的淀粉凝胶和蛋白凝胶组成;乳清蛋白-乙酰化木薯淀粉(WPI-ATS)、乳清蛋白-羟丙基木薯淀粉(WPI-HPTS)以及乳清蛋白-交联木薯淀粉(WPI-CLTS)混合凝胶则呈现为乳清蛋白连续凝胶中穿插着少许的糊化淀粉颗粒片段(图3c)。

图3 乳清蛋白与木薯淀粉形成凝胶的示意图[35]Fig.3 Schematic diagram of gel formation of whey protein and tapioca starch[35]
淀粉/蛋白比例、pH、盐浓度、离子类型以及淀粉的来源和性质均会影响乳清蛋白/淀粉凝胶网络的性质。当淀粉/乳清蛋白比例较大时(淀粉浓度>50%),乳清蛋白作为惰性填料会使得淀粉被稀释,且乳清蛋白和淀粉通过非共价键结合限制了淀粉分子之间氢键的作用,从而弱化玉米淀粉凝胶弹性并提高其黏性[2,17,25,36]。当淀粉/乳清蛋白比例较小时,淀粉会阻碍乳清蛋白的热变性或者由于生物大分子的热不兼容性质发生相分离,从而影响混合凝胶的性质[37−38]。乳清蛋白只有在特定的pH 条件下才可形成稳定的凝胶。程鹏等[39]发现分离乳清蛋白与甘薯淀粉混合凝胶的硬度和溶解度均会随着pH 的增大而减小。Shim 等[40]对分离乳清蛋白和玉米淀粉的混合凝胶的研究也指出,pH 对乳清蛋白-玉米淀粉凝胶的形态和流变特性有着重要影响。盐浓度和离子类型不同,乳清蛋白-淀粉混合凝胶的结构和硬度均不同。程鹏[41]发现随着盐浓度的增加,混合凝胶的硬度成上升趋势;不同的离子,如Na+和Ca2+,会使混合凝胶的细微结构分别呈现多孔网状和颗粒状两种不同的状态,并且由于价态不同,它们还会对蛋白质分子间的静电作用产生不同影响,前者可以降低静电排斥使蛋白溶解度小幅度下降,后者可以有效屏蔽静电作用,促进蛋白质分子聚合。与其他淀粉不同,马铃薯淀粉具有磷酸基团,在与乳清蛋白共存时,马铃薯淀粉的类型和浓度会影响乳清蛋白的聚集。Olsson 等[28]发现高黏度的马铃薯支链淀粉对β-乳球蛋白具有剪切稀化作用,而高浓度的马铃薯支链淀粉的增加会使得β-乳球蛋白形成的聚集体结构更紧密,相分离现象更显著,从而导致体系储能模量和断裂应力的变化。对于变性淀粉如交联蜡质玉米淀粉和辛烯基琥珀酸淀粉酯来说,可与乳清蛋白通过静电相互作用形成较稳定的凝胶从而显著改变其流变学特性,且体系的粘弹性行为的变化与乳清蛋白浓度和pH 等因素有关[14,26,42−43]。
3 牛乳蛋白对淀粉消化性质影响的研究进展
淀粉在消化酶的作用下可转化为葡萄糖为人体提供能量,但淀粉快速消化引起的血糖升高对人体健康不利。目前,已有物理、化学和生物等多种方法被用于降低淀粉的消化性[44]。蛋白质作为食品中的天然成分,具有安全、健康、营养等特征,其与淀粉间的相互作用亦可用于降低淀粉的消化性。蛋白质主要通过以下作用影响淀粉的消化性:第一,蛋白质的物理屏障作用(图4a)。蛋白质可作为一种物理屏障,通过疏水相互作用和氢键的作用包裹在淀粉颗粒表面,从而限制酶对底物淀粉的水解[45]。杨翠红等[2,17]研究发现乳清蛋白网络可包裹淀粉颗粒,形成抵抗酶解的物理屏障。Zou 等[46]利用共聚焦显微镜染色观察意大利面微观结构,发现小麦蛋白形成连续的面筋网络包裹小麦淀粉颗粒,从而降低了面条淀粉消化性。第二,淀粉消化酶对蛋白质的非催化性结合(图4a)。淀粉酶能够结合蛋白质,从而部分地隔离其对淀粉的水解作用。Yu 等[47]提取分离大麦粉中的盐溶性蛋白和水溶性蛋白组分,结果发现水溶性蛋白通过结合α-淀粉酶降低消化体系酶活,降低大麦淀粉的水解。杨翠红等[2,17]发现乳清蛋白水解物可抑制葡萄糖苷酶的活性并增强淀粉和蛋白质间的非极性相互作用,从而显著降低淀粉的消化性。第三,蛋白质对糊化淀粉分子重结晶过程的抑制作用(图4b)。牛乳蛋白的添加可稀释糊化淀粉体系,阻碍淀粉分子间重新排列形成有序结构[48]。Yong 等[10]研究添加乳清分离蛋白的小麦淀粉挤出物的理化性和消化性,结果表明蛋白质稀释淀粉-水相,阻碍了淀粉分子的聚结和重结晶,降低淀粉消化率和血糖负荷值。但值得注意的是,马铃薯淀粉带有较多的磷酸基团,可与蛋白发生较强的静电相互作用,促进支链淀粉在冷却过程中的重结晶,从而促进了抗性淀粉的形成[23]。现有的研究多集中于乳清蛋白对淀粉消化性的影响,酪蛋白对淀粉消化性影响尚未见报道。
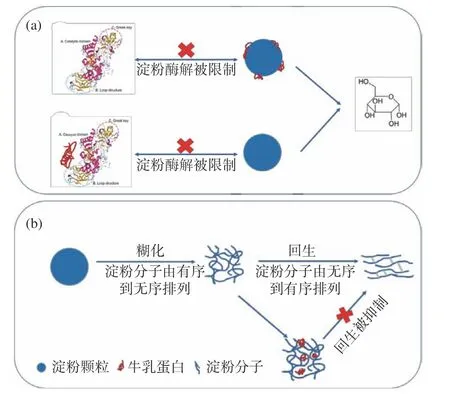
图4 牛乳蛋白影响淀粉消化性质的作用机理示意图Fig.4 Schematic diagram of the mechanism of the effect of milk protein on starch digestion properties
4 结论与展望
牛乳蛋白可通过疏水相互作用吸附于淀粉颗粒的表面,抑制淀粉吸水膨胀和淀粉酶的降解作用,从而改变其热特性、流变学性质和消化性质。变性淀粉分子(带电)、马铃薯淀粉(磷酸基团含量高)与牛乳蛋白尤其是乳清蛋白间存在较强的静电相互作用,可形成稳定的凝胶,体系弹性模量增加。但是,由于生物大分子的热力学不兼容性,天然淀粉(不带电)和牛乳蛋白形成的凝胶不稳定,在冷却过程中,牛乳蛋白之间相互聚集,导致相分离现象,影响淀粉分子链的重排,即淀粉的回生;变性淀粉、马铃薯淀粉与牛乳蛋白形成的稳定凝胶在不适宜的条件下强度会降低,亦可发生相分离现象。目前,国内外关于淀粉和牛乳蛋白相互作用方面的研究已取得较大进展。但是,现有的研究报道主要集中于牛乳蛋白对淀粉糊化和流变学特性的研究,许多方面仍未得到解决。例如,牛乳蛋白与淀粉颗粒表面、牛乳蛋白与淀粉分子间作用力的差异尚不能完全明确;添加牛乳蛋白有时会增加淀粉糊的黏度有时却会使其降低,其中的缘由不明;牛乳蛋白尤其是酪蛋白对淀粉回生性质和消化特性影响的报道还较少。此外,当两种复杂的系统如淀粉和牛乳多成分混合在一起时,相互作用的范围很大。混合系统的物理化学性质取决于它们的相对浓度以及淀粉和牛乳成分的物理化学性质,而牛乳体系成分复杂、影响因素较多,更是增加了研究的难度。因此,为了促进含牛乳蛋白和淀粉新产品的开发与品质的改良,在今后的研究中,不仅需对淀粉与单一牛乳蛋白间的相互作用机理进行进一步探究,还需以富含淀粉和牛乳蛋白的真实食品体系为对象,深入研究牛乳蛋白改变淀粉基食品品质的规律。
