纳武利尤单抗致不良反应的文献分析
2021-11-22何新荣辛海莉解放军总医院医疗保障中心药剂科北京00853重庆医科大学重庆40006
包 涓,卿 磊,何新荣,辛海莉(.解放军总医院医疗保障中心药剂科,北京 00853;.重庆医科大学,重庆 40006)
纳武利尤单抗于2018年6月在中国获批上市,为中国首个批准上市的程序性死亡受体1(programmed death receptor 1,PD-1)抑制剂,作为一种抗肿瘤免疫治疗药物,其与化疗药相比,在多种肿瘤的治疗中显现出疗效好、安全性高的优势[1],但由于该药进入我国时间不长,缺乏安全性经验,临床对其不良反应(adverse drug reaction,ADR)的认识还不充分,笔者通过检索国内外纳武利尤单抗致ADR病例并进行分析,以期探讨该药所致ADR发生的特点和规律,为临床合理用药提供参考。
1 资料与方法
1.1 资料来源
检索中国知网、万方、维普、PubMed、Web of Science数据库,中文以“纳武利尤”、“纳武利尤单抗”、“不良反应”等为检索词,英文以“Nivolumab”、“adverse drug reaction”、“side effect”等为关键词,检索2018年6月 - 2021年1月关于纳武利尤单抗致ADR的文献报道。纳入标准:病历资料齐全、明确纳武利尤单抗与ADR的相关性。排除标准:重复文献、综述、文献信息不完整、临床试验研究。纳入符合条件的文献73篇(中文文献14篇,英文文献59篇),共涉及79例患者。
1.2 方法
对纳入分析的病例用Excel建立病例数据库,将患者一般情况(性别、年龄、原发疾病等)、用药情况(用药剂量、周期等)、ADR发生情况(发生时间、症状等)、临床处理及转归等信息进行整理和统计分析。按照新版WHO-ART术语集对ADR累及系统/器官进行分类,并统计相应临床表现例次。
2 结果
2.1 性别及年龄分布
79例患者中,男性57例(72.15%),女性22例(27.85%),年龄为25 ~ 93岁,平均年龄(65.41±11.70)岁,详见表1。
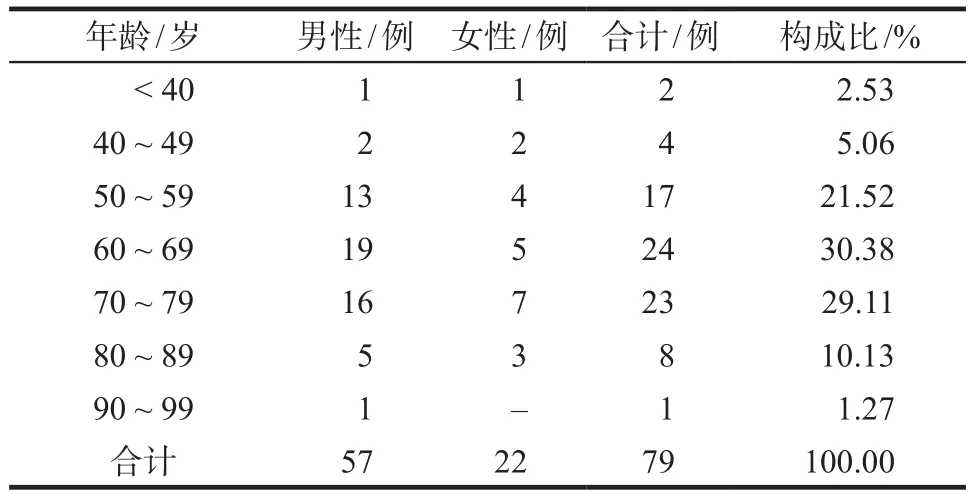
表1 患者性别和年龄分布Tab 1 Distribution of gender and age in patients
2.2 原患疾病及用药剂量
使用纳武利尤单抗治疗的患者中,肺癌患者最多(41.77%),其次为肾癌(18.99%)、黑色素瘤(13.92%)、头颈癌(10.13%)、肝癌(6.33%)、胃癌/食管癌(3.80%)以及结肠癌、膀胱移行细胞癌、子宫内膜癌和胸膜间皮瘤各1例。本研究中符合国内批准适应证40例,超美国批准适应证用药1例(治疗子宫内膜癌)。其中72例患者用药符合药品说明书推荐剂量(3 mg·kg-1或240 mg,q 2 w);6例低于说明书推荐剂量(2 mg·kg-1,q 3 w);1例高于说明书推荐单次用药剂量(480 mg,q 4 w)。
2.3 ADR发生时间
79例患者中,发生ADR的时间最短为输注后约10 min;免疫相关性不良反应最短出现在用药后第4天,最长出现在用药后23个月,多发生于用药后6个月内(74.69%),详见表2。
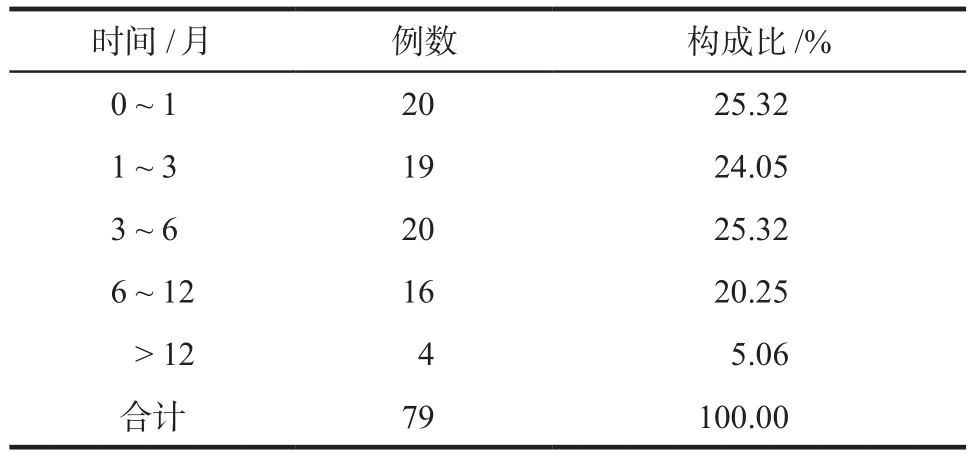
表2 ADR发生时间分布Tab 2 Time distribution of adverse drug reaction
2.4 ADR累及系统/器官及临床表现
79例ADR累及多个系统/器官,共计87例次,主要涉及皮肤及其附件损害、内分泌系统、消化系统和神经系统,详见表3。

表3 ADR累及系统/器官及主要临床表现Tab 3 Systems/organs involved in ADR and major clinical manifestations
2.5 ADR的处理及转归
79例患者经停药和(或)对症治疗后好转或痊愈75例,死亡4例。其中67例给予不同剂型和剂量的糖皮质激素治疗,63例好转或痊愈,4例死亡;9例给予替代激素治疗(左甲状腺素、胰岛素)好转;3例未给予治疗,停药后好转。好转后,再次给予纳武利尤单抗治疗16例,不良反应再次出现1例。
3 讨论
PD-1抑制剂相关不良反应包括免疫相关不良事件(immune-related adverse events,irAEs)和输液反应。免疫治疗较传统化疗的耐受性好,严重不良反应率较低,但若诊疗不及时也可危及生命。免疫检查点抑制剂(immune checkpoint inhibitors,ICIs)是治疗肿瘤的药物之一,由于ICIs在正常组织和肿瘤组织之间无选择性,在抗肿瘤的同时也下调了对自身抗原的相关耐受,导致免疫耐受失衡,在攻击肿瘤细胞的同时对正常组织和器官也造成损伤,从而导致irAEs的发生[2]。
3.1 ADR与患者性别和年龄的关系
本研究中79例ADR患者,男女患者比例约为2.5∶1,从年龄结构分布来看,50 ~ 79岁患者不良反应发生率较高。一项回顾性研究[3]比较了不同年龄段(< 60,60 ~ 69,70 ~ 79和≥80岁)晚期非小细胞肺癌(non-small cell lung cancer,NSCLC)患者接受PD-1抑制剂的疗效和安全性,结果显示安全性未存在明显差异,≥80岁组无论是总生存期还是无进展生存期都明显低于其他年龄组。另有临床试验[1]表明,65 ~75岁患者和< 65岁患者安全性和疗效总体上未存在差异。发生ADR的男性远多于女性,可能是由于该药治疗的瘤种如肺癌、肾癌、黑色素瘤在男性中发病率较高,使用该药的机会增多有关。此外,考虑到种族差异、个体差异等机体方面因素,中国患者使用纳武利尤单抗药动学特征与非中国的亚洲患者以及非亚洲患者相似,未观察到纳武利尤单抗药动学的种族差异[4]。因此,任何年龄段患者在使用该药时,临床上都应预防和监测ADR的发生。
3.2 ADR与用药剂量的相关性
本研究79例患者中,72例患者符合国内药品说明书推荐剂量用药,6例患者低于药品说明书推荐剂量,1例患者单次高剂量用药后出现了严重不良反应。研究[5]显示在接受3 mg·kg-1或240 mg,q 2 w和480 mg,q 4 w治疗后的安全性一致。但通过既往报道的1例肝细胞癌患者使用纳武利尤单抗240 mg,q 2 w,持续1.5年未发现严重不良反应,在给予480 mg纳武利尤单抗的第4天,患者出现了严重右下腹疼痛,诊断为回肠炎,经治疗好转后继续应用纳武利尤单抗240 mg,q 2 w,未再发生胃肠道不良反应,经过评估回肠炎很可能与单次给予高剂量纳武利尤单抗有关[6]。
3.3 ADR的发生时间
本研究显示,在接受纳武利尤单抗治疗的患者中ADR发生时间最快为输注后10 min左右,最长为用药后23个月,甚至发生在停药后。由表2可知,纳武利尤单抗所致ADR在用药后6个月内发生率为74.68%,Eigentler等[7]研究表明,纳武利尤单抗的不良反应通常在1 ~ 6个月内发生,与本研究结果一致。因此,建议临床在纳武利尤单抗输注期间要严密监测输液反应,特别是在前两次输注过程中,同时通过定期对血常规、血生化和脏器功能等检查,早期、及时发现与处理安全隐患。
3.4 ADR累及系统/器官、临床表现与处理
3.4.1 皮肤及其附件 纳武利尤单抗所致皮肤毒性除常见的斑丘疹样皮疹和苔藓样皮疹外,还有罕见的史蒂文斯-约翰逊综合征。皮肤毒性多发生于治疗早期,可发生在治疗后几天或几周内,甚至治疗结束。有研究[8-10]显示在接受纳武利尤单抗治疗后,最先出现的不良反应是皮肤及皮下组织毒性,多发生于用药后一个月左右。在绝大多数情况下,皮肤毒性是自限性的。根据不良事件的通用术语标准分级(CTCAE-v5.0),轻度皮疹可给予局部糖皮质激素治疗,无需中断治疗;中度皮肤反应暂停用药同时给予高剂量糖皮质激素治疗;重度皮肤毒性,如史蒂文斯-约翰逊综合征和中毒性表皮坏死松解症等,应永久停药。临床上要加强患者教育,早期识别皮肤毒性,及时对症治疗,防止免疫治疗中断。
3.4.2 内分泌系统 由表3可知,纳武利尤单抗所致ADR累及内分泌系统表现为肾上腺功能不全、甲状腺功能减退、垂体功能减退。纳武利尤单抗所致ADR较常见的是内分泌毒性。发生irAEs的作用机制尚不明确,多数认为这与免疫检查点在维持机体免疫稳态中发挥的作用有关。肾上腺功能不全大多是继发性的,其临床表现缺乏特异性,通常为乏力、高钾血症等,严重者可发生肾上腺危象,在治疗上应根据不良反应分级选择相应的糖皮质激素进行替代治疗并停用纳武利尤单抗。按照2018年美国临床肿瘤学会针对接受免疫治疗患者的irAEs管理指南分级[8-9],纳武利尤单抗引起的甲状腺功能异常通常为1 ~ 2级,对于无临床症状的患者仅需进行监测,无需治疗。对于有临床症状的,给予左甲状腺素替代治疗,建议暂停免疫治疗直至临床症状消失后再重启治疗。
3.4.3 呼吸系统与其他 纳武利尤单抗所致呼吸系统毒性均为肺炎,表现类型为非特异性间质性肺炎和机化性肺炎。PD-1抑制剂诱导肺炎的可能机制是由于肺间质巨噬细胞和肺泡细胞表达的排斥导向分子b与程序性死亡受体配体2相互作用有关,在8例肺炎报道中,5例是肺癌,有研究[11]表明,PD-1抑制剂致免疫性肺炎与患者肿瘤类型有一定相关性,肺炎等肺部irAEs的发生率在NSCLC中最高,可能与NSCLC患者合并慢性阻塞性气道疾病或既往接受过放疗等因素有关。肺炎的处理根据《免疫检查点抑制剂毒性管理指南》,按照不良反应分级选择不同种类和剂量的糖皮质激素治疗。临床上对高危人群制定相应的预防措施,早发现早干预也是及时控制ADR的关键所在。本文中4例1型糖尿病合并酮症酸中毒,也应重点关注。对于糖尿病合并酮症酸中毒患者,应立即使用胰岛素治疗,并请内分泌科会诊。内分泌毒性在免疫治疗中通常出现较晚,应定期进行生化检测和影像学检查。对于检查结果正常的患者,建议每2 ~ 3周进行血糖和甲状腺激素水平检测。
综上,纳武利尤单抗作为我国首个上市的PD-1抑制剂,给大多数晚期癌症患者带来了生存的希望。尽管不良事件发生率低,但其独特的毒性给临床治疗带来了挑战。因其不良反应潜伏期长,建议临床使用时应评估患者的风险与收益,加强用药安全性监测,警惕不良反应的发生。治疗前应进行患者用药教育,告知常见不良反应症状,早期识别、及时报告与及时处理十分重要。临床药师应重视irAEs毒性、风险因素及特殊人群的识别、治疗过程中监测。在不良反应发生后做到及时对症处理,减少严重不良反应的发生,保障患者用药安全。
