新生儿呼吸窘迫综合征采用肺表面活性制剂对PaO2、a/APO2及临床安全性分析
2021-11-18吴素文易丽霞
吴素文,易丽霞
(黄冈市妇幼保健院新生儿科,湖北 黄冈 438000)
临床中导致新生儿死亡的主要原因就是新生儿呼吸窘迫综合征(NRDS),其主要表现是呼吸性呻吟,呼吸急促,青紫等,严重的会引发呼吸衰竭,威胁患儿的性命[1]。临床认为引发NRDS的主要病理原因就是缺少肺泡表面的活性物质,导致肺泡发生进行性的萎陷,因此早期进行规范、有效的治疗有利于患儿预后的改善。临床通常应用的常规治疗有营养支持,机械通气,抗感染,维持酸碱和水电解质平衡等方法,虽然能暂时缓解患儿的症状,但总治疗效果不佳[2]。医学条件和技术的不断进步,研究不断深入,相关研究指出,应用肺表面活性制剂给予NRDS患者替代性治疗,效果较好[3]。本文主要探讨NRDS应用肺表面活性制剂治疗的效果。现报告如下。
1 资料与方法
1.1一般资料:选2019年10月~2020年10月于我院的新生儿呼吸窘迫综合征患者98例,随机分为两组。研究组共49例,胎龄37~40周,平均(39.2±0.8)周,女23例,男26例,出生体重2 300~5 900 g,平均(2 864±367)g。对照组共49例,胎龄37~40周,平均(38.3±0.9)周,女21例,男28例,出生体重2 301~6 001 g,平均(2 863±347)g。纳入标准[4]:①经影像学检查确诊为新生儿呼吸窘迫综合征的患儿,且主要表现有气促、呻吟、紫绀、三凹征阳性;②患儿家属签订知情同意书;③有低氧血症的患儿;④身体其他指标处于正常范围的患儿。排除标准:①药物过敏的患儿;②合并先天性畸形、遗传代谢疾病、肺内出血、颅内出血、休克的患儿;③身体重要器官存在严重疾患的患儿;④其他原因导致的呼吸困难的患儿;⑤研究前进行过气管插管的患儿。两组一般资料比较,差异无统计学意义(P>0.05),有可比性。本研究已获得伦理委员会准许。
1.2方法:两组患者入院后,均给予抗感染,营养支持,维持水电解质和酸碱平衡等常规治疗。在常规治疗基础上对照组应用气道正压通气治疗,机器应用的Infant Flow System英国新型的鼻塞仪,维持动脉血氧饱和度为0.9,动脉血氧分压是51~72 mm Hg(1 mm Hg=0.133 3 kPa),持续4~5 d的通气时间,如果患儿没有SaO2降低,呼吸暂停,心动过缓的症状,且生命体征处于稳定状态时可以提前撤机。研究组在对照组基础上应用肺表面活性制剂,具体方法:治疗前清理干净患儿呼吸道中的分泌物,从冰箱中取出药物,待药物溶解后,加热到37℃,用气管插管的方式给药,之后为患者加压通气,加速药物分散,改善低氧血症,如有必要,可以在用药6 h后再次给药,剂量是70 mg/kg。如果患儿有呼吸道阻塞的现象,用药6 h内给予吸痰拍背处理。
1.3观察指标:观察比对两组患者不良反应发生情况,其中包含:肺出血,肺部感染以及肺气漏。观察比对两组患者治疗前、治疗24 h后肺功能变化情况,其中包含OI(氧合指数)、PaO2(血氧分压)、a/APO2(动脉-肺泡氧分压比值)、PH值、PaCO2(动脉血二氧化碳分压)。分别于治疗前、治疗24 h后抽取患儿的桡动脉血3 ml,抗凝后通过血气分析仪对PaCO2、PH值、PaO2进行检测。观察比对两组患者的治疗效果:显效:经影像学检查各项指标、症状均恢复正常;有效:经影像学检查有致密影,但和治疗前比优显著好转;无效:影像学检查后症状、各项指标变化不大或有加重痕迹。总有效率=(显效例数+有效例数)÷总例数×100%。

2 结果
2.1两组的不良反应发生情况对比:研究组不良反应发生情况比对照组低,差异有统计学意义(P<0.05)。见表1。

表1 两组不良反应发生情况对比[例(%)]
2.2治疗前、治疗后两组患者的肺功能变化情况对比:研究组治疗后OI、PaCO2比对照组低,pH值、PaO2、a/APO2比对照组高,差异有统计学意义(P<0.05)。见表2。
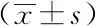
表2 治疗前、治疗后两组的肺功能变化情况对比
2.3两组患者的治疗效果对比:研究组治疗效果比对照组高,差异有统计学意义(P<0.05)。见表3。

表3 治疗效果对比[例(%)]
3 讨论
新生儿常见的一种呼吸系统疾病就是新生儿呼吸窘迫综合征(NRDS),主要表现是呼吸困难和呼吸衰竭,此类表现多发生在新生儿出生后4~12 h之内,发病时会随着年龄的增长不断降低,但体重越轻,患儿的病死率就越高,NRDS是引发新生儿伤残、死亡的主要原因[5]。此病病情急,发展迅速,威胁新生儿的生命。目前临床中暂时没有NRDS的明确发病机制,较多学者认为其主要是因为新生儿的肺部发育不完善,肺泡表面的活血物质分泌不足(或尚未分泌),导致肺表面的张力加大,促使肺部顺应性降低,肺泡无法充分膨胀,肺液体出现转运障碍,且新生儿多数呼吸力量薄弱,容易引发肺部通气、换气障碍,从而导致疾病的发生[6]。因此临床中针对NRDS治疗的关键就是对肺泡表面的活性物质进行补充,消除患儿的呼吸困难症状。临床中常用的治疗方法有营养支持,机械通气,抗感染,维持酸碱和水电解质平衡等方法。气道正压通气是新型的一种通气模式,属于无创操作的一种,可以避免损伤患儿的呼吸道[7]。通过持续气道正压通气可以促使肺泡维持开放,增加肺泡功能和肺泡面积,从而避免出现肺泡萎陷的现象,促使机体的氧合能力提高,降低机体中肺表面活性物质的消耗,改善患儿的通气、换气功能。虽然能暂时缓解患儿的疾病症状,但不能改善患儿体内缺乏肺泡表面活性物质的根本原因,因此治疗效果不佳。
随着医疗水平和技术的不断发展,研究的不断深入,较多学者认为在常规治疗基础上联合应用肺表面活性制剂治疗NRDS效果较好。由肺泡中Ⅱ型细胞分泌的脂蛋白就是肺泡中的表面活性物质,其不仅可以降低肺泡的表面张力,还可以稳定肺泡容积,防范肺泡萎陷,扩张肺部,与此同时可以预防肺泡内积液的形成,有利于肺部的换气[8]。相关研究指出,肺表面活性制剂治疗NRDS效果较好。肺表面活性制剂是一种混合分物质,主要由脂类、碳水化合物以及多种蛋白质组成,主要成分是特异性蛋白和磷脂,用药后在肺泡表面以单分子层的形式进行排列,可以缓解肺表面张力降低的症状,且可以抑制液体分子间的互相吸引,稳定肺泡的容量,与此同时增加的肺表面活性制剂可以提高肺部的顺应性,持续扩张肺泡,可以有效稳定肺泡的容量,从而有效预防发生肺泡萎陷[9]。肺表面活性制剂主要在肺泡液体的分子层表面分布,除上述作用外,还有下述生理功能:①促使毛细支气管末端的表面张力降低,预防发生毛细支气管堵塞、痉挛;②促使肺毛细血管张力降低,提高肺泡中的内氧分压以及肺通气量,加速清除肺液,对肺泡的上皮细胞有显著的保护效果;③对肺泡间的毛细血管的正常流体压力有维持的作用,可以有效预防肺水肿,且可以提高呼吸系统的抵抗力,提高呼吸功能[10]。
机械通气是重要的损伤肺部的因素,也是治疗NRDS的一种常用手段,临床中长通过监测氧合功能片段肺通气灌流的协调状况。而评估患儿通气、换气情况、呼吸衰竭程度的重要、常用指标就是OI[11]。本次研究中,研究组在常规治疗基础上应用肺表面活性制剂,其是一种天然的提取物,磷脂含量最高,占比为90%,多数是PC(磷脂酰胆碱),有表面活性的作用,其余磷脂包括:鞘磷脂,磷脂乙醇胺,磷脂酰肌醇和磷脂酰丝氨酸;另外还有表面活性物质特异性蛋白质SP-C和SP-B[12]。结果显示:研究组治疗后OI、PaCO2比对照组低,PH值、PaO2、a/APO2比对照组高,差异有统计学意义(P<0.05),表明通过肺表面活性制剂治疗NRDS效果较好,可以改善患儿的肺功能。结果还显示:研究组不良反应发生情况比对照组低,差异有统计学意义(P<0.05);研究组治疗效果比对照组高,差异有统计学意义(P<0.05),表明肺表面活性制剂治疗NRDS安全性和治疗效果高,且价格优惠,不良反应少。
综上所述,新生儿呼吸窘迫综合征应用肺表面活性制剂治疗效果较好,值得推广和应用。
