皮肤腐蚀和皮肤刺激替代试验的发展及其在化学品危险性分类的应用
2021-11-17潘叙恩卢章顺黄志鹏何志荣
潘叙恩,卢章顺,杨 光,钟 岸,黄志鹏,何志荣
(广东省科学院测试分析研究所(中国广州分析测试中心),广东省化学危害应急检测技术重点实验室,广东省分析测试技术公共实验室,广州 510070)
近现代科学技术高速发展,目前全球已公布的物质已超过了1.5 亿种[1],化学品的广泛应用一方面改善了人们的生活,同时也提高了人们接触化学品带来的安全风险。 皮肤腐蚀性和刺激性是化学品基于联合国GHS 分类的一种重要的潜在危险特性,准确评估和分类化学品对皮肤的腐蚀和刺激潜力,对加强化学品安全管理,预防和减少化学品事故,具有非常重要的意义。
长期以来,研究人员主要利用动物试验对该课题进行研究,Draize 等[2]建立了利用白化兔评估化妆品对皮肤刺激潜力的方法,该方法逐步发展并在化学品皮肤腐蚀性和刺激性评估中得到广泛的应用,后来被经济合作与发展组织(OECD)采用为试验准则404(TG404),成为GHS 皮肤腐蚀性和刺激性的分类依据。
随着人类认知水平的提高和现代伦理学的发展,动物福利问题得到了越来越多的重视,作为传统的动物试验,Draize 试验备受质疑和争议。 1959年,动物学家Russell 和微生物学家Burch 共同发表了《人道实验技术原则》(The Principles of Humane Experimental Technique),系统性地提出了“3R”(Replacement, Reduction and Reduction)的概念和准则,促使动物试验的开展更符合人道主义精神[3]。“3R”的提出为实验动物替代技术的研究确立了理论基础,替代试验的研究和应用逐渐成为化学品皮肤腐蚀/刺激潜力评估和分类的主要发展方向。
1 替代试验的发展背景
为贯彻3R 原则,各国政府和国际组织进行了大量的工作:一方面,先后将3R 原则引入了实验动物相关的法律法规以改善实验动物的待遇,如中国《关于善待实验动物的指导性意见》、欧盟《关于保护用于科研目的的动物的指令》、美国《美国政府关于在试验、研究和训练中使用和照顾脊椎动物的原则》、英国《动物(科学程序)法案》等[4]。 另一方面,为减少科研活动对动物体内试验的依赖,资助了大批的研究机构、组织和研究项目以支持替代方法的研究,并成立了替代方法验证中心组织系统性的方法验证,如欧盟成立的欧洲替代方法验证中心(ECVAM;后更名为替代动物实验欧盟联合参考实验室EURL ECVAM)和美国的替代方法验证跨部门协调委员会(ICCVAM)等。 随着欧盟和美国、加拿大、日本等国签署了替代方法国际合作协议( International Cooperation on Alternative Test Methods,ICATM),实验动物替代技术进入了快速发展的阶段。
实验动物替代技术的进步,使立法禁止动物体内试验得以成为可能。 在欧盟,有许多法规要求使用替代方法来代替体内试验进行毒理学测试。 欧盟《化妆品法规》[5]禁止了2004 年以来的化妆品成品和2009 年以来的化妆品成分进行动物体内试验,并自2013 年起禁止销售含有经动物体内试验成分的化妆品产品。 此外,欧盟《关于化学品注册、评估、许可和限制的法规》(REACH 法规)[6-7]要求OECD 成员国对化学品的皮肤腐蚀和刺激性评估需利用替代方法进行体外试验,除非该受试化学品不在替代方法适用的范围内或替代方法无法对受试化学品作出准确的分类和风险评估。 欧盟《物质和混合物的分类、标签和包装法规》(EU CLP)[8-9]与REACH 法规相辅相成,在欧盟范围内执行联合国GHS 制度关于化学品分类和标签的规定,该法规在皮肤腐蚀和刺激性分层评估中使用了证据权重(weight-of-evidence,WoE)方法,并鼓励利用来自替代方法的数据。 最后,欧盟《关于保护用于科研目的的动物的指令》[10]规定“在不妨碍禁止某些试验方法的成员国法律的前提下,如利用其它试验方法或策略可以得到所需的结果时,成员国不得利用活体动物进行试验”。 欧盟的立法对全球各国的法规也产生了巨大的影响,以色列、挪威、印度、新西兰、澳大利亚、瑞士等国也先后立法禁止了化妆品产品进行动物体内试验,全球目前已有超过30 个国家和地区实施了关于动物体内试验的相关禁令。
2 分类标准对替代试验的认可
联合国GHS 的分类制度是目前世界范围内最具普适性的化学品分类制度,对皮肤腐蚀性和刺激性化学品进行了明确的定义和分类(见表1)[11],源于OECD 统一分类和标签工作组(OECD Task Force on Harmonization of Classification and Labelling,Task Force on HCL)对健康危害的分类标准。

表1 联合国GHS 分类制度关于皮肤腐蚀性/刺激性的定义和分类Table 1 Categories and definition of skin corrosion/irritation of UN GHS
在较早版本的GHS 中,针对化学品的皮肤腐蚀和皮肤刺激的定义和分类仍基于OECD TG 404 的动物试验。 得益于各国政府和科研工作者的努力,越来越多的体外方法被提出和验证成为OECD 的试验准则,用于替代 TG 404 的动物试验。 目前经OECD 认可的替代试验方法涵盖了离体组织或器官、三维重组人类细胞组织和人造生物皮肤等模型(见表2),已能基本满足联合国GHS 的分类和评估需要。 在2019 年修订的第八版GHS 中,这些替代试验方法得到了进一步的认可被正式列为分类标准,用于皮肤腐蚀(类别1)、皮肤刺激(类别2)的识别。
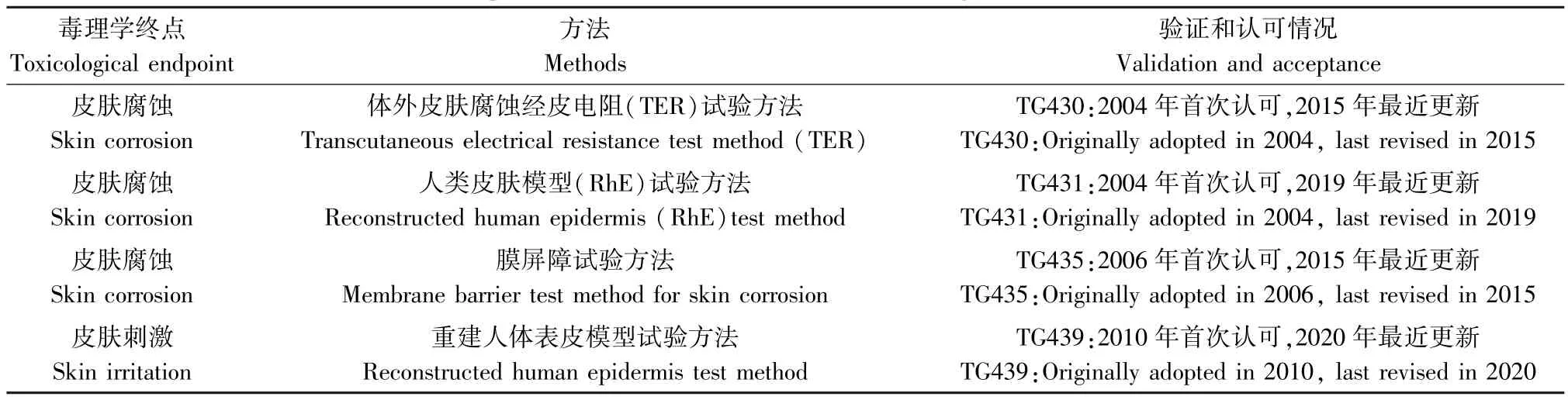
表2 OECD 关于皮肤腐蚀性和刺激性替代试验方法的验证和认可情况Table 2 Validation and acceptance of OECD on the alternative testing methods of skin corrosion and irritation
3 皮肤腐蚀和刺激的试验和评估综合方法
在GHS 第八修订版中,除了对体外试验方法的进一步认可外,还引入了新的分类和评估策略——皮肤腐蚀和刺激IATA。 该策略源于OECD 指南GD 203,其建立的目的是为了适应替代方法发展的新形势,满足3R 原则和保障分类评估准确性的要求,取代原来 OECD TG404 补充文件中的测试和评估策略。
皮肤腐蚀和刺激IATA 主要分为3 个部分:(1)现有的信息、理化性质和非实验方法;(2)证据权重评估;(3)补充实验。 根据数据和信息的来源及功能,该评估策略的信息源被分为8 个模块,这些模块可分别应用于策略中的一个或多个部分(见表 3)[12]。 OECD GD203 指出,该评估策略的目标是在确保人身安全的前提下尽可能减少对实验动物的使用,提出在分类和评估的过程中,应最大程度运用现有的数据合理安排证据权重评估,只有在无法获得准确结果时再利用试验进行分类。

表3 皮肤腐蚀性和刺激性IATA 的组成Table 3 Composition of the IATA for skin corrosion and irritation
4 替代试验在皮肤腐蚀和刺激IATA 中的应用
替代试验在皮肤腐蚀和刺激IATA 中的应用主要体现在两个方面:首先,作为IATA 第一部分现有皮肤腐蚀和刺激属数据的重要组成部分,基于文献和资料所得的替代试验数据可独立用于WoE 评估或结合人类数据和动物试验数据等其他模块的信息用于综合WoE 评估。 其次,皮肤腐蚀和刺激替代试验也是该分类评估策略第三部分补充实验的重要组成部分,研究人员可对WoE 评估无法获得确证结果的化学品执行自上而下或自下而上的试验策略,利用体外试验方法(必要时结合动物试验)进行最终的分类和评估。
在应用这些替代试验方法之前必须明确,目前已经得到认可的方法都存在着一定的局限性,至今仍然没有任何一种单一的体外试验方法可以覆盖全部分类范围。 充分理解每种方法的原理、适用范围和局限性,对于研究人员选择合适的方法非常重要,是有效执行皮肤腐蚀和刺激IATA 评估策略的关键。
5 OECD 认可的皮肤腐蚀/刺激替代试验方法及其适用性
5.1 经皮电阻试验方法
TG430[13]体外皮肤腐蚀经皮电阻(transcutaneous electrical resistance,TER)试验方法利用了离体的大鼠表皮组织对化学品的皮肤腐蚀性进行评估。 受试皮肤片取自安乐处死的28~30 d龄的大鼠。 实验过程中,受试皮肤片安装在测试系统中,把整个测试系统分隔为内外两层。 受试物涂覆在受试皮肤片的表皮面,保持24 h。 通过测定受试皮肤片的经皮电阻,确定角质层的缺失程度和皮肤屏障功能的完整程度来识别受试物的腐蚀性。根据大量化学品的大鼠TER 测试结果,选取了5 kΩ 作为皮肤腐蚀性的判定阈值。 通常,无论对皮肤是否具有刺激性,对活体动物皮肤无腐蚀性的物质,其TER 值都不会低于该判定阈值。 该方法还增加了染色试验,进一步对TER 测试阳性(包括TER接近5 kΩ 的结果)但无明显损伤的皮肤片进行确认。
与其他已得到OECD 认可的替代试验相比,TG430 利用的离体皮肤模型包含了提供主要屏障功能的角质层和表皮细胞层,以及皮脂腺、汗腺和毛囊等所有附属器官,具有完整的皮肤组织结构,可更近似地模拟化学品在体内发生的经皮渗透和吸收。 但是,该方法只能划分皮肤腐蚀(类别1)和非腐蚀性的样品,适用于大量化学品腐蚀危险性的筛查,并不能进一步划分皮肤腐蚀性子类别,也不能识别非腐蚀性的样品是否具有刺激性。
5.2 重建人类表皮模型试验方法
目前已验证的利用体外重建人类表皮模型(reconstructed human epidermis test method,RhE)的皮肤腐蚀和刺激性试验方法有 TG431[14]和TG439[15],其原理是假设腐蚀/刺激性化学物质能够通过扩散或侵蚀作用渗透穿过角质层,对下层的细胞产生毒性作用。 该模型是利用组织工程学技术构建的多层、高度分化的三维表皮模型,包含了基底层、棘细胞层、颗粒层、角质层和脂质等与正常皮肤相似的结构。 由于TG431 和 TG439 的 RhE 模型没有形成血管,因此选择了以细胞活性作为测定终点对细胞和组织的损伤进行评估。
TG431 用于化学品的皮肤腐蚀性的评估,方法是将受试物局部作用在三维RhE 模型上,在特定作用时间后,利用3-(4,5-二甲基-2-噻唑)-2,5-二苯基溴化四氮唑噻唑蓝(MTT)还原法测量受试RhE 组织的细胞活性,然后通过与阈值的比较来识别和分类受试物腐蚀性。
TG439 用于评估化学品的皮肤刺激性,该方法进一步利用了RhE 模型的特点,在试验过程中并不是在与受试物作用后立即测量RhE 组织的细胞活性,而是对经过冲洗的RhE 组织在新培养基中进行足够长时间的培养之后才进行细胞活性的测量。这样既可以使RhE 组织从较弱的细胞毒性作用中恢复,也有足够的时间表达明确的细胞毒性作用。
与其他已获得OECD 认可的替代方法相比,TG431 和 TG439 具有很多优势。 首先,RhE 模型是由人源性的表皮角质细胞培养所得,与被模拟的人体皮肤组织不存在物种差异。 其次,RhE 组织可以通过培养恢复细胞活性,TG439 是目前唯一受OECD 认可的评估皮肤刺激性(类别2)的替代方法。 最后,RhE 试验方法有很多可选用的商业化模型,TG431 和 TG439 分别于 2019 年和 2020 年进行了最新的修订,目前最新版本的试验准则中已得到验证和认可的商业化模型已分别增至5 个和6 个(TG431: EpiSkinTM、 EpiDermTMSCT、 SkinEthicTMRHE、epiCS®、LabCyte EPI-MODEL24 SCT;TG439:EpiSkinTM( SM )、 EpiDermTMSIT ( EPI-200 )、SkinEthicTMRHE、 LabCyte EPI-MODEL24 SIT、epiCS®、Skin+®)。
需要注意的是有些化学品会在试验过程中显色或能与MTT 作用产生非特异的颜色反应,干扰细胞活力的测定结果,虽然通过设置非特异性显色(NSCliving)和非特异性MTT 反应(NSMTT)对照组可对这些干扰进行排除,但是针对阴性对照NSCliving≥50%和/或NSMTT≥50%的结果应十分谨慎。 此外,TG431 和TG439 的分类能力仍存在着局限性,TG431 可用于识别化学品皮肤腐蚀性(类别1 及子类别1A 和1B/1C)和非腐蚀性,但无法进一步分辨子类别1B 和1C;TG439 可以区分皮肤腐蚀/刺激(类别1/2)和皮肤轻度刺激/非刺激(类别3/不划类),但不能进一步对类别1 和类别2 进行识别,也无法分辨类别3 和不划类,这些都是在利用这些试验方法或其数据时必须注意的。
5.3 膜屏障试验方法
在OECD 认可的对皮肤腐蚀性和刺激性的替代试验方法中,TG435[16]膜屏障(membrane barrier)试验方法是唯一一种完全基于人造的非生物皮肤模型(artificial non-viable skin model)的方法。 其测试系统由人造的高分子生物膜和化学检测系统(chemical detection system, CDS)组成,原理是基于人造高分子生物膜与活体皮肤具有相似的腐蚀作用机制的假设,受试物局部作用于高分子生物膜表面,经过特定的作用时间,通过CDS(如pH 指示剂颜色改变、指示剂溶液其他特性改变等)检测高分子生物膜的屏障功能是否受到破坏,受试物是否穿透了高分子生物膜,以此对受试物的腐蚀性进行识别和分类。
目前,TG435 的商业化模型只有Corrositex ®一种,可用于识别化学品皮肤腐蚀性(类别1)和非腐蚀性,基于Corrositex®的子分类标准可利用受试物对生物膜的穿透时间进一步划分腐蚀性子类别1A、1B 和1C。 Corrositex®操作简单,在评估酸、碱以及酸衍生物的皮肤腐蚀性时非常有效[17],但基于该CDS 的特点,不适用于评估pH 值4.5~8.5 及其他无法令CDS 指示剂发生颜色变化的化学品[18]。 虽然该方法无法分辨非腐蚀化学品的皮肤刺激性(类别2/3)和非腐蚀性(不划类),但是在执行一些运输相关法规要求的测试时特别适用,如美国交通运输部的危险物质法规[19]就明确规定了针对TG430 或TG431 划为腐蚀性的危险品,必须利用 TG435 或TG404 对结果进一步确定。
6 其他的皮肤腐蚀/刺激替代试验方法
作为皮肤腐蚀和刺激IATA 模块5a,这些暂未受OECD 认可的皮肤腐蚀和刺激性评估的体外模型和替代方法有许多,除了一些商业化的RhE 模型(KeraSkinTM、EpiKutis ®、EST1000 ®、StrataTest ®、Vitrolife-SkinTM、Phenion ®等)[20-23]、开源的 RhE 模型(OS-Rep[24-25]) 和其他类似的 RhE 模型(如HaCaT 表皮模型[26-27]、LHE 人类表皮模型[28]、基于手术获得的人类皮肤的模型[29]、人类全厚皮肤模型[30]等),还包括了一些正在研究开发的新模型和新方法。
Groux 等[31]研究了RhE 模型响应皮肤刺激物而引起的基因表达变化,并根据基因表达水平开发了一种方法用于划分刺激性(类别2)、轻度刺激性(类别3)和非刺激性(不划类)。 Spiekstra 等[32]研究表明在RhE 模型中利用IL-1α,IL-1RA,IL-8 等生物标志物和MTT 不仅能识别受试物的腐蚀性和刺激性,还可以确定化学物质对皮肤的刺激能力。 除此以外还有许多应用了蛋白质组学和毒物基因组学技术,并非以细胞活力为测定终点的试验方法[33-36]。
另外,Khammo 等[37]和 Muller 等[38]研究组还分别利用从胚胎大鼠背根节神经元提取的感觉神经元和人类诱导性多能干细胞(iPSC)构建了受神经支配的组织工程皮肤(TES)模型,可在体外试验中模拟在体内由神经性炎症造成的刺激和疼痛[39]。
最后,还有更多基于生物打印、器官芯片等新技术应用的新模型和新方法,如Wei 等[40]研究利用3D 生物打印技术构建的可有效应用于皮肤刺激研究的人类全厚皮肤模型,以及Jusoh 等[41]研究以脐静脉内皮细胞(HUVEC)、人类真皮成纤维细胞(HDF)、角质形成细胞和微流控芯片构建的具有血管生成能力的皮肤芯片,还有Tavares 等[42]研究基于微生理系统构建的人类皮肤-肝双器官集成芯片。
7 结论与展望
3R 原则提出以来,实验动物福利的问题得到了更多的关注,实验动物替代技术在科技和法规的双重驱动下获得了很大的发展,人们越来越重视利用体外模型和试验方法代替动物试验进行化学品安全性的研究。 近年来,在化学品皮肤腐蚀性和刺激性的研究方面,无论从替代试验方法的开发还是分类评估试验策略的创新都取得了很大的进步。 越来越多的体外模型和试验方法通过了验证;基于组学技术的应用研究,更多的测定终点被提出;得益于3D 生物打印、干细胞和生物芯片等技术的发展,构建更复杂的体外模型也成为了可能。 随着科技的进步,更多的体外试验方法和模型将被开发和应用。
中国与其他主要发达国家和地区相比,在动物试验替代方法的开发和验证等方面的工作起步稍晚,在管理和发展上还存在着一定的差距。 目前在实验成本方面,替代试验与动物试验相比仍不具备优势。 此外,在GHS 皮肤腐蚀性和刺激性分类的应用上,现有的替代试验方法在适用条件和分类范围等仍存在着局限。 皮肤腐蚀性和刺激性IATA 以3R原则为指导,提出尽可能优先利用现有的数据进行证据权重评估,必要时再结合危险性分类需求合理地制定策略开展试验。 该策略结合目前实验动物替代技术的发展现状,充分优化了皮肤腐蚀性和刺激性的分类试验流程,最大程度地减少不必要的试验和避免了对实验动物的使用,正确利用这一策略对今后有效开展皮肤腐蚀性和刺激性分类评估工作具有非常重要的意义。
