β-环糊精接枝壳聚糖对Cr2O72-的吸附研究
2021-11-13李海丰刘海江
李海丰 刘海江
(新余市渝水生态环境局,江西 新余 338000)
1 引言
铬(Cr)广泛存在于自然界,在水体和大气中均含有微量的铬。铬亦是人体必需的微量元素,它与脂类代谢有密切联系,能辅助胰岛素利用葡萄糖。若大量的铬污染环境,则将对人体健康产生危害。铬的化合物常以溶液、粉尘或蒸汽的形式污染环境,可通过消化道、呼吸道、皮肤和粘膜侵入人体。铬对人体的毒害有全身中毒,刺激皮肤粘膜,引起湿疹、气管炎、皮炎和鼻炎,引起变态反应并有致癌作用,如六价铬可以诱发鼻咽癌和肺癌。
本研究仿文献[1,2,3]方法,将β-环糊精(β-Cyclodextrin,简写β-CD)接枝到壳聚糖(Chitosan,简写CS)合成β-环糊精接枝壳聚糖(CS-CD)吸附剂,利用CS-CD上的氨基在与质子结合后形成阳离子,从而能够吸附带负电的Cr2O72-。以下主要从吸附影响因素、动力学、热力学等几个方面来对CS-CD吸附Cr2O72-的性能进行了初步分析。
2 实验部分
2.1 材料及仪器
壳聚糖(脱乙酰度90%以上,国药集团化学药剂有限公司);CS-CD;重铬酸钾(分析纯,国药集团化学药剂有限公司);硫酸(分析纯);氢氧化钠(分析纯);二苯碳酰二阱(分析纯);磷酸(分析纯)。
紫外-可见分光光度计(UV-2102PC型,尤尼柯上海仪器有限公司);电子天平(JA1003型,上海精密科学仪器有限公司天平仪器厂)。
2.2 实验方法
2.2.1 Cr(Ⅵ)的光度测定及标准曲线的绘制
在酸性溶液中,六价铬与二苯碳酰二阱反应,生成紫红色化合物,在540 nm波长处有最大吸收,从而比色定量[4]。
Cr(Ⅵ)贮备液的配制:称取于120 ℃烘干2 h的重铬酸钾(K2Cr2O7)0.2829 g,用水溶解,移入1000 mL容量瓶中,用水稀释到标线,摇匀。此溶液含有六价铬100 mg/L,作为贮备液。5 mg/L六价铬使用液当天配制。
二苯碳酰二阱显色剂:称取0.2 g二苯碳酰二阱(C13H14N4O),溶解于50 mL丙酮中,加水稀释至100 mL,混匀,置于冰箱中保存。
标准曲线的绘制:取6支50 mL具塞比色管,分别加入0 mL、0.5 mL、1.0 mL、2.0 mL、4.0 mL、6.0 mL使用液,用水稀释至标线,再分别加入1+1硫酸溶液0.5 mL,1+1磷酸溶液0.5 mL,摇匀,最后各加入2 mL显色剂,摇匀,放置5 min-10 min于540 nm波长处,用3 cm比色皿,以空白样为参比,测定吸光度,并作空白校正,绘制标准曲线如图1。

图1 Cr(VI)标准曲线
2.2.2 CS-CD对Cr2O72-的吸附性能试验
称取一定量的CS-CD加入至Cr2O72-溶液中,在不同pH、投加量、初始浓度的条件下进行Cr2O72-的吸附试验,用可见分光光度法测定吸附平衡时滤液中离子的浓度,其吸附量Q(mg/g)的计算公式为:Q=(C0-Ce)V/m
(式1)
其中C0,Cr(VI)的初始浓度,mg/L;Ce,吸附平衡浓度,mg/L;V,溶液总体积,L;m,吸附剂质量,g。
2.2.3 吸附动力学测定
在一系列150 mL具塞锥形瓶中分别加入0.01 g CS-CD和50 mL浓度为15 mg/L的Cr(VI)溶液,旋紧盖子,置于恒温振荡器上。在不同温度(30 ℃、40 ℃、50 ℃)和150 r/min的条件下振荡,在不同时间取出过滤。用分光光度法测定滤夜中的Cr(VI)残留量,根据工作曲线图1,求出Cr(VI)的浓度。
2.2.4 吸附等温线测定
在一系列150 mL具塞锥形瓶中分别加入0.01 g CS-CD和50 mL不同浓度的K2CrO4溶液,旋紧盖子,置于恒温振荡器上。在不同温度(20 ℃、30 ℃、40 ℃、50 ℃)和150 r/min的条件下振荡至吸附平衡,求出平衡浓度,根据公式1计算平衡吸附量,并绘出吸附等温线。
3 结果与讨论
3.1 对Cr2O72-的吸附性能研究
3.1.1 pH对CS-CD吸附效果的影响
在15 mg/L的Cr(VI)溶液中加入10 mg CS-CD,温度为30 ℃,反应时间为10 h的情况下,研究了pH对Cr2O72-的吸附影响,结果如图4.2所示。

图2 pH对CS-CD吸附Cr2O72-的影响
由图2可以看出,pH在3.0左右CS-CD对Cr2O72-的吸附量较大,而当pH进一步增加至6时,其吸附量明显下降。这是因为当pH升高时,H+浓度下降,形成带正电的NH3+也减少了,对Cr2O72-的吸附效果也就变差了。而当pH过低时,对吸附也不利,这是因为在强酸的条件下环糊精从壳聚糖上发生水解,脱落下来,影响了合成物的吸附效果[5]。
3.1.2 CS-CD投加量对吸附效果的影响
在pH=3,Cr(Ⅵ)的浓度为10 mg/L,温度30 ℃的条件下,研究了不同CS-CD的投加量对吸附的影响,结果如图3所示。

图3 投加量对CS-CD吸附Cr2O72-影响
从图3中可以看出,随着投加量的逐渐增多,其吸附量反而减少,这是因为投加量的增大,单位每g的CS-CD与溶液接触的比表面积减少了,故而其单位吸附量也减少了。
3.1.3 初始浓度对CS-CD吸附效果的影响
在pH=3,CS-CD投加量为10 mg,温度30 ℃的条件下,研究了不同Cr(Ⅵ)初始浓度对CS-CD吸附效果的影响,结果如图4所示。由图4可知,当Cr(Ⅵ)浓度增大时,CS-CD对Cr(Ⅵ)的吸附量也逐渐增大,这是因为增加反应物的量有利于反应的进行。
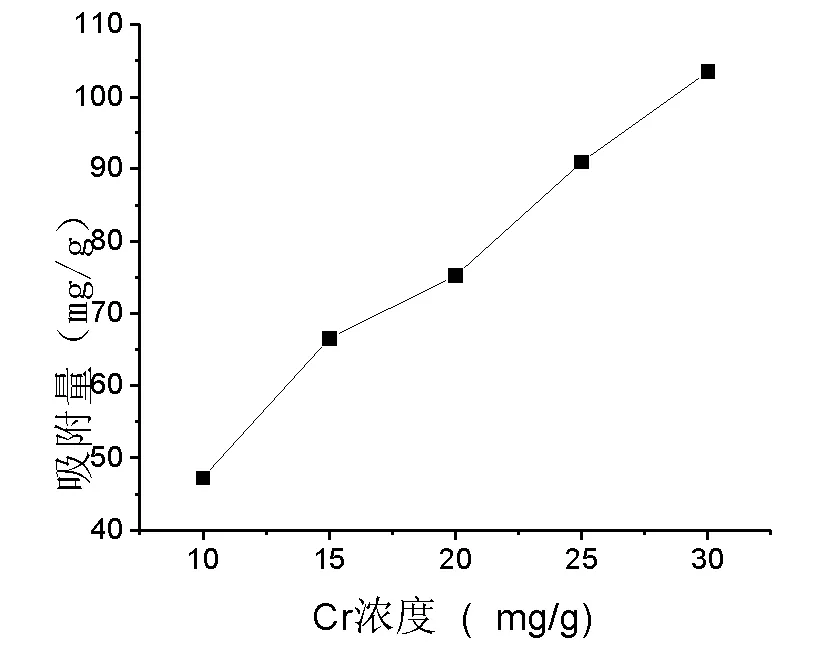
图4 溶液初始浓度对CS-CD吸附Cr2O72-的影响
3.2 吸附动力学
在pH=3,温度30 ℃条件下,把10 mg CS-CD加入到50 mL浓度为15 mg/L的Cr(Ⅵ)溶液中,CS-CD在不同温度条件下对Cr2O72-的吸附动力学曲线如图5所示。图5表明,在3种不同温度条件下,CS-CD对水溶液中Cr2O72-的吸附量随着温度的升高而增大,这说明升高温度有利于吸附的进行,CS-CD对Cr2O72-的吸附属于吸热过程。
对吸附动力学特性的研究用准一级动力学和准二级动力学方程对不同时间的吸附量进行拟合,寻求最优方程,以模型线性化的相关性系数R2大小来判断模型优劣。
准一级动力学方程:ln(qe-qt)=lnqe-k1t
(式2)

图5 Cr2O72-的吸附动力学曲线
准二级动力学方程:t/qt=1/k2qe2+t/qe
(式3)
其中,qe、qt分别为吸附平衡和时间t时刻CS-CD对Cr(Ⅵ)的吸附量(mg/g),t为反应时间,k1为准一级动力学吸附速率常数(1/min),k2为准二级动力学吸附速率常数(g/(mg·min))。
基于以上两个方程式,以ln(qe-qt)为纵坐标,时间t为横坐标;以t/qt为纵坐标,时间t为横坐标,得到的动力学拟合曲线见图6,通过曲线的斜率和截距计算得到动力学模拟参数列于表1。

图6 Cr2O72-的准一级动力学曲线(a)及准二级动力学曲线(b)
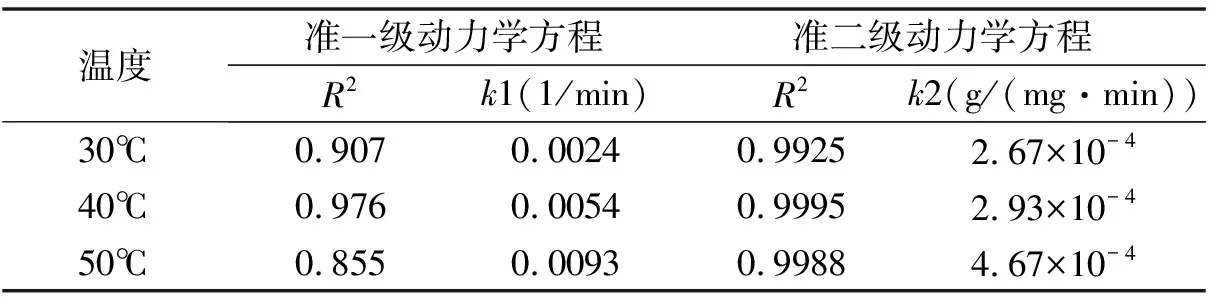
表1 不同温度条件下CS-CD对Cr2O72-的吸附动力学模拟参数
已知反应温度和准二级动力学速率常数k2,采用阿仑尼乌斯(Arhenius)公式常用于表观活化能的求解,其线性表达式为:lnk=lnA-Ea/R·T,式中,k为反应速率常数;T为绝对温度(K);A为指前因子;Ea为经验活化能(J/mol);R为理想气体常数(J/(mol·K)),以lnk2对1/T作图可得一条直线,根据直线得斜率可求得CS-CD对Cr(Ⅵ)的表观活化能Ea为21.85 kJ/mol<25.1 kJ/mol,吸附主要方式为物理吸附。
3.3 吸附等温线
吸附等温线采用Freundlich和Langmuir方程对不同温度下(20 ℃、30 ℃、40 ℃、50 ℃)吸附等温线实验数据进行线性拟合处理。Freundlich等温吸附方程的线性化形式为lgqe=lgK+1/nlgCe,qe为平衡时的吸附量(mg/g);Ce为吸附平衡时溶液中Cr(Ⅵ)浓度(mg/L),以lgqe对lgCe作图,见图7(a)。Langmuir等温吸附方程的线性化形式为Ce/qe=1/(qm·K)+Ce/qm,以Ce/qe对Ce作图,见图7(b)。Langmuir和Freundlich等温模型相关性系数列于表2。

表2 Freundlich和Langmuir两种吸附模型的相关性系数对比

图7 Freundlich(a)和Langmuir(b)吸附等温线
通过表2中Langmuir和Freundlich等温模型相关性系数的比较,可以得出用Langmuir等温模型来拟合CS-CD对Cr2O72-的吸附更优,其相关性系数均在0.99以上。利用Langmuir等温吸附方程的线性化形式拟合实验数据,根据拟合的斜率和截距可以分别计算出CS-CD对两种偶氮染料的最大吸附量qmax 及吸附平衡常数K,结果列于表3。

表3 CS-CD吸附Cr2O72-的Langmuir吸附模型参数
3.4 吸附热力学
吸附热常数包括吉布斯自由能变ΔG(kJ/mol)、焓变ΔH(kJ/mol)和熵变ΔS(kJ/(mol·K))等,它们之间的关可以根据下列公式来确定:
ΔG=-RTlnK=-2.303RTlgK
(式4)
ΔG=ΔH-TΔS
(式5)
根据公式4,由不同温度下的吸附平衡常数K可以计算出吉布斯自由能变ΔG的数值。根据公式5以ΔG为纵坐标,以T为横坐标作图,可得到一条直线,见图8,由线性回归方程求出标准焓变ΔH和熵变ΔS的值,结果列于表4中。

图8 Cr2O72-的吸附热力学直线

表4 Cr2O72-的热力学参数
4 结论
(1)CS-CD在酸性条件下能与H+结合,使得本身带正电,从而能与以负电形式存在的Cr2O72-发生吸附作用。吸附研究结果表明溶液在pH=3时对Cr2O72-的吸附效果最好;投加量减少,增大反应物接触的比表面积,有利于吸附;初始浓度的增加相当于增加了反应物的量,有利于吸附反应的进行。
(2)在实验的不同温度条件下,通过对相关性系数的对比,CS-CD对Cr2O72-的吸附更符合准二级动力学方程。吸附活化能Ea值为21.85 kJ/mol,以物理吸附为主。
(3)CS-CD对Cr2O72-的吸附等温实验数据符合Langmuir模型,其相关性系数R2都大于0.99;吸附反应自由能变△G<0,说明反应是自发进行的;标准焓变值为20.1 kJ/mol>0,这说明CS-CD对Cr2O72-的吸附是吸热反应,以物理吸附为主。
