早期肠内营养联合肠外营养、多种微量元素 对重症高血压脑出血术后患者营养状况的影响
2021-10-28赵冬梅
赵冬梅,刘 洋
(新沂市人民医院重症监护室,江苏徐州 221400)
脑出血是神经系统的常见急症,高血压是主要诱因之一,其可导致脑实质内血管破裂,引发颅内血肿,造成脑组织机械压迫,引发头痛、恶心呕吐、意识障碍等临床症状,且重症高血压脑出血是严重的脑出血类型,具有出血量大、病情发展迅速等特点。肠外营养是针对重症高血压脑出血术后患者的营养支持方式之一,营养成分经静脉途径进入机体,可在一定程度上补充糖、脂肪等营养物质,但未直接进入胃肠,不利于胃肠功能的早期恢复[1]。早期肠内营养支持也是临床重症高血压脑出血术后的一种营养支持方式,有助于增强肠道功能,同时辅助补充多种微量元素,可促进肠黏膜免疫屏障恢复,改善营养状态[2]。本研究探讨了早期肠内营养联合肠外营养、多种微量元素对重症高血压脑出血术后患者营养状况的影响,现将研究结果作如下报道。
1 资料与方法
1.1 一般资料选取2018年12月至2020年9月新沂市人民医院收治的重症高血压脑出血术后患者88例,按照随机数字表法分为对照组与观察组,各44例。对照组患者中男性24例,女性20例;年龄39~78岁,平均(63.46±9.25)岁;格拉斯哥昏迷指数(GCS)评分[3]5~8分,平均(6.82±0.75)分。观察组患者中男性25例,女性19例;年龄40~79岁,平均(63.72±9.18)岁;GCS评分4~8分,平均(6.76±0.71)分。两组患者一般资料经比较,差异无统计学意义(P>0.05),组间具有可比性。诊断标准:参照《高血压脑出血预防与治疗》[4]中的相关诊断标准。纳入标准:符合上述诊断标准,且经头颅CT或MRI检查确诊为重症高血压脑出血者;既往有高血压史者;进行颅内血肿清除术者等。排除标准:合并消化系统疾病者;既往存在营养不良、癌症、糖尿病等疾病者;对本研究药物过敏者等。本研究经院内医学伦理委员会批准,患者家属均签署知情同意书。
1.2 方法对照组患者在术后24~48 h内给予早期肠外营养联合多种微量元素治疗:静脉输入糖、脂肪及氨基酸等营养物质配制成的全静脉营养混合液,同时使用多种微量元素注射液(II)(百正药业股份有限公司,国药准字H20057799,规格:10 mL),将10 mL药物加入5%葡萄糖溶液500 mL中进行静脉滴注,1次/d。观察组患者在对照组的基础上给予早期肠内营养治疗,选用肠内营养混悬液(TPF)[纽迪西亚制药(无锡)有限公司,国药准字H20030011,规格:1.5 kcal/mL],经鼻胃管持续营养泵泵入肠内,第1天控制在患者所需量的25%,速度控制在20 mL/h,之后按每天25%的量递增,直至全量,速度控制在40 mL/h,最大泵入速度不超过125 mL/h,1次/d。两组患者均连续治疗14 d。
1.3 观察指标①营养指标。采集两组患者治疗前后空腹静脉血5 mL,取其中3 mL,以3 000 r/min的转速离心10 min取血清,采用全自动生化分析仪检测两组患者血清白蛋白(Alb)、前清蛋白(PA)、血红蛋白(Hb)及血清总蛋白(TP)水平;采用流式细胞分析仪检测总淋巴细胞计数(TCL)。②免疫功能。血液采集方法同①,取剩余2 mL血液,采用流式细胞仪检测两组患者外周血CD3+、CD4+、CD8+百分比,并计算CD4+/CD8+比值。③并发症、死亡率。比较两组患者并发症发生情况,包括肺部感染、颅内感染、应激性溃疡、腹泻腹胀等,并统计死亡率。
1.4 统计学分析采用SPSS 21.0统计软件分析数据,计数资料以[ 例(%)]表示,行χ2检验;计量资料以(±s)表示,行t检验。以P<0.05表示差异有统计学意义。
2 结果
2.1 营养指标治疗后,两组患者血清Alb、PA、Hb及观察组患者TP水平均显著升高,且观察组显著高于对照组,差异均有统计学意义(均P<0.05);而两组患者治疗前后和组间TCL与对照组患者治疗前后TP水平经比较,差异均无统计学意义(均P>0.05),见表1。
表1 两组患者营养指标比较(±s)
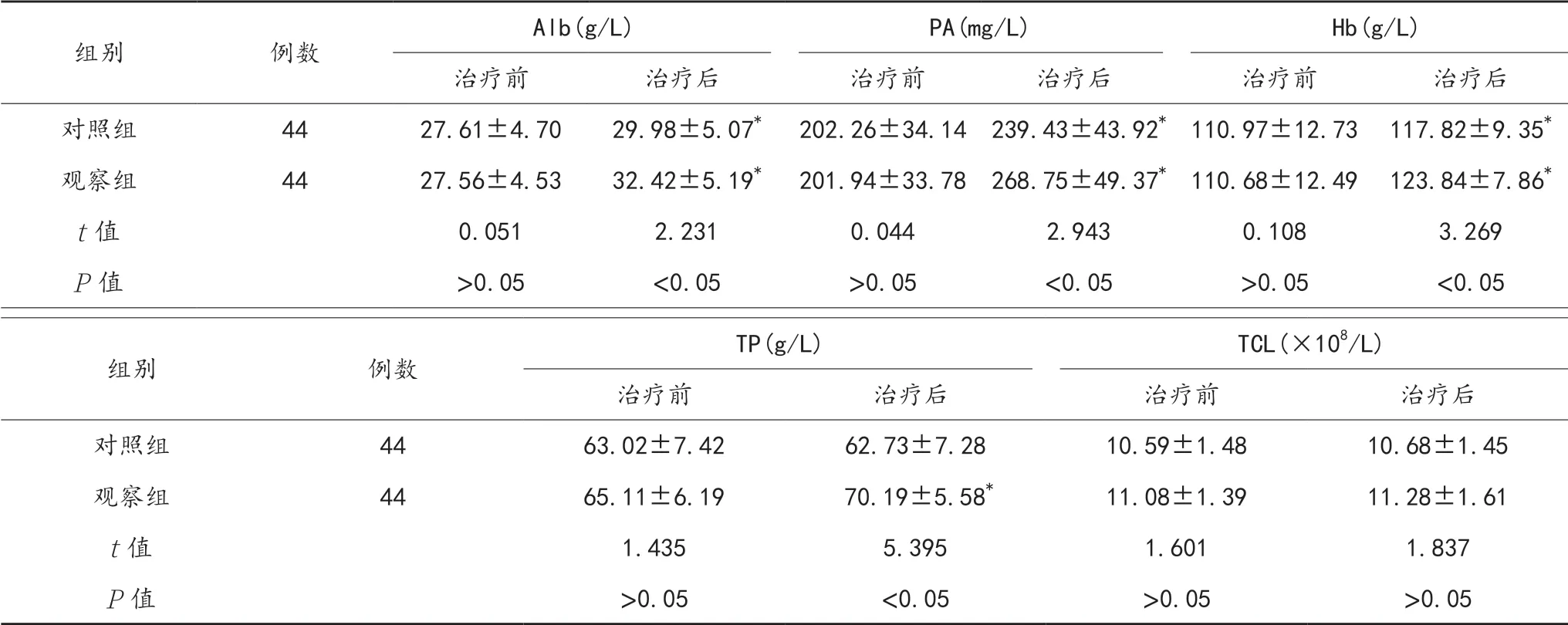
表1 两组患者营养指标比较(±s)
注:与治疗前比,*P<0.05。Alb:白蛋白;PA:前清蛋白;Hb:血红蛋白;TP:血清总蛋白;TCL:总淋巴细胞计数。
组别 例数Alb(g/L) PA(mg/L) Hb(g/L)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照组 44 27.61±4.70 29.98±5.07* 202.26±34.14 239.43±43.92*110.97±12.73 117.82±9.35*观察组 44 27.56±4.53 32.42±5.19* 201.94±33.78 268.75±49.37*110.68±12.49 123.84±7.86*t值 0.051 2.231 0.044 2.943 0.108 3.269 P值 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05组别 例数TP(g/L) TCL(×108/L)治疗前 治疗后 治疗前 治疗后对照组 44 63.02±7.42 62.73±7.28 10.59±1.48 10.68±1.45观察组 44 65.11±6.19 70.19±5.58* 11.08±1.39 11.28±1.61 t值 1.435 5.395 1.601 1.837 P值 >0.05 <0.05 >0.05 >0.05
2.2 免疫功能治疗后,两组患者外周血CD3+、CD4+百分比、CD4+/CD8+比值均显著升高,且观察组显著高于对照组,观察组患者外周血CD8+百分比显著降低,且显著低于对照组,差异均有统计学意义(均P<0.05);而对照组患者治疗前后外周血CD8+百分比经比较,差异无统计学意义(P>0.05),见表2。
表2 两组患者免疫功能指标比较(±s)
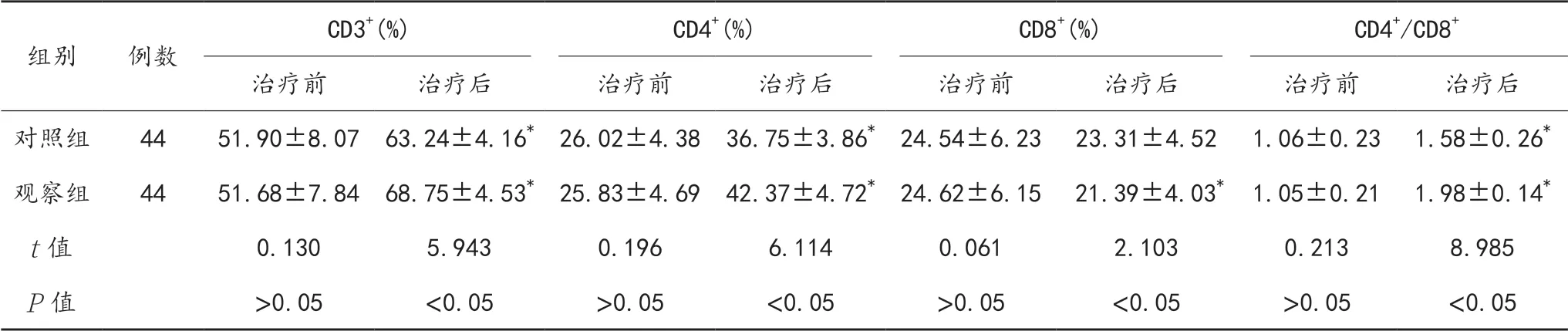
表2 两组患者免疫功能指标比较(±s)
注:与治疗前比,*P<0.05。
组别 例数CD3+(%) CD4+(%) CD8+(%) CD4+/CD8+治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照组 44 51.90±8.07 63.24±4.16*26.02±4.38 36.75±3.86*24.54±6.23 23.31±4.52 1.06±0.23 1.58±0.26*观察组 44 51.68±7.84 68.75±4.53*25.83±4.69 42.37±4.72*24.62±6.15 21.39±4.03* 1.05±0.21 1.98±0.14*t值 0.130 5.943 0.196 6.114 0.061 2.103 0.213 8.985 P值 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05
2.3 并发症与死亡率治疗后,两组患者并发症发生率与死亡率经比较,差异均无统计学意义(均P>0.05),见表3。

表3 两组患者并发症发生率与死亡率比较[ 例(%)]
3 讨论
重症高血压脑出血极易发生多种并发症,早期手术清除颅内血肿是释放颅内压、改善脑血液循环的常用治疗方法,但患者机体处于高代谢与负氮平衡状态,免疫力下降,增加了感染和其他并发症的发生风险。肠外营养支持是以往临床常用的营养供给方式,经静脉途径给药简单易行,减轻了机体胃肠负担,且可降低胃肠对营养物质的不耐受性,但肠外营养只可在特定的短时间内使用,且易产生饱感综合征,在一定程度上抑制了胃蠕动,不利于术后患者胃肠功能的恢复[5]。
经鼻饲给予早期肠内营养支持是重症高血压脑出血术后患者重要的营养供给方式,通过鼻饲注入营养液,可促进胃肠蠕动,加快胃肠功能的恢复,并提供机体代谢必需的营养物质,改善负氮平衡,从而促进免疫功能恢复[6]。临床研究显示,高代谢状态下的危重症患者对微量元素的需求明显增加,尤其是机体炎症反应较重时,对锌、铜、锰等微量元素的消耗显著增加[7]。T淋巴细胞亚群主要用于抵御病原体与稳定T细胞受体结构,其水平的高低可直接反映机体免疫功能高低。本研究结果显示,治疗后,观察组患者外周血CD3+、CD4+百分比及CD4+/CD8+比值均显著高于对照组,外周血CD8+百分比显著低于对照组,提示早期肠内营养联合肠外营养、多种微量元素治疗重症高血压脑出血可增强患者免疫功能,且安全性良好。
在重症高血压脑出血术后患者的恢复中,因机体缺乏营养供给,营养指标随疾病发展不断下降,且术后患者处于高代谢状态,加快了自身营养成分的消耗,进而影响术后恢复。血清Alb、PA、Hb、TP、TCL水平是反映机体营养状态的重要指标,经鼻饲给予肠内营养支持,不足的部分由多种微量元素补充,可通过机体消化酶的分泌,使营养得到全面的吸收,且有助于肠黏膜结构与功能的完整性[8]。本研究结果显示,治疗后,观察组患者血清Alb、PA、Hb、TP、TCL水平均显著高于对照组,提示早期肠内营养联合肠外营养、多种微量元素治疗重症高血压脑出血可有效提升患者的营养指标,促进机体恢复。
综上,早期肠内营养联合肠外营养、多种微量元素可提升重症高血压脑出血术后患者的营养指标,增强免疫功能,且安全性良好,值得临床推广与应用。
