彩超联合超声造影定量参数对肺癌的评估价值
2021-10-28孙永军
孙永军
(商丘市第二人民医院 超声科,河南 商丘 476000)
肺癌的明确诊断主要依靠病理学检查,可通过穿刺活检或术后病理学检查进行定性,但该种方式具有一定创伤,且部分患者存在手术禁忌证,临床运用受限[1]。因此,需寻找更有效的评估肺癌方法。彩超多普勒血流技术可通过观察肿块内部血流信号的分布及数量来反映恶性肿瘤新生血管生成情况,对鉴别肺部良恶性病变具有重要意义[2]。但彩超对低速血流及分布紊乱的小血管不敏感,且受患者呼吸影响较大,易出现误诊、漏诊情况[3]。超声造影(contrast-enhanced ultrasound,CEUS)通过注射造影剂可更清晰显示病灶组织内微血管分布情况,且低机械指数条件下可实时动态观察造影剂灌注情况,能够弥补超声检查的不足,在肺部疾病评估中应用较广[4]。但彩超相关参数联合CEUS定量参数评估肺癌的研究较少,鉴于此,本研究旨在分析彩超联CEUS定量参数评估肺癌的价值。
1 资料与方法
1.1 一般资料本研究经商丘市第二人民医院医学伦理委员会批准。选取2018年3月至2021年3月医院收治的80例周围型肺部肿块患者为研究对象,患者及家属均签署知情同意书。(1)纳入标准:①入院时经CT检查可见肺周围型占位性病变,且肿块>1 cm;②接受彩超、CEUS检查;③接受手术为主的综合治疗;④患者意识清晰,依从性良好,可获得手术病理结果。(2)排除标准:①合并重度肺动脉高压或高血压未控制的患者;②具有严重性心肺功能疾病的患者;③对造影剂过敏的患者;④因各种原因导致检查的图像质量不清的患者;⑤合并其他部位恶性肿瘤的患者;⑥具有放化疗手术史的患者;⑦肿瘤深度≥5.5 cm的患者。入选的80例患者中,男51例,女29例;年龄45~75岁,平均(63.96±3.42)岁;病灶最大直径1.78~9.78 cm,平均(5.39±1.01)cm。
1.2 检查方法
1.2.1彩超检查 选择仪器为西门子彩色多普勒超声诊断仪,探头频率设置为1.5~4.0 MHz。患者取仰卧位,根据患者CT检查结果确定病变大体位置,尽量拉开肋间隙以增大透声窗,利用二维超声对患者肺部进行全面探查,观察病灶位置、大小、形态、内部回声等情况,对病灶进行初步判断;嘱咐患者屏住呼吸至少10 s,以此减少运动伪影,将仪器调整为彩色多普勒血流成像模式,彩色增益应调至不出现噪音的位置,利用脉冲多普勒进行血流参数采集,探查病灶及周边1 cm范围内的血流情况,寻找到动脉血管,声速与血流夹角<60 °,宽度为1 mm,确定血流频谱类型,测量动脉峰值流速(peak velocity,Vp)、阻力指数(resistance index,RI),每个指标检测3次,取平均值。
1.2.2CEUS检查 将多普勒超声探头频率设置为4 MHz,模式为增强造影模式,机械指数为0.19,嘱咐患者平静呼吸,经肘前静脉团注2.4 mL声诺维造影剂(Bracco International B.V,批准文号H20171213),3 s内完成,快速推注5 mL生理盐水冲管,注射造影剂后用实时灰阶谐波超声成像扫查病灶,启动计时器,患者保持姿势不变,尽量保持呼吸平稳,连续观察病灶5 min后存储病灶,动态图像以数字化形式进行储存;观察肺部肿块的开始增强时相、模式和程度,利用计算机软件,观察肿块的增强表现,并根据病灶内造影剂增强的程度不同,将感兴趣区(region of interest,ROI)放置于病灶高灌注或低灌注区,ROI面积相同,根据计算机显示的时间-强度曲线获得峰值强度(peak Intensity,PI)、达峰时间(time to peak,TTP)、病灶始增时间(arriving time,AT)。均检测3次,取平均值。
1.2.3手术病理学检查 影像学参数检查后,所有患者均接受手术治疗,术中取组织送入病理科进行组织病理检查,将标本进行常规处理(脱水、石蜡包埋、切片、HE染色等),于显微镜下观察标本,由2名经验丰富的病理科医生与主治医生参照《中国原发性肺癌诊疗规范(2015年版)》[5]结合手术情况对周围型肺部肿块进行定性评估。记录术后病理结果、彩超与CEUS检查相关参数,以术后病理学结果为“金标准”,分析彩超联合CEUS定量参数评估肺癌的价值。

2 结果
2.1 术后病理结果80例周围型肺部肿块患者经术后病理检查结果显示,44例确诊为肺癌,占55.00%(44/80)。
2.2 彩超定量参数检查结果肺癌组动脉RI值大于良性组,差异有统计学意义(P<0.05);两组Vp值比较,差异无统计学意义(P>0.05)。见表1。
表1 两组彩超检查结果比较
2.3 CEUS定量参数检查结果肺癌组PI大于良性组,TTP小于良性组,差异有统计学意义(P<0.05);两组AT值比较,差异无统计学意义(P>0.05)。见表2。
表2 两组CEUS检查结果
2.4 彩超与CEUS检查相关参数单独及联合评估肺癌的价值以周围型肺部肿块检查情况作为状态变量(“1”=肺癌,“0”=良性病变),将动脉RI、PI、TTP值(均为连续变量)作为检验变量,绘制ROC曲线图(图1)结果显示,RI、PI、TTP值单独及联合评估肺癌的AUC分别为0.750、0.871、0.835、0.916,均有一定评估价值,且当RI值取0.675,PI值取63.757%,TTP值取23.705 s时,可获得最佳评估效能。见表3。
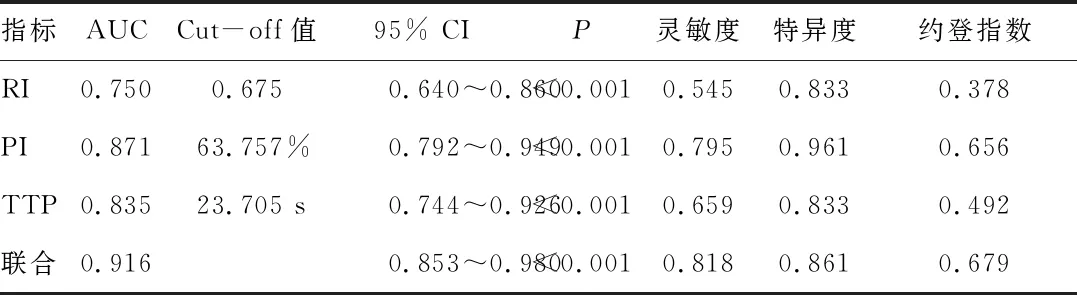
表3 彩超与CEUS检查相关参数评估肺癌价值

图1 RI、PI、TTP值单独及联合评估肺癌价值的ROC曲线图
3 讨论
病灶的形态学和血供特征可为肺癌良恶性的鉴别提供重要信息,以往临床常用的X线、CT影像学技术无法提供血供特征,导致肺癌检出率较低,应用受限。组织活检虽然检查准确率较高,但创伤较大,患者接纳度低。因而,采取更为安全有效的方法评估肺癌具有必要性。
彩超是一种无创、可重复获得器官组织血流动力学信息的一种检查方法。而肺癌血供主要来源于支气管动脉,肺部血流动力学指标可反映肿瘤血供情况,为鉴别良恶性肿瘤提供信息。本研究结果显示,肺癌组动脉RI值大于良性组,初步提示RI值对评估肺癌可能具有一定价值。恶性病灶内新生血管数量较多,随着血供不断增加可形成压力梯度,导致恶性病灶内RI值增加[6]。此外,慢性炎症与肺癌密切相关,而炎症性纤维组织可使肺动脉血管出现变形、闭塞,加上新生小血管压迫肺动脉小分支,引起病灶内微循环障碍,使肺动脉血流速度减慢,RI值变大[7]。但是本研究中,两组Vp值之间无差异性,可能是由于血流不仅与新生血管生成相关,还与病灶大小、细胞凋亡等具有一定关系,部分恶性肿瘤病灶较小,且炎症疾病也可引起病灶内部循环障碍,进而导致两组Vp值差异不大。
CEUS主要利用造影剂来增强病灶内血流灌注信号强度,可客观反映肺癌的血流动力学,尤其可显示肿瘤微血管的数量、走形等情况,为评估肺癌提供影像学依据[8]。有研究指出,CEUS定量参数不仅取决于肿瘤内部的微血管数量,还与其微血管的形态、结构有关,而肺部良恶性病变的血管形态、结构具有差异[9]。可见,利用CEUS定量参数可评估肺癌。本研究结果显示,肺癌组PI大于良性组,TTP小于良性组,表明PI、TTP值对评估肺癌可能具有一定的价值。血管来源是鉴别良恶性肿瘤的重要方式,肺部恶性肿瘤内部具有大量新生血管,新生血管特点为中层平滑肌缺乏,动静脉短路等,因此,造影剂在早期可快速进入病灶内,并达到最大增强强度,因而PI值较大,TTP值较小[10]。此外,病灶数量、直径等与恶性程度呈正相关,恶性肿瘤内新生血管生成导致病灶之间的密度变大,因而注射造影剂后可快速集聚于病灶内的某一个区域,TTP值较低,并出现PI值升高特征[11]。但是本研究中,两组AT值之间无差异性,主要是由于部分良性病变病灶内血流较为丰富,导致AT值与恶性病变较为相似。
本研究进一步绘制ROC曲线结果显示,RI、PI、TTP值单独及联合评估肺癌的AUC均>0.7,具有一定的诊断价值,且当RI值取0.675,PI值取63.757%,TTP值取23.705 s时可获得最佳评估效能。可见,彩超联合CEUS定量参数评估肺癌价值较高。但受声窗、肺内气体等影响,彩超检查时可出现图像质量不清情况;此外,CEUS的时间-强度曲线受心搏、病灶位置与血供、ROI选择等影响,因而两者联合检查时仍可出现误诊或漏诊情况,建议临床可结合其他影像学技术(如CT、X线等)综合评估肺癌。
综上所述,彩超联合CEUS定量参数评估肺癌具有一定价值,临床可考虑通过彩超联合CEUS定量参数评估肺部占位性病变。
