基于多特征融合的睡眠分期
2021-10-27熊馨罗剑花王春武易三莉刘瑞湘贺建峰
熊馨 罗剑花 王春武 易三莉 刘瑞湘 贺建峰
0 引言
睡眠是人体中不可缺少的一种生理活动,睡眠质量的好坏直接影响人的健康、工作和情绪。因此,睡眠分期的研究对睡眠障碍及相关疾病的诊断和睡眠质量的评估具有重要的意义。目前国际上通用的睡眠分期原则是R&K(Rechtschaffen和Kales)的分期准则[1],将睡眠分为清醒期(wake,W)、非快速眼动期(no-rapid eye movement,NREM)和快速眼动期(rapid eye movement,REM),其中非快速眼动期又分为N1期、N2期和N3期。
睡眠分期包括数据采集、预处理、特征提取和分类4个过程,其中,特征提取的方法对分类结果具有重大影响,因此特征提取在睡眠分期过程中至关重要。针对睡眠生理信号的特性,有时域、频域、时频域和非线性特征提取方法。时域方法包括方差分析等,频域方法包括功率谱估计等,而时频(小波包变换等)分析方法把时域和频域结合起来,可以描述出脑电(electroencephalogram,EEG)、肌电(electromyogram,EMG)、眼电(electro-oculogram,EOG)等在时间和频率上的能量和谱密度[2]。非线性分析方法为提取EEG、心电(electrocardiogram,ECG)等的非线性特征开辟了新途径,常用的非线性分析方法有样本熵、模糊熵、最大Lyapunov指数和去趋势波动等[3-4]。
程佳[5]采用小波、小波包、功率谱熵和多尺度熵的方法,证明这些方法可用于睡眠分期;唐其彪[6]运用小波包、样本熵和模糊熵的方法,睡眠分期的平均准确率达到91.4%;郑声涛等[7]将小波包能量用于睡眠分期,发现脑电节律是研究睡眠分期的关键环节。然而上述这些研究仅仅在健康被试中进行了验证,并没有在睡眠障碍患者中验证算法的性能。目前同时在健康受试者和睡眠障碍患者中验证算法性能的研究较少。比如,Boostani等[8]的研究结果显示对于健康受试者和睡眠障碍患者,采用小波熵系数+随机森林,睡眠分期的准确率分别为87.06%和69.05%。除此以外,目前关于睡眠分期研究大多数仅采用EEG通道[5-6,8],没有充分利用睡眠生理信号的多样性且睡眠分期的识别率没达到令人满意的效果。曾有吕甜甜等[9]研究结果证实采用EEG、EMG、ECG通道和呼吸信号的均值睡眠分期的准确率为92.95%,交叉验证后的平均准确率是85.15%,比仅采用EEG通道准确率提高9.65%。叶仙等[10]针对EEG和EOG信号,采用精细复合多尺度熵,睡眠分期的准确率达到85.3%。何垣谛[11]利用卷积神经网络和长短期记忆循环神经网络,EEG、EOG和EMG通道的睡眠分期准确率达到了85.56%。Khalighi等[12]对40名患者进行睡眠分期,采用最大重叠小波变换提取时频特征,针对EEG、EOG和EMG信号,睡眠分期的准确率为81.74%。这些研究显示采用多特征、多通道的方法可以有效提高睡眠分期的准确率,但是准确率还有待提高。为此本文拟提出采用样本熵、小波包能量和去趋势波动提取特征的方法,并针对EEG、ECG和EMG信号,对睡眠分期进行研究,同时在健康受试者和睡眠障碍患者中验证。
1 研究方法
1.1 数据来源
实验数据来源于葡萄牙科英布拉大学睡眠医学中心的ISRUC-Sleep数据集[13],这些生理信号(EEG、ECG和EMG信号等)的持续时间均为8 h。选取Subgroup-Ⅰ的前10名睡眠障碍患者,这些患者均有呼吸暂停的症状,平均年龄为51岁,部分患者因为其他并发症正在接受药物治疗,均在没有机器帮助的情况下呼吸。对照组选取Subgroup-Ⅲ的10名健康受试者,平均年龄为40岁。选取6个EEG通道(F3-A2、C3-A2、O1-A2、F4-A1、C4-A1、O2-A1)、1个ECG通道(X2)和1个下颌EMG通道(X1)。降采样率为100 Hz,对EEG信号进行50 Hz的陷波滤波和带通滤波(1~40 Hz);ECG信号进行50 Hz的陷波滤波;EMG进行50 Hz的陷波滤波和带通滤波(10~70 Hz)。将数据分割成30 s的一个片段,其中,健康受试者共8 914段数据,睡眠障碍患者共9 263段。
1.2 多特征提取
1.2.1 样本熵
设原始生理信号的时间序列为{y(i)},i=1,2,3,…,N。样本熵[14]的计算步骤如下所示:
(1) 对时间序列Y(i)组成一组m维序列:
Y(i)=[y(i),y(i+1),…,y(i+m-1)]
(1)
其中1≤i≤N-m+1。
(2) 计算矢量Y(i)和矢量Y(j)之间的距离:
d[Y(i),Y(j)]=max|y(i+k)-y(j+k)|
(2)
其中0≤k≤m-1。i,j∈(1,N-m+1),并且i≠j。
(3) 对于给定的相似容限r,计算d[Y(i),Y(j)]小于r的数目,并计算该数目与距离总数N-m+1的比值,记为Bim(r),即:
(3)

(4)
(5) 同理,按照式(1)~(4)可求得m+1维序列的平均数量为Bm+1(r):
(5)
(6) 该序列的样本熵表达式为:
(6)
(7) 当N为有限值时,式(6)可简化为:
SampEn(m,r,N)=-ln[Bm+1(r)/Bm(r)]
(7)
由式(7)可知,样本熵的值m和r有很大的关系。m的取值一般选择1或2,r=(0.1~0.25) std(y)。
1.2.2 小波包变换
小波包变换比小波提供了一种更加精细的特征提取方法[15]。
(1) 对小波包进行分解,小波包分解的算法为:


(9)
(3) 对计算出来的能量构造特征向量。对分解出来的这些节点系数分别用范数计算出能量值,构造特征向量:
V=[Ei,j]
(10)
式中:i为小波包分解的层数;j为第j个节点频段。
(4) 将特征向量归一化。即各节点(i,j)能量占总能量的比值:
V=[Ei,j]/E
(11)
1.2.3 去趋势波动分析
去趋势波动分析(detrend fluctuation analysis,DFA)可用来找出时间序列中的长期统计相关性[16]。对时间序列为X(i),i={1,2,…,N}的EEG、ECG等信号进行DFA分析,计算步骤如下。
(1) 根据原始生理数据X(i)计算出它的平均值Xave,然后计算出X{i}-Xave的值,最后再对这些值进行求和,即:
(12)
(2) 对长度为L的和序列Y(k)进行数据分割,分割成多个等间隔的子序列l,然后对每个子序列运用最小二乘法进行多项式拟合,得到拟合序列Yn(k)。
(3) 去除波动趋势,并计算出波动标准差:
(13)
f(l)会随着子片段长度l的增加而增加,根据它们之间的幂函数相关性,可以得出:
f(l)∝lα
(14)
式中:α为标度指数。
(4) 计算标度指数α的值。以lg[f(l)]为纵坐标、以lgl为横坐标,α的值它们二者线性拟合得到的值,即曲线的斜率。从标度指数α即可观察出EEG信号的长程幂律相关性。
2 实验结果与分析
2.1 样本熵
健康受试者和睡眠障碍患者不同睡眠时期样本熵的均值如表1所示,其中,N取3000,m取2,r取0.2。

表1 健康患病个体各睡眠时期的样本熵均值
由表1可以看出,健康受试者清醒期EEG和ECG的样本熵均值最大。这是因为清醒期大脑接收到的信息量比较大,神经细胞比较活跃,复杂性较高[17]。当进入非快速睡眠时期,样本熵均值逐渐降低,代表进入睡眠以后,人脑还进行着一定的神经活动,但是强度相对于清醒期降低了,随着睡眠深度的深入复杂度也降低了,并在N3期达到了最低点,δ节律占比超过50%,此时已进入深睡眠状态。快速眼动则介于清醒期和非快速眼动期,这时会出现呼吸不均匀,血压忽高忽低,眼球快速转动,说明人处于做梦状态,具有一定的意识,所以神经元的活动又开始增强。睡眠障碍患者EEG的样本熵均值随着睡眠深度的加深而降低,但清醒期的样本熵均值并不是最大的,N1期的样本熵均值最大,这跟健康受试者的表现不同。ECG的样本熵均值清醒期是最大的,随着睡眠深度的加深呈现出“Λ”的形势,REM期达到最低点。
2.2 小波包能量
2.2.1 提取脑电节律
本文选择db4的6层小波包分解[18]。按照小波包系数的频带范围,选择节点(6,1)+(5,1)+(6,4)代表δ节律,频率范围为0.78125~3.125;选择节点(5,3)+(6,8)代表θ节律,频率范围为4.6875~6.25;选择节点(4,3)+(6,16)代表α节律,频率范围为9.375~12.5;选择节点(2,2)代表β节律,频率范围为12.5~25。
肌电信号的高频范围是10~70 Hz之间,因此本文采用sym3小波基对肌电信号进行三层小波包分解,产生8个节点系数,选择(3,5)+ (3,6)+ (3,7)+ (3,8)这几个节点,即肌电信号的高频部分。
2.2.2 计算各睡眠时期的脑电节律能量比
健康受试者和患病受试者各睡眠时期的脑电节律能量占比和肌电信号的能量占比,如图1所示。

图1 各睡眠时期的EEG节律能量占比和EMG信号能量占比
从以上结果可知,各睡眠时期的脑电节律成分是不一样的,健康受试者清醒时期α和β节律比较明显,随着睡眠的深入,θ和δ所占的能量比重在增大,α和β节律的能量比重在减少,睡眠眼动时期的脑电节律则介于清醒期和非快速眼动时期,这时期既含有θ节律又含有α节律,这一规律符合睡眠分期指标的规定。睡眠障碍患者的δ节律和β节律比较明显,随着睡眠的深入,各脑电节律的能量比逐渐下降。健康受试者的EMG能量比随着睡眠深度的深入逐渐减小,N3期的能量占比达到最大值,睡眠眼动时期能量比最小。说明人在进入深度睡眠时肌肉能量比较大。患病受试者的EMG能量随着睡眠的深入也在逐渐减小,除了N3期和REM期以外,能量比都高于健康受试者。
2.3 去趋势波动
去趋势波动可以通过标度指数α来观察各睡眠时期脑电信号的波动性[19],当α<0.5时,表示原序列相互独立;当α=0.5时,表示原序列为白噪声;当0.5<α<1.0时,原序列长程幂律相关;当α=1.0时,是1/f噪声;当1<α<1.5时,原序列是相关的,但不是幂律的关系;当α=1.5时,表明原序列为布朗噪声。表2即为各个睡眠时期与标度指数的关系。
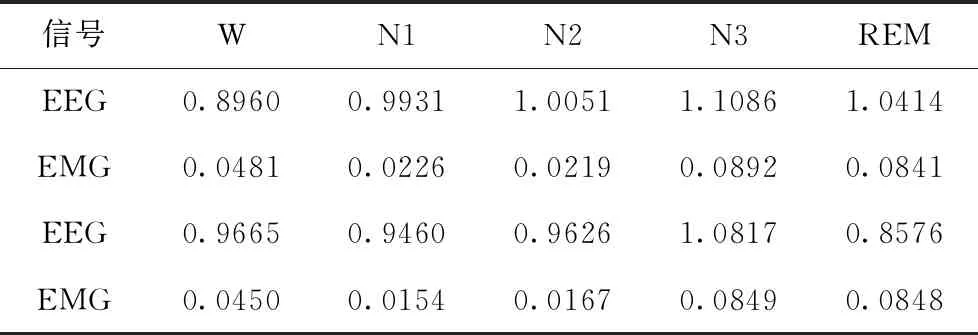
表2 每个睡眠期的标度指数
从表2可以看出,随着睡眠深度的加深,健康受试者EEG(N1~N3)的标度指数是增加的,这时大脑的活跃性也逐渐降低,清醒期的标度指数最小,证明健康受试者在不同睡眠时期在时间上具有长程相关性,对不同的睡眠状态具有一定的区分度。睡眠障碍患者的标度指数在N1~N3也在逐渐增大,呈现出部分长程相关性。健康受试者EMG信号的标度指数呈现出一个“V”形的长程趋势,睡眠障碍患者标度指数呈现的趋势与健康受试者相似,区别在于患病受试者的标度指数比健康被试小。
2.4 睡眠分期
本文运用样本熵、小波包变换和去趋势波动三种方式来提取健康受试者和睡眠障碍患者的特征值。将所提取到的特征值用SVM模型计算睡眠分期的准确率。观察不同特征提取方式下EEG和加入ECG、EMG后的准确率,实验结果如表3所示。
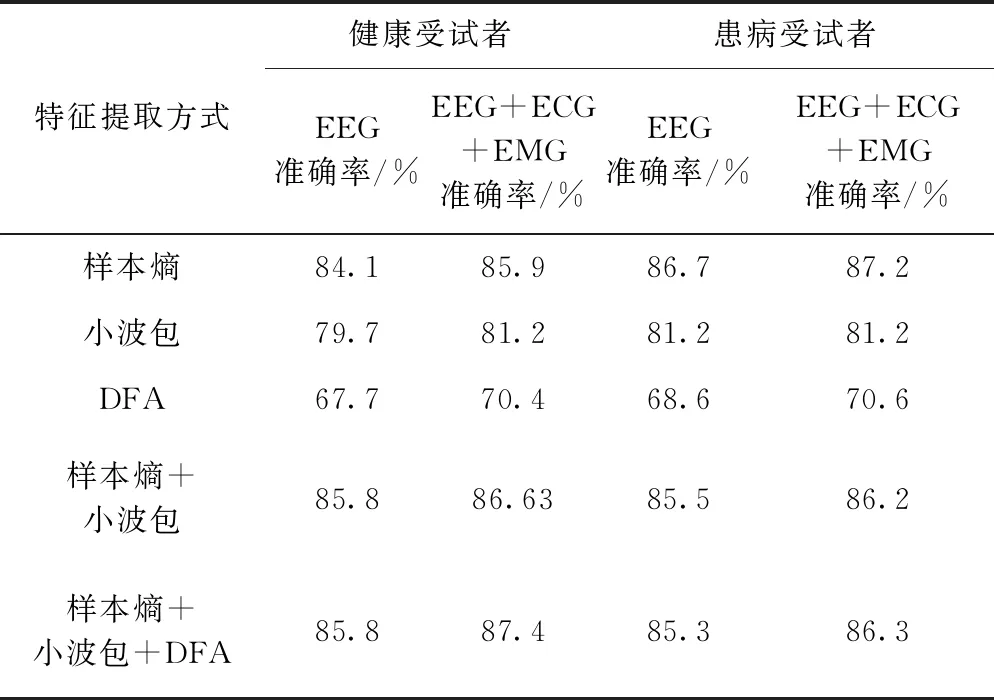
表3 基于SVM多特征融合的睡眠分期的准确率
从实验结果可知,健康人多通道、多特征单一的识别率高于EEG单一的识别率,并且这3种方法特征融合的睡眠分期准确率已经达到87.4%,说明多通道、多特征的分期准确率更好。患病受试者多通道、多特征睡眠分期的准确率也高于EEG的准确率,其中样本熵的识别效果最佳。说明无论睡眠障碍患者还是健康受试者,多通道、多特征有更高的准确率,而且健康受试者的准确率相对于睡眠障碍患者更好。
针对上述健康受试者和睡眠障碍患者SVM最终的准确率,得到睡眠分期的准确率、召回率和F1分数。其中,0代表W期(清醒期),1代表N1期(非快速眼动1期),2代表N2期(非快速眼动2期),3代表N3(非快速眼动3期),4代表REM(快速眼动期)。实验结果如表4和表5所示。

表4 健康被试各睡眠时期的准确率、召回率和F1分数

表5 患病被试各睡眠时期的准确率、召回率和F1分数
从上述分析结果可以得出,健康受试者和患病受试者清醒期睡眠分期的准确率、召回率和F1分数最高,随着睡眠深度的深入(N1→N3)准确率、召回率和F1分数逐渐增加,REM期的准确率、召回率和F1分数则介于清醒期和非快速眼动期。
3 讨论
本文运用样本熵、小波包能量和去趋势波动的特征提取方法,来证实多通道、多特征方法的可行性。文献[9]采用了EEG、ECG、EMG和呼吸信号4种生理信息,文献[10]采用了EEG和EOG两种生理信息,文献[11]采用了EEG、EOG和EMG 3种生理信号,本文采用的是EEG、ECG和EMG三种生理信号。文献[9]比本文多了一种生理信号,采用EEG和ECG睡眠分期的准确率为85.11%,本文运用EEG和ECG时达到85.9%,睡眠分期的准确率比其高0.79%;二者都是采用样本熵来处理EEG和ECG,但是采用的数据集不同,预处理方法也不同,本文采用的是巴特沃斯滤波器,而文献[9]采用的是小波去噪。文献[10]采用精细复合多尺度熵,准确率为85.3%,本文计算了EEG和EOG的样本熵,但是识别效果不佳,准确率为53.1%,计算EEG和ECG的样本熵,识别效果好,准确率是85.3%,可能原因是ECG比EOG包含更多关于睡眠分期的信息。文献[11]运用卷积神经网络和长短期记忆循环神经网络的准确率达85.56%,本文运用样本熵、小波包能量、DFA的特征提取方法也分析了EEG、EOG和EMG信号,睡眠分期的准确率为86%,比文献[11]高了0.44%。
除了在健康受试者中验证提出的方法,还对20名睡眠障碍受试者进行验证,睡眠分期的准确率达到69.05%,本文中10名睡眠障碍受试者的睡眠分期准确率达到85.8%,文献[8]采用的是单通道EEG信号,而本文采用的是多通道信号,多通道脑电的睡眠分期分类性能更好。文献[12]和本文使用的数据集都是ISRUC-Sleep数据集,并且预处理的方式也相同,文献[12]中采用了最大重叠小波变换提取时频特征,睡眠分期的准确率达到81.74%,而本文采用样本熵、小波包能量和去趋势波动相结合的方式,对多通道生理信号进行分析,实验发现EEG、ECG和EMG组合的效果最好,睡眠分期的准确率为86.3%。
4 结论
本文提出了一种多通道、多特征融合的方法,并在健康受试者和睡眠障碍患者中进行实验,实验结果表明,不论是在健康受试者还是睡眠障碍患者中,EEG+ECG+EMG睡眠分期的准确率都优于EEG睡眠分期的准确率,并在W期、N2期、N3期和REM期的准确率都有所提高。
