低共熔溶剂在油脂改性中的应用研究进展
2021-10-27李道明钟小荣易玖宏张佳浩
李道明,钟小荣,易玖宏,张佳浩
(陕西科技大学 食品与生物工程学院,陕西 西安 710021)
0 引言
自20世纪90年代就出现了“绿色化学”一词,为推动绿色化学和可持续发展,人们正试图寻找更安全、更清洁、更高效且经济上可行的绿色生产工艺,可持续性的绿色溶剂成为了当前研究的热点.离子液体(ionic liquid solvents,ILs)是一种完全由离子组成的绿色溶剂[1],与传统的溶剂相比,其具有可设计性、不易挥发、热稳定性好、溶剂化能力强等优点[2-4].而基于ILs的毒性、离子组分降解性差且制备成本较高等缺点,低共熔溶剂(Deep eutectic solvents,DESs)逐渐代替ILs成为新一代绿色溶剂[5,6].
2003年,Abbott等[7,8]首次发现由氯化胆碱和尿素形成的液体混合物具有独特的溶剂性质,这一混合物与ILs的性质类似,但是熔点的降低程度小于类似的金属氯酸盐体系.目前研究表明氢键相互作用是形成DESs的主要原因,且氢键的强度直接影响DESs的熔点等热力学性质[9].DESs作为一种新型绿色溶剂,既具备前述的ILs所具有的优势外,又克服了其缺点.DESs与ILs具有相似的应用,但因DESs的成分安全且价格低可用于食品与药品领域.目前,DESs在萃取[10]、有机合成[11]、酶催化反应[12]、二氧化碳吸附[13]、生物柴油合成[14]、电化学[15]、材料制备[16]等领域都有广泛的应用.目前在油脂改性领域中,DESs主要用于合成生物柴油、功能性油脂及提取反应副产物等,但DESs在油脂改性领域中的应用仍有许多问题需要解决.例如,关于DESs的制备和表征方法的统一标准、DESs的性质与结构的关系及DESs对生物催化规律的影响等.
基于已有的研究表明DESs在油脂改性领域得到广泛的关注,但目前还没有关于这方面的综述性文章.因此,本文是基于近十年DESs在油脂改性领域中的应用,对其进行总结与展望.为推动DESs在油脂改性领域中的工业化应用提供参考.
1 DESs的定义与分类
DESs是两种或多种固体组分在一定温度下按一定摩尔比制备形成的液体混合物,也可定义为由氢键供体(Hydrogen bond donors,HBDs)和氢键受体(Hydrogen bond receptors,HBAs)按一定摩尔比形成的低共熔混合物[17].HBAs一般为季铵盐,HBDs主要包括酰胺类、有机酸类、氨基类、糖类、醇类等.图1为常用的HBAs和HBDs.

图1 制备DESs的HBDs和HBAs的结构图
Abbott 等[8]将 DESs的通式定义为R1R2R3R4N+X-Y-.并根据所用络合剂的性质对DESs进行分类,如表1所示.主要包括四种类型的DESs,I型DESs由季铵盐和金属氯化物组成,如氯化胆碱和金属氯化物形成的DESs.II型DESs由季铵盐和金属氯化物水合物组成.许多水合金属盐的成本相对较低,且对空气和水分的不敏感性,使其可应用于工业过程中.III型DESs由季铵盐和羧酸、醇类及胺等组成.IV 型DESs由金属氯化物和醇类及酰胺类物质组成[18].

表1 DESs的四种类型
2 DESs的制备方法
目前DESs的实验室制备方法主要包括加热法、研磨法和冷冻干燥法[11],如表2所示.加热法是在确保DESs中的水分含量的前提下,将一定比例的HBDs和HBAs经过干燥预处理后混合.由于DESs的吸湿性,需在惰性气体环境下加热(通常在60 ℃~100 ℃)[19],后用磁力搅拌器加热搅拌直至出现透明澄清的液体,冷却后立即密封以避免水分吸收,并储存在干燥器中以备日后使用.研磨法主要应用于药学,将化合物干燥后,混合放置在研钵内,室温下进行研磨,直至形成透明均一的液体,随后密封保存.该法制备的溶剂纯度相对加热法高,且水分含量相对加热法低,其缺点在于长期暴露使溶剂水分难以控制[20].冷冻干燥法制备DESs,首先精确称量各组分将其混合,并加入少量的水将其溶解后离心,随后在一定温度下冷冻,最后将加入的水通过冻干除去直至恒重[21].该法制备的溶剂纯度较高,但操作复杂、对设备要求较高.因加热法操作简单是目前制备DESs的主要方法.

表2 DESs的制备方法
3 DESs的性质
3.1 熔点
DESs是由两种固体混合通过氢键相互作用在适当的温度下形成的液体,DES的熔点低于各组分纯物质的熔点.如当氯化胆碱和尿素以1∶2的摩尔比混合制备的DESs的熔点为12 ℃,而氯化胆碱和尿素单独存在时各自的熔点分别为302℃和133 ℃[8].目前报道的大部分DESs的熔点低于150 ℃.DESs的熔点受到多种因素的影响,如HBAs与HBDs的摩尔比,氯化胆碱和尿素的摩尔比为1∶1时熔点大于50℃而摩尔比为1∶2时熔点为12 ℃.此外HBAs的种类也会影响DESs的熔点,如尿素与不同的胆碱阴离子结合形成的DESs的熔点依的顺序下降[8].Abbott等[22]研究表明熔点与有机酸的分子量相关,熔点随分子量的降低而降低.因DESs的熔点受多种因素的影响,根据DESs的类型可以总结出一些关于熔点变化的规律:(1)Ⅰ型DESs是由无水金属卤化物(ZnCl2、ZnBr2、SnCl2等)和季铵盐中的卤化物阴离子相互作用形成的具有相似生产焓的卤金属酸盐.这类DESs要在环境温度下形成低共熔化合物,金属卤化物的熔点一般需要在300 ℃左右或更低;(2)Ⅱ型DESs由水合金属卤化物和HBDs形成.由于金属盐的水化作用降低了晶格能,导致其熔点低于无水盐;(3)Ⅲ型DESs的熔点取决于氢键相互作用和盐/HBDs的摩尔比;(4)Ⅳ型DESs的熔点均在10 ℃下[23].
3.2 黏度
黏度是DESs研究的一个重要参数,大部分的DESs在室温下粘度相对较大都在100 cp 以上.DESs作为一种绿色溶剂在食品、药品等领域具有潜在应用,开发低粘度的DESs具有一定实践意义.DESs的黏度主要受氢键相互作用和范德华力的影响,并与DESs组分的性质、摩尔比、温度和含水量等因素有关[24].如Abbott等[25]研究发现氯化胆碱和乙二醇(摩尔比1∶4)在20 ℃黏度为19 cp,而氯化胆碱和甘油在相同条件下黏度为503 cp,结果表明DESs的黏度与HBDs的种类有关.其次Gajardo Parra等[26]研究发现DESs的黏度会随着温度的升高而显著下降.目前研究表明空穴理论可用于设计低黏度DESs,为DESs的应用提供参考.
3.3 极性
一般来说,分子间的吸引力越大,极性就越大.因此,极性通常是一种增溶性质.溶剂的极性可以通过其极性标度Et(30)来评估,Et(30)是探针染料(如Reichardt′s Dye 30)在溶剂中的电子跃迁能.通过紫外可见分光光度计进行检测,使用Reichardt′s Dye 30,可以用下列公式(1)计算ET(30)[27].

Abbott等[28]使用Reichardt′s Dye方法测定了不同摩尔比的DES(氯化胆碱-甘油)的极性,研究表明随着氯化胆碱/甘油摩尔比的增加,DESs的ET(30)值增加.此外,ET(30)随氯化胆碱浓度的增加而增加.秦晓洁[29]研究发现HBA 是氯化胆碱的DESs普遍比四甲基氯化铵的DESs极性高.
3.4 毒性
DESs作为一种新型绿色溶剂,其可逐步替代ILs主要由于DESs具备一定优势,例如基于氯化胆碱的DESs具有良好的生物兼容性,在许多研究报道中被认为是低毒性、热稳定性好、可生物降解的优良溶剂[30].2013年,Hayyan等[31]首先研究了基于氯化胆碱和基于季膦盐DESs的毒性和细胞毒性,HBDs 为甘油、乙二醇和尿素.研究发现DESs的毒性和细胞毒性随所用成分的结构而异.基于氯化胆碱的DESs 毒性小于基于季膦盐的DESs.随后,有不同的团队评价了不同类型DESs的毒性,某些DESs显示出一定程度的毒性.但由于反应的类型和用途不同,目前关于DESs的毒性研究还存在一定的局限性.
4 DESs在油脂改性领域的应用
4.1 改性油脂生产生物柴油
4.1.1 生物柴油的制备
面对石油供应减少、持续燃烧化石燃料带来的环境和气候问题和基于可再生能源的发展,生物柴油已成为一种可再生、可降解的有吸引力的燃料[32].生物柴油是指由长链烷基酯组成的柴油燃料,通常由脂质与醇发生化学反应生成脂肪酸单酯制成(如图2所示).生物柴油可以从丰富的植物油、动物脂肪、餐饮废油等中制备.目前制备生物柴油的常规化学方法有许多局限性,如腐蚀仪器、乳化问题及脂肪酸皂化等问题.与传统化学法相比,酶法具有反应条件温和、反应副产物少和低废物处理等优点,但酶法合成生物柴油也面临着许多困难,其中之一就是缺乏与脂肪酶相容的非水溶剂.因DESs具有廉价、低毒性、可生物降解、和脂肪酶相容的特点,可作为制备生物柴油的催化剂和溶剂(如表3所示).

表3 在制备生物柴油中的应用

图2 生物柴油的制备原理
2010 年,Long 等[33]在研究中采用由Ch Cl/ZnCl2(1∶2,mol/mol)组成的DESs作为路易斯酸催化剂从大豆油中制备生物柴油,在70 ℃反应72 h,酯交换反应的转化率为54.52%,是制备生物柴油的一种有效的方法.Isahak等[34]从棕榈油中制备了生物柴油,当采用ChCl/ZnCl2(1∶2,mol/mol)和ChCl/FeCl3(1∶2,mol/mol)作为催化剂时,产率分别为70.4%和89.5%.在Ch Cl/ZnCl2(1∶2,mol/mol)溶剂体系中加入H2SO4(20 wt%)催化反应时,产率可提高到92.0%.在脂肪酸含量较高的油脂中,DESs可作为制备生物柴油预处理酯化阶段的催化剂.Hayyan等[35]在脂肪酸含量为9.5%的低级粗棕榈油(Low grade crude palm oil,LGCPO)中,用摩尔比为1∶3 的N,N-二乙基乙醇氯化铵/对甲苯磺酰胺一水化合物组成DEAC-DES 作为催化剂,在优化条件下,LGCPO 中脂肪酸的含量可降至1%以下.DEACDES可作为一种高活性、可循环利用的催化剂.同年,Hayyan等[36]制备了由烯丙基三苯基溴化磷/对甲苯磺酰胺一水化合物(1∶3,mol/mol)组成的P-DES作为一种可回收催化剂,在制备生物柴油过程中可将脂肪酸的含量从9.3%降到2%以下.此外,基于DESs的催化剂可作为多相催化剂的潜在替代品,其可以通过消除过滤和催化剂预处理过程来简化下游操作[37].Zhang等[38]在DESs体系中采用微波辐射的方法从文冠果油中酶法制备生物柴油,该方法在最优条件下转化率可达95%,研究表明该法可代替传统的酯交换法制备生物柴油.
DESs也可作为一种低成本、低粘度、高生物降解性和脂肪酶具有良好相容性的绿色溶剂.Zhao等[39]发现由Ch OAc/Gly(1∶1.5,mol/mol)组成的DES与脂肪酶Novozym 435 具有良好的生物相容性,在该DES中Novozym 435催化Miglyol oil 812 制备生物柴油的酯交换转化率可达97%,研究也表明DESs是生物柴油酶法生产的潜在介质.随后,Zhao等[40]又发现ChCl/Gly(1∶2,mol/mol)组成的DES与Novozym 435也具有良好的生物相容性,催化大豆油酯交换转化率可达88%,且在DES中脂肪酶可重复使用4批次后仍具有良好活性.2014 年,Huang等[41]制备了多种DESs并研究了其对酶性能的影响,研究表明当DESs作为从种籽油中生产生物柴油的反应介质,Novozym 435 比PEL(Penicillium expansum lipase)具有更好的转化率,在Ch Ac/Gly(1∶2,mol/mol)中可获得的最大产率.2018 年,Merza等[42]比较了DES (Ch Cl/Gly)和IL ([bmim][PF6])从废油中酶法制备生物柴油的应用效果.结果表明在DES 中的产率及产量更高,反应4 h后,在DES中的产率比在[bmim][PF6]中的产率高63%.
部分DESs可以与金属催化剂结合,在制备生物柴油中起到良好的效果.2013 年,Huang等[43]制备了一种由ChCl/Gly(1∶2,mol/mol)组成的DES,作为CaO 催化菜籽油酯交换反应制备生物柴油的溶剂.在反应体系中,除作为溶剂外,DES还能通过去除固体催化剂CaO 表面的CaCO3和Ca(OH)2非活性层,激活Ca O 作为酯交换反应的催化剂.且研究表明,添加DESs后的脂肪酸甲酯回收率可达91.9%,而不添加DESs时脂肪酸甲酯回收率仅为4.0%.2015 年,Gu 等[44]将DES(ChCl/Gly)作为NaOH 催化菜籽油酯交换合成生物柴油的共溶剂,在优化反应条件下,脂肪酸甲酯产率可达98%,且减少了副反应(如皂化反应),使生物柴油能够直接分离提纯.
4.1.2 生物柴油的提纯
生物柴油作为一种清洁燃料已引起学术界和工业界的关注,而生产过程会产生大量甘油,从而降低柴油品质.目前已经制定了相关国际标准,如ASTM 标准要求甘油和总甘油的含量必须分别小于0.02 wt%和0.24 wt%[46].DESs作为一种低毒性、低成本且具有良好生物相容性的溶剂正被广泛地研究和应用于生物柴油的提纯,表4总结了部分使用DESs提取甘油的研究.
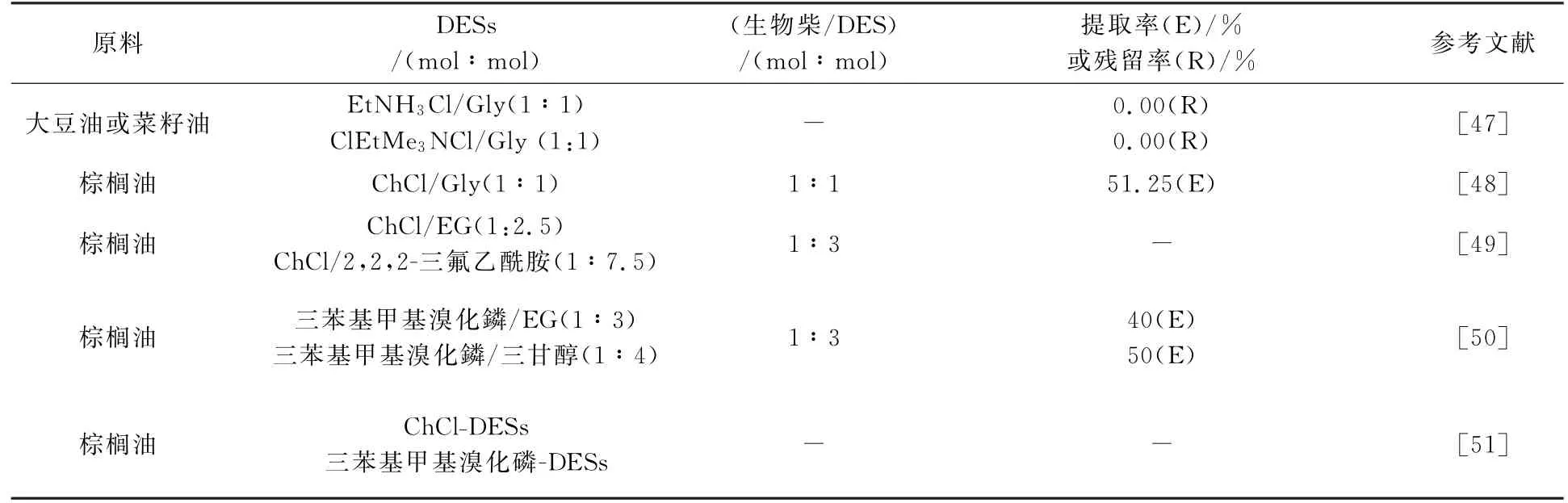
表4 DESs在提取甘油中的应用
2007年,Abbott等[47]比较了不同种类、摩尔比的DESs从生物柴油中提取甘油的能力.研究发现Et NH3Cl/Gly(1 ∶1,mol/mol)和 ClEt-Me3NCl/Gly(1∶1,mol/mol)作为提取溶剂时,生物柴油中甘油的残余率可从0.15%降到0.00%.并且这一研究成功的证明了DESs能够从生物柴油中提取甘油,但甘油和盐类的各自回收值需进一步探索.2009年,Hayyan等[48]研究了棕榈油生物柴油中甘油分离的技术,研究表明甘油提取速率与DESs与生物柴油的比例及DESs的组成有关,当DESs与生物柴油的摩尔比为1∶1 时,萃取率最高可达51.25 wt%.2010 年,Shahbaz等[49]使用ChCl∶乙二醇(1∶2.5)和Ch Cl∶2,2,2-三氟乙酰胺(1∶7.5)组成的DESs提取甘油,配制的DESs与生物柴油摩尔比分别为2.5∶1和3∶1时,能有效地从生物柴油中萃取甘油.2011 年,Shahbaz等[50]研究发现DES4(三苯基甲基溴化磷/乙二醇(1∶3,mol/mol))和DES8(三苯基甲基溴化磷/三甘醇(1∶4,mol/mol))是降低总甘油含量最有效的溶剂,去除率分别达40%和50%.随后,Shahbaz等[51]研究了以氯化胆碱和三苯基甲基溴化磷为原料合成了不同类型的DESs,并利用人工智能技术(基于神经网络的模型,ANN)预测基于铵盐和磷盐的DESs脱除生物柴油中甘油的效果.一方面研究表明基于磷盐的DESs具有更好的甘油脱除效果,另一方面将模型预测的甘油脱除量与实验结果进行比较,平均绝对偏差为6.46%,表明了ANN模型的可靠性.2013年其又研究了基于非甘油的DESs消除游离甘油和减少总甘油的效果.研究表明,铵盐-非甘油的DESs均能成功去除基于棕榈油生物柴油中的甘油[52].2017年,Homan等[53]研究了一种新型低能耗、环保的生物柴油制造工艺,即使用长链醇(丙醇和丁醇)取代甲醇降低传质阻力,从而获得高纯度的脂肪酸丙酯和脂肪酸丁酯.随后用两种不同类型的DESs对其进行纯化,研究发现乙二醇基DESs比甘油基DESs提纯效率更高.
4.2 在脂肪酶催化油脂改性中的作用
脂肪酶因其具有独特的结构特点及催化特性,而广泛的应用于油脂改性领域.溶剂的选择是脂肪酶催化反应的关键因素之一,目前研究表明,有机溶剂具有强毒性、易挥发的特点;ILs虽具有不易挥发、热稳定性好、溶剂化能力强的优势,但其毒性较强、生物降解性差;而DESs兼具ILs的优点,还具有毒性低、生物降解性好的优势,是一种极具潜力的绿色溶剂.本文将从以下几个小节说明DESs对脂肪酶催化反应的作用,表5为部分在DESs体系中脂肪酶催化反应的研究.

表5 DESs在脂肪酶催化反应中的应用
4.2.1 提高脂肪酶的催化活性
2008年,Kalzauskas 等首次报道了在DESs中进行生物催化反应.尽管DESs中的部分组分单独存在时会导致酶失活,如10 mol/L 的尿素或5 mol/L的氯化胆碱都会使脂肪酶CALB(Candida antarcticalipase B)失活,并且DESs中包含的卤化物成分存在于离子液体中时也会导致酶失活.但CALB在ChCl和尿素组成的DESs中能保持较高活性,且在DESs中的稳定性是在单独组分中的20~35倍[54].研究者也表明这种显著的稳定性主要归因于DESs的氢键网络,它降低了DESs组分对酶的化学反应活性.Gorke等[55]研究发现与典型的离子液体相比,在DESs中固定化脂肪酶CALB催化酯交换反应的初始活性更高,同时研究发现固定化脂肪酶CALB 在DESs中的氨解反应速率比在离子液体中高出5 倍.这一研究进一步证明了DESs在生物催化反应中的应用潜力.随后,Durand等[56]以月桂酸乙烯酯酯交换为反应模型,选择不同链长的醇为反应底物.结果表明,固定化CALB的粉碎程度是脂肪酶活性的关键参数,一些来自DESs的氢键供体组分可以与醇解反应竞争,导致副产物的生成并破坏了DESs,但大部分的DESs由于氢键网络的作用降低了本身的反应性.且与有机溶剂相比,在DESs 中醇类的链长对CALB的影响较小,对蛋白质结构的破坏性最小,并且保持了其活性.

续表4
4.2.2 提高脂肪酶的选择性
DESs作为一种安全、便宜、生物相容性较好的绿色溶剂,相关研究表明其可有效的提高脂肪酶的选择性,有助于合成1,3-甘油二酯(1,3-Diacylglycerol,1,3-DAG)及富含多不饱和脂肪酸的功能性油脂.1,3-DAG 是天然存在的食用油脂中的微量成分,其具有减肥、降低餐后血脂、抑制心血管疾病等功能[57].2015 年,Zeng等[58]研究了在DESs中脂肪酶催化甘油与脂肪酸酯化反应快速有效合成高纯度1,3-DAG 的方法.研究表明酶的选择性主要取决于季铵盐的种类,添加ChCl的DESs体系可以提高脂肪酶Novozym 435对1,3-DAG 的选择性,1 h内1,3-DAG 的含量可达42.9 mol%.且随着ChCl含量的增加,DAG 选择性和1,3-DAG 选择性都在逐渐增加.该研究的发现也为寻找更多在DESs体系下具有独特位置选择性的脂肪酶提供了思路.富含n-3多不饱和脂肪酸(n-3 Polyunsaturated fatty acids,n-3 PUFAs)的功能性油脂对人体具有潜在的保健功能,如减少炎症、心血管疾病、动脉粥样硬化和癌症的风险,而目前的合成方法面临合成效率低、操作复杂、环境污染等缺点[59,60].2017 年Xu等[61]报道了甘油与n-3 PUFAs在DESs中酯化合成富含n-3 PUFAs的甘油三酯(Triacylglycerol,TAG).与无溶剂体系相比,DESs体系中TAG 的产率提高了1.2倍.在酯化反应过程中,DESs对水的吸附有助于反应平衡正向进行,从而提高转化效率,在最优条件下产率可达55%.2021年,Wang等[62]使用固定化脂肪酶MAS1在DESs体系中催化甘油与n-3 PUFAs的酯化反应高效合成n-3 PUFAs-TAG.研究发现固定化脂肪酶MAS1 对二十碳五烯酸(C20∶5n3,EPA)和二十二碳六烯酸(C22∶6n3,DHA)的选择性较弱,但在DESs体系中n-3 PUFAs-TAG 含量是无溶剂体系的1.38 倍.有趣的是,固定化脂肪酶MAS1在无溶剂和各种DESs体系中没有区域特异性,对1,3-DAG 和1,2-DAG 具有相似的选择性.研究发现在DESs体系中的酯化反应机理与Xu等[61]的研究结果一致,因DESs吸收了产物中的水,使反应正向进行.目前关于DESs对脂肪酶位置特异性的研究较少,也是研究者需要研究的方向,为结构脂质的制备提供参考.
4.2.3 提高酶促反应产率
DESs可有效的提高脂肪酶的活性及选择性,可作为酶的保护剂应用于水解反应[63]、酯交换反应[64]、氨解反应[11]、酯化反应[58]等催化反应中,且可有效的提高反应产物的产率.研究发现DESs的水分含量对脂肪酶催化反应产率有较大影响.例如,Durand等[65]发现在纯的或轻微水合的DESs(2%,v/v)中脂肪酶催化对香豆酸甲酯和阿魏酸甲酯的底物转化率较低,但水分含量达8%时其转化率提高了4倍.Bubalo等[66]以乙酸酐与1-丁醇反应生成短链乙酸丁酯为反应模型,研究发现使用纯的DESs或ILs作为绿色溶剂时酯化产率较低(<5%,w/w),在DESs中加入水可以大大提高酶的活性和反应产率.其中以水含量为5%(w/w)的DES(Ch Cl/EG,1∶2)效果最好,酯化率可达80%.研究表明Ping-Pong Bi-Bi机理可用来描述在DESs与水混合物体系中脂肪酶催化的酯化反应.在DESs中加入水可提高反应产率可能是由于加入的水可以降低粘度、改善传质和保持酶的良好催化活性.2018 年,Hümmer等[67]提出了一个新概念,在薄荷醇和脂肪酸组成的DES中合成薄荷醇脂肪酸酯,研究发现皱纹假丝酵母脂肪酶在该体系中具有一定催化活性,且其表明在DESs中加入水可提高反应产率,这可能是由于酶的界面活化.其次,研究者采用Novozym 435催化没食子酸丙酯与甲醇在DESs与水的混合体系中酯交换制备没食子酸甲酯.在相同的反应条件下,对比有机溶剂与DESs的(ChCl/Gly)反应效果,研究发现在DESs中具有更高的底物溶解度和产率(提高了6.4%),底物摩尔比是影响转化率和产率的最关键参数,而DESs中水含量和酶浓度对水解也具有决定性的影响[68].
DESs作为一种新型绿色溶剂在油脂改性领域具有广阔的应用前景,图3对其在油脂改性领域的应用进行了总结.
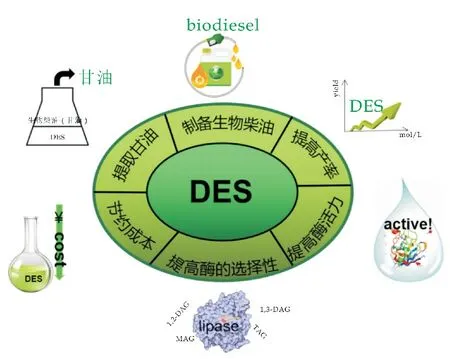
图3 DESs在油脂改性领域的应用
5 结论
DESs因其具备低毒性、制备简单、可设计性强、可生物降解性和生物相容性好等特点,已逐步代替传统有机溶剂及离子液体成为新一代绿色溶剂.DESs在油脂改性领域已获得广泛关注,本综述主要从油脂改性的角度论述DESs的特点及作用,其可作为制备生物柴油时的催化剂及反应溶剂并且能够除去其中的副产物甘油,提高产率并简化反应步骤.在脂肪酶催化反应中,DESs能够提高酶的活性和选择性,从而能够更加精准高效的合成结构脂质.
尽管在油脂改性领域DESs展现了巨大的应用潜力,目前的研究仍需要进一步深入从而使其能够更好的满足现实应用的需要.如DESs的水分含量对于反应体系的粘度、传质速率及脂肪酶的催化活性具有较大影响,需研究者对其进行精准调控.目前在脂肪酶催化反应中研究较多的DESs体系是氯化胆碱和甘油、氯化胆碱和尿素及添加一定量水分的体系,因此需开发更多适用于生物催化的DESs体系.
