表面增强拉曼光谱在乳和乳品有害物质检测中的研究进展
2021-10-24桑潘婷郭亚辉张倩瑶成玉梁谢云飞姚卫蓉
桑潘婷,郭亚辉, ,张倩瑶,成玉梁,于 航,谢云飞,姚卫蓉,钱 和
(1.江南大学食品学院,江苏无锡 214122;2.桐庐县检验检测中心,浙江杭州 311500)
乳是一种营养全面近乎完美的食品,被称为“白色血液”,是酸奶、奶酪、冰淇淋等众多受欢迎乳制品的主要原料,对保障国民健康和增强国民体质具有不可替代的作用。另一方面,在乳品产业快速发展的同时,由养殖、流通及加工制造过程中引入的有害物质如农兽药残留[1−2]、真菌毒素[3−4]、重金属以及非法添加等,对民众的生命健康造成了潜在安全风险。2008年我国婴儿奶粉中的三聚氰胺污染导致300000人患病,50000名婴儿住院治疗,6例死亡病例,经济损失巨大,严重影响了消费者对乳品产业的信心。
乳及乳制品中有害物质常见的检测方法包括化学反应法[5]、微生物法[6]、免疫分析法[7−8]和仪器分析法[9−10]。其中,化学反应法和微生物法由于灵敏度较低,一般用于定性或半定量检测。而免疫分析法由于其便捷性,应用较为广泛,主要有试纸条和ELISA试剂盒等产品。此类方法检测时间短,成本较低,可应用于牛奶中多种有害物质的检测[11−12],但一般根据肉眼观察得出结果,因此检测灵敏度不高,只能用于定性或半定量检测。高效液相色谱法等仪器分析法虽然灵敏度高,可同时测定多个样品,但设备昂贵,维护费用较高,而且存在样品预处理和分析程序复杂,检测时间长等问题[13]。
拉曼光谱由于其灵敏度高、可无损检测等优点,近几年来在食品有害物质检测中逐渐发展起来。表面增强拉曼光谱(SERS)是作为一种经典的拉曼光谱法,是根据样品本身的非弹性散射,可以提供几乎所有分子的结构以及定量信息[14]。它的原理是将具有特殊纳米结构的贵金属,如Au、Ag等作为活性基底,通过放大拉曼信号来定量检测目标物,因此有望作为一种方便快捷,并且灵敏度高的方法,应用于乳和乳制品中有害物质的检测。本文就SERS法在乳及乳制品中有害物质的检测方面的研究做出如下论述。
与传统的测定技术相比,SERS显示出许多独特的优势,它可以将信号放大到105~106倍,而且具有极高的分子特异性,不依赖于外部染料分子,具有抗光漂白性和抗光降解性的优点,可以重复检测,信号误差较小[15]。但大量数据表明,一般物质的拉曼光谱信号较弱,限制了SERS在食品安全检测领域的应用范围。实验证明,利用特殊的SERS检测探针和基底、分子识别技术以及核酸扩增等其它技术,可以显著改善拉曼平台的检测性能[16]。本文论述了SERS在乳和乳品有害物质检测中的研究进展及其发展趋势。
1 基于不同检测探针和基底的SERS方法
1.1 金属纳米检测探针
金属纳米颗粒的形态尺寸对SERS信号的增强效果至关重要。传统的SERS法主要以单金属纳米颗粒作为检测探针,如AgNPs、AuNPs等。研究表明,AgNPs的拉曼增强效果最明显,但Ag极易氧化,所以稳定性较低,而AuNPs虽然信号增强效果欠佳,但稳定性显著高于AgNPs。因此,近几年新开发出的双金属核壳纳米颗粒(Au@AgNPs)得到了快速发展,由于其具有AuNPs和AgNPs的双金属协同作用,稳定性得到改善,光学性能优异,信号增强作用明显,被广泛使用作为拉曼检测探针。William等[17]通过优化Au/Ag比,合成了一种马铃薯发芽状的Au-Ag双金属纳米颗粒。当Au/Ag比为10:7时,观察到的SERS信号强度比10:6的信号强度高出约7倍,推测可能是由于纳米颗粒上的尖芽有助于热点的聚集。为验证该假设,利用数值模拟技术建立两种芽尖锐度不同的马铃薯状模型,测定电场强度,根据电磁理论,SERS信号的强度直接取决于纳米颗粒的局部电场。结果证实,尖芽引起的电场增强比钝芽高5倍,而且取向一致并彼此靠近的尖端能够产生更高的电场增强。
除了经典的金纳米球外,金纳米棒、金纳米星等特殊性形态的纳米颗粒也被用于制备SERS检测探针。金纳米棒由于其独特的各向异性结构可以产生强电磁场,显著增强了拉曼信号。先前的研究表明,在基板上合成垂直排列的AuNRs单层可作为理想的SERS基底[18]。Mei等[19]在金纳米球上沉积垂直取向的金纳米棒形成了杨梅状Au核,然后在核结构上通过还原合成Ag NPs,制备了如图1所示的3D Au@Ag NP,该结构所产生的热点使其具有优异的SERS增强能力,增强因子高达3.4×106。另外,改变3D Au@Ag NP上的硫醇配体,可以应用在不同场合,如以NT、PBAT为代表的硫醇配体在特征峰处能够产生SERS信号,可以用作内标物校准纳米颗粒的状态和测量变化;而基于MEA的纳米颗粒显示空白的SERS信号,可用于孔雀石绿,三聚氰胺的检测。

图1 3D Au @ Ag NP[19]Fig.1 3D Au@Ag NP structure[19]
另外,直接合成不规则的特殊形态纳米颗粒对于反应条件和操作的要求较为严苛,而且纳米探针的一致性难以保证。研究发现,可以借助SiO2、Al2O3等材料制备出特定形态的模板,并以其为基底在表面直接反应制备多形态金属纳米颗粒,有助特殊形态的纳米探针的合成,并能够保证产品的一致性。Zhai等[20]以ZnO为模板,通过两步法制备了可再生的3D角状ZnO/Ag@Au,用于检测牛奶中的抗生素,该结构显著增加了纳米颗粒的表面积,SERS增强因子可以达到1.48×109,对牛奶中磺胺吡啶的检测限低至1×10−9mol/L。而且由于ZnO具有光催化性能,ZnO/Ag@Au可以将磺胺吡啶经紫外降解后回收利用,因此可以满足现场检测的需要。
1.2 新型固相SERS平台
除了改变纳米探针的形态外,SERS检测的平台也至关重要。一般来说,溶液中的检测不利于便携式传感器的制备,很难满足乳及乳制品中有害物质高通量、低成本和快速即时的检测需求。近几年来,大部分研究集中于制备具有高“热点”的便携式固相SERS平台。如图2所示为[21]一种基于PS胶体的Au/Ag碗状结构(BPHAN)。首先在ITO玻璃板上沉积一层金膜,得到Au/ITO基底,吸附上PS单层后,经电沉积并去除PS后获得Ag BPHAN,经氧化还原反应获得Au/Ag BPHAN。将该SERS活性平台用于奶粉中三聚氰胺的快速检测,检测限低至0.1 ppm。
为降低检测成本,Marques等[22]制备了一种用于检测牛奶中四环素的SERS纸基平台,该平台由压制的纤维层,聚合物涂层和铝层组成,铝层顶部存在一层薄的天然氧化物层,解决了AgNP易氧化的问题,在纸基上沉积6 nm的AgNP膜,即可测定牛奶中的四环素含量。该方案检测成本低,可回收,而且稳定性高,灵敏度低至0.1 ppm。
为提高检测效率,满足高通量的检测需求,可以将SERS与毛细管/移液管相结合,制备微量移液器,从而实现取样、检测一步到位。Zhou等[23]利用干燥的罗勒种子与移液管结合形成便携式设备,由于干燥的罗勒种子具有紧密复杂的纤维状结构,使得沉积在罗勒种子上的银纳米粒子与包含分析物的牛奶样品保持紧密接触,提高了检测灵敏度,该设备对牛奶中三聚氰胺的检出限为0.85 μmol/L(0.107 ppm)。此外,微流控与SERS相结合也能够大大提高检测效率,Nguyen等[24]以石墨烯和金纳米颗粒复合材料为基底,通过生物素-链霉亲和素作用连接上包含卡那霉素适配体序列的发夹结构,卡那霉素与适配体结合后,发夹结构的两端被展开,添加带有纳米标签的光学探针与其中一端杂交,显示出SERS信号。将该纳米感应体系建立在微流控设备上,对牛奶中卡那霉素的回收率为98.9%,检测限低至0.75 nmol/L。
总之,从单金属纳米颗粒到双金属协同作用,从规则的纳米球、纳米棒到不规则的纳米花和纳米星,从传统的固相基底和液体微珠到微流体芯片,再到纸质基质,光纤和疏水性基底,SERS检测体系的多样性使得其应用越来越广泛[25]。这些不同的SERS体系适用于不同的场所和要求,如利用微珠在液相中进行检测,可以增加反应动力学;而微流体平台则实现了大量小体积样品的同时分析;为实现远程控制现场检测,光纤基底逐渐兴起;另外,纸质基底有利于降低检测成本;而超疏水性基底被开发用于富集目标分子,具体应用如表1所示。
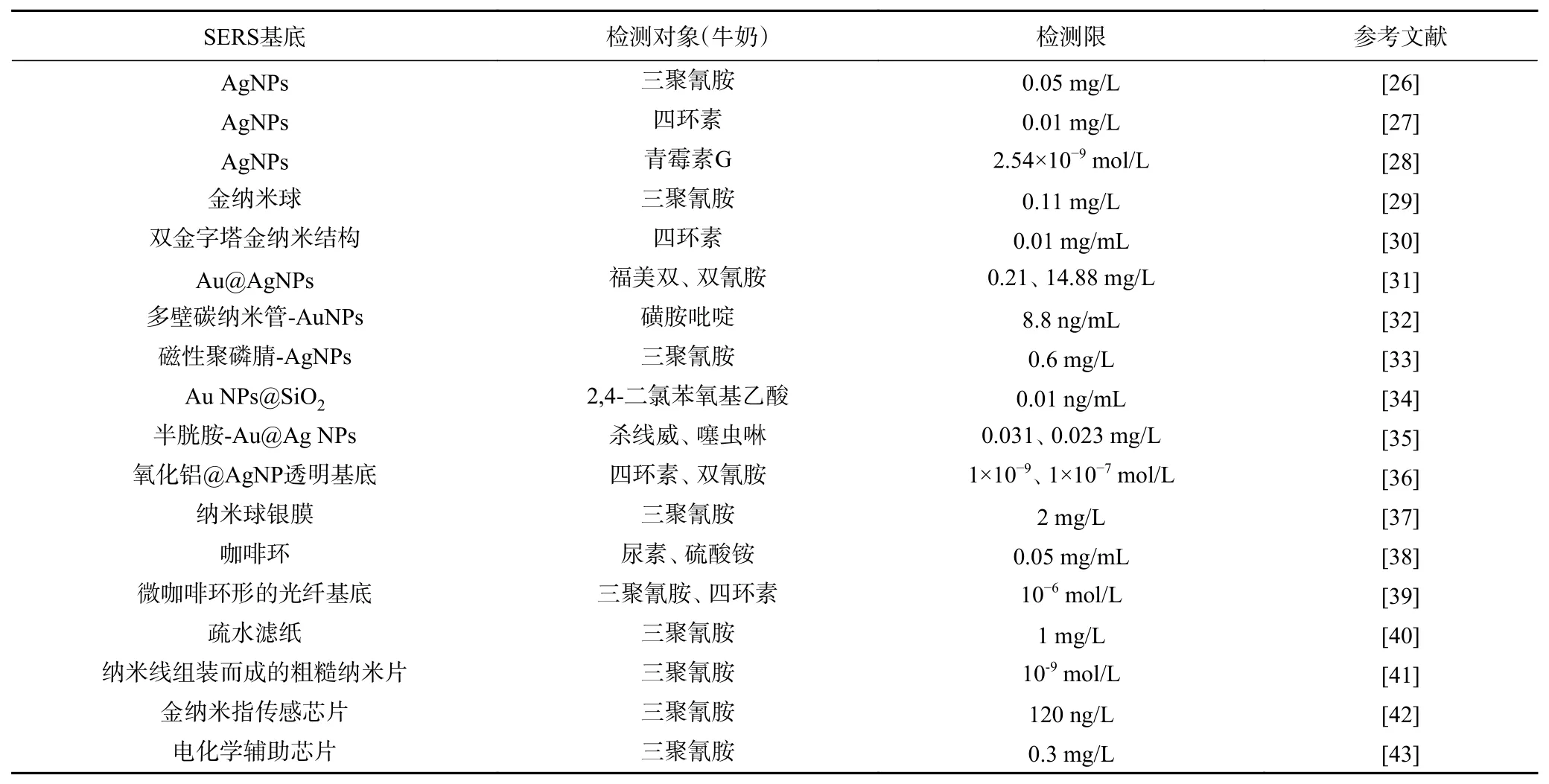
表1 基于不同检测探针和基底的SERS方法Table 1 SERS methods based on different enhanced substrates
2 基于不同分子识别技术的SERS方法
目前,SERS技术已经广泛运用于乳及乳制品检测中,但是复杂的样品基质对SERS平台的目标物富集能力提出了更高的要求,疏水性的基底在一定程度上提高了样品的富集效果,但大部分平台在样品的蒸发过程中,还是会存在钉扎效应,形成大小不一的咖啡环,很难将目标物和纳米检测探针聚集到同一位置,降低了检测准确度。因此,为提高SERS平台的样品富集能力,增强检测的特异性和灵敏度,在SERS平台中引入抗体、适配体、分子印迹聚合物等作为识别分子,构建检测传感器,有利于目标物更加紧密、牢固地结合在SERS平台上,改善检测效果。
SERS-免疫体系主要有两部分组成,免疫底物以及SERS免疫探针[44]。以非竞争性体系为例,免疫底物被捕获抗体修饰,用于捕获分析物,而SERS探针由金属纳米颗粒,拉曼报告分子以及检测抗体组成,用于特异性识别免疫底物捕获的分析物,发出SERS信号。如图3a所示为以芯片为代表的非竞争性夹心结构,目标分子夹在捕获抗体与SERS探针之间,用于检测大分子物质,如蛋白质等。图3b为竞争性SERS-免疫体系,以球状颗粒为代表,包被抗原被标记作为SERS免疫探针,目标分子与探针竞争结合抗体,检测信号强度与目标物浓度呈负相关。

图3 SERS-免疫体系Fig.3 SERS-immuno system

Transformation Heat treatment ED of Ag bowl Removal of PSs Etch by HAuCl4 solution Removal of AgCl
由于高灵敏度,多路复用以及方便快捷等优点,基于SERS的免疫方法在食品监管领域的应用越来越广泛。目前已经开发了多种免疫自动检测平台,如试纸条、微流控芯片等。Yang等[45]提出了一种基于竞争性免疫测定和磁分离技术的用于氯霉素(CAP)残留检测的SERS传感器。以4,4’-DP为拉曼报告分子,在GNPs上偶联CAP-BSA,作为SERS探针。再在MNPs上修饰CAP抗体,形成antiCAP-MNPs。由于antiCAP-MNPs可同时捕获游离的CAP和SERS探针,两者存在竞争性免疫反应。经磁分离富集后,通过测定上清液中的SERS信号,可获得溶液中CAP的浓度。Shi等[46]制备了一种基于SERS-免疫层析试纸条,其中,免疫探针由新霉素单克隆抗体(NEO-mAb)和拉曼报告分子4-氨基硫酚(4-PATP)标记的SERS纳米标签构成,由于待测样品中的游离NEO与试纸条上的包被抗原(NEO-OVA)之间存在竞争性免疫作用,因此可以通过测试线上的PATP的拉曼强度获得新霉素的含量。该方案检测时间约15 min,对牛奶中新霉素的检测限为0.216 pg/mL。
适配体作为一种理想的抗体替代物,合成周期远小于抗体,而且易于修饰,因此逐渐用于构建新型的SERS传感器[47−49]。如图4所示为一种以四环素为检测对象的适配体传感器[50],磁性纳米颗粒-适配体作为识别单元以提供磁性;cDNA-APS产生拉曼信号,两者通过适配体与cDNA杂交结合在一起。当加入含有四环素的样品时,四环素与适配体结合,释放一定量的cDNA-APS,经过磁分离后,根据上清液的SERS信号,获得牛奶中四环素的含量。该传感器显示出良好的稳定性和可再现性,检测限为0.001 ng/mL。

图4 一种磁性适配体传感器原理图[50]Fig.4 Schematic diagram of a magnetic adapter sensor[50]
分子印迹聚合物(MIP)不仅具有抗原抗体的特异性识别能力,还具有结构稳定、可预测等优点,因此适用范围较广。将SERS与MIP结合应用,基本原理如图5所示,将模板分子(与目标物结构相似)与功能单体混合形成预聚合物,此时单体通过共价或非共价相互作用围绕模板分子排列,呈分子聚集体状。添加交联剂通过聚合使单体分子交联后,去除模板分子,留下与模板分子互补的空间结构,可以有选择地将目标分子捕获到金属表面以生成SERS信号[51−52]。Xie等[53]提出了一种MIP-SERS传感器,用于检测牛奶中的氯霉素残留。首先通过沉淀聚合制备MIP,并提取模板分子,然后将该聚合物置于柠檬酸钠还原反应中以制备CAP-MIP-Au底物,该底物同时具有MIP的良好的吸附能力和SERS增强作用,可直接添加到牛奶样品中检测氯霉素的含量,检出限为0.1 μg/mL。

图5 MIP-SERS结构Fig.5 MIP-SERS structure
基于免疫的SERS检测方案目前应用较为广泛,将免疫法的选择性与SERS信号表达的高灵敏性结合起来,有利于实现高通量,高选择性的快速检测。而适配体由于其易于体外大量合成,稳定性高,相较于抗体,适配体的靶标广泛,包括农兽药、毒素等一系列有害物质,而且易于标记,因此也被逐渐用于SERS传感器的构建。另外,以分子印迹技术为基础的SERS检测目前在乳制品中应用较少,有待进一步研究,具体如表2所示。

表2 基于不同分子识别技术的SERS方法检测乳制品中有害成分Table 2 SERS methods based on different molecular recognition technologies
3 基于信号放大技术的SERS方法
为进一步提高检测的灵敏度,可以结合聚合酶链式反应(PCR)和等温核酸扩增技术,如重组酶聚合酶扩增技术(RPA)和杂交链反应(HCR)等,先将低水平的目标分子扩增到可以检测的水平,再进行检测,从而达到放大SERS信号的目的[67−68]。重组酶聚合酶扩增技术(RPA)作为一种等温核酸扩增技术,在无需热循环设备的情况下,利用酶高效的催化活性,达到放大信号的目的。Liu等[69]基于AuMBA@Ag探针开发了一种可同时检测单核细胞增生李斯特菌和肠炎沙门氏菌的免疫试纸条——RPA-LF-SERS试纸条,具体如图6所示。该试纸条的测试线1被标记上FITC抗体(anti-FITC),测试线2被标记上地高辛抗体(anti-digoxin),对照线上修饰有链霉亲和素抗体(anti-streptavidin)。RPA首先被用于扩增生物素-Digoxin和生物素-FITC标记的目标DNA,纯化后的RPA产物通过生物素-链霉亲和素作用与AuMBA@Ag结合后,被测试线上对应的抗体捕获,形成橙黄色的视觉带。该试纸条对牛奶中肠炎沙门氏菌的检出限为31 CFU/mL,单核细胞增生李斯特氏菌的检出限为36 CFU/mL。除了酶辅助的核酸扩增技术外,Lv等[70]基于无酶介导的等温核酸扩增——杂交链反应(HCR),制备出一种超灵敏SERS平台,用于检测牛奶中的食源性致病菌。该平台以单克隆抗体和引发DNA标记的AuNPs作为探针,当目标病原体存在时,探针上的相应引发DNA识别出匹配的发夹结构,触发特异性杂交,形成多色荧光串联体作为信号放大器,观察到相应的荧光。该方法可同时检测牛奶中的大肠杆菌O157:H7、霍乱沙门氏菌和单核细胞增生李斯特菌,检测限分别为34、6.4、70 CFU/mL。

图6 RPA-LF-SERS 试纸条[69]Fig.6 RPA-LF-SERS assay[69]
4 基于其它技术的SERS方法
SERS可以根据分子的结构信息,对化合物进行鉴别,而色谱法对样品混合物具有良好的分离效果,利用SERS对色谱预处理的分离液进行分析,可以改善样品中有害组分的检测效果[71]。Zhao等[72]利用TLC-SERS(薄层色谱-SERS)对1~250 ppm的含有三聚氰胺的牛奶样品进行薄层色谱分离,再将AuNPs沉积到分离后的浓缩点上,利用便携式拉曼光谱仪测定SERS光谱,并结合四元数主成分分析法提高定量的准确性,该方法显示出对牛奶中三聚氰胺的良好检测性能。
5 总结与展望
目前SERS在乳及乳制品检测中的大部分应用仍只能在实验室实施,为使其在乳制品检测中广泛应用,需要解决一些难题。首先,乳和乳制品中一般的有害物质拉曼信号较低,以单金属纳米颗粒作为检测探针的稳定性和灵敏度有待提高,利用双金属的协同作用,可以显著改善信号强度。另外,通过一些易成型的材料形成特殊形状的基底,以其为模板可以制备出具有较强的电磁场或者丰富“热点”的理想的金属纳米颗粒。其次,作为一种新兴的食品安全检测技术,拉曼光谱仪的价格昂贵,对于中小型乳制品企业来说,生产成本偏高,可以结合微流控、玻璃毛细管等开发出低成本、高性能的SERS基底,降低成本的同时,可以实现取样、检测一体化。
由于SERS平台的钉扎效应,乳及乳制品中的目标物很难被富集起来并与检测探针充分作用,除了制备疏水性平台外,可以引入抗体、适配体和分子印迹聚合物等分子识别技术来捕获目标物,从而提高检测的特异性和灵敏度。此外,将免疫与PCR以及一些等温核酸扩增技术也可以用于乳及乳制品中微量物质的检测,其中抗体作为捕获单元用于捕获目标物,而核酸扩增技术用于放大检测信号。为防止乳制品的复杂组成产生的基质效应影响到检测结果的准确性,可以结合色谱技术对样品进行简单的分离预处理,再进行SERS检测。随着灵敏度、特异性和便捷性等方面的改善,SERS有望成为日常评估乳和乳制品的常规工具。
