冠状动脉支架内慢性完全闭塞的介入治疗
2021-10-06宫明莲综述毛懿柳景华审校
宫明莲综述,毛懿、柳景华审校
慢性完全闭塞(CTO)病变经皮冠状动脉介入治疗(PCI)是当代心脏介入治疗中最复杂的操作之一。支架内慢性完全闭塞(IS-CTO)在CTO 中占5%~25%[1-4],是 CTO 病变介入治疗中难度最高、最有挑战性的病变。IS-CTO 的危险因素、病理机制及冠状动脉造影特征与非IS-CTO 不同[5],其特殊的病理机制导致导丝及球囊通过困难,因此血管开通率较低。随着杂交策略的应用,IS-CTO 的血管开通率较前明显升高,但仍低于非IS-CTO 的血管开通率。IS-CTO PCI 后再狭窄和再闭塞的发生率较高,且IS-CTO 是晚期血运重建的独立预测因素。
1 冠状动脉支架内慢性完全闭塞的流行病学
Christopoulos 等[1]发表的一项注册研究显示,支架内再狭窄(ISR)所致的IS-CTO 发生率为10.9%;Abbas 等[2]一项纳入78例患者的研究显示,ISR 所致的CTO 发生率为25.0%;Wilson 等[4]报告的349例CTO PCI 中,ISR 的发生率为14.9%;Werner 等[3]通过文献回顾及Meta 分析发现,ISR 所致的CTO 发生率为5%~10%。然而,目前PCI 后支架内再闭塞的真实发生率不得而知。
2 冠状动脉支架内慢性完全闭塞的介入现状
2.1 冠状动脉支架内慢性完全闭塞的经皮冠状动脉介入治疗成功率
IS-CTO PCI 一直被认为与较低的血管开通率相关。Abbas 等[2]研究了一组在裸金属支架时代(占研究人群的25%)接受IS-CTO PCI 的患者,其PCI 成功率低于原位血管CTO 患者(63% vs.70%),导丝通过困难是两组PCI 失败的主要原因,但在IS-CTO组,球囊不能通过及不能充分扩张的发生率更高。Werner 等[3]报道,IS-CTO组患者尽管应用逆向策略,但PCI 成功率仍然低于原位血管CTO组(70%vs.85%)。Abdel-Karim 等[6]发表的一项小样本研究显示,由于导丝通过困难,IS-CTO PCI 成功率仅71%。在de la Torre Hernandez 等[7]一项纳入233例IS-CTO 患者的单中心研究中,PCI 成功率为82%。随着新技术、新器械的出现以及杂交策略的使用,IS-CTO PCI 成功率得到明显提高。在PROGRESS 注册研究中,IS-CTO 在CTO 中占10.9%,其中三分之一应用逆向策略,PCI 成功率虽然高达86%,但仍低于原位血管CTO组(90.3%)[1]。
2.2 冠状动脉支架内慢性完全闭塞的病理机制
ISR 所致IS-CTO 与ISR 的形成机制一样,是由于支架弹性回缩、支架膨胀不全、病变未完全覆盖、长支架或小支架、支架断裂等因素引起平滑肌细胞增生(新生内膜增生),从而导致支架内完全闭塞[8]。裸金属支架更容易发生ISR[9],随着药物洗脱支架的应用,ISR 的发生率已经大幅降低。由ISR引起的CTO,其闭塞段主要是由坚硬且致密的纤维组织构成,因此与其他原因所致的CTO 不同,其闭塞段微通道较少,这也是应用较软的锥形导丝会失败的原因[10]。然而在某些情况下,支架内膜增生表现为一种岛状增生,因此导丝很容易不受控制地滑入内膜下,即使穿过支架后重新到达远段真腔,也会导致后续球囊及其他器械输送困难。
某些支架内闭塞是由先前置入的支架形成的血栓机化所致,即支架内血栓所致IS-CTO。支架置入时一些机械性因素比如支架贴壁不良、远段夹层、慢血流或无复流,以及急性冠状动脉综合征置入支架均可引起支架内血栓形成。早期支架内血栓所致的支架内闭塞的比例尚不明确。如上所述,支架内闭塞可由支架内膜增生、支架内血栓形成两种机制导致,或二者兼有(图1)。
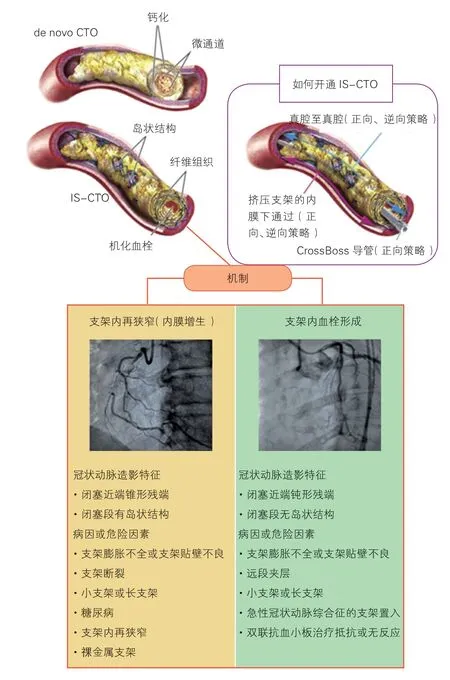
图1 冠状动脉支架内慢性完全闭塞病变介入治疗特点
3 冠状动脉支架内慢性完全闭塞的造影特征
支架内闭塞的机制不同时,其冠状动脉造影显示的特征也有所不同(图1)。ISR 所致的支架内闭塞近段纤维帽多表现为锥形残端,存在岛状结构的闭塞病变中,部分病例存在可视的微通道,这就是应用CrossBoss 导管(波士顿科学公司,美国)更容易通过支架内闭塞病变的机制。支架内血栓所致的支架内闭塞,冠状动脉造影显示为近段纤维帽模糊,闭塞段不存在岛状结构,通常为支架内的完全闭塞,通常闭塞近段纤维帽位于支架近段入口。支架内闭塞病变的血管开通率相对较低,这与其特殊的病理机制有关[11]:(1)闭塞段的支架存在着膨胀不全或贴壁不良,导丝更容易进入内膜下,且岛状结构的存在也更容易使导丝滑入内膜下,从而导丝通过闭塞段失败;(2)支架断裂,支架结构的破坏甚至一个支架丝的存在都会导致导丝以及其他器械输送困难,在迂曲的血管中尤其困难;(3)长时间的CTO 病变多为致密坚硬的纤维组织和钙化组织构成,增加了导丝、球囊以及其他器械通过的难度,这对于术者更加具有挑战性。
4 提高冠状动脉支架内慢性完全闭塞经皮冠状动脉介入治疗成功率的策略
Christopoulos 等[1]开展的一项多中心研究表明,杂交策略可有效提高IS-CTO 的PCI 成功率,与原位血管 CTO 相比,IS-CTO PCI 具有相似的技术成功率(89.4% vs.92.5%,P=0.43)和操作成功率(86.0%vs.90.3%,P=0.31)。该研究显示,IS-CTO 最常用的导丝通过方法是正向导丝升级技术(41.1%),其次是逆行策略(31.4%),夹层再进入真腔的比例为27.4%;54.4%的IS-CTO 患者使用CrossBoss 导管,而原位血管CTO 患者中CrossBoss 导管使用率为26.7%。
与原位血管 CTO 不同,IS-CTO 无论采用正向还是逆向导丝升级技术,尽量使用操控性与扭矩性较好的导丝,减少使用聚合物护套类导丝,以避免导丝进入支架下或者血管内膜下结构。CrossBoss 导管的使用可以作为IS-CTO PCI 的首选策略。
如何提高IS-CTO PCI 的成功率?或许新器械CrossBoss 导管的应用会带来新的希望。杂交策略在全球的广泛应用奠定了CrossBoss CTO 导管在CTO PCI 中广泛使用的基础,当CrossBoss 导管的头端越过闭塞病变段以后,可以使用Stingray 球囊及Stingray 导丝(波士顿科学公司,美国),最终使导丝进入血管真腔。FAST-CTO 研究确定了CrossBoss CTO 导管在CTO PCI 中的应用;该研究表明,采用CrossBoss CTO 导管不但可以提高手术成功率,还可缩短手术时间,减少对比剂的使用,而且不增加不良事件的发生风险[12],但该研究排除了ISCTO 患者。一项欧洲多中心研究探索了CrossBoss CTO 导管在复杂、难治性CTO 患者中的应用,首次提到了CrossBoss CTO 导管在IS-CTO PCI 中的有效应用,但仅1例IS-CTO 患者应用CrossBoss 系统成功开通血管[13]。随后许多小样本研究证实了CrossBoss CTO 导管在IS-CTO PCI 中的有效性。例如,Papayannis 等[14]报道,在应用CrossBoss CTO 导管的IS-CTO PCI 中,成功率达到83%;Wilson 等[4]报道应用该方法的IS-CTO PCI 成功率可达到90%。此后,CrossBoss CTO 导管在IS-CTO PCI 中的应用比例越来越高。Christopoulos 等[1]报告,CrossBoss导管在IS-CTO PCI 中的使用率为54.4%,最终技术成功率为89.4%;Wilson 等[4]的研究显示,应用CrossBoss 导管时,只要远段纤维帽位于闭塞的支架内或者支架末端,88%的病例可实现真腔到真腔的通过策略,因此可避免应用夹层重新再进入技术。CrossBoss 导管的成功基于以下事实:支架结构会阻止器械进入血管内膜下腔,从而使导管的钝头通向远端血管真腔;另外,CrossBoss 导管的应用降低了PCI 操作时间,来自英国的IS-CTO 注册研究报道,应用CrossBoss 导管后通过闭塞支架的中位时间为8 min[4]。CrossBoss 导管在IS-CTO 患者中的应用价值仍需进一步研究来证实。
5 改善冠状动脉支架内慢性完全闭塞经皮冠状动脉介入治疗预后的方法
成功的冠状动脉 CTO 介入治疗可以减少患者远期主要不良心血管事件的发生率[15]。与原位血管CTO 相比,IS-CTO PCI 的长期预后并不乐观,主要不良心血管事件和再次血运重建发生率均高于原位血管PCI。Azzalini 等[5]进行的一项多中心注册研究共纳入899例CTO 患者(IS-CTO 患者111例,原位血管CTO 患者788例),中位随访471 d 时,与原位血管CTO组相比,IS-CTO组的主要不良心血管事件(20.8% vs.13.9%,P=0.07)和再次血运重建发生率(16.7% vs.9.4%,P=0.03)均明显高于原位血管CTO组,且IS-CTO 是主要不良心血管事件和再次血运重建的独立危险因素。来自西班牙的一项ISCTO 注册研究共纳入233例患者,中位随访20 个月时,再次血运重建发生率为15%。与非CTO PCI相似,ISR 是IS-CTO PCI 远期发生再狭窄事件的独立危险因素[7]。
进一步优化治疗对于减少IS-CTO PCI 后主要不良心血管事件及再次血运重建也至关重要。防治相关危险因素是基本措施,IS-CTO PCI 后患者应严格控制血压、血糖及血脂水平,同时要戒烟、限酒、适量运动等。对于此类极高危患者,使用最大耐受剂量他汀类药物联合依折麦布治疗后低密度脂蛋白胆固醇水平如果仍未达标,推荐联合使用前蛋白转化酶枯草溶菌素9(PCSK9)抑制剂[16]。越来越多的临床医生开始重视氯吡格雷抵抗问题[17],并根据细胞色素P4502C19(CYP2C19)基因多态性指导噻吩吡啶类抗血小板药物的临床应用。对于携带CYP2C19功能缺失型等位基因的冠心病患者,PCI后可将氯吡格雷更换为新型 P2Y12受体拮抗剂,如替格瑞洛或普拉格雷。适当延长双联抗血小板治疗时程可使因 ISR 再次置入支架的患者获益[18]。
对于一些复杂病变,在手术操作中应根据病变特点尽可能地使用一些有利的成像技术和设备,如血管内超声(IVUS)和光学相干断层扫描(OCT),用来指导介入治疗并评价其效果。OCT 能更加清楚地显示血管壁情况,以便对治疗方案做出更好的决策。有研究表明,IVUS 可以提供有关IS-CTO机制的重要信息(用小球囊预扩张后),更重要的是可优化支架置入,以最大程度地降低后续随访期间不良事件的发生风险[19]。该研究为一项纳入3 192例患者的随机临床研究,比较IVUS 指导的支架置入术(IVUS 指导组)与冠状动脉造影指导的支架置入术(冠状动脉造影指导组)预后。随访15 个月时,IVUS 指导组的主要不良心血管事件(6.5%vs.10.3%;OR=0.60,95% CI:0.46~0.77,P<0.0001)和再次血运重建发生率(4.1% vs.6.6%,OR=0.60,95% CI:0.43~0.84,P=0.003)显著低于冠状动脉造影指导组,心原性死亡(0.5% vs.1.2%,OR=0.46,95% CI:0.21~1.00,P=0.05)和支架内血栓形成(0.6%vs.1.3%,OR=0.49,95% CI:0.24~0.99,P=0.04)也低于冠状动脉造影指导组,说明IVUS 指导的支架置入术明显优于冠状动脉造影指导的支架置入。来自韩国的一项多中心CTO 注册研究表明,IVUS 指导的CTO PCI 与较低的支架内血栓形成风险及长病变靶病变血运重建有关[20]。另一项韩国研究比较IVUS 指导下IS-CTO PCI 与原位血管CTO PCI 的疗效,结果发现,两组的5年靶血管失败率(11.0%vs.10.7%,P=0.99)和靶血管重建率(4.2% vs.3.7%,P=0.81)无明显区别;这说明,IVUS 指导优化ISCTO PCI 可以获得与原位血管CTO PCI 相似的长期疗效[21]。IVUS 与OCT 在IS-CTO PCI 中的应用有助于术者减少技术及操作上的失误,从而降低ISR 的发生率,并可通过使用多模态成像来了解首次支架置入失败的病因,协助导丝通过,使用辅助方法来优化支架的扩张,以争取获得最佳的手术结果。血流储备分数也是一项介入指导技术,用于评估PCI后靶血管血流改善的程度及预测PCI 后ISR 的发生。既往的研究证实,血流储备分数的应用可降低PCI后再次血运重建的发生率[22]。已成功开通IS-CTO的患者如有症状,应及时就诊,及早发现再狭窄,及时诊治,以免发展成长段的IS-CTO。相信随着对ISR 病理生理学机制的深入研究和科学技术的进步,我们能找到更加科学、有效的预防和治疗手段。
总之,尽管近年来随着新技术及新器械的应用,在高手术量CTO 中心IS-CTO PCI 获得了令人欣慰的成功率,但是改善IS-CTO PCI 的长期预后仍是临床面临的重大挑战。对于IS-CTO 患者,应该用更多的时间、精力以及更加细致的PCI 技术来开通病变,必须给予更加科学、有效的预防和治疗手段,以改善其预后。
利益冲突:所有作者均声明不存在利益冲突
