人类免疫缺陷病毒感染者预防人乳头瘤病毒相关肿瘤的研究现状
2021-09-30卢洪洲
章 清, 卢洪洲
艾滋病是全球性公共健康问题,据联合国艾滋病规划署(Joint United Nations Programme on HIV/AIDS,UNAIDS)[1]于2020年发布的报告显示,截至2019年底全球现存活HIV感染者为3 800万,新发感染人数为170万,接受抗反转录病毒治疗(antiretroviral therapy,ART)者为2 540万,覆盖率达67%。ART能够有效降低HIV感染的发病率和病死率,使患者获得预期寿命并提高生活质量[2]。然而,HIV感染者患艾滋病相关肿瘤和非艾滋病定义性肿瘤的危险性很大,其中包括了人乳头瘤病毒(HPV)相关癌症。目前宫颈癌被认为是艾滋病定义性肿瘤,而肛门癌被认为是非艾滋病定义性肿瘤[3]。绝大多数情况下,HPV感染具有自限性,在引起疾病之前能够被机体免疫系统所清除[4],但在感染HIV的女性患者中,由于HIV导致HPV高感染率和低清除率,从而具有更高的低级别鳞状上皮内病变(low-grade squamous intraepithelial lesions, LISL)、高级别鳞状上皮内病变(high-grade squamous intraepithelial lesions, HISL)的发病率和发生宫颈癌 (cervical cancer) 的风险[5-6]。尽管在HIV的治疗与护理方面取得了巨大进展,在接受有效ART的HIV感染者中,肛门HPV感染和HSIL的流行率仍然很高,HPV相关的肛门癌症发病率持续上升[7]。本文通过分析HIV感染者发生HPV相关肿瘤的风险,提出了HPV联合预防策略,以减少HIV感染者发生HPV相关肿瘤的风险、降低HPV相关癌症的发病率和死亡率,为我国管理HIV结合控制HPV相关肿瘤的方法提供参考。
1 HIV是HPV相关肿瘤的危险因素
1.1 人群HPV感染率:HIV阳性人群显著高于HIV阴性人群
HIV和HPV之间存在相互作用,HPV感染是HIV感染的危险因素,HIV感染是发生HPV相关癌症的危险因素[3]。大量研究发现HIV感染人群的HPV患病率明显高于未感染HIV人群:一项单中心前瞻性队列研究共纳入了297例男性HIV感染者,其中192例为男男同性恋者(men who have sex with men,MSM),结果发现整体HPV感染率为61%,其中HPV感染率在MSM中为77%,异性恋者为29%;高危型HPV感染率在MSM中为69%,异性恋者中为23%[8]。研究说明了HIV感染者中鳞状上皮内病变的发生率很高,MSM的发病率明显高于异性恋者,MSM是肛门鳞状上皮内病变的独立危险因素。一项meta分析评估了非艾滋病患者癌症风险因素在HIV感染者中的流行率[9],其中18宗研究报告了HPV的流行率,宫颈HPV总体流行率为64%,宫颈高危型HPV的总体流行率为46%,大多数关于肛门HPV感染的研究人群为MSM,其中肛门任一类型HPV总体流行率为91%,高危型HPV的总体流行率为68%。万建玉等[10]选取了2017—2018年广东深圳进行宫颈癌筛查的HIV感染女性,以同期进行筛查的HIV未感染(阴性)女性作为对照各550例,结果显示HIV感染女性的HPV感染率、高危型HPV感染率、多重HPV感染、细胞学异常发生率以及其他阴道疾病感染率均显著高于HIV未感染女性。高鸣等[11]共纳入140例HIV感染MSM人群进行检测,结果发现MSM人群中HPV感染为109例,阳性率为77.86%,其中高危型HPV感染为81例,阳性率为57.8%;在109例HIV阳性合并HPV感染的MSM人群中,以多重HPV感染为主,占71.56%。
1.2 HIV患者发生HPV相关肿瘤的风险增加
HIV感染人群获得相关肿瘤的风险较HIV阴性人群更高,这与HIV感染相关的免疫抑制降低了控制致癌病毒过程的能力有关[12]。HPV感染可引起相关肿瘤的发生和发展,在这个过程中,高危型HPV长期持续感染为引起癌症的主要原因,高危型HPV持续感染可引起子宫颈、外阴、阴道、肛门等部位的癌前病变,最终可进展为浸润性癌。一项meta分析显示,与HIV未感染女性相比,HIV感染女性感染HPV的风险更高、HPV清除率更低,从而具有更高的HPV感染率、LISL、HISL发病率以及宫颈癌的发病率[5]。Clifford等[6]纳入了86项研究共19 883例来自不同国家的HIV感染女性,对其高危型HPV流行率进行了系统评价和meta分析,发现细胞学检查正常的HIV感染女性占比59%,非典型鳞状细胞、LISL、HISL、1级宫颈上皮内瘤变、2级宫颈上皮内瘤变、3级宫颈上皮内瘤变以及侵入性宫颈癌分别占9%、11%、6%、6%、2%、3%和4%。其中非洲是最具有代表性的地区,发生的侵入性宫颈癌事件占总事件的96.7%;HPV-16、HPV-18和HPV-45在侵入性宫颈癌HPV感染中所占比例大。因此,HPV感染尤其是高危型HPV感染,应值得HIV感染女性特别关注。肛门癌是HIV感染者中越来越常见的非艾滋病定义性癌症,其中HPV-16是70%肛门癌中最常见的基因型[12]。HPV在年轻和性活跃人群中非常普遍,因为HPV是通过任何涉及皮肤至皮肤、皮肤至黏膜的性活动进行传播,包括了阴道、肛门和口交[13],这意味着MSM也具有一定发生HPV感染和HPV相关癌症的风险;其中,HIV感染的MSM肛门HPV感染率极高,可近100%[7]。一项横断面研究对320例HIV感染的MSM进行肛管细胞学检查,198例肛门细胞学检查正常,在122例细胞学异常的患者中,36%患者为肛门LSIL;51%为肛门HSIL,通过多因素分析发现,接受ART≥24个月与肛门HSIL减少有关,即长期接受ART对肛门癌的进展具有潜在保护作用[14]。
研究发现HPV感染以及相关肿瘤的危险因素包括了低CD4+T淋巴细胞计数和高HIV病毒载量[15-17]:与CD4+T淋巴细胞计数大于500/mm3的女性HIV感染患者相比,CD4+T淋巴细胞计数小于200/mm3和在200~500/mm3的女性HIV感染患者清除HPV的可能性分别降低了71%和32%[15]。ACTG 5298研究探讨了4价HPV疫苗对预防HIV阳性MSM和女性发生肛门HPV持续感染的效果[16],共纳入了575例受试者,其中男性为472例,女性为103例;其中98%参与者接受了联合ART,平均持续时间为4.9年;研究发现有33%参与者肛门活检为HISL,与未发生HISL的受试者相比,该部分参与者的绝对和最低CD4+T细胞计数较低,病毒载量>50拷贝/mL。一项随机安慰剂对照试验分析了关于肛门黏膜中感染高危型HPV相关的风险因素,多变量分析显示病毒载量≥200拷贝/mL是高危型HPV感染的风险预测因素,年龄增长是防止感染的保护因素[17]。
2 预防HPV相关肿瘤的联合策略
2.1 HPV疫苗接种
目前,针对HPV感染最有效、最特异的手段是预防性接种HPV疫苗,它能够从根本上阻断HPV传播,是一项重要的初级预防策略。2020年UNAIDS发布了2025年艾滋病防控目标[18],其中包括了95%育龄妇女接受艾滋病、性健康和生殖健康服务,而性健康和生殖健康服务中则包含了接种HPV疫苗、宫颈癌监测和管理。目前上市的HPV疫苗有3种,分别是2价、4价以及9价疫苗 (见表1)。研究发现HPV疫苗对成年HIV感染者来说是安全且具有高度免疫原性的[17,19]:一项随机双盲安慰剂对照试验[17]评估了4价HPV疫苗在HIV感染MSM中的安全性和免疫原性,该研究于2012—2014年共纳入了162例受试者,其中91.8%受试者接受ART,平均CD4细胞计数为688.5/μL,肛门黏膜中高危型HPV感染率达73.7%;最终纳入的129例受试者被随机分配为接种疫苗组(66例)和安慰剂组(63例),结果显示76% HIV患者在接种第3剂疫苗后的第1个月具有可测量的抗体水平,未发生与疫苗接种相关的严重不良事件;另一项开放标签队列研究评估了4价HPV疫苗对HIV阳性妇女的安全性和免疫原性,该研究于2008—2012年在加拿大14所艾滋病门诊诊所招募了372例女性,共310例至少接受了一剂HPV疫苗,277例接受了3剂,72%参与者在基线时病毒载量已被抑制(<40拷贝/mL),CD4+T细胞计数中位数为510/mm3,结果发现与未接种疫苗的参与者相比,首次接种疫苗的妇女抗体反应峰值高出1.74~3.05倍,因此计划在病毒抑制时接种HPV疫苗是最大限度地提高疫苗免疫反应的最佳选择[19]。此外,研究结果提供了强有力的证据表明老年HIV阳性妇女仍然可以从HPV疫苗接种中受益。Mcclung等[20]为了进一步评估疫苗的影响,分析了来自5个站点的人口监测数据,对年龄为18~39岁、诊断为2~3级宫颈上皮内瘤变或原位腺癌(CIN2+)妇女的标本进行了37种HPV类型的检测,在10 206例中,HPV16/18阳性CIN2+病例的比例和估计数量从2008年的52.7%下降至2014年的44.1%,其中在接种疫苗的妇女中下降幅度最大。研究表明在美国推出HPV疫苗的8年内,18~39岁女性中由HPV疫苗类型引起的宫颈癌前病变比例和估计数量总体呈下降趋势,证明了HPV疫苗接种计划在美国的高度有效性影响。
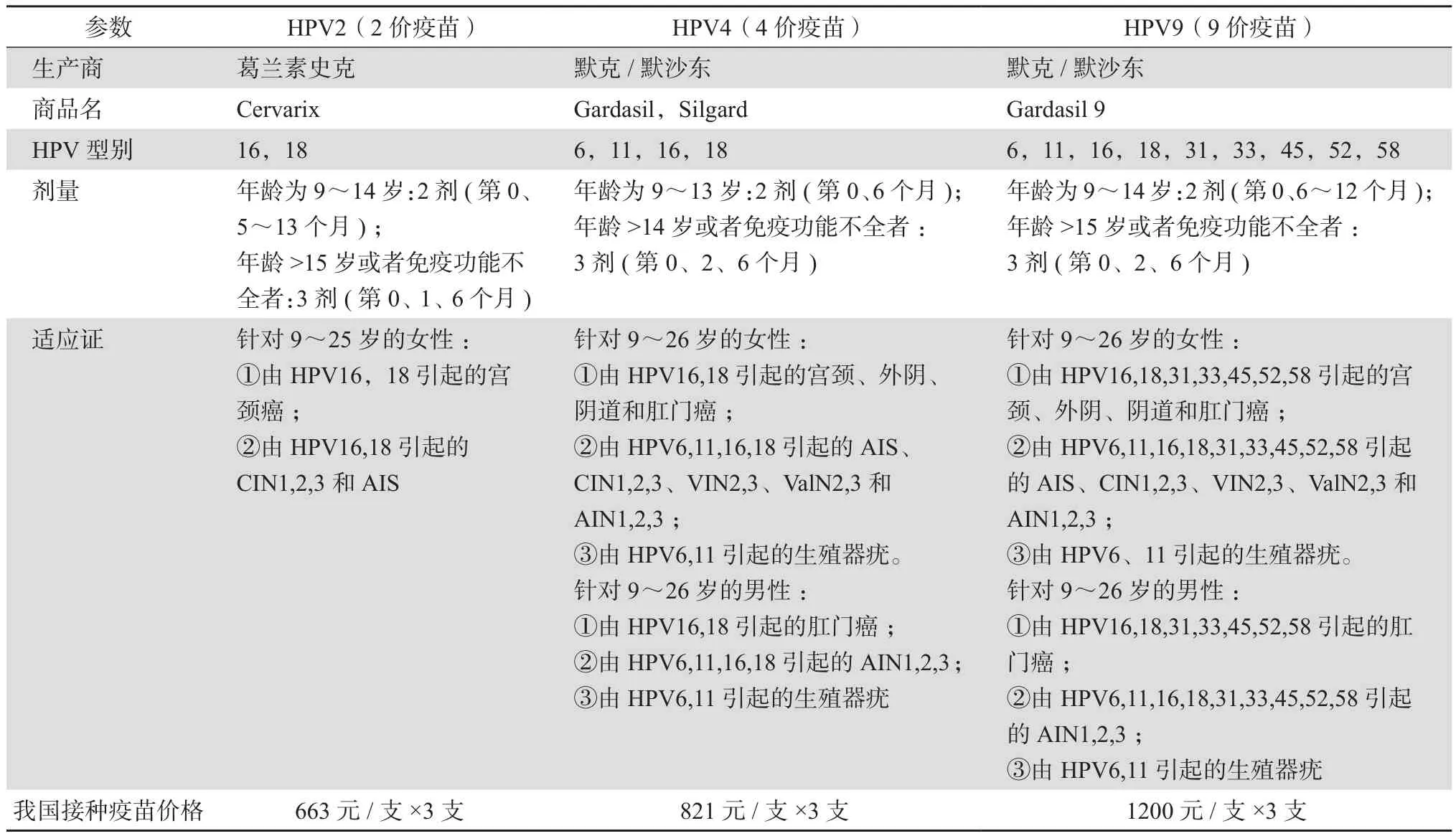
表1 目前可用的预防性HPV疫苗之间的比较
以上研究表明预防性接种HPV疫苗对HIV感染者是安全且具有免疫原性的,因此应将HPV疫苗纳入HIV感染者的肿瘤预防计划中。但需要注意的是,最易患肛门癌的人群是与男性发生性关系的HIV阳性男性[21],如果只对女性人群进行疫苗接种,这部分人群则无法获得群体免疫保护,因此有必要将该部分人群也纳入疫苗接种计划中。
2.2 早期筛查
由于宫颈癌和肛门癌均是可预防的疾病,因此进行常规筛查是一项重要的预防和控制措施。一项前瞻性研究评估了672例HIV抗体阳性和阴性妇女宫颈癌的患病情况,发现HIV阳性宫颈癌患者的平均年龄要比HIV阴性宫颈癌患者小15岁,感染HIV的妇女患宫颈癌的时间要比未感染HIV妇女早10~15年,意味着HIV感染状态加速了宫颈癌的进展[22]。因此,针对HIV感染者需要尽早开始筛查,并且缩短筛查间隔时间。一般而言,建议从确诊HIV感染起对所有成年妇女进行筛查,并且根据当地实际HPV检测的不同情况,建议每隔1~3年进行一次筛查[23]。一项meta分析评估了埃塞俄比亚HIV感染女性宫颈癌筛查的流行率及其相关因素,发现埃塞俄比亚HIV感染女性接受宫颈癌筛查的比例很低,宫颈癌筛查的总流行率为18.17%,其中教育水平、对宫颈癌的了解情况以及感知水平与HIV感染女性的宫颈癌筛查情况密切相关;研究结果表明,除了提供筛查服务外,还需要改进现有的国家宫颈癌筛查策略,加强生殖健康教育和宣传;此外,宫颈筛查服务应与常规护理和治疗相结合,以便HIV感染妇女更易获取相关咨询服务[24]。
尽管已经提出了各种各样的肛门癌筛查策略,但目前没有一种策略在随机对照试验中得到评估,国际上对最佳的肛门癌筛查策略也没有达到共识[25]。但由于肛门癌与宫颈癌的相似性以及HIV感染人群中日益增加的肛门癌负担,对肛门癌进行筛查是合理的。因此,应对感染HIV的MSM进行早期肛门细胞学筛查,以实现早诊断、早治疗,从而降低肛门癌发生的危险。此外,在HPV相关癌症的早期筛查中,对于筛查方法的选择应主要取决于各个国家和地区实际的医疗资源提供情况和人群的接受程度,以实现最大规模的人群筛查队列。
3 总结与展望
随着HIV感染者预期寿命的不断增加,延长的生存期为宫颈癌、肛门癌和其他HPV相关癌症的发生发展提供了更多的时间,这意味着人群预防HPV相关癌症的需求也将逐渐增加,因此亟需有效的HPV预防和管理策略。
HPV疫苗可有效预防发生HPV相关肿瘤,已有国家对HIV感染者提出了进行HPV疫苗接种的建议。在我国,HPV疫苗对HIV感染者的预防作用知之甚少。一项横断面研究评估了我国乌鲁木齐MSM对HPV疫苗的态度和可接受性,调查结果显示MSM对HPV的了解很少,但大部分的MSM在咨询后愿意接受HPV疫苗,其中感染HIV的MSM更愿意进行疫苗接种并愿意支付疫苗接种费用[26]。因此医务人员不仅需要关注HIV感染者的HPV感染情况,同时应在HIV感染者中大力推广HPV疫苗,对该人群进行相关知识宣教例如HPV感染的危险性、早期进行HPV筛查的必要性以及相关疫苗接种的建议等,以促进人群对疫苗的认识和了解,从而进一步提高对疫苗的接受程度。此外,在提出疫苗接种建议时,医务人员需要针对不同年龄、不同性别人群进行相关疾病和疫苗知识的宣教,指导人群选择符合个体健康状况以及经济条件的疫苗类型,从而大大提高疫苗的有效性。
对于年龄太大无法接种疫苗,或在接种疫苗之前已经接触过HPV16和HPV18的男性或女性HIV感染者,早发现、早诊断和早治疗的二级预防可能是降低其患癌症风险的重要手段。因此,针对该部分人群,需要重点关注肿瘤筛查和相关管理方案,以降低HIV感染者发生后续癌症的危险。此外,需要注意的是安全性行为措施也是减少HPV传播和感染风险的重要因素,因此在宣教的过程中应告知人群减少危险性行为,从而降低将HIV传播给性伴侣的风险,同时避免传播HPV。
