以肺部感染为主的惠普尔病1例
2021-09-30曾灏瑜佘德宇
曾灏瑜, 佘德宇
1 临床资料
患者男,28岁,以“活动后气促1个月,反复腹泻半个月,气促加重2 d”为主诉于2020年10月14日就诊我院。患者于入院前1个月开始出现活动后气促,上楼梯1~2层即气促明显。入院前半个月患者无明显诱因出现腹泻,每日大便3~5次,解稀水样便,无黏液脓血,患者自行口服抗生素治疗(具体不详)后腹泻逐渐好转,但气促症状仍进行性加重,夜间不能平卧,伴有咳嗽、咯痰、全身乏力。入院当天患者出现呼吸困难加重,由家属送至我院就诊。入院时患者精神极差,呼吸急促,应答不利,当天解稀便1次,尿量少,近半个月体重下降约2 kg。
既往史: 近5年有嗜酒史,每日饮5~8瓶啤酒,发病期间仍间断饮酒。否认发病前有不洁饮食史;否认“高血压”“糖尿病”“冠心病”等病史;否认“结核”“乙肝”等传染病史。
入院查体:体温36.8℃,脉搏124次/min,呼吸32次/min,血压103/55 mmHg。急性面容,神清,精神极差难以应答及配合查体。双侧瞳孔等大等圆,对光反射灵敏。口唇苍白,咽充血,双侧扁桃体未见肿大,可闻及咽部有痰鸣音。双肺呼吸音粗,双侧肺底可闻及广泛细湿啰音。心、腹查体未见明显异常。余神经系统查体患者不能配合。
辅助检查:入院行实验室检查,PaO268 mmHg,PaCO211.8 mmHg,乳酸 8.5 mmol/L,pH 7.44,白细胞 11.72×109/L,降钙素原 0.796 μg/L,天冬氨酸转氨酶 76 U/L,γ-GT 262 U/L,白蛋白36.7 g/L,肌酐 121.0 μmol/L,血钠 113.6 mmol/L,血氯 79.9 mmol/L,血糖 9.2 mmol/L,前脑利钠肽(pro-BNP) 21 031 ng/L,肌红蛋白 178.8 μg/L,超敏肌钙蛋白I 445.8 μg/L。粪便霍乱弧菌、沙门菌、志贺菌等培养均为阴性。
腹部超声示:①肝实质弥漫性病变(酒精肝?);②胆、脾、胰、双肾、膀胱未见明显异常。心脏超声:①心包少量积液;②心内结构未见明显异常;③心功能正常;左室射血分数(LVEF)66%,左心室缩短率(FS) 36%。胸部CT提示:①双肺实变病灶,以双下肺为主;②心包少量积液;③双侧胸腔少量积液。入院诊断:①中毒性心肌炎;②急性心功能不全 NYHA Ⅲ级;③肺部感染;④电解质紊乱(低钠低氯血症);⑤代谢性酸中毒并呼吸性碱中毒;⑥急性肾功能不全(肾前性);⑦酒精性肝病;⑧急性肠炎?⑨多浆膜腔积液。
入院后心电监护,行气管插管有创呼吸机辅助通气,予护胃护肝、平喘化痰、纠正电解质紊乱、利尿减轻心脏负荷等对症支持治疗,经验性给予“头孢噻肟-舒巴坦+莫西沙星+利巴韦林”抗感染、抗病毒治疗,患者腹泻好转,但仍可吸出大量黄白脓痰,间有发热,体温多波动于37.0~38.5℃,行纤维支气管镜吸痰,取肺泡灌洗液送检病原学高通量DNA基因测序。于入院第3日检出惠普尔养障体,余细菌、真菌、病毒、寄生虫及非典型病原体均未检出。当天调整抗感染治疗方案为:“头孢曲松+甲氧苄啶-磺胺甲唑”后,患者热峰即明显下降,入院后1周起未再出现发热,精神明显好转,痰量减少,肺部啰音消退,复查血象、降钙素原恢复正常,复查胸部CT示双肺感染灶较前明显吸收;双侧胸腔少量积液;心包少量积液同前无明显变化(图1)。病情平稳好转,于入院后第8天转出重症医学病房,继续抗感染、纠正水电解质紊乱等对症支持治疗后于入院第10天好转出院。
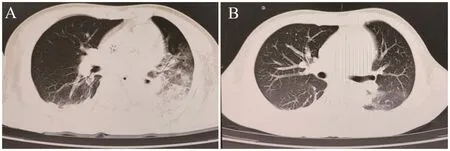
图1 患者入院时和住院1周后肺部CTFigure 1 Pulmonary CT scans of the patient at admission and after one-week treatment
出院诊断:①惠普尔病;②中毒性心肌炎;③急性心功能不全 NYHA Ⅲ级;④肺部感染;⑤电解质紊乱:低钠低氯血症;⑥代谢性酸中毒并呼吸性碱中毒;⑦急性肾功能不全(肾前性);⑧酒精性肝病;⑨急性肠炎;⑩多浆膜腔积液;低蛋白血症。
2 讨论
该患者为青年男性,近5年有大量酗酒史,既往无特殊病史,以腹泻伴气促症状起病,伴有营养不良,腹泻逐渐好转同时肺部症状却逐渐加重,入院时有明显呼吸困难,需呼吸机持续辅助通气改善低氧血症,伴严重电解质紊乱。入院后行经验性抗感染治疗后,肺部感染仍进一步加重,肺泡灌洗液病原学高通量DNA基因检测检出惠普尔养障体后针对性调整抗感染治疗,患者体温逐渐下降,结合实验室及影像学检查均支持感染明显好转,病情持续平稳好转后出院。
惠普尔病是由一种革兰阳性菌——惠普尔养障体引起罕见的全身性感染疾病,多见于有污水、污土接触史及免疫缺陷的人群[1-2],据报道欧洲地区年发病率仅有百万分之三[3-4],以慢性感染为主,偶见急性感染起病,一旦起病多器官均可受累及,因此临床表现多样而不易被及时诊断,未及时治疗有致死性[4]。
惠普尔病可累及胃肠道、心血管系统、呼吸系统、中枢神经系统、骨骼系统及皮肤等全身多系统。典型惠普尔病最常见的症状为体重下降,多伴有腹泻,其他较常见的症状有游走性关节炎、心包炎、心内膜炎、葡萄膜炎及多种神经系统受累症状[5]。据报道,在典型的惠普尔病中,有30%~40%患者发生肺部受累,出现胸腔积液、肺浸润或纵隔肉芽肿性腺病[6]。惠普尔病累及胃肠道的最常见的临床表现为肠道脂肪代谢障碍,胃镜下多可见十二指肠及空肠黏膜组织学上的损伤,小肠绒毛增粗变形,活检组织内巨噬细胞PAS染色阳性或可在电镜下发现惠普尔养障体。诊断主要依赖于十二指肠活检标本PAS染色、惠普尔养障体PCR检测及相关临床表现,此外若胸膜、肺、肝等活检或阑尾病理显示有本病典型的组织学改变者,结合有阳性病原学发现,亦可确立诊断[7]。
迄今惠普尔病的治疗仍未有广泛的共识,主要的治疗原则为针对惠普尔养障体的抗感染治疗、营养支持、纠正水电解质紊乱。由于病例罕见,缺乏大量病例的临床治疗经验,抗感染治疗方案均为经验性治疗,缺乏足够的依据支持。在过去四环素一度被列为一线治疗药物,但却被发现治疗后复发率很高(平均28%)。随后还先后提出了包括氯霉素、青霉素G、链霉素等抗感染方案。但即使有上述特定的抗感染治疗方案,平均5年后仍有2%~33%的病例出现临床复发,且复发通常以神经系统受累为特征[2,8]。目前抗菌药物治疗的标准倾向于选择能够跨越血脑屏障的抗菌药物,如甲氧苄啶-磺胺甲唑。
在一项包括40例的随机对照试验中使用了静脉注射美罗培南1 g, 3次/d或头孢曲松2 g,1次/d,持续14 d,然后口服甲氧苄啶-磺胺甲唑160~800 mg,2次/d,口服1年的方案,治疗过程中仅有2例死于其他病因,且其余患者在随后10年随访均未出现复发,达到临床治愈[9]。而在另一项前瞻性非随机对照研究中对此方案进行了改良,予以静脉注射头孢曲松2 g,1次/d,连续14 d,口服同等剂量甲氧苄啶-磺胺甲唑,疗程缩短至3个月,但治疗效果与前无明显差异[10]。而在另一项29例惠普尔病的队列研究中则提出了联用多西环素及羟基氯喹治疗1年,然后使用多西环素终生治疗的治疗方案,并在体外实验中也同样取得良好的疗效[11]。回顾本病例,患者有长期大量饮酒史,存在潜在的免疫功能低下状态导致机会性感染可能,以腹泻症状起病,伴有低蛋白血症、严重低钠低氯血症等营养不良表现,在入院时患者以严重的肺部感染为主要表现,结合患者上述症状及肺泡灌洗液中检出惠普尔养障体,从而作出惠普尔病诊断。诊断后迅速调整抗菌药物,应用了目前推荐的头孢曲松及甲氧苄啶-磺胺甲唑。由于考虑患者同时存在严重肺部及消化道感染,导致了严重内环境紊乱,单用头孢曲松抗感染力度不足的可能性大,因此同时使用头孢曲松及甲氧苄啶-磺胺甲唑抗感染治疗。经治疗后患者消化道症状迅速消退,1周后复查胸部CT提示双肺感染灶较前明显吸收,证实了调整方案后抗感染治疗效果显著,也进一步支持了惠普尔病的诊断。遗憾的是,患者出于经济原因而未完善内镜检查及获得进一步的病理学证据。
多数文献报道此病主要集中于消化道症状及关节炎、葡萄膜炎、心内膜炎等表现,肺部病变的相关报道十分稀少,报道病例中患者多表现为气短、咳嗽,伴或不伴有胸痛,胸部CT可见双肺基底部病灶,肺内结节影及纵隔病变[12-16]。与报道病例相仿的是,本病例肺部症状主要为咯痰、呼吸困难、发热,伴有低氧血症,且影像学同样提示双肺实变病灶主要位于基底段。而与报道不符的是本病例并无关节炎表现,且消化道、肺部症状呈序贯性发展,肺部CT未见结节及纵隔病灶,整个病情转归过程持续1个月余。在治疗选择上,不同于推荐的头孢曲松、甲氧苄啶-磺胺甲唑序贯抗感染方案,本例选择了两种抗菌药物同时联用,并取得了显著的治疗效果,提示了现存的推荐抗感染治疗方案或仍存在较大的调整空间,但由于这种疾病病例数少,需要很长时间的随访,因此有必要通过其他研究来进一步调整治疗方案。本报道这一病例并提供影像学表现以供参考,提示当遇到相似临床表现病例时应疑诊这一罕见病,积极寻找活检及病原学证据,及时明确诊断以调整抗感染治疗方案。
