LR6型碱性锌锰电池两节串联放电特性研究
2021-09-27张奇尧
徐 伟,张奇尧
(中银(宁波)电池有限公司,浙江 宁波 315040)
1 引言
碱性锌锰电池是目前应用范围较广的电池品种之一,在家用电器、通信、医疗器械、电动玩具等领域均有广泛应用。电性能的提升[1-2]、安全和防漏性能的改善[3-4]以及新材料、新工艺的应用[5-6]也一直是电池行业研究的热点。
随着科技的发展,用电器功耗逐步降低,要求电池在较低的工作电压下也能正常使用。而多数用电器无低电压报警提示功能,一直放置于用电器内的电池会引起过度放电造成漏液[7-8]。为提升客户满意度,电池的过度放电、小电流放电[9]近年来也逐渐得到了关注。但这些研究往往以单节电池作为试验对象,而实际用电器使用中,电池使用多以串、并联组合形式出现,单节使用的情况较少。这就造成实验室研究与实际应用场景之间往往会出现不匹配的情况。
数字电视机顶盒遥控器是日常生活中最为常见的用电器之一,多为两节AA电池串联使用。本文以遥控器的使用为切入点,对LR6碱锰电池两节串联及单节使用情况下的电压变化、漏液及内部反应情况进行对比,并从电化学角度对放电特性进行分析,以期对碱性锌锰电池的串联使用特性引起关注。
2 实验部分
2.1 遥控器使用模式测试
选取使用两节AA电池的数字电视机顶盒遥控器一只(DZ40-1A,浙江产)。恒温(20±2) ℃条件下,使用直流稳压电源(IT6121,ITECH)自3.2 V开始并以0.2 V递减进行电压输出,电流表(C31/1-A型,上海良表仪器仪表有限公司)测量相应电压下的工作电流,直至遥控器无法工作为止。
2.2 电压变化测试
选取市场上常见的电池品牌:S(保质期10年,有效期:03-2029)、N(2019-01生产),分别按以下(1)、(2)进行测试,数量各10组。
(1)恒温(20±2) ℃条件下,取两节同品牌电池(1#、2#)搭载负载R(苏州产)按图1(a)方式进行连接,测量每节电池的电压变化情况。
(2)恒温(20±2) ℃条件下,取一节电池(3#)搭载负载R′(R′=1/2R,苏州产)按图1(b)方式进行连接,测量电池的电压变化情况。
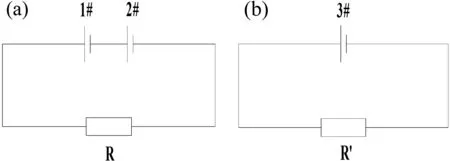
图1 实验装置图Fig.1 Scheme of experiment.
2.3 电池漏液及解剖情况
测试结束后,将电池从试验装置中取出,恒温(20±2) ℃条件下放置30天,统计漏液率。同时对电池进行解剖,分离正极、负极、铜钉,观察反应情况。
3 结果与讨论
3.1 遥控器使用模式测试
图2为不同输出电压下遥控器工作电流的变化曲线。图中数据点相连曲线的趋势线为直线,斜率为0.082。由此推断遥控器使用为大电阻恒阻模式,阻值R为82 Ω。
3.2 电压变化曲线

图3 电压特性变化曲线Fig.3 Curves of voltage characteristics.
图3分别是S、N电池实验过程中的电压变化曲线。从曲线的变化情况来看,S、N电池具备相同的反应特征,均可分为A、B两段。为方便讨论,两节串联使用中电压上升的电池统一标识为1#,电压下降的电池统一标识为2#,单节使用的电池统一标识为3#。
A段,即起始至电压0.9 V。这一阶段,1#、2#、3#电池电压呈现均匀下降,无明显差异。
正负极活性物质被缓慢消耗,电化学极化和浓差极化使得电压逐步下降,电池正负极反应机理一致。一般认为,正极中二氧化锰的放电机理,分为两步进行[10],这一阶段以第一步反应(式1)为主。该反应是由一种固体结构(MnO2)转化成另一种固体结构(MnOOH)。真正发生的是电子与质子进入晶格中而未改变其基本的(或本质的)结构,过程是一个均相反应。MnO2还原速度较大,但质子在固相中扩散速度较慢,质子堆积在表面层来不及扩散到内部,电极极化增大,电极电位负移。
MnO2+H2O+e-→MnOOH+OH-
(1)
负极中锌在OH-作用下主要发生氧化反应(式2和3),Zn表面OH-浓度下降,产生浓差极化。但同时,Zn的粒径逐渐变小,反应活性增强。总体来看,这一阶段负极电位基本保持不变[11]。
Zn+4OH-→[Zn(OH)4]2-+2e-
(2)
[Zn(OH)4]2-→Zn(OH)2+2OH-
(3)
在B段,即电压0.9 V至结束。这一阶段,串联使用与单节使用的差异性开始显现。串联的两节电池电压逐步分化,其中1#电池略微升高,最终维持在0.8 V~1.0 V;2#电池则急剧下降,并出现负电压,最终维持在-0.8 V~-1.0 V;3#电池电压快速下降,最终维持在0.03 V~0.2 V。
二氧化锰这一阶段以第二步反应为主(式4)[10],分为三个连串步骤:(1)Mn3+自MnOOH中以诸如Mn(OH)4-铬离子的形式溶液于电解质溶液中;(2)在碳表面上,Mn(OH)4-电化学还原为[Mn(OH)4]2-(相当于Mn3++e-→Mn2+);(3)Mn(OH)2自[Mn(OH)4]2-饱和溶液中沉淀。这个过程是一个多相反应,因为包括两个不同的固相,一个初始固相(MnOOH)转化成另一个终了固相[Mn(OH)2]。电化学反应是通过溶解了的离子物质而进行的。反应过程中伴随着反应式(5)的发生,Mn(OH)2逐渐生成非活性的Mn3O4,生成的Mn3O4既不能被氧化,也不能被还原[12]。
MnOOH→Mn(OH)4-+e-→[Mn(OH)4]2-→Mn(OH)2
(4)
2MnOOH+Mn(OH)2→Mn3O4+2H2O
(5)
负极中一方面随着Zn的进一步消耗,以及OH-浓度的进一步降低,反应活性降低,另一方面,负极产物ZnO、Zn(OH)2等大量形成(式6),附着在Zn粉表面,阻碍了Zn与OH-的接触,从而增大了电化学反应阻力。负极电位迅速正移。
Zn(OH)2→ZnO+H2O
(6)
由于碱锰电池设计一般为负极过剩正极限容的形式。正极中活性锰首先耗尽,继续放电则会出现过放。负极中过剩的Zn的溶解和析氢反应(式7)替代了原来的放电过程[13-14]。此时电压出现陡降。
2H2O+2e-→2OH-+H2↑
(7)
串联电池中,2#电池首先失效成为负载,未失效的1#电池对2#电池进行充电。这时2#电池出现反极,严重过放。内部反应剧烈,OH-氧化生成O2(式8),电压表现为负值[15-16]。
4OH-→2H2O+O2↑+4e-
(8)
1#电池电压略有上升。原因可能是随着电池输出能力的降低,电流下降。反应剧烈程度降低,电化学极化和浓差极化降低,质子固相得到扩散的结果。
电池单独使用时,3#电池在正极活性锰消耗后电压也出现快速下降现象,负极中过剩的Zn同样会出现溶解和析氢反应,但内部碱液还没被氧化。总体反应程度较2#电池轻微,表现为曲线下降幅度较2#电池小。
3.3 电池漏液及解剖情况
将测试结束后的S、N电池从试验装置中取出,在恒温(20±2) ℃条件下放置30天,漏液率情况列于表1所示。由表1可知,2#电池漏液率均最高,3#电池次之,1#电池最低。这是由于2#、3#电池在反应后期均有析氢反应发生,生成的氢气使得电池内部压力持续增大,直至超过密封圈防爆压力,泄压阀打开,出现漏液。其中2#电池在负电压情况下发生析氧反应,生成的氧气与氢气叠加,使得内部压力增长较多,漏液也越多。3#电池由于未出现过放情况,内部产生气体较少,故无漏液情况发生。
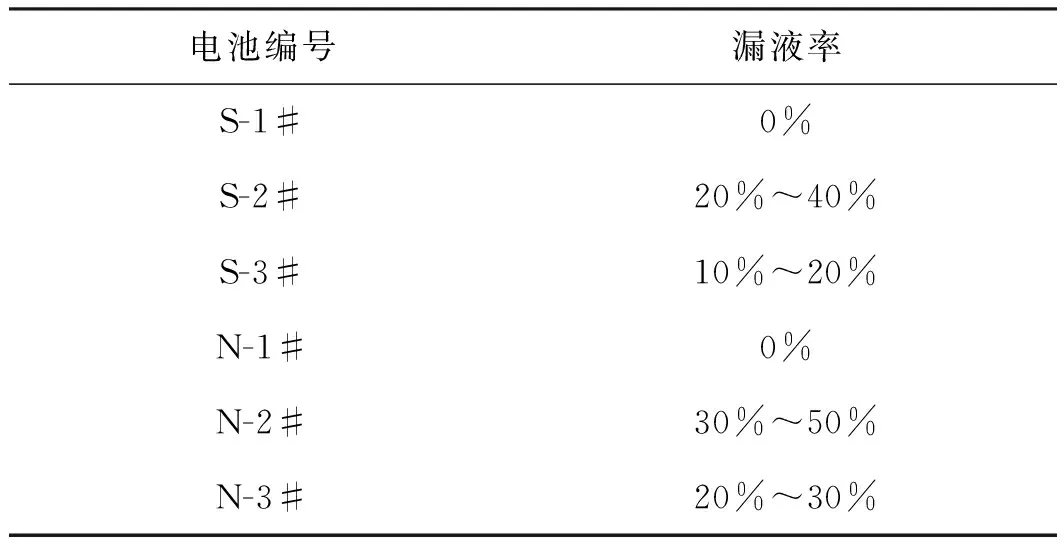
表1 S、N电池贮存30天的漏液率Table 1 Leakage of S and N batteries after 30 days storage.
测试结束后对电池进行解剖,观察各部位反应情况,发现S、N电池情况一致,具体见表2。其中2#电池反应最剧烈、最彻底,3#电池次之,1#电池相对最轻微。特别是铜钉部分,2#电池除表面有黑色斑点外表面还存在凹凸不平、露铜情况。推测在过放及反充过程中,铜钉(Cu-Zn合金)在负电压状态下也参与反应,铜和镀层溶解脱落。

表2 电池不同部位解剖情况Table 2 Reaction situation of battery for different parts.
4 结论
以数字电视机顶盒遥控器使用模式为切入点,对LR6碱性锌锰电池在两节串联及单节使用情况下的电压变化情况进行测试。试验结果表明:两节LR6电池串联使用时,部分电池会出现严重过放、反充现象,电池电压特征表现为负电压;与单节LR6电池使用相比,串联使用中出现负电压的电池内部反应更剧烈,也更容易引起漏液。
