肺结核合并机化性肺炎1例
2021-09-24胡炜燚高卫卫曾谊
胡炜燚 高卫卫 曾谊
作者单位:211132 江苏 南京,南京中医药大学附属南京医院 南京市第二医院 南京市公共卫生医疗中心 结核三科
机化性肺炎(organizing pneumonia,OP)指以肺泡腔、肺泡管、呼吸性细支气管及终末细支气管腔被疏松的纤维结缔组织充填为病理学特征的疾病[1]。继发性机化性肺炎(secondary organizing pneumonia SOP)属于病因明确的机化性肺炎,有别于隐源性机化性肺炎(cryptogenic organizing pneumonia COP),常见的致病因素有感染(细菌、病毒、支原体等)、结缔组织疾病、药物(胺碘酮、博来霉素等)、放射线、器官移植等[2]。感染继发SOP临床确诊比较困难。结核分枝杆菌(Mycobacterium tuberculosis MTB)感染引起的SOP更鲜有报道。现将南京市第二医院结核科收治的一例与MTB感染相关的SOP报道如下。
病例资料
患者男性,39岁,因“咳嗽、咳痰两个月”于2019年5月10日入住我院结核科。患者两个月前受凉后咳嗽,咳白色泡沫痰。予口服头孢克肟抗感染治疗一周,症状无缓解。2019年04月01日在外院呼吸内科胸部CT发现右肺上叶后段实变,病灶周围可见磨玻璃影(见图1-2)。血常规、C反应蛋白、降钙素原、呼吸道病原学抗体、隐球菌荚膜抗原、G试验、GM试验、抗核抗体、自身免疫抗体均为阴性。结核感染T细胞试验:阳性。给予静滴哌拉西林舒巴坦、莫西沙星抗感染,症状无缓解。2019年04月09日行支气管镜检查:右肺上叶后段黏膜充血水肿,未见溃疡、坏死物。可见白色泡沫样分泌物,在该处收集支气管肺泡灌洗液(BALF)送检。BALF细菌培养、真菌培养及抗酸杆菌涂片均为阴性。支气管镜活检:肺间质纤维组织增生伴炎细胞浸涧,局部见马松小体,组织学倾向机化性肺炎(见图3)。于2019年04月19日行CT引导下经皮肺穿刺活检,组织病理学:右肺上叶组织肺间质纤维组织增生伴淋巴细胞、浆细胞浸润,肺泡和呼吸性细支气管内可见肉芽组织构成的松散栓子,未见肿瘤细胞,考虑OP(见图4-5)。遂加用“泼尼松30mg/日”治疗。2019年05月06日复查胸部CT:右肺上叶大片实变及磨玻璃影范围较前增大,纵隔窗实变区密度均匀,未见明显低密度坏死,可见支气管充气征(见图6-9),患者症状加重,咳嗽加剧,痰量增多,伴胸闷、气喘、呼吸困难。血气分析:PH值 7.39,PaO271 mmHg,PaCO226 mmHg。2019年05月06日将肺穿刺活检标本重新进行病理学复检,特殊染色:抗酸染色阳性(一条/400倍视野),GMS(-),革兰氏(-)(见图10)。考虑MTB感染引起SOP可能性大,为进一步诊治,于2019年5月10日转入我院结核科。入院后查痰涂片抗酸染色阴性。于2019年05月20日再次行支管镜检查:右肺上叶后段开口稍狭窄,黏膜充血水肿,无粟粒样结节及溃疡坏死,无干酪样坏死物及肉芽增生,不考虑支气管结核。灌洗液Gene-Xpert MTB/RIF 结核杆菌 阳性,利福平耐药 阴性。根据上述实验室及病理学检查结果,诊断明确为:继发性肺结核、继发性机化性肺炎(MTB感染引起SOP)。给予异烟肼(H,300mg/日)、利福平(R,600mg/日)、吡嗪酰胺(Z,1 500mg/日)、乙胺丁醇(E,750mg/日)抗结核及泼尼松40mg/日治疗。经抗结核药物及糖皮质激素治疗后患者咳嗽、咳痰逐渐好转,胸闷症状消失。2019年06月10日(治疗1月后)复查CT示右上肺实变较前明显吸收(见图11-12)。2019年09月10日(治疗4个月后)病灶进一步吸收伴局部纤维条索形成(见图13-14)。
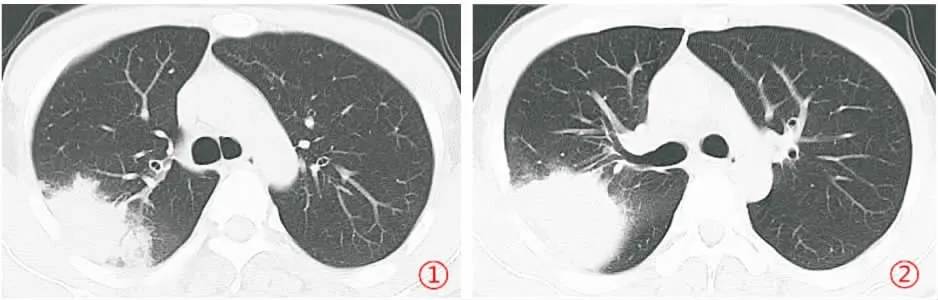
图1-2 胸部CT(2019年4月1日)右肺上叶后段肺实变伴病灶周围磨玻璃影。

图3 经支气管镜肺穿刺活检病理(2019年04月09日)右肺上叶组织可见肺间质纤维组织增生伴淋巴、浆细胞浸润,肺泡腔内可见Masson 小体形成(箭头),未见肿瘤细胞。(×400倍)

图4-5 CT引导下经皮肺穿刺活检组织病理学(2019年04月19日)右肺上叶组织肺间质纤维组织增生伴淋巴细胞、浆细胞浸润,肺泡和呼吸性细支气管内可见肉芽组织构成的松散栓子,未见肿瘤细胞。(×400倍)
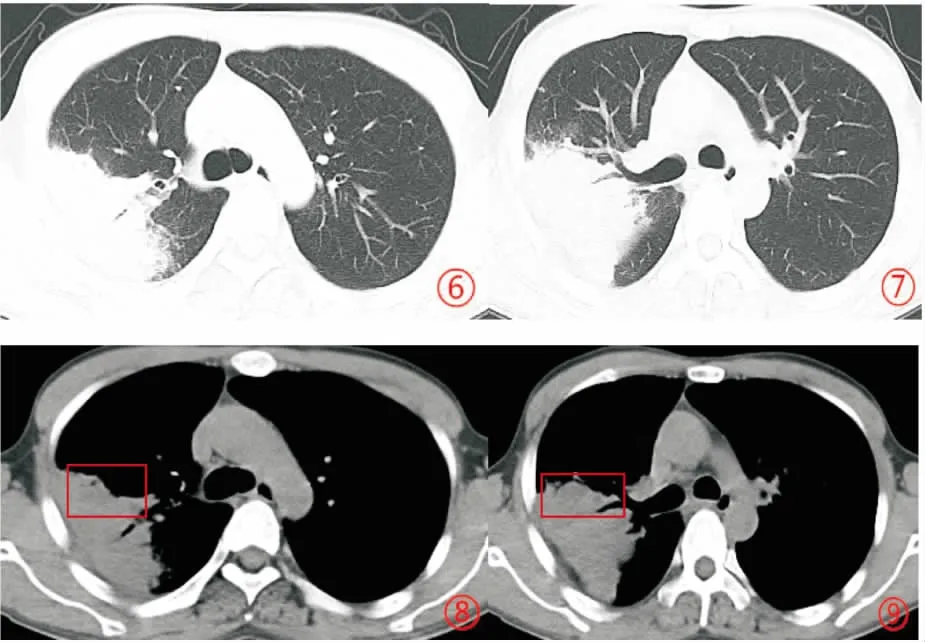
图6-9 胸部CT(2019年05月06日)右肺大片实变及磨玻璃影范围较前增大,纵隔窗实变区密度均匀未见明显低密度影,可见支气管充气征。

图10 特殊染色×400抗酸染色(一个阳性杆菌),GMS(-),革兰氏(-)。
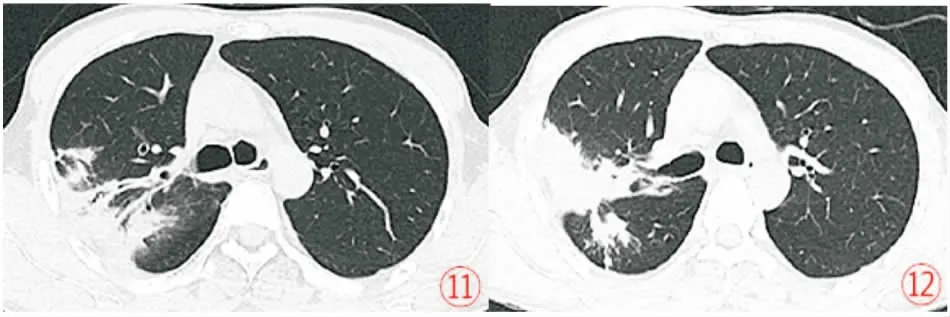
图11-12 胸部CT(2019年6月10日)右肺上叶后段实变范围明显缩小,伴上叶后段支气管管壁增厚

图13-14 胸部CT(2019年9月10日)右肺上叶后段病灶进一步吸收,伴局部纤维条索形成
讨 论
OP是一种病理概念,即肺泡腔、肺泡管和呼吸性细支气管内的炎性渗出物机化,伴有纤维母细胞、肌纤维母细胞增生。肺泡内的纤维灶称为Masson小体,可伴有淋巴细胞、浆细胞及单核细胞浸润[2]。2002 年,美国胸科协会/欧洲呼吸病学会提出了将OP分为COP和SOP。COP为不明原因的OP,SOP是有明确诱因的引起的OP,已发现SOP的病因有药物、结缔组织病(其中以肌炎和皮肌炎最常见)、肿瘤,肾移植等[2]。感染也是SOP的常见原因。国外研究相对较多的是病毒感染,如H1N1甲型流感病毒、B型流感病毒等。国内报道的有鲍曼不动杆菌、大肠埃希菌、金黄色葡萄球菌、铜绿假单胞菌、副流感嗜血菌、H1N1甲型流感病毒、白色念珠菌、烟曲霉菌、隐球菌等各种病原体[3-5]。MTB感染引起的SOP国内、外仅有少数病例报道。检索2000年1月至2019年12月的中外文献,仅收索到4篇7例MTB感染引起的SOP病例报道[6-9]。
OP是肺损伤后增殖修复的过程中某个特定时期的表现,并非某种疾病所特有,药物、肿瘤等各种继发因素均可产生OP的病理学改变[10]。本病例主要表现为右上叶后段进行性发展的肺实变,2019年4月09日和2019年4月19日分别经支气管镜肺穿刺和经皮肺穿刺两次活检,取自病灶不同部位,均呈现OP的典型病理学特征,而未见肺结核常见的渗出、增殖、坏死性病变。说明病灶的病理以OP为主导。故可诊断为SOP。与以往的MTB相关性SOP的病例报道相符[6-9]。结核分枝杆菌感染引起SOP的研究较少,其详细机制尚不完全清楚。根据已有对感染所致SOP的研究[11]推测,MTB感染后损伤肺泡上皮细胞,随后触发T淋巴细胞及中性粒细胞的聚集、增殖及活化,导致各种炎性细胞因子的分泌,包括各种促纤维因子,最终引起纤维母细胞的活化增生,启动纤维化的进程。如能及早识别MTB感染并尽快抗结核干预,这个过程是可逆的。但如果不能早期识别,虽应用糖皮质激素,亦无法扭转其病理学进程,最终可发展为肺纤维化,导致不可逆的肺功能受损。
总结本例及既往的7例文献报道,MTB感染所致的SOP具有以下特点:1) 临床症状:缺乏特异性,主要表现为咳嗽、咳痰、胸闷、发热等非特异性症状,均缺乏午后低热、咯血、盗汗等结核特征性的临床表现。2) 影像学表现:均表现为局限性或两下肺为主的肺实变伴病灶周围的磨玻璃影和支气管充气征。与COP和常见的肺结核均有所不同。COP常见的影像学表现为两肺多发的、多形态、游走性的实变影[12]。感染继发的SOP,则因病原体感染灶的部位而相对固定,较少发生游走,表现为局灶性机化性肺炎(FOP),与COP 和其他继发的SOP有所区别[13]。同时所有报道都缺乏肺结核典型的树芽征、干酪样坏死、虫蚀样空洞等表现。肺结核干酪性肺炎也会表现为叶段分布的大片实变影,伴支气管充气征。发生于结核杆菌量多、毒力强时,以干酪样坏死为主要病理改变,常发生现液化,经排出后形成虫蚀样空洞。同时伴有渗出和增殖,故病灶密度不均,局部低密度影。而机化性肺炎密度相对均匀,无低密度区。3)实验室检查:结核分枝杆菌的检出率低。本例病人初期反复进行痰及灌洗液的涂片和结核分枝杆菌DNA检测均为阴性。将肺活检标本反复进行特殊染色,经过经验丰富的病理科专家多次仔细查找,仅找到了1条抗酸杆菌,证实了肺结核诊断。总结既往文献报道的7例病人,仅有1例痰涂片阳性。其病原学依据均为经过肺活检病理抗酸染色阳性或灌洗液的PCR及灌洗液结核分枝杆菌培养阳性,得以确诊。说明MTB感染引起的SOP,肺结核的特征性不强,其结核分枝杆菌负载量低和毒力相对较低,使得诊断更为困难。
治疗上主要有两方面。第一,抗结核治疗:对于SOP的治疗方案首要的是针对原发病的治疗。MTB感染引起的SOP必然是使用敏感的抗结核药物。第二,糖皮质激素的使用。糖皮质激素是一把双刃剑,它是治疗OP,尤其是COP的首选药物。对COP有效率可达90.7%[14]。同时激素引起全身代谢紊乱而影响机体的免疫功能。促进结核分枝杆菌代谢和繁殖,从而导致结核病变广泛、进展。对于MTB继发SOP单纯的使用糖皮质激素会加重肺结核原发病的进展,必须在有效的抗结核治疗的前提下进行激素的治疗。该患者初期使用仅使用糖皮质激素疗效不佳的原因就是没有针对结核分枝杆菌这一原发因素进行治疗,反而促进了疾病的进展。
总之,MTB感染后SOP的诊断主要依靠病原学、影像学特点、排除其他已知原因(如结缔组织疾病、肿瘤、药物、器官移植等)、且病理学具有OP的特征。虽然肺结核引起的SOP较为少见,但必须保持警惕。在病理明确OP后将MTB感染作为一个必须排除的诱发因素。必要时进行反复的支气管镜灌洗及肺穿刺活检。否则在没有有效的抗结核治疗下使用糖皮质激素会促使病情的加重,贻误病情。早期发现早期干预是治疗成功的关键。
利益冲突:所有作者均声明不存在利益冲突。
