RP-HPLC法同时测定苓桂术甘汤中的甘草苷和原儿茶酸含量
2021-09-23王来兵于姝燕郭晓宇陈建平
孟 园,王来兵,于姝燕,郭晓宇,王 敏,于 娟,李 冰,刘 涛,陈建平*
(1.巴彦淖尔市医院药剂科,内蒙古 巴彦淖尔 015000;2.内蒙古医科大学药学院)
苓桂术甘汤来自《伤寒杂病论》中的“金匮要略方剂”部分。苓桂术甘汤由四味常见药材,即茯苓、桂枝、甘草、白术组成。此汤剂为祛湿剂,主治因中阳不足所致的心胸满闷、短气而咳、起则头眩、气上冲胸等症[1,2],具有健脾利湿、温阳化饮等功效。在现代临床医学上,苓桂术甘汤常用于治疗慢性支气管炎、过敏性鼻炎、梅尼埃综合征、神经官能症、慢性肾小球肾炎水肿、心源性水肿、慢性心力衰竭等症,还可联合短期低热量饮食来控制Ⅱ型糖尿病患者的血糖[8,9]。苓桂术甘汤疗效显著、毒副作用低,具有较高的临床应用价值[3~10]。
据文献调研发现,目前对苓桂术甘汤的研究主要集中在临床应用以及药理作用方面,对其物质基础的研究报道相对缺乏。为了充分研究苓桂术甘汤中的有效化学物质,本研究首次建立高效快速的反相高效液相色谱(RP-HPLC)测定该方剂中甘草苷和原儿茶酸含量的方法,为苓桂术甘汤的质量控制及药效物质基础等研究提供新的依据及参考。
1 仪器与药品
1.1 仪器
AB135-S电子分析天平(瑞士,MettlerToledo);Ultimate 3000高效液相色谱仪(美国,ThermoFisher);KM-410C型数控超声波清洗器(昆山市超声仪器有限公司)。
1.2 药品
茯苓、桂枝、白术、甘草饮片购自内蒙古天立药业,所有药材经由内蒙古医科大学药学院生药学教研室渠弼副教授鉴定,均符合2020年版《中华人民共和国药典》要求。
甘草苷标准品(批号:G-009-181216,纯度>98%,成都瑞芬思公司),原儿茶酸标准品(批号:110809-201205,99.9%,中国食品药品检定研究院),乙腈(色谱纯,美国,Merck),甲醇(美国,Fisher,色谱纯),磷酸(85%水溶液,北京伊诺凯),超纯水为实验室自制,其余所用试剂药品均为分析纯。
2 试验方法与结果
2.1 色谱条件
色谱柱:Eclipse Plus C18(4.6 mm×250 mm,5 μM);在260 nm波长处检测,柱温25℃,流速1.0 mL·min-1,梯度洗脱(见表1),流动相为乙腈-0.1%磷酸水,进样量为10 μL。此条件下,原儿茶酸及甘草苷能与其他化学成分完全分离,且原儿茶酸理论塔板数>100000,甘草苷理论塔板数>200000。
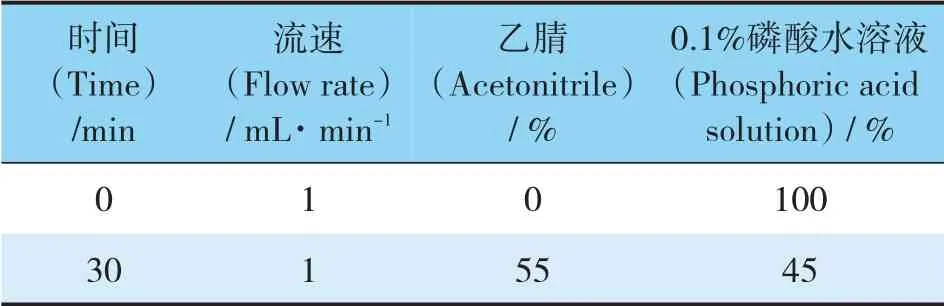
表1 梯度洗脱Tab.1 Gradient elution
2.2 对照品溶液的制备
精密称取干燥至恒重的甘草苷和原儿茶酸对照品。分别为4.23 mg和2.72 mg,置于烧杯中,加入少量甲醇溶液溶解后置于100 mL容量瓶中定容,配制成含42.3 μg·mL-1的甘草苷和27.2 μg·mL-1的原儿茶酸的甲醇混合液。
2.3 供试品溶液的制备
精密称取药材粉末2.75 g(粉碎并过60目筛的茯苓1 g、桂枝0.75 g、甘草0.5 g、白术0.5 g),放置于具塞锥形瓶中,加入甲醇溶液25 mL,密塞,称定重量,在功率40 kHz,频率为200 W,超声处理30 min,放至室温,补足差重,摇匀,湿法抽滤,即得。
2.4 线性关系考察
精密量取“2.2”项下对照品溶液0.25 mL、0.5 mL、1 mL、1.5 mL、2 mL、2.5 mL,分别置于5 mL容量瓶中,加甲醇至定容。按照“2.1”项下的条件检测,以进样量为横坐标。峰面积为纵坐标,测绘标准曲线,得甘草苷的回归方程为Y=145.0X+0.089(r=0.9992;n=6)、原儿茶酸的回归方程为Y=632.7X+0.074(r=0.9993;n=6)。结果表明,原儿茶酸、甘草苷浓度分别在1.36~13.60 μg·mL-1与2.12~21.15 μg·mL-1范围内呈良好的线性关系[11]。
2.5 精密度试验
精密量取同一批样品溶液,按照“2.1”项下条件连续进样6次,测定得甘草苷和原儿茶酸含量的RSD分别为0.18%、0.15%,结果表明该实验方法精密度良好。
2.6 稳定性试验
精密量取一定量的药品溶液,分别在0 h、2 h、4 h、6 h、8 h、10 h、12 h进行测定,测得甘草苷、原儿茶酸含量的RSD分别为0.33%、0.77%,实验结果显示样品溶液在12 h内稳定性较好。
2.7 重复性试验
精密称取同批次药材,按照“2.3”项下的实验方法,平行制备6份溶液,并按“2.1”项下实验条件检测,结果测得甘草苷和原儿茶酸的平均含量分别为618.6 μg·g-1和49.09 μg·g-1,RSD均为0.9%,实验结果表明该方法重复性良好。(见表2)。

表2 含量测定结果Tab.2 Content determination results
2.8 干扰性试验
分别量取空白溶剂适量、供试品试液适量、混合对照品试液适量于样品瓶中,按“2.1”项下实验条件检测。供试品溶液色谱图,在混合对照品试液的甘草苷和原儿茶酸相应的位置上,有保留时间相同的色谱峰,且空白溶剂中没有相应保留时间的色谱峰,空白溶剂对甘草苷及原儿茶酸的测定无干扰,说明该方法专属性良好(见图1)。
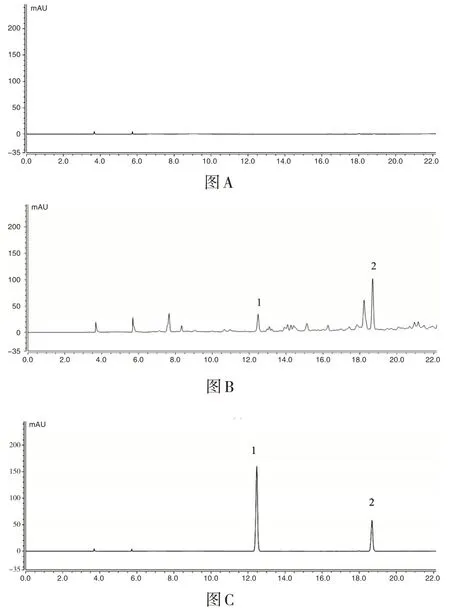
图1 干扰性试验Fig.1 Interference test
2.9 回收率试验考察
精密称取同批次已知含量的供试品6份,分别加入80%、100%、120%的甘草苷和原儿茶酸对照品试液各2份,按照“2.3”项下方法制备,按照“2.1”项下条件进样检测,测得甘草苷和原儿茶酸的平均回收率分别为98.37%,RSD=0.9%和98.51%,RSD=1.1%。结果表明该实验方法加样回收率良好[12](见表3)。
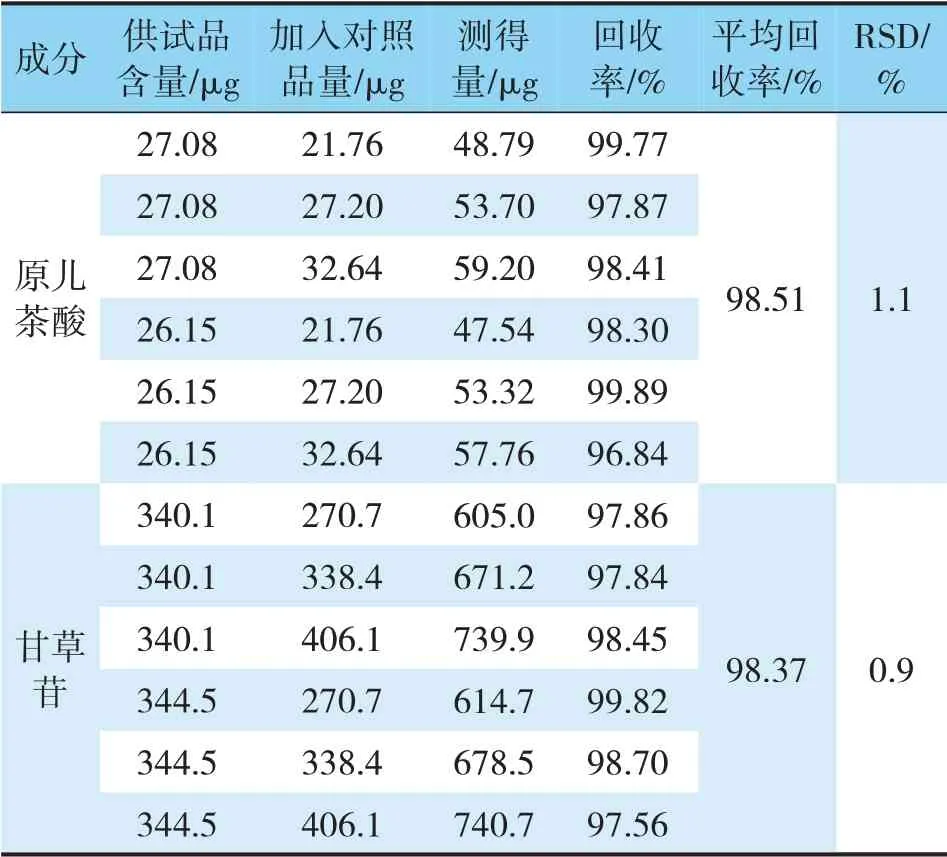
表3 加样回收率试验结果Tab.3 Test results of sample addition rocovery
3 讨论
3.1 提取方法的选择
样品溶液制备的预实验中,分别采用甲醇、无水乙醇、70%乙醇和水作为溶剂超声处理提取样品。测定显示,以甲醇作为提取溶剂,被测定成分溶解度好,提取率高,得到的两成分色谱峰峰形、高度均良好。
3.2 流动相的选择
分别采用了乙腈-0.1%磷酸水和甲醇-0.1%磷酸水进行梯度洗脱。结果表明用乙腈-0.1%磷酸水进行梯度洗脱,甘草苷及原儿茶酸均有较好的峰型和分离度;而用甲醇-0.1%磷酸水,甘草苷峰无法分开,仅原儿茶酸峰型和分离度良好。
3.3 检测波长的选择
在200~400 nm范围内用紫外-可见分光光度计对甘草苷和原儿茶酸进行扫描,结果表明甘草苷和原儿茶酸分别在278 nm和260 nm处有最大吸收。由于苓桂术甘汤中原儿茶酸的含量比甘草苷的含量低,若以278 nm作为检测波长时,原儿茶酸的峰面积太小,难以测量,而甘草苷在260 nm处峰型稳定,故选择260 nm作为检测波长同时对两组成分进行测定。
本试验成功建立了RP-HPLC法同时测定苓桂术甘汤中原儿茶酸和甘草苷的含量,通过方法学考察表明,所建立的方法简单灵敏、快速高效、易于操作,为苓桂术甘汤的质量控制研究提供理论参考。
